我院骨瓜提取物临床应用及安全性回顾性评价
2015-01-11孔飞飞张雨洁叶光明郭良君谭俊铭
孔飞飞 吴 英 沈 洁 张雨洁 叶光明 郭良君 谭俊铭▲
1.解放军第九八医院药械科,浙江湖州313000;2.解放军第九八医院骨六科,浙江湖州313000;3.解放军第九八医院医务处,浙江湖州313000
我院骨瓜提取物临床应用及安全性回顾性评价
孔飞飞1吴 英1沈 洁2张雨洁1叶光明3郭良君1谭俊铭2▲
1.解放军第九八医院药械科,浙江湖州313000;2.解放军第九八医院骨六科,浙江湖州313000;3.解放军第九八医院医务处,浙江湖州313000
目的分析解放军第九八医院(以下简称“我院”)骨瓜提取物应用情况及安全性,为临床应用和药品监管部门决策提供参考。方法采用病历回顾性研究方法,对我院2010年10月~2012年12月期间使用骨瓜提取物的完整住院病历进行调查,自建数据库,进行统计分析。结果共收集到3124份应用骨瓜提取物的住院患者病历,30~<60岁人群使用骨瓜提取物最多,占64.98%;适应证比较规范,用法均为静脉滴注,用量、溶媒选择、用药浓度及用药疗程上存在超说明书现象;不良反应发生率为1.92%,属常见范畴;主要表现为各种过敏反应,严重者可致过敏性休克,临床表现多样;累及全身多个系统,按发生率高低依次为皮肤及附件系统、呼吸系统、全身性、肝胆系统、神经系统、消化系统损害。结论骨瓜提取物临床应用不良反应发生率较低,安全性较高;不合理应用给临床用药安全性增加了风险,应加强生化药注射剂临床合理使用监管。
骨瓜提取物;临床应用;安全性;回顾性;评价
骨瓜提取物是近年来应用于骨伤科的复方新药制剂,主要用于风湿、类风湿关节炎、腰腿疼痛、骨折创伤修复等。目前对其的研究尚不多见,主要集中在骨瓜提取物单用或联合其他治疗手段的临床疗效观察及细菌内毒素检查方法等方面,亦有多篇骨瓜提取物致不良反应的病例报道[1],但对其在临床特别是创伤骨科应用中的安全性尚未有客观、系统的评价。解放军第九八医院(以下简称“我院”)拥有全军创伤骨科中心,收治包括军人、士兵、地方群众在内的各种骨伤科病患,年收治病人达十万人次,为促进创伤修复,多数会使用骨瓜提取物、骨肽、鹿瓜多肽等制剂。为进一步促进骨瓜提取物在临床使用的安全、合理、有效,对其安全性进行一个客观、系统的评价十分必要。因此,为了更进一步了解骨瓜提取物临床应用的安全性,发现其不良反应规律,本研究采用病历回顾性研究方法,开展病历调查,对骨瓜提取物的不良反应和危险因素进行分析,为其在临床的合理应用和药品监管部门决策提供参考。
1 资料与方法
1.1 一般资料
收集2010年10月~2012年12月期间我院应用骨瓜提取物的所有住院患者病历。
样本量的确定[2-3]:根据国际医学科学组织委员会推荐,用下列术语和百分率表示药品不良反应发生频率:十分常见(≥10%),常见(1%~<10%),偶见(0.1%~<1%),罕见(0.01%~<0.1%),十分罕见(<0.01%)。假设不良反应发生符合二项分布,不良反应的发生率为0.5%(包括偶见的不良反应)。利用概率论原理计算药品不良反应发生例数≥1的概率(P)为:P=1-P(0)=1-C0n×(0.005)0(1-0.005)n,即P=1-0.995n。如果要求P≥0.8,即有80%的可能性来保障不良反应发生例数≥1,则1-0.995n≥0.8,n≥322,即例数大于322例即有80%的把握保证总不良反应发生例数≥1。
1.2 研究方法
采用病历回顾性研究方法,通过医院信息管理系统检索获得使用骨瓜提取物的病历号,再提取相应病历,由5名经过培训的研究人员按要求填写骨瓜提取物使用情况调查表(电子版),记录用药科室、患者姓名、病历号、性别、年龄、出院诊断、过敏史、药品信息(包括规格、厂家、用法用量、溶媒、用药天数等)、不良反应、合并用药等相关信息,重点了解骨瓜提取物的药品不良反应/药物不良事件及其相关情况。
1.3 不良反应关联性评价与分类
不良反应因果关系评价采用国家药品不良反应监测中心制订的6级标准(肯定、很可能、可能、不太可能、未评价和无法评价),其中将关联性评价为肯定、很可能、可能的不良事件评价为不良反应。参照《WHO药品不良反应术语集》将不良反应按照累及的系统进行分类。
自建EXCEL数据表,将5名研究人员的调查表进行合并汇总,并统计分析。
2 结果
2.1 骨瓜提取物临床使用情况
2.1.1 患者性别及年龄构成情况此次调查共收集病历3124例,其中,男2167例,女957例,男女比例为2.26∶1;患者年龄最小为2岁9个月,年龄最大为93岁,中位年龄45.14岁。各年龄阶段分布情况见表1。
2.1.2 病种分布情况使用骨瓜提取物的疾病(以出院诊断为准)如下:各种类型的骨折2321例次,软组织损伤(含皮肤挫裂伤、韧带损伤、肌腱损伤等)1108例次,骨折术后633例次,腰椎损伤(包括椎间盘突出、椎管狭窄、椎盘不稳、椎体滑脱等)166例次,关节炎116例次,关节损伤16例次,脊柱损伤3例次,骨瘤(骨囊肿/骨巨细胞瘤)2例次,腰扭伤1例次,胸椎结核1例次,股骨头缺血性坏死1例次,骨质疏松1例次。因骨外伤疾病多同时合并两种或以上损伤,故总例次大于病例数,其中合并骨折和软组织损伤的有820例次。
2.1.3 既往过敏史情况本次调查中,有19例患者既往有药物过敏史,分别是青霉素过敏13例,头孢类过敏5例,1例不详。
2.1.4 品种分布情况此次调查的时间段内,骨瓜提取物先后有4个品种,具体分布情况见表2。
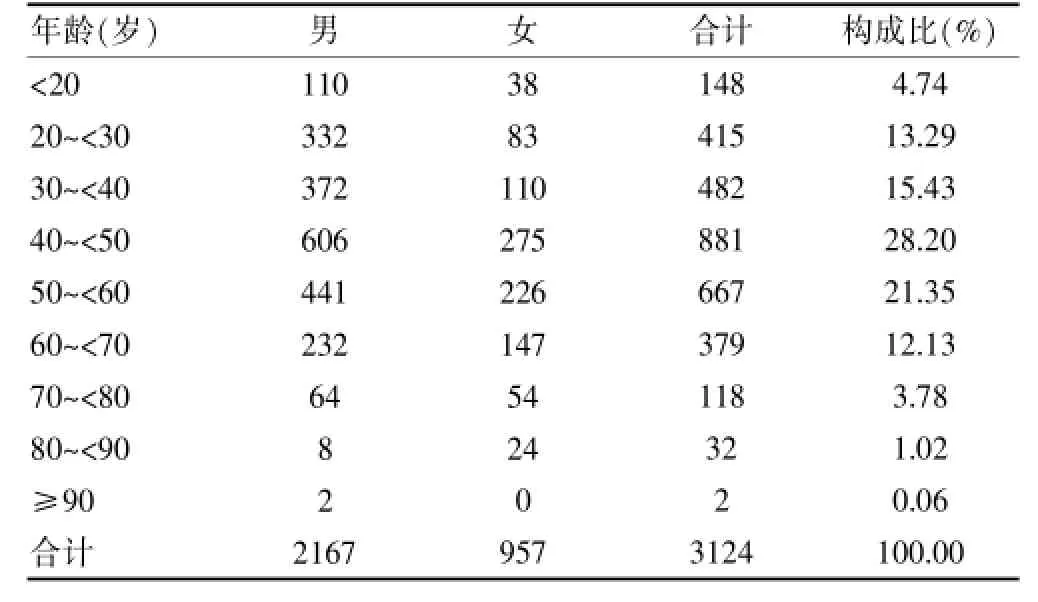
表1 使用骨瓜提取物患者年龄分布(例)
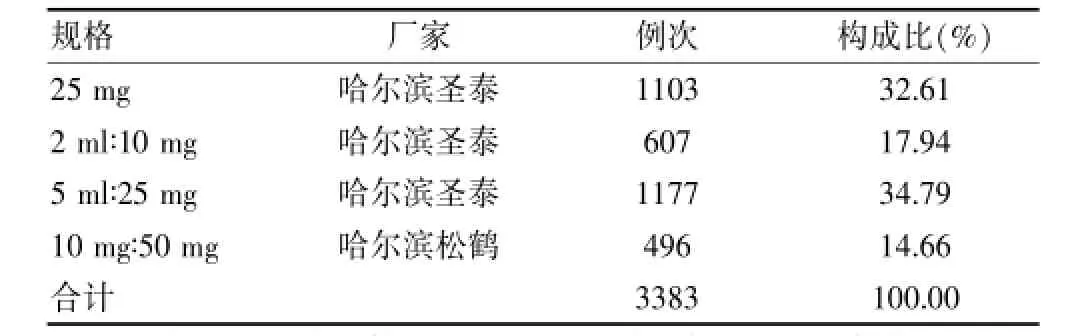
表2 骨瓜提取物使用品种分布
2.1.5 使用剂量情况在3124份病历中,均采用静脉滴注给药,1 d 1次。最小用量为10 mg,最大为500 mg,其中使用频率最高的剂量为100、50、75 mg,依次为1168例次(33.18%)、1157例次(32.87%)、801例次(22.76%)。具体使用剂量见表3。
2.1.6 使用疗程情况从使用疗程来看,骨瓜提取物平均使用天数为13.49 d,最少为仅使用1 d,即1次,最多为133 d。仅有93例使用疗程在21~30 d,占2.98%;2~7 d的1483例,占47.47%;8~20 d的1303例,占41.71%;39例>30 d,占1.25%;另有206例仅使用1次,占6.59%。具体疗程分布见表4。
2.1.7 溶媒选择情况具体为“0.9%氯化钠注射液”1665例次(48.02%),“葡萄糖氯化钠注射液”912例次(26.31%),“5%葡萄糖注射液”592例次(17.08%),“果糖注射液”127例次(3.66%),“果糖氯化钠注射液”109例次(3.14%),“转化糖注射液”42例次(1.21%),“10%葡萄糖注射液”9例次(0.26%),“转化糖电解质注射液”8例次(0.23%),“复方氯化钠注射液”3例次(0.09%)。因部分患者在使用中存在更换品种及输液的现象,故总例次大于总例数。
2.1.8 用药浓度情况本次调查的3124份病历中,溶媒用量在100~500 mL之间,但因剂量不同,致使最终用药浓度有很大差异,最大浓度为1.50 mg/mL,最小浓度为0.02 mg/mL,最常用的用药浓度为0.40 mg/mL,其次为0.20、0.30、0.10 mg/mL。见表5。
2.1.9 合并用药情况本次调查中,联合用药的有2949例,占94.40%,其中合并使用1种药物的有459例(14.69%),合并2种药物的有815例(26.09%),合并3种药物的有803例(25.70%),合并4种药物的有507例(16.23%),合并5种药物的有241例(7.97%),合并6种药物的有95例(3.04%),合并7种药物的有14例(0.45%),合并8种及以上药物的有15例(0.48%),最多合并使用12种药物。
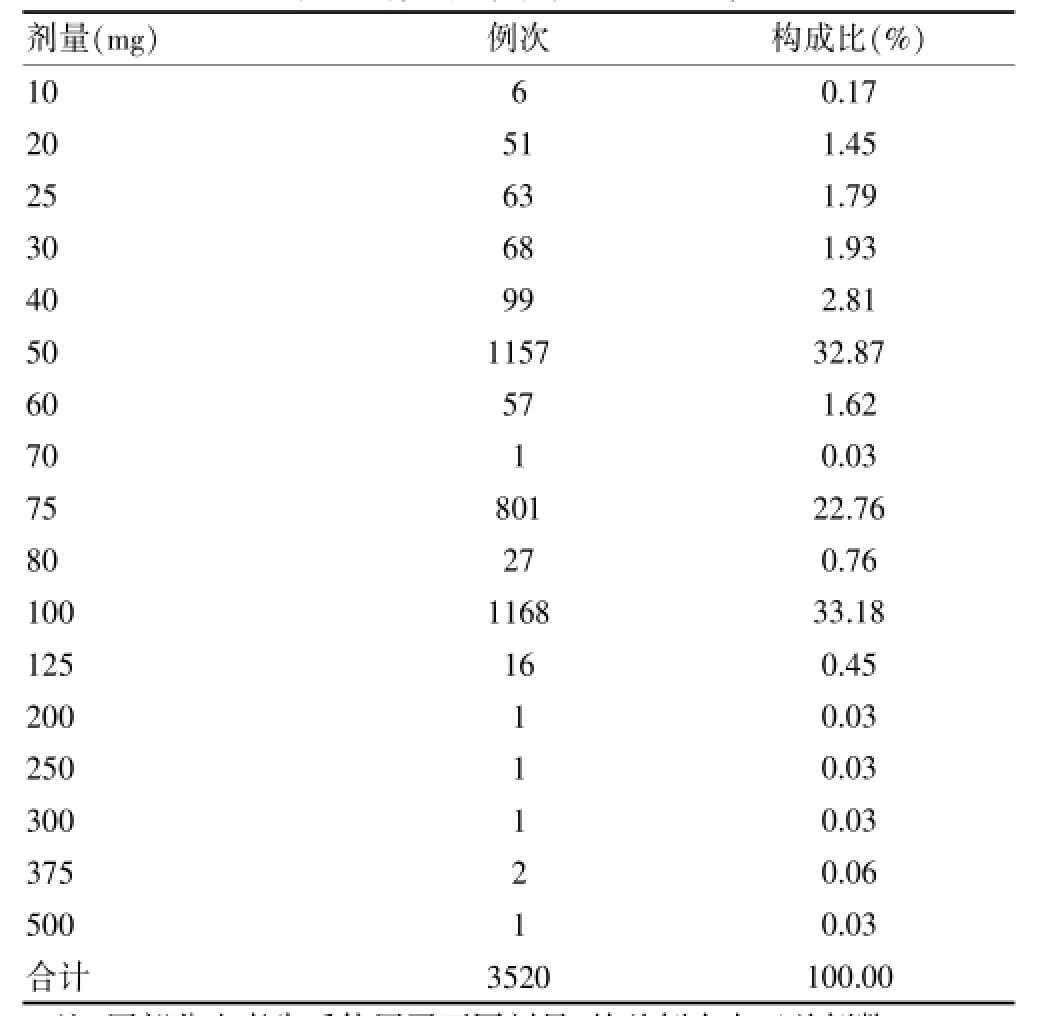
表3 骨瓜提取物使用剂量分布

表4 骨瓜提取物使用疗程分布
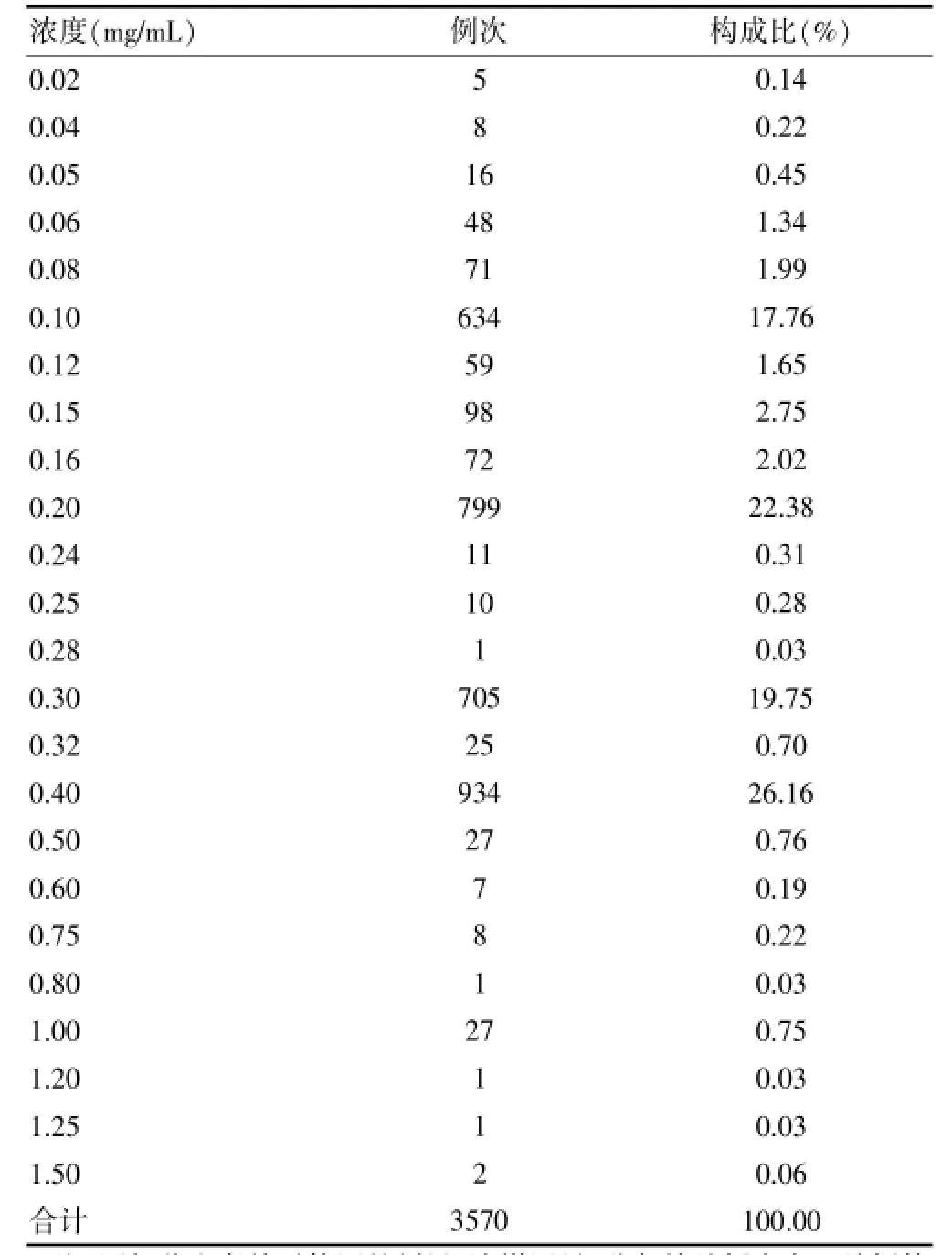
表5 骨瓜提取物最终用药浓度分布
2.2 骨瓜提取物不良反应发生情况
本次调查研究的3124份病历中,疑似发生不良反应的有63例,按照国家药品不良反应监测中心制订的评价标准,进一步对这63份病历分别进行评价,其中有4例在输注其他药物过程中出现,停药对症治疗后即好转,并未停用骨瓜提取物,因此评价与骨瓜提取物的关联性为不太可能。最终评价结果为:肯定的2例,很可能的18例,可能的39例,共计发生不良反应59例,其不良反应发生率为1.92%,属于常见范畴(1%~<10%)。
从不良反应的临床表现来看,主要表现为皮疹、瘙痒、胸闷、气急、呼吸困难、寒战、高热、荨麻疹、头痛、肝酶升高、恶心等,严重者可致过敏性休克,临床表现多样,涉及系统按发生率高低依次为:皮肤及附件系统、呼吸系统损害、全身性损害、肝胆系统损害、神经系统损害、消化系统损害及其他。见表6。
3 讨论
3.1 骨瓜提取物临床使用情况
骨瓜提取物在临床上使用非常广泛,合理用药显得尤其重要,其用药安全性特别值得关注。本次研究表明,骨瓜提取物在临床使用过程中可能存在一些不合理现象。
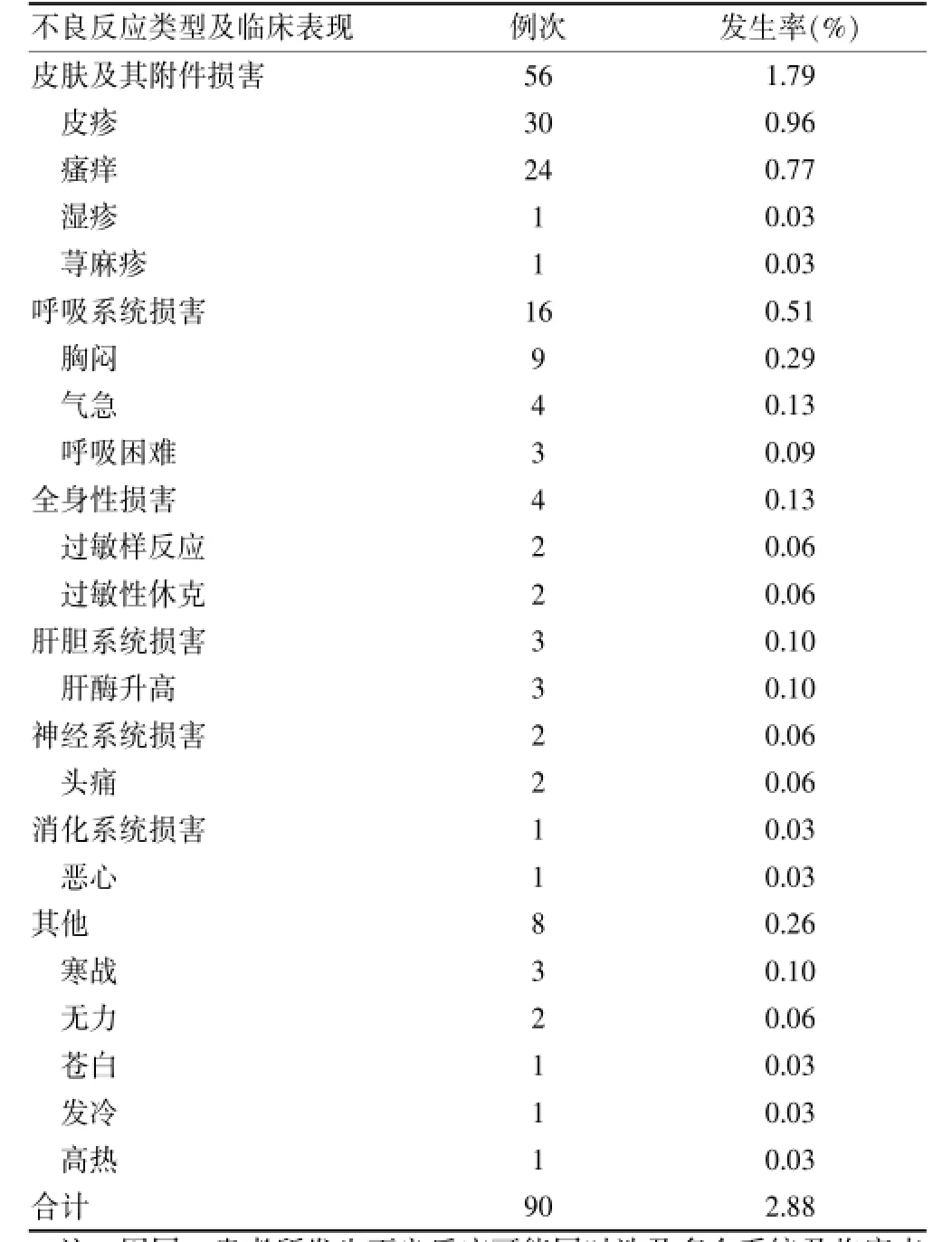
表6 骨瓜提取物不良反应的类型、临床表现及发生率
3.1.1 特殊人群的用法用量未能明确本次研究显示,使用骨瓜提取物的患者中男女比例为2.26∶1,30~<60岁之间使用骨瓜提取物的人数最多,共计2030例,占64.98%,这可能与收治患者的病种特点有关。从研究结果来看,使用骨瓜提取物的患者年龄最小者仅2岁9个月,最大者为93岁,由于生理原因,老人与儿童在药物的吸收、分布、代谢、排泄等方面具有特殊性[4-5],药品说明书中未注明这些特殊人群的用法用量,仅在注意事项下指出“考虑到老年人机体功能下降,且耐受力差,建议不宜使用,若使用,临床用药不建议用到最大剂量”,临床医师对这类人群完全凭经验用药,其安全性值得担忧。
3.1.2 使用指征基本符合,个别超说明书说明书规定,骨瓜提取物的适应证为风湿、类风湿性关节炎、骨关节炎、腰腿疼痛、骨折创伤修复。本次调查发现,我院骨瓜提取物临床使用的指征规范率为99.94%,但仍有个别不符合要求,如用于骨瘤是否合适等。由于药品说明书更新较慢,不可能及时覆盖临床实际用药情况,超适应证用药难以避免,但毕竟不是说明书核准的适应证,医师和药师都面临一定的风险,一旦出现意外情况,极易导致医疗纠纷[6],建议临床医师严格按照说明书的适应证使用。
3.1.3 用量、溶媒选择、用药浓度存在超说明书现象本品说明书中规定,静脉注射时,一次50~100 mg,加入250 mL生理盐水或葡萄糖注射液中,每日1次,20~30 d为1个疗程。在本次调查中发现,用法均为静脉滴注,符合说明书规定。但在用量、溶媒选择、用药浓度上存在超说明书现象。用量方面,按说明书选择50~100 mg的有3126例次,占研究总例次的88.81%,仍有287例次选择了50 mg以下剂量,有22例次选择了100 mg以上剂量,其中最大者达到了500 mg。通过调查发现,部分临床医师存在认识误区,在不熟悉用量的情况下,通过随意加大用量的方法来增强疗效,这种无依据增加剂量的用法,会增加毒性及不良反应的发生[7],因为超剂量使用可能会导致稀释后不溶性微粒增加,同时还会使药液浓度增大,在相同的滴注速度下更易引发由药理作用增强所致的A类不良反应的发生[8]。药品说明书注意事项中也明确指出,严格按照说明书推荐的用法用量使用,严禁超剂量。
溶媒选择上,说明书推荐用生理盐水或葡萄糖注射液,本次调查发现,按照说明书选择溶媒的有2257例次,占65.10%,有1210例次选择了葡萄糖氯化钠注射液、果糖注射液、果糖氯化钠注射液、转化糖注射液、10%葡萄糖注射液、转化糖电解质注射液、复方氯化钠注射液。溶媒品种选择不合理,可能导致pH值改变、变色、混浊、产生气泡等[9],目前关于骨瓜提取物与输液配伍方面的文献未见报道,本研究发现,其外观、pH值及不溶性微粒并未有显著改变,将另行撰文探讨。同时建议有关厂家进行相关研究,完善药品说明书,以规范临床合理用药。在此之前,建议临床医师按照说明书选择溶媒。
在最终用药浓度方面,说明书中没有明确规定,但按照说明书注明的50~100 mg溶解在250 mL溶媒中计算,最终用药浓度应在0.2~0.4 mg/mL。本研究发现,临床使用浓度在0.2~0.4 mg/mL范围内的有2485例次,占69.61%;最大浓度达到了1.5 mg/mL,最小浓度仅为0.02 mg/mL。作为来源于动物骨头和植物提取物的生化药,其成分复杂,浓度过小是否能达到预期治疗效果尚未可知,但因溶媒用量过多,输液量增加而致药物浓度过低可能会影响药物的治疗作用,增加患者的经济负担[9]。浓度过大是否能被机体完全吸收利用、是否会对机体产生一定的副作用尚不得而知。有研究显示,浓度过大可能使不溶性微粒、内毒素等随之增加,易引发不良反应[9]。建议有关部门尽快进行相关研究,以规避可能的用药风险。
3.1.4 用药疗程存在超说明书现象骨瓜提取物的说明书中规定,静脉注射时,20~30 d为1个疗程。骨伤科疾病的治疗多为长期的过程,疗程过短尤其是仅使用一次是否能达到预期的治疗效果,值得商榷。而疗程过长可能会使药物在体内蓄积引起中毒或产生依赖性,增加不良反应的发生。
3.2 骨瓜提取物不良反应发生率相关探讨
本次调查显示,骨瓜提取物不良反应发生率为1.92%,根据国际医学科学组织委员会推荐的药品不良反应发生频率的表示方法(常见1%~<10%),本药的不良反应较为常见。骨瓜提取物不良反应累及全身多个系统,按发生率高低依次为皮肤及附件系统、呼吸系统、全身性、肝胆系统、神经系统、消化系统损害。该结果可作为临床医师临床使用骨瓜提取物参考以权衡利弊。
3.3 不良反应相关因素探讨
骨瓜提取物所致不良反应的相关因素比较复杂,据课题组的前期研究报道,可能与骨瓜提取物的质量、微粒变化、患者个体差异、合并用药等因素有关。
3.3.1 药物自身的因素骨瓜提取物系列产品是复方新药制剂,系由猪骨和甜瓜籽提取精制而成,含有多种骨代谢物的活性肽类,对人体而言是一种异种蛋白,存在致敏因素。可能与多肽类注入体内可产生抗体有关,再次输入时可发生变态反应,甚至过敏性休克[1,10-11]。同时,在精制过程中亦可能混入组胺、类组胺样具有降压作用的物质,从而影响药物治疗和产生不良反应[12-16]。建议厂家加强对产品有效成分的纯度控制,提高杂质检测、降压物质检测标准,从而提高产品质量,减少不良反应发生。
3.3.2 药物辅料骨瓜提取物粉针剂产品中含有辅料右旋糖酐40或右旋糖酐20,该物质为蔗糖经发酵后生成的高分子葡萄糖聚合物,国家药品不良反应监测中心发布的《药品不良反应信息通报》第3期中明确提示,右旋糖酐40可引起过敏性休克。亦有文献报道,右旋糖酐可引起过敏性反应甚至休克[17-18]。
3.3.3 个体差异过敏反应的发生与患者的体质有关,过敏体质者更易发生严重不良反应。但本次调查中,记载既往药物过敏史的19例患者并未发生不良反应,而发生不良反应的59例患者其病历中并未记载药物过敏史,与李映辉等[10]对注射用骨瓜提取物致不良反应流行病学特点的报道一致,值得进一步深入探讨。经研究组进一步深入临床调查发现,病历中未记录过敏史的患者有相当一部分是患者自己回忆不起来的。为保证临床用药安全,临床医师在使用前仍应详询患者药物过敏史,过敏体质者慎用,对本品过敏者禁用。
3.4 本次研究的缺陷
本次调查中,采用了集中监测的方法,进行不良反应的回顾性病历分析。该方法是指在一定时间(数月或数年)、一定的范围(某一地区、几所医院或几个病房)内根据研究目的详细记录药物和药品不良反应的发生情况[19],能够统计特定药物在特定应用范围内的不良反应发生率,数据真实可靠,具有可参考性。但因只是在一定时间、一定范围内进行,数据量有限,难以发现有些罕见、严重的不良反应。
3.5 结论
通过本次调查发现,作为一所军队综合性三甲医院,我院骨瓜提取物多用于骨伤科患者,其适应证、用法比较规范,用量、溶媒选择及用药疗程与说明书要求有一定差距。骨瓜提取物在我院不良反应发生率为1.92%,属于常见范畴。不良反应症状大多较轻,主要表现为皮疹、瘙痒、胸闷、气急、呼吸困难、过敏样反应、头痛、肝酶升高、恶心、寒战、高热、荨麻疹,严重者可致过敏性休克。临床使用该制剂时,应严格按照说明书规定用药,对特殊人群用药需加强监护,首次使用本品时,宜选用小剂量,缓慢滴注,滴速控制在30滴/min以内,在静滴前30 min要密切观察,以备不测。
[1]孔飞飞,郭良君,王翔,等.骨瓜提取物致不良反应文献分析[J].中国医药,2014,9(1):113-117.
[2]郑青山,孙瑞元,陈志扬.新药临床试验最低例数规定的安全性评价[J].中国临床药理学与治疗学,2003,8(3):354-355.
[3]朱玲琦,周昕,杜蕾,等.我院参麦注射液应用情况及不良反应分析[J].中国药物警戒,2013,10(2):111-114.
[4]郭淑敏.规范特殊人群用药安全性标[J].中国医院药学杂志,2008,28(8):657-659.
[5]闫佳佳,李佳.650份药品说明书中特殊人群用药情况调查分析[J].中国处方药,2014,12(5):40-41.
[6]洪顺福.我院门急诊西药超适应症用药处方分析[J].海峡药学,2013,25(6):254-255.
[7]刘辽,蒋丹,贾萍,等.门急诊“超说明书”用药处方点评分析[J].中国药物警戒,2013,10(3):178-181.
[8]付联群.超剂量使用红花注射液引起的不良反应病例分析[J].中国中西医结合杂志,2012,32(1):124-125.
[9]梁少华,桑国优.中药注射剂临床合理使用调查[J].中国药师,2011,14(5):706-708.
[10]李映辉,陈辉清.注射用骨瓜提取物不良反应报告相关因素分析及预防[J].中国医药导报,2013,10(11):108-112.
[11]孔飞飞,郭良君,谭兴起,等.骨瓜提取物致药物不良反应20例分析[J].中国新药杂志,2013,22(8):979-982.
[12]潘智然.不同剂量甲氨蝶呤治疗类风湿性关节炎的不良反应探讨[J].中国当代医药,2014,21(34):92-93,96.
[13]邓丽娟,梁成罡,范慧红.几种多组分生化药注射剂降压物质的探讨[J].中国药事,2010,24(6):546-549.
[14]钱钦.中药注射剂不良反应发生原因及防治措施分析[J].中国医药科学,2014,4(18):79-81.
[15]吴煊.57例舒血宁注射液不良反应报告分析[J].中国当代医药,2014,21(11):73-74.
[16]罗金娥,姜学辉.地塞米松治疗上呼吸道感染的疗效及不良反应分析[J].中国医药科学,2014,4(6):99-100,171.
[17]张翼.右旋糖酐40致过敏性休克2例[J].医药导报,2010,29(5):690.
[18]贾凤华.右旋糖酐20葡萄糖注射液致过敏性休克1例[J].中国药事,2011,25(6):封3.
[19]王永铭,李端.临床药理学[M].2版.上海:上海医科大学出版社,1999:39.
A retrospective evaluation on the clinical application and safety of Gugua Extract Injection
KONG Feifei1WU Ying1SHEN Jie2ZHANG Yujie1YE Guangming3GUO Liangjun1TAN Junming2▲
1.Department of Drug and Equipment,98th Hospital of People's Liberation Army,Zhejiang Province,Huzhou313000, China;2.The 6th Department of Orthopaedics,98th Hospital of People's Liberation Army,Zhejiang Province,Huzhou 313000,China;3.Medical Department,98th Hospital of People's Liberation Army,Zhejiang Province,Huzhou 313000,China
Objective To analyze the application and safety on Gugua Extract Injection in 98th Hospital of People's Liberation Army(“our hospital”for short),as references for proper clinical application and policy decisions from Drug Administration.Methods Cases on Gugua Extract Injection between October 2010 and December 2012 in our hospital were reviewed retrospectively and analyzed statistically on self-built database.Results In 3124 cases,64.98%patients who took Gugua Extract Injection were aged 30-<60.Gugua Extract Injection was used under clinical indications by intravenous drip.In some cases,dosage,solvent,drug concentration and course of treatment were beyond specification. The incidence of ADRs was 1.92%;anaphylaxis was the main manifestations,severe cases could cause anaphylactic shock,diversity of clinical situation;ADRs involving multiple systems,included damage of skin and its appendages, respiratory system,systemic,hepatobiliary system,nervous system,digestive system.Conclusion The ADRs occurrence rate of Gugua Extract Injection is low,which has high security.Irrational clinical application can increase risk.The supervision of clinical application of biochemical drug injection should be strengthened.
Gugua Extract Injection;Clinical application;Safety;Retrospective;Evaluation
R969.3
A
1673-7210(2015)06(b)-0038-06
2015-03-11本文编辑:程铭)
浙江省药学会医院药学专项科研基金项目(2012ZYY24)。
▲通讯作者
