新型降胆固醇药物(PCSK9靶向抑制剂)的研究现状和进展
2015-01-03周巧霞王炳银
刘 峰 周巧霞 王炳银
上海交通大学医学院附属苏州九龙医院心脏中心,苏州 215021
新型降胆固醇药物(PCSK9靶向抑制剂)的研究现状和进展
刘 峰 周巧霞 王炳银▲
上海交通大学医学院附属苏州九龙医院心脏中心,苏州 215021
低密度脂蛋白胆固醇在动脉粥样硬化性心血管疾病(ASCVD)的发生、发展中起着重要作用,他汀类制剂是预防和治疗ASCVD的基石,但使用足量他汀降脂不理想而又有较高心血管疾病风险者、家族性高胆固醇血症患者,因副作用无法耐受足量他汀治疗者等均需要其他新的有效、安全降脂药。前蛋白转换酶枯草溶菌素9(PCSK9)抑制剂能够显著升高肝细胞表面LDL-C受体,进而结合更多的LDL-C而降低血LDL-C水平。多种标靶PCSK9抑制剂蛋白的单克隆抗体已陆续问世。大量的基础和临床研究均已证实,PCSK9抑制剂能明显降低血LDL-C水平,且耐受性和安全性良好。初步的研究资料显示,PCSK9抑制剂能减少心血管事件,结果令人鼓舞。
胆固醇;家族性高胆固醇血症;降胆固醇药:PCSK9靶向抑制剂;心血管疾病
低密度脂蛋白胆固醇(low density lipoprotein cholesterin,LDL-C)在动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)发生、发展中起着重要的主导作用,大量的循证医学证据表明,他汀类制剂是预防和治疗ASCVD的基石。尽管他汀是防治心血管事件最有效的药物,但仍有部分患者有额外的治疗需求,如部分心血管疾病高危患者接受足量他汀后降脂不理想,仍存在较高的心血管疾病风险;又如家族性高胆固醇血症患者 (familial hypercholesterolemia,FH)LDL-C水平明显升高,超过50%的此类患者在服用大剂量强效他汀后LDL-C水平仍未能达标;部分患者因副作用(如肌痛和横纹肌溶解等)难以足量服用他汀。美国的一项调查显示,约12%的患者会中止他汀治疗,其中62%的患者是由于副作用的原因[1-2]。此外,有资料显示,强化剂量他汀治疗会增加新发糖尿病的发生率,从而有可能进一步限制最大剂量他汀的使用[3-4],因此,寻找一种能够安全有效地降低LDL-C水平的药物十分必要,已成为降脂领域的研究热点。近年来的研究显示,前蛋白转换酶枯草溶菌素9(proprotein convertase subtilisin/kexin 9,PCSK9)是一种分泌型丝氨酸蛋白酶,对肝细胞表面LDL-C受体表达的调节起着关键作用,可使肝细胞表面的LDL受体(LDL-R)减少,进而使肝细胞对LDL-C颗粒的清除能力下降。抑制PCSK9能够明显升高肝细胞表面LDL-C受体,进而能够结合更多的LDL-C而降低血LDL-C水平,由此引发了众多的关于PCSK9抑制剂的开发和研究,多种标靶PCSK9抑制剂蛋白的单克隆抗体已陆续问世。大量的基础和临床研究均已证实,PCSK9抑制剂能明显降低血LDL-C水平,且耐受性和安全性良好。初步的研究资料显示,PCSK9抑制剂能减少心血管事件,结果令人鼓舞[5-6]。部分专家预测,随着PCSK9抑制剂大规模临床试验结果的陆续公布,其有可能撼动他丁调脂的霸主地位[7]。本文通过查阅相关文献,对PCSK9抑制剂的研究现状进行综述并推测其近期发展趋势以供同行参考。
1 PCSK9的发现
自1990年以来,哺乳类动物中前蛋白转换酶的8个亚型及其相关分泌性前体的组织特异性已陆续阐明。2003年加拿大临床研究所神经内分泌生物研究实验室Seidah教授[8]发现了一种新的前蛋白转换酶成分,其主要在肝脏合成,少部分在肠道和肾脏合成,前体由692个氨基酸(分子量75 kD)组成,在细胞的内质网内裂变和分子的自动催化后合成的可溶性酵素酶进入细胞的分泌通道被释放到血循环,命名为神经凋亡调节转换酶1(NARC1),是PCS家族kexin分型中的新成员。2003年,法国学者Abifadel观察到2例NARC1基因功能获得性变异患者(血胆固醇明显升高和早发心血管死亡),这是除LDLR、ApoB外,第3个与常染色体显性家族性高胆固醇血症有关的基因 (autosomaldominanthypercholesterolemia,ADH),研究发表在Nature Genetics上,NARC-1从此正式更名为PCSK9。此后,PCSK9的确切胆固醇调节作用机制在大量的动物实验研究中逐渐被阐明[9-10]。
2 PCSK9的在胆固醇平衡调节中的作用机制
血循环中大量的低密度脂蛋白胆固醇是在肝细胞表面被LDL-C受体清除(图1)。
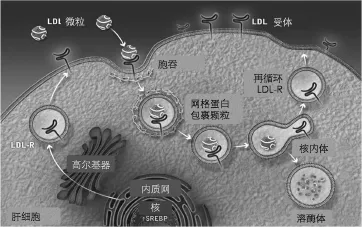
图1 肝细胞表面LDL受体结合血LDL颗粒后降解LDL后再循环示意图
LDL-C颗粒与肝细胞表面的LDL受体结合形成复合物,然后被吞噬进入细胞内。当胞内的pH值降低时,LDL受体与LDL-C颗粒解离,重返肝细胞表面,再次循环上述过程,而LDL颗粒则被溶酶体降解成胆固醇在细胞内储存或作他用。一般而言,LDL受体反复循环150次,能够结合足量的LDL颗粒以有效降低血LDL水平。LDL受体活性在转录过程中受甾醇调节元件结合蛋白2(sterol regulatory elementbinding protein 2,SREBP-2)的调节,转录后受PCSK9影响。PCSK9表达增加能直接下调LDL受体活性,或通过与LDL受体不可逆结合后与LDL一起被溶酶体降解,使LDL受体无法再循环,从而降低了与血LDL的结合能力,使血LDL水平明显增高(图2)[11]。

图2 PCSK9与LDL受体不可逆结合和LDL颗粒一起被溶酶体降解过程图
3 PCSK9水平的波动与变化
研究显示,在肝细胞的转录中,PCSK9和LDL受体均受细胞内胆固醇浓度的影响并通过SREBP-2调控。人群中PCSK9水平变异加大,可相差100倍。高龄、女性、绝经期、高体重指数、高LDL-C水平、高血糖和高胰岛素血症、糖尿病、高C反应蛋白水平均会使PCSK9明显升高。另外,PCSK9也呈现昼夜变化,PCSK9在3:00 pm~9:00 pm处于低谷,凌晨4:30左右达峰值水平,这种变化部分与白天食物的摄入有关,有助于细胞内胆固醇储存,PCSK9转录下调,而夜间相对空腹,细胞内胆固醇储存下降,PCSK9转录上调[12]。白天给予消胆安,其结合肠道和胆管内的胆酸能够促进肝脏胆固醇转化为胆酸,减少细胞内胆固醇浓度,肝细胞试图储存胆固醇会出现HMGCoA还原酶、LDL-R和PCSK9转录上调,次日这种昼夜变化会消失。他汀通过HMGCoA还原酶抑制胆固醇合成,另一方面,其也呈剂量依赖性地通过SREBP-2诱导PCSK9 和LDL受体基因的表达,进而在一定程度上限制了他汀剂量依赖性降脂作用,贝特类降脂药物也同样通过SREBP-2上调PCSK9水平[13]。
4 PCSK9突变
PCSK有2种突变方式,即功能获得性突变(GOF)和缺失性突变(LOF)。顾名思义,GOF是基因突变引起PCSK9血浆水平增加,或与LDL-R结合能力增加,两者均使能血LDL-C水平升高,前者突变基因位于R218S和F216L,后者在D374K和S127R[14]。90%的杂合子家族性高胆固醇血症(HeFH)患者主要是由于LDL-R基因突变所致,4%~10%与Apo-B有关,但极少数特别是极严重患者也与PCSK9的GOF直接相关[15-16]。LOF是基因突变引起PCSK9分泌衰减使血浆水平降低,或造成与LDL-R结合能力下降,进而导致血LDL-C水平降低。如果正常血LDL-C水平为105 mg/dl左右,那么LOF突变可使LDL-C平均水平下降到55~88mg/dl。有资料显示,由Y142X和C679X引起的LOF在非裔美国人群中占2%,其平均LDL-C水平下降28%,冠心病风险下降88%。同样,在社区人群超过15年的ASCVD风险观察评估中,由R46X引起的LOF平均LDL-C下降15%,冠脉事件风险下降47%[13-15]。
5 PCSK9靶向抑制剂研究动向
目前,有3种类型的PCSK9靶向抑制剂正处于研发和临床研究的不同阶段,包括PCSK单克隆抗体、小干扰性RNA和反义寡核苷酸(表1)[13]。

表1 PCSK9靶向治疗各研发公司的研发药物和临床研究状况
5.1 单克隆抗体
目前研究最多且在临床上最常应用的PCSK9抑制剂为单克隆抗体(mAbs)。自2009年以来,多家公司参与其研究开发。PCSK靶向的单克隆抗体竞争性绑定到PCSK9和LDL-R的结合位点,从而阻断了PCSK9与LDL-R之间的有效结合。早期的动物实验研究表明,抗PCSK9单克隆抗体能增加肝细胞表面LDL-R,降低LDL>30%,现在大部分单克隆抗体都已进入三期临床研究[17-18]。现有资料显示,单克隆抗体PCSK9抑制剂能够降低血LDL-C呈时间和剂量依赖性。图3为静脉注射Alirocumab后的血浆PCSK浓度和LDL-C变化曲线[19]。

图3 注射单克隆抗体PCSK9抑制剂血浆PCSK9和LDL-C的变化曲线
5.2 小分子干扰RNA
抑制PCSK9的另一个途径是通过注射纳米级类脂质的小单片段RNA(siRNA)去结合PCSK9的mRNA,使PCSK9mRNA沉默。动物研究显示,注射siRNA能使近一半的PCSK9mRNA沉默,血PCSK9浓度下降,LDL降低50%~70%,并且其作用快速,持续和可逆转。目前临床一期研究在健康受试者中也证实,siRNA能使循环血PCSK9浓度降低70%,血LDL水平下降40%。有研究观察到最大剂量siRNA寡核苷酸ALN-PCS02效应最强,无明显的严重不良反应[20-21]。
5.3 反义寡核苷酸
第3种方法是利用反义核苷酸(ASOs)干扰mRNA的作用。在最初的研究中,抑制PCSK9分泌的主要靶标为mRNA。动物实验中,一种靶向PCSK9的短核苷酸片段 (ASO)能够使mRNA降低92%,LDL下降30%。在猴实验中,ASO能使血PCSK9降低85%,LDL水平下降35%,并且可维持3周[15,22],但目前还没有进入临床研究。
6 近期公布的一些关于PCSK9靶向抑制剂的临床试验
近年来,关于Alirocumab和Evolocumab两个单抗PCSK9抑制剂一定样本量的三期临床研究陆续被公布。在依折麦布或者在不同强度他汀应用基础上加用PCSK9抑制剂能使LDL-C、ApoB、Lp(a)水平进一步下降,HDL水平轻度升高,三酰甘油水平降低,且其疗效不受年龄、宗教、种族和体重指数影响[15,20],提示这两种药物在强化他汀治疗LDL-C未达标者、他汀不耐受者和家族性高胆固醇三类人群中的作用显著。DESCARTES-2是迄今为止随访时间最长(52周)的一项研究,其纳入了901名接受大剂量他汀治疗后LDL-C>75mg/dl的非冠心病或冠心病患者,参与者随机接受每4周1次的Evolocumab 420mg或安慰剂治疗,除此之外,参与者同时还分别接受单独饮食调整、阿托伐他汀10mg及饮食调整、阿托伐他汀80mg或阿托伐他汀80 mg+依择麦布10 mg的基础治疗。从基线期到第52周,Evolocumab使低心血管风险和冠心病患者的LDL-C水平降低了57%,超过安慰剂[23]。在一组307例对至少两种他汀不耐受的患者中,给予Evocolumab 140 mg每2周1次和420 mg每4周1次,治疗12周,其LDL-C水平分别下降53%和55%[7-14]。另一组研究包括314例平均胆固醇水平为190 mg/dl的患者,其因肌痛不耐受他汀,被随机分为应用Alirocumab组(75 mg每2周1次和150 mg每2周1次)、依折麦布组(10 mg/d)和阿托伐他丁组(20mg/d),结果显示,Alirocumab降低LDL-C水平最显著,其LDL-C绝对值下降84 mg/dl,并且肌痛发生率最低(Alirocumab 33%,依折麦布44%,阿托伐他丁46%)[7]。Evolocumab已经完成纯合子和杂合子FH独立三期临床试验,将331例患者分为HeFH Evolocumab 140 mg每2周1次组和420mg每4周1次组,并设置安慰剂对照组,结果显示,Evolocumab降低LDL-C达60%(90~95mg/dl)。同样,在2个试验共732例已接受最大耐受量他丁和其他降脂药物治疗的HeFH患者中,给予Alirocumab 24周后,LDL-C下降51%~58%(66~85 mg/dl)。唯一一项50例纯合子FH三期临床研究显示,在标准12周降脂治疗后,应用Evocolumab能够使LDL-C水平进一步降低31%,其绝对值下降93mg/dl[16]。
最近公布的两项更大样本量和观察时间更长的三期临床试验OSLER1和ODESSEY研究结果能更充分地提供PCSK9抑制剂的长期疗效和安全性信息,受到广泛关注。OSLER1研究入选了1104例患者,分别应用Evolocumab加标准降脂治疗和单独的标准降脂治疗,并进行非盲对照,观察52周。结果显示,Evolocumab组始终较对照组LDL-C降低52%左右。Evolocumab的长期耐受性良好,不良反应发生率为3.7%,严重不良事件与对照组相似(7.1%vs.6.3%),不良事件在LDL-C<25 mg/dl和高LDL-C组之间无显著性差异[6]。ODESSEY研究包括2431例高胆固醇高危心血管患者,观察24周后也获得类似结果。更令人鼓舞的是,尽管两项研究观察时间还不够长,但已经显示出这两种PCSK9抑制剂降低心血管的终点事件(图4)[7]。
7 正在进行的一些PCSK9靶向抑制剂大规模临床预后试验
目前,据有关文献显示,有4项PCSK9抑制剂大规模临床预后试验正在进行中,包括ODYSSEY OUTCOME、FOURIER、SPIRE-1和SPIRE-2,共纳入70 000研究对象,均为急性冠脉综合征后LDL-C水平>70mg/dl的高危心血管患者,观察时间3~4年,大部分研究结果预计在2017年底前后公布。这些研究结果的公布将进一步明确PCSK9降低LDL-C的疗效及其对心血管事件影响的重要意义[24-26]。
8 小结与展望
综上所述,PCSK9的发现和新型降胆固醇药物—PCSK9抑制剂的基础和临床研究均显示出鼓舞人心的数据和初步结果,且大规模临床预后试验正在进行中。相关临床试验已证实以下几方面内容:①作为一种新型降低胆固醇药物,PCSK9抑制剂在降低LDLC水平方面效果显著且严重副作用少;②对于他汀类药物疗效欠佳的严重高脂血症患者(包括家族性高脂血症)和他汀不耐受的患者则可考虑使用PCSK9抑制剂;③PCSK9抑制剂的作用不受年龄、体重指数、LDL-C、服用他汀类药物或者他汀剂量的影响;④PCSK9抑制剂的成本及成本效益尚未确定。有关PCSK9抑制剂的大规模临床试验结果将陆续公布,期盼其在高脂血症治疗方面能够有重大进展。
[1]Boekholdt SM,Arsenault BJ,Mora S,et al.Very low levels of atherogenic lipoproteins and the risk for cardiovascular events:ameta-analysis of statin trials[J].JAm Coll Cardiol,2014,64(5):485-494.
[2]Mansi I.Statin adverse events in primary prevention:between randomized trials and observational studies[J].Am J Med Sci,2015.[Epub ahead of print]
[3]van de Woestijne AP,van der Graaf Y,Westerink J,et al. Effect of statin therapy on incident type 2 diabetesmellitus in patientswith clinically manifest vascular disease[J]. Am JCardiol,2015,115(4):441-446.
[4]Ruscica M,Macchi C,Morlotti B,et al.Statin therapy and related risk of new-onset type 2 diabetesmellitus[J].Eur J Intern Med,2014,25(5):401-406.
[5]Ferdinand KC,Nasser SA.PCSK9 Inhibition:discovery,currentevidence,and potentialeffectson LDL-Cand Lp(a)[J]. Cardiovasc Drugs Ther,2015.[Epub ahead of print]
[6]Koren MJ,Giugliano RP,Raal FJ,et al.OSLER Investigators.Efficacy and safety of longer-termadministration of evolocumab (AMG145)in patients with hypercholesterolemia:52-week results from the open-label study of long-term evaluation against LDL-C (OSLER)randomized trial[J].Circulation,2014,129(2):234-243.
[7]Giugliano RP,Sabatine MS.Are PCSK9 Inhibitors the Next Breakthrough in the Cardiovascular Field?[J].J Am Coll Cardiol,2015,65(24):2638-2651.
[8]Sniderman AD,Williams K,Contois JH,et al.The secretory proprotein convertase neural apoptosisregulated convertase 1 (NARC-1):liver regeneration and neuronal differentiation[J].Proc Natl Acad Sci USA,2003,100(3):928-933.
[9]Abifadel M,Varret M,Rabes JP,et al.Mutations in PCSK9 cause autosomal dominanthypercholesterolemia[J].Nat Genet,2003,34(2):154-156.
[10]Timms KM,Wagner S,Samuels ME,et al.A mutation in PCSK9 causing autosomal-dominanthypercholesterolemia in a Utah pedigree[J].Hum Genet,2004,114(4):349-353.
[11]Leren TP.Mutations in the PCSK9 gene in Norwegian subjects with autosomal dominant hypercholesterolemia[J]. Clin Genet,2004,65(5):419-422.
[12]Cohen JC,Boerwinkle E,Mosley TH Jr,et al.Sequence variations in PCSK9,low LDL,and protection against coronary heart disease[J].N Engl JMed,2006,354(12): 1264-1272.
[13]Roth EM,McKenney JM,Hanotin C,et al.Stein EA.A-torvastatin with or without an antibody to PCSK9 in primary hypercholesterolemia[J].NEngl JMed,2012,367(20): 1891-1900.
[14]Maxwell KN,Breslow JL.Proprotein convertase subtilisin kexin 9:the third locus implicated in autosomal dominant hypercholesterolemia[J].Curr Opin Lipidol,2005,16 (2):167-172.
[15]Urban D,Pöss J,Böhm M,et al.Targeting the proprotein convertase subtilisin/kexin type 9 for the treatment of dyslipidemia andatherosclerosis[J].JAm CollCardiol,2013,62(16):1401-1408.
[16]Di Taranto MD,D′Agostino MN,Fortunato G.Functional characterization ofmutant genes associated with autosomal dominant familial hypercholesterolemia:integration and evolution of genetic diagnosis[J].Nutr Metab Cardiovasc Dis,2015.[Epub ahead of print]
[17]Kereiakes DJ,Robinson JG,Cannon CP,etal.Efficacy and safety of the proprotein convertase subtilisin/kexin type 9 inhibitor alirocumab among high cardiovascular risk patients on maximally tolerated statin therapy:The ODYSSEY COMBOⅠstudy[J].Am Heart J,2015,169(6): 906-915.
[18]Robinson JG,Farnier M,Krempf M,et al.Efficacy and safety of alirocumab in reducing lipids and cardiovascular events.ODYSSEY LONG TERM Investigators[J].N Engl JMed,2015,372(16):1489-1499.
[19]Stein EA,Mellis S,Yancopoulos GD,et al.Effect of a monoclonal antibody to PCSK9 on LDL cholesterol[J].N Engl JMed,2012,366(12):1108-1118.
[20]Fitzgerald K,Frank-Kamenetsky M,Shulga-Morskaya S,et al.Effect of an RNA interference drug on the synthesis of proprotein convertase subtilisin/kexin type 9(PCSK9) and the concentration of serum LDL cholesterol in healthy volunteers:a randomised,single-blind,placebocontrolled,phase 1 trial[J].Lancet,2014,383(9911):60-68.
[21]Banaszewska A,Piechota M,Plewa R.Proprotein convertase subtilisin/kexin type 9:a new target molecule for gene therapy[J].CellMol Biol Lett,2012,17(2):228-239.
[22]Visser ME,Witztum JL,Stroes ES,et al.Antisense oligonucleotides for the treatment of dyslipidaemia[J].Eur Heart J,2012,33(12):1451-1458.
[23]Blom DJ,Hala T,Bolognese M,et al.A 52-week placebo-controlled trial of evolocumab in hyperlipidemia[J].N Engl JMed,2014,370(19):1809-1819.
[24]Shimada YJ,Cannon CP.PCSK9 (Proprotein convertase subtilisin/kexin type 9)inhibitors:past,present,and the future[J].Eur Heart J,2015.[Epub ahead of print]
[25]Bays H,Gaudet D,Weiss R,et al.Alirocumab as add-on to atorvastatin versus other lipid treatment strategies: ODYSSEY OPTIONSⅠRandomized Trial[J].JClin Endocrinol Metab,2015.[Epub ahead of print]
[26]Langslet G,Emery M,Wasserman SM.Evolocumab(AMG 145)for primary hypercholesterolemia[J].Expert Rev Cardiovasc Ther,2015,13(5):477-488.
Research status and progress of cholesterol-lowering drugs(target PCSK 9 protein inhibitors)
LIU Feng ZHOU Qiao-xia WANG Bing-yin▲
Heart Centre,Suzhou Kowloon Hospital affiliated to Shanghai Jiaotong University School of Medicine,Suzhou 215021, China
The low density lipoprotein cholesterol plays an important role in occurrence and development of atherosclerotic cardiovascular diseases (ASCVD).Statins preparation is the foundation that prevention and treatment of ASCVD,however,for some patients,the lipid-lowering effect is not ideal when using the adequate statins but have a higher risk of cardiovascular disease,with familial hypercholesterolemia or can′t tolerate the side effects of enough statin treatment need other new effective and safe lipid-lowering drug.PCSK9 inhibitor can significantly elevate the surface of LDL-C receptor of liver cells and bond more LDL-C to decrease the level of LDL-C.Multiplemonoclonal antibodie of target PCSK9 protein inhibitors have been published in succession.A lot of basic and clinical research have been confirmed that PCSK9 inhibitors can significantly reduce blood LDL-C and have good safety and tolerability.Preliminary research data show that PCSK9 inhibitors can reduce the cardiovascular events,the results are encouraging.
Cholesterol;Familial hypercholesterolemia;Cholesterol-lowering drugs;Target PCSK9 protein inhibitors; Cardiovascular disease
R972+.6
A
1674-4721(2015)09(c)-0022-05
2015-07-20 本文编辑:祁海文)
刘峰(1963-),硕士,主任医师,博士研究生导师,心脏中心主任,主要从事心血管病临床工作,研究方向:冠心病与心律失常的诊治;周巧霞(1977-),博士,副主任药师,研究方向:心血管病药理与防治
▲通讯作者:王炳银(1949-),医学博士/博士后,主任医师,心脏中心副主任,主要从事心血管病临床与基础研究工作,研究方向:冠心病与心律失常的诊治、心功能
