离子液体修饰碳糊电极测定海红果中的槲皮素
2014-12-23李梅杜芳艳温俊峰吴欢欢
李梅,杜芳艳,温俊峰,吴欢欢
(榆林学院 化学与化学工程学院,陕西 榆林 719000)
槲皮素是一种多羟基黄酮类化合物,具有多种生物学活性及很高的药用价值[1],广泛存在于植物的花、叶、果实中,是人类饮食中最主要的生物类黄酮。已知有100 多种中草药中含有槲皮素[2]。槲皮素对多种肿瘤具有抑制作用、具有较好的祛痰、止咳、平喘、抗菌、抗病毒、抗炎、抗过敏、抗心律失常、抗血小板凝聚、抗氧化及清除自由基作用,此外还有降糖降压、降血脂、免疫调节及对心血管系统的保护作用等,近年来倍受人们的关注[3-5]。
槲皮素含量的测定方法有光度法、光谱法、高效液相色谱法、高效毛细管电泳法、电化学法等[6-13]。光度法测定槲皮素含量时,会受到其它黄酮类化合物的干扰,影响测定结果;高效液相色谱法和毛细管电泳法操作复杂,仪器和试剂比较贵。电化学检测具有灵敏、快速、设备成本低等优点而得到广泛研究和应用。Xiao Ping 等[14]采用碳纳米管修饰石墨电极检测槲皮素,灵敏度较高,但是芦丁对检测产生严重干扰,电极的选择性有待提高。离子液体是近年来一种新型的绿色有机溶剂,具有高导电率和粘度相对较大的特点,从而在医药、食品、化工及化学等多种领域有着广泛的应用。
海红果为蔷薇科植物海红子(Malus micromalus Makino)的果实,学名西府海棠[15],海红果中富含黄酮类化合物,海红果中槲皮素测定尚未见报道。因此,我们制备了离子液体修饰碳糊电极,研究槲皮素在该修饰电极上的电化学行为,建立了一种新的测定槲皮素的电化学方法。该法具有操作简单、分析快速、灵敏度高和选择性好等优点。用于海红果中槲皮素含量的测定,结果令人满意。
1 实验部分
1.1 材料与仪器
海红果,陕西省府谷县产;1-甲基-3-丁基咪唑六氟磷酸盐([bmim]PF6),分析纯;槲皮素对照品,生化试剂;石墨粉,光谱纯;液体石蜡;0.2 mol/L 的BR 缓冲溶液(pH 3.2 ±0.1)等均为分析纯;水为二次蒸馏水。
CHI660D 电化学工作站,三电极系统:工作电极为离子液体修饰碳糊电极(IL/CPE,自制),参比电极为饱和甘汞电极(SCE),对电极为铂丝电极;红外线烘烤箱;HH-1 数显恒温水浴锅;SHZ-D(Ⅲ)型循环水真空泵;ESJ60-4 电子天平;pHS-25 酸度计。
1.2 离子液体修饰碳糊电极的制备
将1.0 g 石墨粉与0.5 mL 混合液([bmim]PF6∶液体石蜡=1 ∶0.5)混合均匀,并在红外线烘烤箱内烘烤0.5 h(温度约为80 ℃)。将糊状物填充入内径3 mm 的PVC 管中。另一端与铜丝相连,紧密压实。制备好的电极在金相砂纸上进行粗打磨,然后在称量纸上打磨光滑,即得修饰电极(IL/CPE)。每次测量前都要对电极进行更新。将碳糊挤出2 ~3 mm 后,在纸上抛光并洗净,将电极置于0.2 mol/L的B-R 缓冲溶液中于0.0 ~0.6 V 电位以100 mV/s的扫速循环伏安扫描若干圈,使修饰电极保持活性。
1.3 实验方法
准确称取1.69 mg 槲皮素,溶解在热的无水乙醇中,定容至100 mL,得浓度0.5 mmol/L 的槲皮素乙醇标准储备液,保存备用。用时稀释至所需浓度的工作溶液。
移取一定量的0. 5 mmol/L 槲皮素储备液于25 mL 容量瓶中,加入0. 2 mol/L B-R 缓冲溶液10.00 mL,用二次蒸馏水定容,静置10 min。采用三电极系统在0 ~0.6 V 电位,以100 mV/s 扫速进行循环伏安扫描。同法测定海红果中槲皮素的含量。
2 结果与讨论
2.1 槲皮素在IL/CPE 上的电化学行为
图1 是0.2 mmol/L 槲皮素在B-R 缓冲溶液中于IL/CPE 和CPE 上产生的电化学响应。
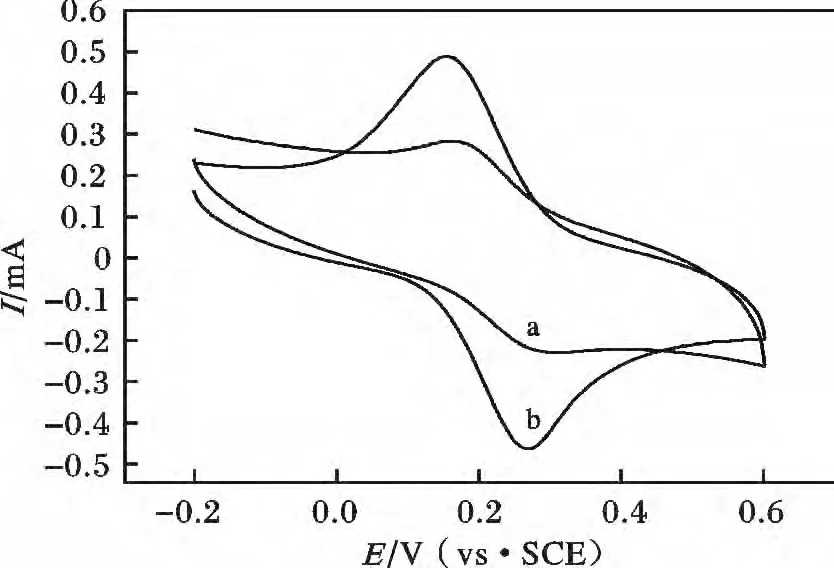
图1 槲皮素在CPE(a)和IL/CPE(b)上的循环伏安图Fig.1 Cyclic voltammograms of quercetin at a CPE (a)and an IL /CPE (b)
由图1 可知,在CPE 上,槲皮素产生了一对氧化还原峰(图1a),氧化峰电位是0.308 V,还原峰电位是0.164 V,峰电位差(ΔEp)为0.144 V;在槲皮素IL/CPE 上也产生了一对氧化还原峰(图1b),但氧化峰电位负移到0. 299 V,还原峰电位负移至0.177 V,ΔEp 减小为0.122 V,电流响应显著增大,是其在CPE 上的4.5 倍,表明IL/CPE 既降低了槲皮素氧化还原反应的过电位,又显著提高了其电流响应,说明IL/CPE 对槲皮素的氧化还原反应有电催化作用。这是由于离子液体具有较好的导电性,把它作为修饰剂加入到碳糊电极中,可以减小由不导电的有机粘合剂液体石蜡产生的电阻,改善电极的导电性,加快电极上的电子交换速度。
2.2 支持电解质
分别考察了电解质B-R、HAc-NaAc、Na2HPO4-NaH2PO4(PBS)、NH3· H2O-NH4Cl 溶液中对0.1 mmol/L槲皮素电流响应的影响。结果显示,在0.2 mol/L 上述缓冲溶液中,槲皮素有一灵敏的氧化还原反应峰出现,其中在B-R 缓冲溶液中峰形尖锐,对称性好,峰电流Ip大,所以选择0.2 mol/L 的B-R 缓冲溶液中作为支持电解质。
2.3 底液的酸度
在0.2 mol/L pH 为2. 0 ~9. 0 B-R 缓冲溶液中,对0.1 mmol/L 的槲皮素进行循环伏安扫描。结果显示,当pH <3.0 时,峰电流随着pH 值的增大而增大;当pH >3.8 时,峰电流随着pH 值的增大而减小;当pH 超过8.5 时,槲皮素的氧化-还原反应峰逐渐消失。可以推断,当溶液碱性增大时,会减弱槲皮素在电极表面的吸附,致使氧化-还原反应峰消失。当pH 3.2 时,峰电流达到最大。考虑到峰形及峰电流的影响,选择pH 为3.2 ±0.1 的B-R 缓冲溶液作为支持电解质。
2.4 扫速的影响
在0.2 mol/L B-R 缓冲溶液中,用循环伏安法研究了扫速对0.2 mmol/L 槲皮素电化学行为的影响,结果见图2。
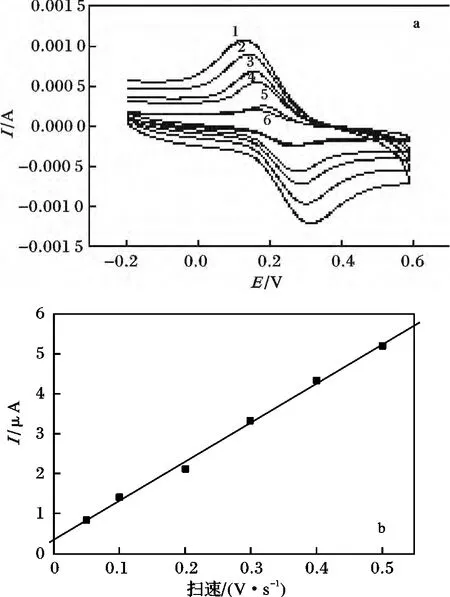
图2 槲皮素在IL/CPE 上不同扫速时的循环伏安曲线及IP-v 关系图Fig.2 Cycle voltammogramms of quercetin at IL/CPE with various scan
由图2 可知,槲皮素的峰电流随着扫速的增加而增大,且与扫速呈良好的线性关系,Ip(μA)=-10.075v +0.280,R2=0.998 9,表明槲皮素在IL/CPE 上的电极反应受吸附控制。
2.5 电极的重现性与测定精密度
用同一根离子液体修饰碳糊电极对浓度为5 ×10-5mol/L 的槲皮素平行测定10 次,相对标准偏差(RSD)为1.22%,说明该电极的稳定性较好。用6支不同批次制备的IL/CPE 进行测定,RSD 为1.55%。表明该电极重现性好。
2.6 标准曲线
在优化的实验条件下,槲皮素的氧化峰电流与其浓度在0.1 ~50 μmol/L 范围内呈良好的线性关系,线性回归方程为:Ip(μA)=3.943 3 +0.211 9c(μmol/L),线性相关系数为0.999 4,检出限为3.0×10-8mol/L (S/N=3)。
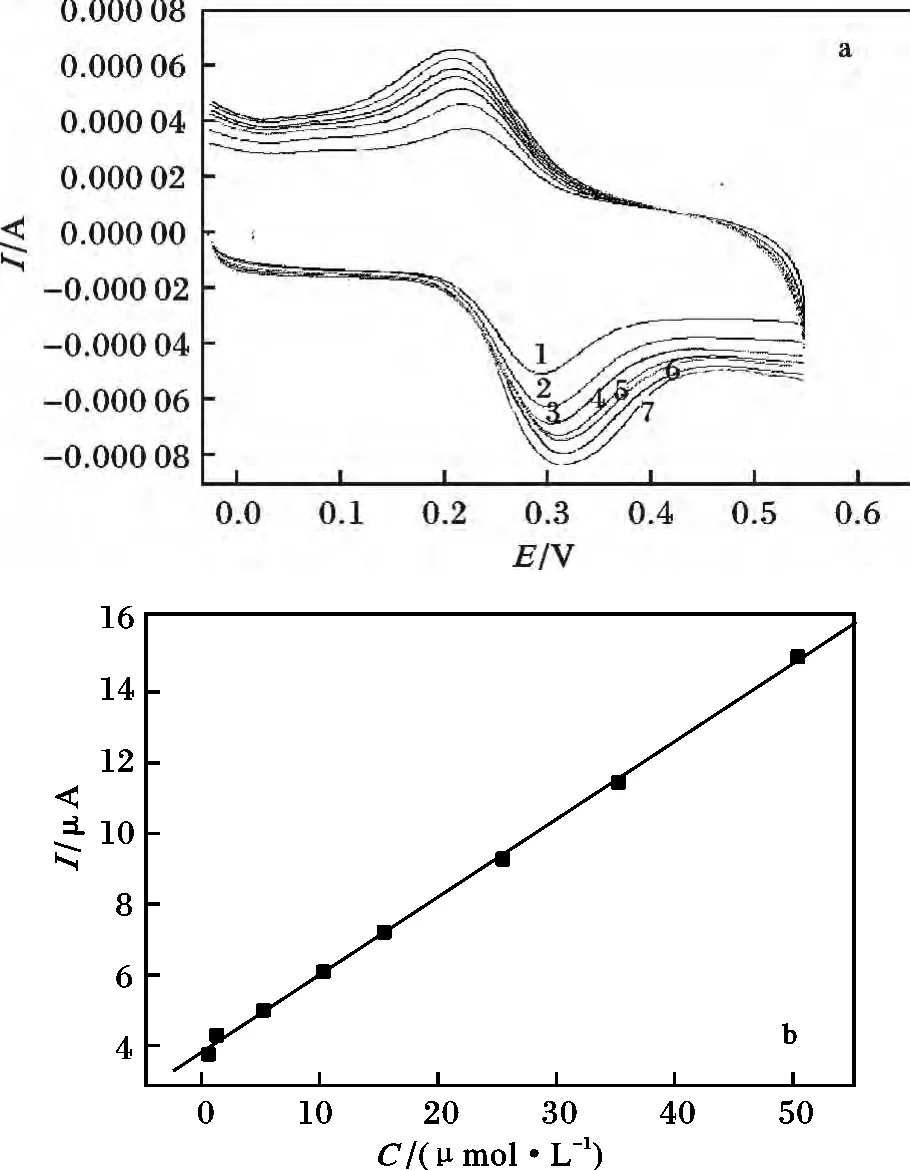
图3 不同浓度槲皮素在IL/CPE 上的CV 曲线及IP-c 关系图Fig.3 CV curves of different concentration of quercetin at IL/CPE
2.7 海红果中槲皮素的测定
取海红果粉10.0 g,加入0.06%果胶酶,按照料液比为1 ∶9 加水,于50 ℃恒温水浴浸提4 ~5 h,过滤,得海红果汁,定容至500 mL。海红果中槲皮素含量,6 次测定的平均值为47.77 mg/g,相对标准偏差为1.96%。
取已知含量的样品溶液,加入一定量的槲皮素标准溶液,进行加标回收实验,回收率为95.8% ~104.8%。
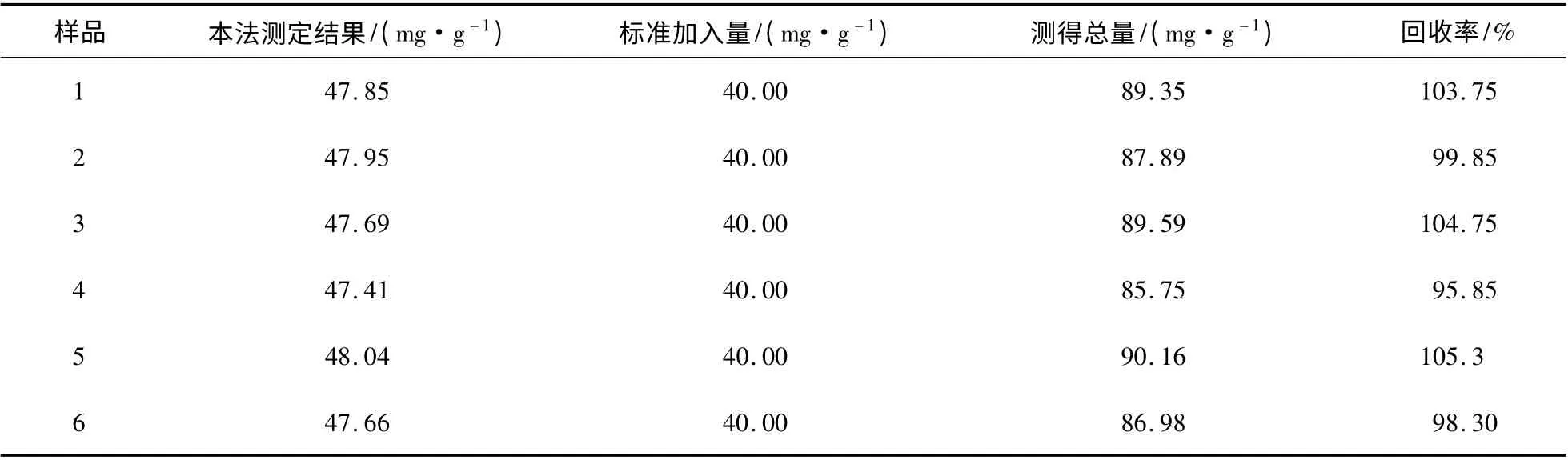
表1 海红果中槲皮素的加标回收率(n=6)Table 1 Determination results of quercetin in Malus micromalus Makino and recoveries (n=6)
3 结论
(1)IL/CPE 修饰电极对槲皮素在该电极上的氧化、还原有电催化作用,在循环伏安曲线上,槲皮素的峰电流与其浓度在0.1 ~50 μmol/L 呈良好的线性关系,其线性方程为ip(μA)=3.941 3 +0.211 9 c(μmol/L),线性相关系数为0.999 4,检出限为3.0 ×10-8mol/L。
(2)用离子液体修饰碳糊电极循环伏安法测得海红果中的槲皮素的含量为47.77 mg/g。
[1] 孙涓,余世春.槲皮素的研究进展[J].现代中药研究与实践,2011,25(3):85-89.
[2] 钱景时,张彬锋,王玮,等. 冬青叶兔唇花化学成分研究[J].中草药,2012,43(5):869-872.
[3] 裴天仙,徐长庆,李滨,等. 槲皮素对阿霉素致小鼠心肌损伤的保护作用及其机制[J]. 药学学报,2007,42(10):1029-1033.
[4] Zhang Huaxin,Chen Kongsai. Biophysical studies on the site selective binding of a synthesized selenium quercetin complex on a protein[J]. Solution Chem,2012,41(6):915-925.
[5] 吴春,余迎春,王丽萍.槲皮素微乳对亚硝化反应的抑制活性研究[J]. 天然产物研究与开发,2008,20:12-15.
[6] 尚永辉,李华,孙家娟,等.偏最小二乘法-分光光度法同时测定芦丁与槲皮素的方法研究[J]. 分析测试学报,2011,30(4):457-460.
[7] Pejic N,Kuntic V,Vujic Z,et al.Direct spectrophotometric determination of quercetin in the presense of ascorbic acid[J].Il Farmaco,2004,59(1):21-24.
[8] Lei R,Xu X,Yu F,et al.A method to determine quercetin by enhanced luminal electrogenerated chemiluminescence(ECL)and quercetin antoxidation[J].Talanta,2008,75(4):1068-1074.
[9] Zu Yuangang,Li Chunying,Fu Yujie,et al. Simultaneous determination of catechin,rutin,quercetin kaempferol and isorhamnetin in the extract of sea buckthorn(hippophae rhamnoides L.)leaves by RP-HPLC with DAD[J]. J Pharm Biomed Anal,2006,41(3):714-719.
[10]杨玲娟,焦成瑾,葛勐,等. 高效液相色谱法测定旋复花中槲皮素的含量[J]. 化学分析计量,2010,19(1):65-66.
[11]刘菁,李志,郑芳,等. 高效毛细管电泳法测定绞股蓝中芦丁和槲皮素的含量[J]. 中南医药,2009,7(12):920-923.
[12]徐帅,卫茂超. 以β-环糊精修饰碳糊电极测定槲皮素[J].济南大学学报:自然科学版,2012,2(5):23-26.
[13]陈小印,王宗花,张菲菲,等. 槲皮素在聚对氨基苯磺酸修饰电极上的电化学研究[J]. 青岛大学学报,2010,25(1):54-59.
[14]Xiao Ping,Zhao Faqiong,Zeng Baizhao.Voltammetric determination of quercetin at a multi-walled carbon nanotubes paste electrode[J]. Microchem J,2007,85(2):244-249.
[15]王菱.陕晋蒙三角区特有果树——海红子[J].自然资源,1990,3(1):48.
