超微细碳酸锰合成影响因素控制
2014-10-17胡修权李桂玲曹海华贺爱平
胡修权,孙 猛,李桂玲,曹海华,贺爱平,周 毅
(中南冶金地质研究所,湖北宜昌 443003)
高纯碳酸锰粉体是制造电子信息器材软磁铁氧体重要的功能基础材料之一,是合成氧化锰和制造其他锰盐的重要前驱体。常用于医药、冶金、化工等行业,用作电焊条辅料、脱硫催化剂、饲料添加剂;同时还被广泛用作瓷釉、涂料和清漆的颜料。碳酸锰粉体质量与其粒度密切相关,为了控制产品粒径,袁明亮等[1]通过调整结晶温度和溶液过饱和度,可将碳酸锰平均粒度控制在5 μm以下。为了制备超微细碳酸锰粉体,吕春玲等[2]通过超声处理和降低反应温度,获得了400~500 nm的超细立方晶形产品。通过调整溶液pH、离子浓度、改变反应器结构及加料方式等,可以改变碳酸锰晶体形貌、粒径及表观密度等[3-4]。彭清静等[5]以尿素和硫酸锰为原料,于115℃高温水热条件下均匀沉淀制备出高纯超细碳酸锰。蒋春芳等[6]以三聚氰胺和氯化锰为原料也在水热条件下合成了高质量的碳酸锰。采用有机电解质作分散剂对碳酸锰粉体的晶形及粒径进行控制是比较有效的方法,六偏磷酸钠(SHMP)和十二烷基硫酸钠(SDS)的应用,获得了 0.5~3.1 μm 的超微细碳酸锰粉体[7-8]。 马照军等[9]采用十六烷基三甲基溴化铵(CTAB)/醇/水体系合成了 1 μm 高活性的表面活性剂与超微细碳酸锰的复合体。笔者采用氨化聚丙烯酸(PAA)-乙醇(Et)-H2O 体系,并结合其他条件的控制,制备出高质量超微细的碳酸锰粉体,其粒径 D90达 1.8 μm。
1 实验部分
1.1 主要仪器
K100 L碳化罐,ZX-3A真空泵,φ30抽滤桶,XSYS-81红外干燥箱,JJ-1变速搅拌机,6511衬塑球磨机。
1.2 主要原材料及试剂
高纯硫酸锰溶液:Mn2+质量浓度为70 g/L,经过一系列提纯处理;碳酸氢铵溶液:150 g/L,农业级,含N质量分数≥17.1%,原料中检测不出碱金属、钙、镁及重金属元素;氨化PAA:质量分数约为45%;乙醇:体积分数≥95%,AR级。
1.3 实验步骤
在碳化釜中加入一定量经纯化后的MnSO4溶液,搅拌作用下,按体积比为1∶1加入Et,再加入一定量经氨化的PAA。搅拌均匀后,在快速搅拌下加入化学计量的NH4HCO3溶液进行碳化。随着反应进程的不断加快,复分解产生的CO2气体逐渐增多,应密切关注,避免跑冒漏现象发生。加料完毕,继续搅拌30 min,待气泡冒尽,陈化24 h。
将上层清液放入塑料槽中,用于回收副产硫铵。将沉淀转入抽滤桶中抽滤,并以去离子水洗涤至滤液无反应(以BaCl2溶液检验)。将滤饼放入远红外干燥箱中于105℃烘干。冷却后,以聚氨酯衬里的高能球磨机打散后包装。
2 结果与讨论
2.1 碳化体系各介质对MnCO3粒径的影响
2.1.1 Et-H2O溶液的影响
粉体合成一般遵循化学晶核形成动力学理论,粒子的晶核形成和增长与溶液的过饱和度有关。要获得小颗粒的沉淀物,一方面晶核形成速率要快,另一方面又要抑制晶粒的增长。随着过饱和度的增加,成核速率和生长速率均增加,但粒子半径减小;当进一步提高过饱和度时,成核速率增长占优势。因此,过饱和度的提高有利于晶粒向微细化方向发展。
乙醇作为具有低介电常数的极性分子,可以与水以任意比例进行混溶,可大大降低反应溶液体系的介电常数,提高体系过饱和度。同时,乙醇的加入还可以防止非架桥羟基同颗粒表面以氢键相连,起到一定的空间位阻效应,阻止颗粒相互靠近,减轻团聚,有利于分散独立细小颗粒的形成。而采用一般水溶液合成,颗粒较大且产生明显团聚,沉降迅速。图1为在不同介质中合成碳酸锰粉体的偏光显微照片。乙醇的加入量选择与硫酸锰溶液体积比为1∶1。
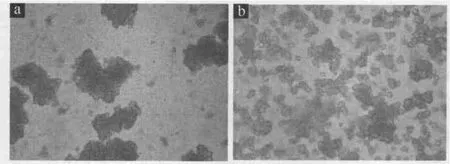
图1 两种介质中合成粉体的表观显微照片
2.1.2 氨化PAA的作用
在通常的水相介质中,碳化剂加入的瞬间,溶液中Mn2+与HCO3-形成的MnCO3一次粒子尺寸很小,比表面积很大,总表面能高。根据“物质构成的体系总是稳定在能量最低状态”的能量最低原理,一次粒子很快发生团聚形成二次粒子,随着碳化进程不断深入,反应时间不断增加,这种二次粒子越来越多,得到的沉淀粒子尺寸越来越大。为了阻止一次粒子团聚,尽量减少二次粒子形成,有效的方法是在反应体系中添加一定量的表面活性剂作为分散剂。
针对物质的带电性质,将表面活性剂分为阴离子型、阳离子型、两性和非离子型等几种类型。在低浓度下,表面活性剂分子吸附在粉体的表面和界面上,从而大大降低粉体颗粒的界面能,使粒子的总表面能极小化,同时产生强的空间位阻效应,阻止粒子间团聚。根据体系和粒子的表面性质来选择使用不同类型的表面活性剂。
根据MnCO3粒子表面电性,选择加入经氨化的有机聚电解质PAA,对MnCO3粒子具有显著的分散效果,如图2所示。
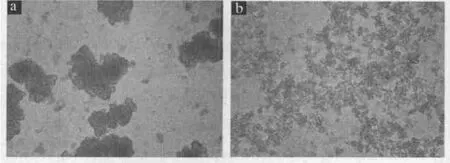
图2 两种介质中合成MnCO3粒子表观现象对比
结果表明,氨化后的PAA中绝大多数羧基都以羧酸根负离子(—COO-)形式存在。对MnCO3而言,粒子表面存在大量的水羧基,这些水羧基可以部分电离而使粒子表面带有负电荷。当加入氨化了的PAA时,一方面由于—COO-可以与MnCO3粒子表面的锰离子结合,另一方面,由于通过氢键的作用而使分散剂与MnCO3粒子表面的水羧基或电离产生的氧负离子结合,从而大骨架羧酸根负离子牢固地吸附在粒子表面。因此,当加入PAA后,MnCO3粒子表面所带负电荷大大增加,即增加了粒子的Zeta电位(动电位),从而使得带相同负电荷的超细颗粒间保持较大斥力而彼此分散开来。
与此同时,由于PAA分子量很大,具有较强的空间位阻效应,能有效地阻止MnCO3粒子团聚。因此,在反应体系中加入合适量的氨化PAA对制备超微细MnCO3是有利的。
2.1.3 碳化体系介质的确定
在以碳酸氢铵为碳化剂的反应体系中,加入一定量乙醇能有效降低溶液介电常数,提高溶液过饱和度,能使反应生成的MnCO3粒子迅速成核,形成大量细小微粒;同时,往溶液中加入经氨化后的PAA,PAA被生成的MnCO3粒子表面所吸附,由于PAA强大的双电层作用及空间位阻效应,使得MnCO3粒子彼此保持一定间距,阻止其硬团聚。实验结果表明,合成产品在体系中处于良好的悬浮稳定分散状态,放置较长时间也没有明显的沉降发生。因此,确定碳化合成体系介质为Et-PAA-H2O。
2.2 碳化体系介质影响因素
2.2.1 乙醇用量
乙醇在反应体系中主要起降低溶液的介电常数,提高溶液的过饱和度的作用。加入量太少,效果不明显;反之,由于乙醇是易挥发性有机试剂,如果加入量太多,不但会增加生产成本,同时还会影响生产环境,带来潜在的不安全因素(为降低成本,要考虑乙醇的回收)。选择乙醇与硫酸锰溶液体积比为1∶1能达到较好效果。
2.2.2 PAA用量
氨化后的PAA作为一种有效的阴离子表面活性剂,其加入量太少,所起吸附作用及空间位阻效应有限;如果加入量太大,不但起不到分散作用,相反,会起反作用,会使生成的MnCO3粒子裹抱成团,形成大量软团聚的“大粒子”,且一旦形成不容易分散开,不利于后续处理(如干燥工序),对产品质量产生不良影响。结果表明,当控制PAA用量为MnCO3质量的0.5%~0.9%时具有明显效果,且在此范围内无明显差异。
2.3 碳化体系温度及反应时间对产品粒径及晶形的影响
2.3.1 碳化体系温度影响
在碳化体系中,由于表面活性剂的加入,改变了MnCO3粉体的粒径分布和团聚状态。晶核生成和成长发生在表面活性剂胶团中,随着温度的升高,表面活性剂的临界胶团变小,反应速度加快,粉体粒径变小。因此,升高温度有利于超微细MnCO3粉体的快速生成。但是,碳化剂对温度很敏感,随着温度的升高,碳化剂分解速率加快,会增加碳化剂用量,影响碳化效率,增加碳化成本。所以,应选择低温碳化。
由于MnCO3的溶度积常数很小,25℃时Ksp为1.8×10-11,其在常温下的溶解度非常小,在低温时,Mn2+的碳化速度很快,两种溶液接触的瞬间便能完成碳化过程。因此,碳化体系温度应控制在35℃以下。
2.3.2 碳化反应时间的影响
碳化反应是在Mn2+与碳化剂接触的瞬间完成。在Et-H2O体系中,陈化有利于提高无机粉体的BET值,增加其活性;同时,陈化还有利于碳化剂分解产生的CO2气体的排出和微量杂质元素的析出。但是,如果陈化时间过长,晶体逐渐长大,有的变成四方晶形,如图3所示。
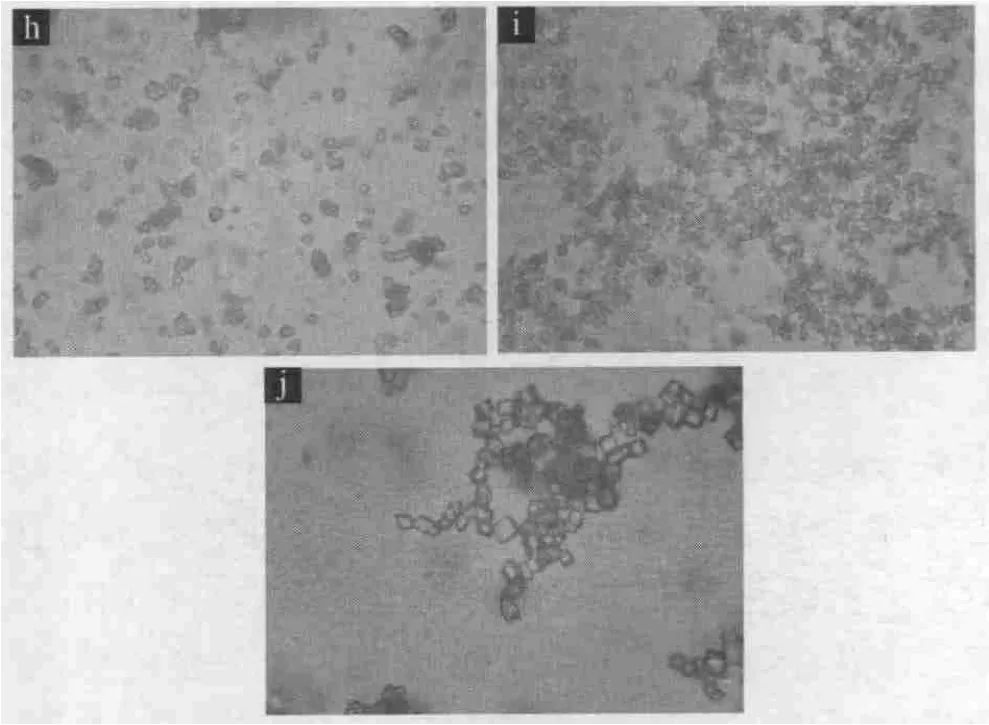
图3 陈化静置不同时间产品显微特征
由图3可以明显看出,h基本都是独立分散的不规则状或球形颗粒;i有部分明显长大并开始团聚,少数晶体转变为四方菱形;j晶体继续生长,绝大部分转变为四方菱形。为了获得高质量的超微细MnCO3粉体,确定碳化反应完成后静置陈化24 h。
2.4 碳化体系酸度控制
当体系pH太低时,碳化剂中的作用基团CO32-首先与体系中的大量游离H+结合转变为CO2气体从碳化体系中逸出,起不到碳化作用。此外,若pH太低,PAA中的羧酸根负离子(—COO-)会与H+结合生成电离度差的羧酸(—COOH),起不到分散作用。反之,当体系pH过高时,会提高反应体系中羟基(—OH)浓度,使溶液中的部分游离Mn2+与—OH结合形成胶状 Mn(OH)2和 Mn2(OH)2CO3,这些胶状物以聚合胶团形式存在于体系中,对体系中残存的其他微量杂质元素吸附力很强,影响产品纯度和粒子尺寸。
结果显示,最合适酸度范围为pH为6.0~6.5,此时锰的碳化效果最佳,回收率最高。在本碳化过程中,经提纯后的锰溶液与碳化剂混合反应时的体系酸度基本上维持在此范围,不需要另外加酸碱剂进行调节。
2.5 应用
根据所确定的碳化条件,按照实验步骤进行操作,获得分散度、均匀性良好的超微细碳酸锰粉体,经激光粒度分析仪进行检测,中位粒径D50为1.28 μm,D90为 1.8 μm,最大粒径为 2.0 μm 。
3 结论
1)乙醇的加入可大大降低反应体系的介电常数,有效提高体系过饱和度,减少粒子团聚,其应用对获得独立分散的超微细MnCO3粉体十分有用。2)经氨化后的PAA分子能通过其表面大量的羧酸根负离子(—COO-)吸附于MnCO3粉体表面,起到强大的空间位阻作用,有效阻止MnCO3粒子聚合。PAA在反应体系中的浓度至关重要,浓度太高或太低都不利于微细MnCO3粒子生成,只有当体系中PAA占体系中 MnCO3质量的 0.5%~0.9%时能产生最佳效果。3)碳化温度和碳化时间也是要加以控制的因素。碳化温度过高,会加快碳化剂自身分解速度;碳化搅拌太久会增加粒子的碰撞机会,陈化时间过长,会使晶体生长变大。控制低温(室温)碳化,搅拌时间30 min,陈化24 h以内。4)在本合成工艺中,碳化体系 pH 为 6.0~6.5,靠体系自我调节,不需使用外来酸度调节剂。
[1]袁明亮,邱冠周.高纯微晶碳酸锰制备中的粒度和质量控制[J].中南工业大学学报:自然科学版,2001(5):473-476.
[2]吕春玲,张景林.亚微米碳酸锰的制备及形貌控制[J].硅酸盐学报,2007(3):377-380.
[3]粟海锋,屈雄,文衍宣,等.球形碳酸锰微晶制备过程中的形貌控制[J].过程工程学报,2008(2):280-284.
[4]胡修权,韩军,高山.高视密度碳酸锰的制备工艺[J].化工技术与开发,2004(6):50-51.
[5]彭清静,傅伟昌,邹晓勇.用均匀沉淀法制备高纯碳酸锰[J].吉首大学学报:自然科学版,2001(3):48-50.
[6]蒋春芳,黎燕,梁福沛,等.水热条件下由配体分解制备碳酸锰晶体[J].广西师范大学学报:自然科学版,2007(1):58-61.
[7]周晚珠,叶红齐,韩凯,等.球形 MnCO3粉的制备及其粒径控制[J].稀有金属与硬质合金,2011(4):13-16.
[8]粟海锋,黄飞雪,文衍宣,等.液相沉淀法制备单分散亚微米级球形碳酸锰[J].无机盐工业,2009,41(8):18-20.
[9]马照军,金达莱,王勇,等.CTAB/醇/水体系制备碳酸锰的性质研究[J].浙江理工大学学报,2006(4):405-408.
