吡蚜酮在大鼠体内的毒代动力学研究
2014-10-15林立红孙常松孟庆贺李晓磊段明郁
于 巍,林立红,王 刚,孙常松,孟庆贺,李晓磊,段明郁
(1.沈阳化工研究院安全评价中心,辽宁 沈阳110021;2.沈阳科创化学品有限公司,辽宁 沈阳110144)
吡蚜酮化学名4,5-二氢-6-甲基-4-(3-吡啶亚甲基氨基)-1,2,4-3(2 H)-酮,属非杀伤性新型杀虫剂,具有高效、低毒、高选择性、对环境生态安全等特点,主要通过食物链途径进入人体[1]。目前已报道的吡蚜酮检测方法包括高效液相色谱串联质谱法[2-3]、气相色谱-质谱法等[4-5],多用来检测烟草、烟碱、水果及蔬菜中的残留量[6-7],但用于检测动物体内血浆药物浓度尚未见报道。作者在此采用液质联用仪检测不同染毒剂量下SD大鼠血浆中吡蚜酮的浓度,并研究其在大鼠体内的毒代动力学过程,拟为进一步的深入研究提供依据。
1 实验
1.1 试验动物、试剂与仪器
SPF级SD雄性大鼠(质量合格证号:211002300000434)11只,体重250~300g,辽宁长生生物技术有限公司。实验前禁食18h。
吡蚜酮原药(纯度98.0%),沈阳科创化学品有限公司;吡蚜酮标准品(纯度99.5%),沈阳化工研究院有限公司农标室;乙腈(色谱纯),Fisher公司;50%甲酸(色谱纯),Fluka公司;CO2(麻醉用);玉米油(金龙鱼牌非转基因油)。
LC-20A/AB API3200 型 液 质 联 用 仪 (LC-MS/MS),配备 Analyst1.5.1软件,岛津公司;T18型匀浆机,IKA公司;Sartorius BP211D型电子天平(十万分之一);3K15型高速离心机,Sigma公司;移液器,Eppendorf公司。
DAS Ver2.0软件,上海中医药大学药物临床研究中心编制。
1.2 方法
1.2.1 测试条件
色谱柱为 Phenomenex Luna C18(50mm×4.6 mm,5μm);流动相为水-乙腈(含0.1%甲酸),梯度洗脱程序:水-乙腈(95∶5,体积比,下同),0.5min;水-乙腈(5∶95),2.0min;水-乙腈(95∶5),3.1min;水-乙腈(95∶5),5.0min;流速0.6mL·min-1;柱温为室温;进样量10μL;保留时间2.3min。
离子源为ESI源;离子源温度500℃;喷雾电压5 000V;CAD值3.00;EP值4.00V;CEP值15.91;GAS1值50.00;GAS2值55.00;气帘气值25.00;检测方式为 MRM;定量离子对为218.30/105.30;DP值100.00V;CE值30.00;CXP值10.00。
1.2.2 溶液的配制
标准曲线工作溶液:精确称量吡蚜酮标准品,用乙腈配制成1.00g·L-1的吡蚜酮母液,并稀释成浓度(mg·L-1)为 1.00、2.00、4.00、8.00、20.0、80.0、160、200的梯度溶液。
质控样品工作溶液:用乙腈将1.00g·L-1的吡蚜酮母液稀释成浓度(mg·L-1)为4.00、40.0、160的梯度溶液。
1.2.3 血浆样品处理
向190μL空白大鼠血浆样品(实验前从空白大鼠采集)中加入10μL吡蚜酮溶液,涡旋1min;取150 μL,加入300μL乙腈,涡旋混匀,置于离心机中以15 000r·min-1离心10min;取上清液100μL,加入900μL超纯水稀释后,进样分析。
取给药大鼠血浆样品30μL,加入60μL乙腈,涡旋混匀,置于离心机中以15 000r·min-1离心10 min;取上清液50μL,加入450μL超纯水稀释后,进样分析。
1.2.4 毒代动力学研究
实验设高、低两个剂量组,单次染毒。根据雄性大鼠急性经口毒性LD50为5 820mg·kg-1,高剂量设定为限量剂量[8],即1 000mg·kg-1;低剂量设定为雄性大鼠高剂量的1/10,即100mg·kg-1。
大鼠称重,按100mg·kg-1和1 000mg·kg-1的剂量采取经口灌胃方式,一次给足设计剂量,给药后将大鼠放回代谢笼内,自由进食、饮水。空白对照于给药前采集血样,高剂量组于投药后的10min、30min、1h、2h、4h、7h、24h、31h、48h、72h、96h,低剂量组于投药后的10min、30min、1h、2h、4h、5.5h、7h、12h、24h,经眼眶静脉丛采血0.1mL至肝素处理的离心管中,混匀,以8 000r·min-1离心10min,取上层血浆,置于-70℃冰箱冷冻保存,待测。
1.2.5 数据处理与统计分析
用DAS Ver2.0软件对数据进行拟合,计算毒代动力学参数,包括达峰时间(tmax)、峰值浓度(cmax)、消除半衰期(t1/2β)、表观分布容积(Vz)、体内总清除率(CLz)、毒时曲线下面积[AUC(0~t)、AUC(0~∞)],并进行统计分析。采用梯形法计算AUC、cmax与tmax均为实测值。
2 结果与讨论
2.1 分析方法的方法学考察
2.1.1 特异性
分别将空白大鼠血浆样品、空白大鼠血浆加入吡蚜酮标准品、给药1 000mg·kg-11.0h后的大鼠血浆样品按1.2.3方法前处理,进行LC-MS/MS分析,结果见图1。
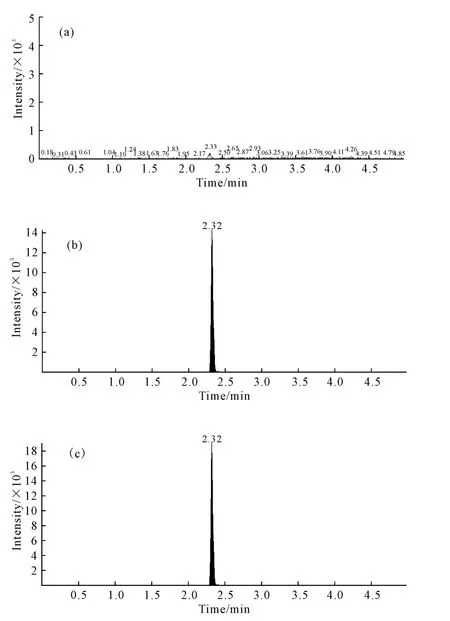
a.空白大鼠血浆 b.空白大鼠血浆添加吡蚜酮标准品c.给药1 000mg·kg-11.0h后的大鼠血浆样品
图1 不同样品的LC-MS/MS图谱
Fig.1 LC-MS/MS Chromatograms of different samples
由图1可见,血浆中内源性杂质对吡蚜酮的分析没有影响,方法的特异性良好。
2.1.2 标准曲线
用空白大鼠血浆稀释标准曲线工作溶液,配制成浓度(mg·L-1)分别为0.050、0.100、0.200、0.400、1.00、4.00、8.00、10.0的标准曲线样品。按1.2.3方法前处理,进行LC-MS/MS分析。以吡蚜酮的峰面积(Y)对浓度(X)绘制曲线,拟合得回归方程为Y=aX2+bX+c,结果见表1 。
由表1 可知,吡蚜酮在0.050~10.0mg·L-1范围内相关性良好。

表1 吡蚜酮大鼠血浆标准曲线回归方程参数Tab.1 Parameters of regression equation of pymetrozine in rat plasma
2.1.3 准确度和精密度
用空白大鼠血浆稀释质控样品工作溶液,配制成考察准确度与精密度的质控样品(QC),吡蚜酮浓度(mg·L-1)分别为0.200、2.00和8.00,按1.2.3方法前处理,进行LC-MS/MS分析,每天配制一套标准曲线和QC样品,平行进行3d,考察方法的准确度、批内精密度与批间精密度,结果见表2 。
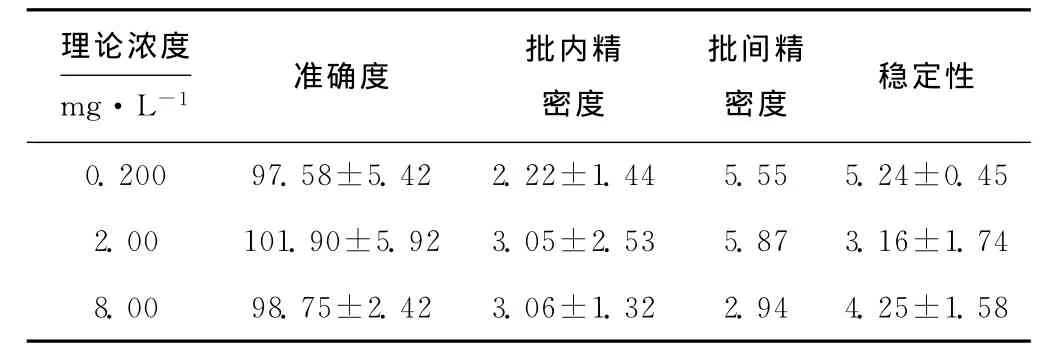
表2 吡蚜酮在大鼠血浆中的准确度、精密度和稳定性/%Tab.2 Recovery,precision and stability of pymetrozine in rat plasma/%
由表2 可知,准确度和精密度结果符合方法学要求。
2.1.4 稳定性
用空白大鼠血浆稀释质控样品工作溶液,配制成吡蚜酮浓度(mg·L-1)分别为0.200、2.00和8.00的质控样品,各12份,其中6份室温放置0h、4h、6h后按1.2.3方法前处理,进行LC-MS/MS分析,考察其室温稳定性;另外6份分别在-70℃冰箱保存1周、2周和4周后按1.2.3方法前处理,进行LC-MS/MS分析,考察其-70℃冰箱保存稳定性;另外配制3种浓度的吡蚜酮血浆样品保存于-70℃冰箱中,于24h、48h和72h取出反复冻融,按1.2.3方法前处理,进行LC-MS/MS分析,考察其冻融稳定性,结果见表2 。
由表2 可知,各条件下吡蚜酮样品均稳定。
2.2 吡蚜酮在大鼠体内的毒代动力学参数测定
大鼠经口灌胃给予吡蚜酮后,血浆药物浓度-时间曲线如图2所示,经DAS Ver2.0软件处理,采用统计矩模型计算,结果见表3 。
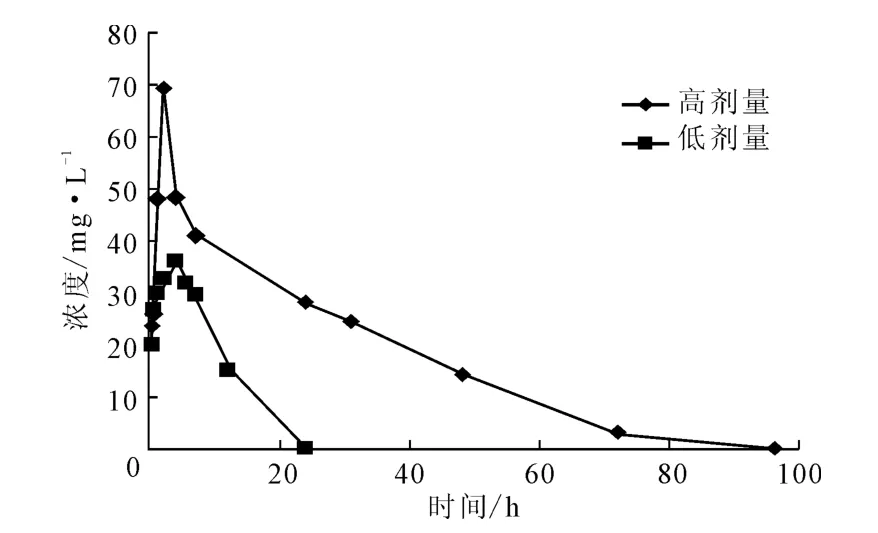
图2 吡蚜酮大鼠血浆药物浓度-时间曲线Fig.2 Concentration-time curves of pymetrozine in rat plasma
由图2可知,SD大鼠经口灌胃给予吡蚜酮后,血浆中10min即可检出毒物,给药后低、高剂量组分别在4h和2h药物浓度达峰,而后随时间延长逐渐下降,分别在24h、48h时血浆药物浓度均低于cmax的5%。
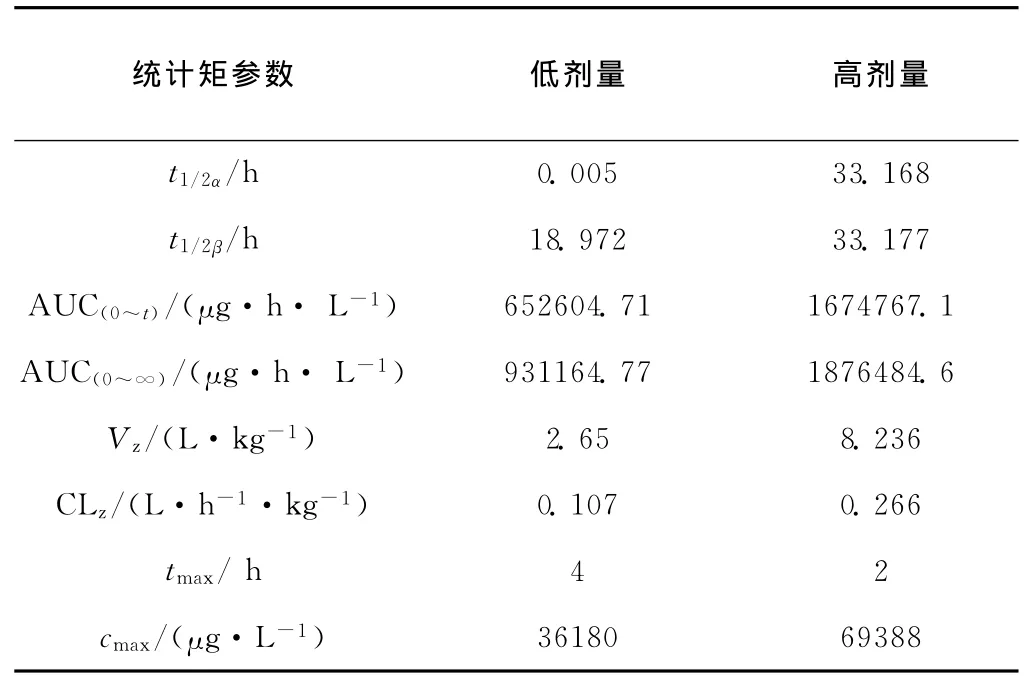
表3 吡蚜酮主要毒代动力学参数(n=5)Tab.3 Toxicokinetics parameters of pymetrozine(n=5)
由表3 可知,低、高两个剂量组:达峰时间(tmax)分别为4h和2h;峰值浓度(cmax)分别为36 180μg·L-1和69 388μg·L-1;消除半衰期(t1/2β)分别为18.972h和33.177h,高剂量较长,提示其消除较慢,可能在体内蓄积,且1 000mg·kg-1剂量组已基本达吸收饱和;表观分布容积(Vz)较小,分别为2.65L·kg-1和8.236L·kg-1,说明吡蚜酮对血浆外组织亲和力较弱;体内总清除率(CLz)分别为0.107L·h-1·kg-1和0.266L·h-1·kg-1;毒 时 曲 线 下 面 积 [AUC(0~t)]分 别 为652 604.71μg·h· L-1和1 674 767.1μg·h· L-1;AUC(0~∞)分 别 为 931 164.77 μg· h· L-1和1 876 484.6μg·h· L-1。
2.3 讨论
吡蚜酮为低毒农药,临床未见有急性中毒的报道。本研究表明,吡蚜酮能迅速吸收进入血液,随后快速分布,缓慢消除。经DAS Ver2.0软件处理数据,采用统计矩模型计算,得到低、高剂量组的 AUC(0~t)的比值为0.39、AUC(0~∞)的比值为0.50,提示其与给药剂量不成比例(给药剂量比为0.10),呈现出非线性代谢动力学特征。
3 结论
采用LC-MS/MS分析方法研究不同染毒剂量下吡蚜酮在SD大鼠体内的毒代动力学特征。色谱柱为Phenomenex Luna C18(50mm×4.6mm,5μm),采用ESI离子源,定量离子对为218.30/105.30。结果表明,大鼠经口灌胃给予吡蚜酮后,由统计矩参数表示的低、高两个剂量组主要毒代动力学参数如下:达峰时间(tmax)分别为4h和2h;峰值浓度(cmax)分别为36 180 μg·L-1和69 388μg·L-1;消除半衰期(t1/2β)分别为18.972h和33.177h;表观分布容积(Vz)分别为2.65 L·kg-1和8.236L·kg-1;体内总清除率(CLz)分别为:0.107L·h-1·kg-1和0.266L·h-1·kg-1;毒时曲线下面积[AUC(0~t)]分别为652 604.71μg·h·L-1和1 674 767.1μg·h· L-1;AUC(0~∞)分别为931 164.77μg·h· L-1和1 876 484.6μg·h·L-1。在毒性剂量下,吡蚜酮在大鼠体内的毒代动力学过程具有非线性动力学特征。值得注意的是,1 000 mg·kg-1剂量组消除半衰期较长,易发生蓄积。
采用LC-MS/MS进行检测,方法准确、灵敏,可为吡蚜酮毒代动力学的深入研究提供方法学依据,进而为毒理学试验设计奠定基础。
[1]张梅凤,于乐祥,张秀珍.高毒农药替代品种吡蚜酮的研究[J].今日农药,2009,(6):21-23.
[2]严会会,胡斌,刘惠民,等.高效液相色谱串联质谱法分析烟草中15种农药残留[J].烟草科技,2011,(7):43-47.
[3]刘建华,张小峰,季美娟,等.吡蚜酮原药高效液相色谱分析[J].农药,2008,(10):741-742.
[4]许秀莹,施海燕,王鸣华.气相色谱-质谱联用测定大米中6种烟碱类农药残留[J].质谱学报,2012,33(2):99-103.
[5]华乃震.吡蚜酮国内外进展、加工剂型和应用[J].农药市场信息,2013,(16):4-7.
[6]胡璇,沈国清,陆贻通,等.甘蓝中吡蚜酮残留量的高效液相色谱分析[J].农药,2008,47(3):184-185,189.
[7]唐俊,朱仁杰,何成鹏,等.大米、苹果中吡蚜酮残留量测定[J].中国农学通报,2008,24(11):109-112.
