木糖苷三氮唑鹰嘴豆芽素A的合成与结构表征
2014-10-11景临林范小飞马慧萍樊鹏程贾正平
景临林,范小飞,2,马慧萍,樊鹏程,贾正平*
(1.兰州军区 兰州总医院药剂科,甘肃 兰州730050; 2.兰州大学 药学院,甘肃 兰州730000)
鹰嘴豆芽素A(biochanin A,4′-甲氧基-5,7-二羟基异黄酮)属于天然异黄酮家族,在豆类植物和红三叶草中含量丰富.它能竞争性的与雌激素受体结合,发挥与雌激素一样的作用,是一种重要的植物雌激素[1].经常食用鹰嘴豆芽素A,对人和动物的健康是有益的,可用于骨质疏松症和更年期综合症等疾病的预防和治疗[2].近年来的许多研究表明,鹰嘴豆芽素A还具有抗菌、抗炎、抗氧化、抗骨质疏松、降血糖、抑制黑色素生成和神经保护等多种生物活性[3-9],但是其溶解性差,在体内代谢和清除速率快,生物利用度很低.
1,2,3-三氮唑是多种抗真菌、抗细菌、抗结核、抗癌药物中关键的功能团分子[10],主要通过Cu催化的“Click chemistry”得到.将糖基引入到三氮唑类分子中可增强其亲水性和导向性,改变药代动力学性能,增强其生物活性[11],已经成为设计合成结构新颖、活性优异的新化合物的重要手段之一.
为了提高鹰嘴豆芽素A的药理活性、增加其代谢稳定性和生物利用度,本文作者以D-木糖,炔丙基溴和鹰嘴豆芽素A为原料,根据药物拼合原理,将糖基化三氮唑分子与鹰嘴豆芽素A结合,合成得到三氮唑木糖苷化鹰嘴豆芽素A,产物结构经1H NMR、红外光谱、质谱和元素分析确认.目标化合物合成路线见图1和图2.

图1 β-D-三乙酰木糖叠氮化物的合成路线Fig.1 Synthesis ofβ-D-O-acetyl-xylopyranosyl azide
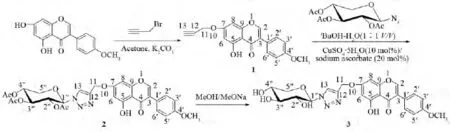
图2 木糖苷三氮唑鹰嘴豆芽素A的合成路线Fig.2 Synthesis of xylosyltriazole biochanin A derivative
1 实验部分
1.1 仪器与试剂
X-4B型显微熔点仪(温度计未校正),上海精科实业有限公司;NEXUS 670型傅立叶变换红外光谱仪,KBr压片,美国尼高力分子光谱仪器公司;Vario EL cube型元素分析仪,德国艾力蒙塔公司;Brucker AVANCE III 400型核磁共振波谱仪,瑞士Brucker Biospin公司;API 3200型LC/MS/MS质谱仪,美国应用生物系统公司.
鹰嘴豆芽素A(纯度98%),陕西慈缘生物技术有限公司;732阳离子树酯,阿拉丁试剂公司;柱层析硅胶(200~300目)和 GF254高效薄层硅胶板(10×20cm),青岛海洋化工厂分厂;CDCl3和 DMSO-d6,内标TMS,sigma公司,其他试剂均为市售分析纯.无水的溶剂经脱水干燥处理.
1.2 三乙酰木糖叠氮化物参考文献[12]方法制备
1.3 4′-甲氧基-5-羟基-7-炔丙氧基异黄酮(1)
将2.84g(10mmol)鹰嘴豆芽素 A、3.36g(20mmol)K2CO3和100mL无水丙酮加入单口瓶中,剧烈搅拌下缓慢加入2mL溴丙炔,回流反应3h.TLC监测反应完全后,体系降至室温,加入100mL水,45℃减压除去丙酮,过滤,滤饼依次用200mL蒸馏水、100mL 1mol/L盐酸溶液和200mL蒸馏水洗涤,真空干燥后得到3.09g浅黄色固体,产率96%.m.p.:152.1~154.7℃;1H NMR(CDCl3,400MHz)δ:12.88(1H,s,C5-OH),7.89(1H,s,C2-H),7.46(2H,d,J=8.4Hz,C2′-H,C6′-H),6.99(2H,d,J=8.8 Hz,C3′-H,C5′-H),6.50(1H,d,J=2.0Hz,C6-H),6.46(1H,d,J=2.0Hz,C8-H),4.76(2H,d,J=2.0Hz,C11-H),3.85(3H,s,C4′-OCH3),2.59(1H,s,C13-H);ESI-MS(m/z):323[M+H]+.IR (KBr):3 443,2 123,1 755,1 665,1 614,1 577,1 516,1 358,1 303,1 245,1 216,1 187,1 051,817.
1.4 4′-甲氧基-7-(1-((2′,3′,4′-三乙酰基-β-D-木糖基)-1,2,3-三氮唑-4-基)甲氧基)-5-羟基异黄酮(2)
将3.23g(10mmol)化合物1分散于100mL叔丁醇和水(体积比1∶1)的混合溶剂中,搅拌下依次加入4.48g(12mmol)三乙酰木糖叠氮化物、0.2mmol抗坏血酸钠和0.1mmol五水硫酸铜,55℃剧烈搅拌反应6h,将反应体系降至室温,加入20mL 2mol/L HCl,用100mL CH2Cl2萃取一次,有机相用水洗涤(100 mL×2),无水硫酸钠干燥12h,过滤,减压除去溶剂后快速柱层析分离,浓缩干燥后得5.42g白色固体,产率83%.m.p.:217.6~218.8℃;1H NMR(CDCl3,400MHz)δ:12.86(1H,s,C5-OH),7.89(1H,s,C2-H),7.85(1H,s,C13-H),7.46(2H,d,J=8.8Hz,C2′-H,C6′-H),6.98(2H,d,J=8.8Hz,C3′-H,C5′-H),6.43(1H,d,J=2.0Hz,C6-H),6.43(1H,d,J=2.0Hz,C8-H),5.81(1H,d,J=8.4Hz,C1″-H),5.46~5.35(2H,m,C2″-H,C4″-H ),5.27(2H,s,C11-OCH2),5.15(1H,m,C3″-H),4.31(1H,dd,J=5.6,11.6Hz,C5″-H),3.85(3H,s,C4′-OCH3),3.60(1H,t,C5″-H),2.08(3H,s,COCH3),2.05(3H,s,COCH3),1.89(3H,s,COCH3);ESI-MS (m/z):624 [M+H]+.IR(KBr):3 440,1 752,1 658,1 612,1 579,1 516,1 371,1 249,1 224,1 181,1 047,835.A-nal.calcd.for C30H29N3O12:C 57.78,H 4.69,N 6.74;found C 57.81,H 4.72,N 6.63.
1.5 4′-甲氧基-7-(1-((2′,3′,4′-三羟基-β-D-木糖基)-1,2,3-三氮唑-4-基)甲氧基)-5-羟基异黄酮(3)
将0.62g(1mmol)化合物2置于100mL三口烧瓶中,加入50mL甲醇,冷却至0℃,氮气保护下缓慢滴加1.2mL 1.0mol·L-1甲醇钠的甲醇溶液,升温至室温继续反应3~4h,利用TLC监测反应完全后,用732阳离子树酯调节体系至中性,有大量白色不溶物析出,冷却后过滤,用冰甲醇洗涤滤饼数次,真空干燥后得0.46g白色固体,为目标化合物3.产率92%.m.p.:172.5~174.4℃;1H NMR(DMSO-d6,400MHz)δ:12.94(1H,s,C5-OH),8.51(1H,s,C2-H),8.48(1H,s,C13-H),7.53(2H,d,J=8.4Hz,C2′-H,C6′-H),7.02(2H,d,J=8.8Hz,C3′-H,C5′-H),6.85(1H,d,J=1.6Hz,C6-H),6.54(1H,d,J=1.6Hz,C8-H),5.52(1H,d,J=9.2Hz,C1″-H),5.46(1H,d,J=6.4Hz,C4″-OH),5.30(2H,s,C11-OCH2),5.20(1H,d,J=4.8Hz,C2″-OH),3.84~3.81(3H,m,C3″-OH,C4″-H,C5″-H),3.80(3H,s,C4′-OCH3),3.76(1H,d,J=9.2Hz,C2″-H),3.49(2H,m,C3″-H,C5″-H);ESI-MS(m/z):498[M+H]+.IR(KBr,cm-1):3 397,1 653,1 610,1 578,1 515,1 450,1 252,1 179,1 152,1 050,835.Anal.calcd.for C24H23N3O9:C 57.95,H 4.66,N 8.45;found C 57.80,H 4.73,N 8.50.
2 结果与讨论
2.1 合成方法
1,2,3-三氮唑及其衍生物在自然界至今尚未发现,只能通过有机合成的方法获得.Cu(I)催化端基炔和叠氮化合物进行的“Click chemistry”反应是快速、高效、高立体选择性获得大量1,2,3-三氮唑衍生物的可靠方法[13].文献有关 “Click chemistry”反应条件的报道很多,通过对反应条件进行优化,我们以叔丁醇∶水(体积比1∶1)体系为溶剂、五水硫酸铜/抗坏血酸钠为催化剂、55℃条件下反应时间6h,最终以83%的产率得到了目标化合物2.在去除化合物2中的乙酰基时,为了避免糖苷键在酸性条件下水解,本文作者采取了碱性水解法,反应结束后用强酸性阳离子交换树脂调节pH,经过简单过滤、洗涤即得目标化合物3,操作简便,避免了柱色谱分离,产率较高.
2.2 结构表征
在化合物2和3的1H NMR谱中,鹰嘴豆芽素A分子中5-位羟基质子信号分别出现在12.86和12.94,7.85和8.51处的尖锐单峰为三氮唑结构中质子信号,-CH2-的质子信号分别出现在5.27和5.30处,证明三氮唑基团成功地引入到鹰嘴豆芽素A分子结构中.当化合物2水解完全后,2.00附近三个乙酰基的质子信号消失,化合物3在3.84~5.35出现羟基质子信号.
在化合物2和3的红外谱图中,3 440和3 397cm-1出现典型羟基吸收峰;1 650cm-1附近为异黄酮结构中羰基的特征吸收峰;1 750cm-1为乙酰基中羰基的特征吸收峰.化合物3中1 750cm-1附近的吸收峰消失,证明分子结构中的乙酰基被完全水解.
3 结论
为了获得代谢稳定性更好、活性更强、生物利用度更高的新型鹰嘴豆芽素A衍生物,本文作者以D-木糖,炔丙基溴和鹰嘴豆芽素A为原料,将鹰嘴豆芽素A与木糖苷通过1,2,3-三氮唑结构相连,合成了一种新型木糖苷三氮唑鹰嘴豆芽素A衍生物.该合成路线短、操作简单,反应条件温和、产率较高,产物结构经波谱分析与目标化合物一致,为鹰嘴豆芽素A的开发利用和生物活性研究奠定了基础.
[1]NYNCA A,SWIGOSKA S,PIASECKA J,et al.Biochanin A affects steroidogenesis and estrogen receptor-βexpressionin porcine granulosa cells[J].Theriogenology,2013,80(7):821-828.
[2]SU S J,YEH Y T,SGYU H W.The preventive effect of biochanin a on bone loss in ovariectomized rats:involvement in regulation of growth and activity of osteoblasts and osteoclasts[J].Evid Based Complement Alternat Med,2013,2013:594857.
[3]SEO Y J,KIM B S,CHUN S Y,et al.Apoptoticeffects of genistein,biochanin-A and apigenin on LNCaP and PC-3cells by p21through transcriptional inhibition of polo-like Kinase-1[J].J Korean Med Sci,2011,26(11):1489-1494.
[4]KOLE L,GIRI B,MANNA S K,et al.Biochanin-A,an isoflavon,showed anti-proliferative and anti-inflammatory activities through the inhibition of iNOS expression,p38-MAPK and ATF-2phosphorylation and blocking NFκB nuclear translocation[J].Eur J Pharmacol,2011,653(1/3):8-15.
[5]LIU Guoxing,LIANG Junchao,WANG Xuelin,et al.In vitro synergy of biochanin A and ciprofloxacin against clinical isolates of staphylococcus aureus[J].Molecules,2011,16(8):6656-6666.
[6]HARINI R,EZHUMALAI M,PUGALENDI KV.Antihyperglycemic effect of biochanin A,a soy isoflavone,on streptozotocin-diabetic rats[J].Eur J Pharmacol,2012,676(1/3):89-94.
[7]BREIKAA R M,ALGANDABY M M,El-DEMERDASH E,et al.Biochanin A protects against acute carbon tetrachloride-induced hepatotoxicity in rat[J].Biosci Biothchnol Biochem,2013,77(5):909-916.
[8]TAN J W,THAM C L,ISRAF D A,et al.Neuroprotective effects of biochanin A against glutamate-induced cytotoxicity in PC12cells via apoptosis inhibition[J].Neurochem Res,2013,38(3):512-518.
[9]LIN V C,DING H Y,TSAI P C,et al.In vitro and in vivo melanogenesis inhibition by biochanin A from trifolium pratense[J].Biosci Biotechnol Biochem,2011,75(5):915-918.
[10]王 艳,周成合.三唑类药物研究新进展[J].中国科学:化学,2011,41(9):1429-1456.
[11]CHINTHAKINDI P K,SANGWAN P L,FAROOQ S,et al.Diminutive effect on T and B-cell proliferation of non-cytotoxic alpha-santonin derived 1,2,3-triazoles:A report[J].Eur J Med Chem,2013,60:365-375.
[12]李一鸣.以叠氮糖为中间体设计合成具有生物活性的杂环化合物[D].天津:南开大学,2010:38-39.
[13]KOLB H C,FINN M G,SHARPLESS K B.Click chemistry:diverse chemical function from a few good reactions[J].Angew Chem Int Ed,2001,40(11):2004-2021.
