新型生物可降解雷帕霉素药物洗脱输尿管支架的构建及性能评估
2014-05-02王忠新谭海颂许永德符伟军王晓雄
王忠新,谭海颂,曹 磊,许永德,李 钢,符伟军,王晓雄
(1.中国人民解放军总医院海南分院泌尿外科,海南 三亚 572014;2.中国人民解放军总医院泌尿外科,北京 100853;3.中国人民解放军第309医院泌尿外科,北京 100091)
新型生物可降解雷帕霉素药物洗脱输尿管支架的构建及性能评估
王忠新1,2,谭海颂2,曹 磊2,许永德2,李 钢3,符伟军1,2,王晓雄2
(1.中国人民解放军总医院海南分院泌尿外科,海南 三亚 572014;2.中国人民解放军总医院泌尿外科,北京 100853;3.中国人民解放军第309医院泌尿外科,北京 100091)
目的 构建一种新型生物可降解雷帕霉素药物洗脱输尿管支架并评估其机械性能及药物释放特性。方法 采用聚乳酸为原料,将其溶于氯仿后加入雷帕霉素粉末,通过溶液挥发法构建螺旋形生物可降解雷帕霉素药物洗脱输尿管支架。通过万能压力机检测新型生物可降解雷帕霉素输尿管支架力学性能,并分别在3周、6周、9周和12周时通过色谱分析仪评估其药物释放特性。结果 成功构建的生物可降解雷帕霉素药物洗脱输尿管支架,长度为50 mm,内径为0.8 mm,外径1.4 mm,厚度为200 μm,带宽为1 mm。支架不仅具有良好的力学性能,并可有效持续释放药物,支架平均雷帕霉素含量为2 755 μg,3周后支架平均含药量为2 670 μg,6周后支架平均含药量为2 533 μg,9周后支架平均含药量为1 541 μg,12周后支架平均含药量为744 μg。结论 构建的生物可降解雷帕霉素药物洗脱输尿管支架具有良好的机械性能,可有效释放药物,有望为输尿管损伤或狭窄的治疗提供一种新的简单有效的材料和方法。
生物可降解;药物洗脱支架;输尿管支架
1978年,现代化的双猪尾支架被Finney首次报道,随后各种类型的输尿管支架广泛应用于泌尿外科多个领域[1]。输尿管损伤或狭窄可能会造成损伤侧上尿路的梗阻,从而导致肾积水及肾功能受损等一系列并发症发生。输尿管支架广泛应用于输尿管损伤或狭窄治疗中,其可用来恢复并维持上尿路的通畅引流。双J管是目前临床上应用最广泛的一种输尿管支架类型,它可有效维持尿路通畅引流。但随着输尿管支架的广泛应用,支架相关的一些并发症,如腰背痛、血尿、尿频、尿急以及膀胱输尿管返流、支架移位、被覆皮壳、尿路感染甚至上皮细胞增生和纤维化导致再狭窄等,严重影响患者的生活质量,已成为制约支架进一步应用的主要因素[2-3]。
为了尽可能地避免这些支架相关并发症的发生,各种类型的材料被尝试用于构建输尿管支架,包括生物可降解材料、各种涂层材料及药物缓释材料等。药物缓释支架技术近来取得了显著的进展,有望显著降低支架相关并发症发生率[4]。因此,本研究在前期成功构建的单纯生物可降解输尿管支架基础上,进一步探讨生物可降解药物洗脱输尿管支架的构建,期望为输尿管损伤和狭窄的治疗提供一种新的材料,不仅可有效恢复并维持输尿管管腔通畅,还能显著降低支架相关并发症的发生。
1 材料与方法
1.1 新型生物可降解药物洗脱输尿管支架制备 将黏度分子量为15×104g/mol的左旋聚乳酸(L-polylactic acid,PLLA)和消旋聚乳酸(PDLLA)按2:1的比例混合后,聚乳酸混合物溶于氯仿,配制成2%(g/ml)的溶液,加入雷帕霉素纯品粉末。搅拌24 h后,将悬浊液按照1 ml/cm3的比例倾倒在玻璃模具中,在23℃~28℃、相对湿度20%的条件下挥发形成薄膜,薄膜被进一步塑形成约1 mm宽度带状结构,再将其缠绕定形为螺旋型结构。后放入真空烘箱,65℃干燥21 d,包装后60Co灭菌,备用。
1.2 新型生物可降解药物洗脱输尿管支架的力学性能测定 调定万能压力机(INSTRON),以10 mm/min的加压速度,匀速压缩螺旋形支架。当被测试支架管压缩形变达到25%时,测量所得压力为支架侧压25%变形时的力,测量3次,取平均值。
1.3 药物洗脱支架有效药物释放量测定 将12根生物可降解雷帕霉素输尿管支架随机分为三组,每组4根。在3周、6周、9周、12周时,分别从三组中各选取一根支架测定其有效药物释放量。将雷帕霉素药物洗脱支架放于离心管中,用足量氯仿溶解。开口通风干燥72 h使氯仿完全挥发,用甲醇20 ml完全溶解离心管中的雷帕霉素。标准品用甲醇溶解成10µg/ml。使用HPLC(Aglient l100,Agilent Technologies)色谱分析仪检测支架的药物释放情况。HPLC检测条件:色谱柱,Alltech C18反相性;流动相,乙腈:水=60:40;检测波长,278 nm;恒温箱,30℃;流速,l.2 ml/min。进样量:标准品进样10µl,测试样品进样10µl。计算公式:支架载药量(µg)=200×样品检测值/标准品检测值。取3次测试的平均值为支架藏药量。
2 结果
2.1 生物可降解药物洗脱输尿管支架的构建 制备的新型生物可降解药物洗脱输尿管支架长度为50 mm,外径为1.4 mm,内径为0.8 mm,厚度为200µm,带宽1 mm(图1)。

图1 新型生物可降解雷帕霉素输尿管支架实物图及示意图
2.2 生物可降解药物洗脱输尿管支架的力学性能测定结果 新型生物可降解药物洗脱输尿管支架管发生25%形变时,需要的平均载荷压力为174 N(见图2)。

图2 新型生物可降解药物洗脱输尿管支架3次25%形变时的载荷压力
2.3 支架有效药物释放量测定结果 采用HPLC(Aglient 1100)色谱分析仪检测支架含药量,测试的平均值见图3~图8。新型生物可降解药物洗脱输尿管支架含有雷帕霉素2 755µg,3周后支架含药量为2 670µg,6周后支架含药量为2 533µg,9周后支架含药量为1 541 ug,12周后支架含药量为744µg。可见,生物可降解雷帕霉素药物输尿管支架成功构建,支架可有效释放药物,早期药物释放平缓,后期快速释放。

图3 标准样品检测图

图4 测试样品检测图:雷帕霉素含量为2 755 μg

图5 3周时测试样品检测图:雷帕霉素含量为2 670 μg
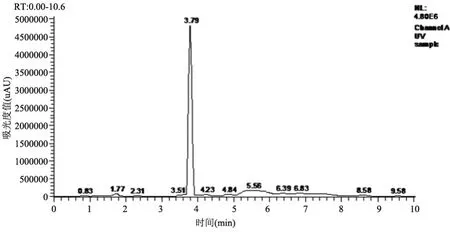
图6 6周时测试样品检测图:雷帕霉素含量为2 533 μg

图7 9周时测试样品检测图:雷帕霉素含量为1 541 μg

图8 12周时测试样品检测图:雷帕霉素含量为744 μg
3 讨论
各种类型的输尿管支架目前已被广泛用于输尿管损伤或狭窄的治疗中,因为无论输尿管管腔阻塞是由于外源性因素还是内源性因素导致,支架都是一种最简单的恢复并维持肾盂输尿管通畅引流的微创手段。但前期研究表明局部尿路上皮增生是支架植入后最主要的问题,支架植入后的长期慢性刺激会影响到输尿管的尿路上皮、黏膜层及肌肉层,严重制约支架的长期应用。随着生物材料和组织工程技术的发展进步,心血管领域应用的支架很好地将药物缓释与各种涂层技术结合在一起,试图来预防心血管支架最常见的并发症,即内皮增生和再狭窄的发生,并表现出不错的应用前景[5]。但目前关于生物可降解药物输尿管支架的研究仍处于尝试阶段,因此本研究拟探讨一种新型生物可降解雷帕霉素输尿管支架的构建,进而评估其力学性能和药物释放特性。
药物缓释支架通常由支架平台、药物载体和荷载药物三部分组成[6]。支架平台和药物载体在实现药物可控释放的同时,也可能会诱导机体促炎症反应,因此需要探索生物相容性更佳的材料来构建支架平台和药物载体。完全生物可降解聚合物材料,比如聚乳酸(PLA)和聚乳酸-羟基乙酸共聚物(PLGA),在机体内最终都可降解代谢为二氧化碳和水,具有很好的生物相容性。本研究中构建的新型药物洗脱输尿管支架,其支架平台和药物载体采用的材料均为聚乳酸。聚乳酸广泛分布在自然界中,因其有不对称取代的碳原子,因而以左旋聚乳酸(L)和消旋聚乳酸(D)两种对映异构体形式存在。PLLA是半结晶性,其力学强度大,而PDLLA为无定形形态,其力学强度低,因而这两种异构体在降解速度上有明显差异[7]。本研究中支架构建所采用的材料为PLLA和PDLLA的共聚物,其物理特性取决于这两种异构体形态的相对含量。随着PDLLA含量的增加,这种共聚物材料的无定形部分和降解速度也会随之增加。生物可降解聚合物聚乳酸(PLA)已被证实具有很好的生物相容性,它被用于制作缝合材料已经30多年[8]。本研究中构建的新型生物可降解药物输尿管支架是以PLLA和PDLLA按比例混合作为原材料,这样不仅保证了支架的机械强度,以实现对输尿管腔的有效支撑作用,同时调控了支架的降解速度。
多种活性药物被作为荷载药物来构建药物缓释支架,包括紫杉醇和雷帕霉素等。雷帕霉素是一种大环内酯类免疫抑制剂,能阻断细胞由G1期向S期转化,从而抑制细胞增殖和迁移,使细胞静止在增殖周期的早期阶段但并不破坏细胞。这些特点使得雷帕霉素能成为一种较为理想的支架荷载药物。一个理想的药物缓释支架,其药物释放动力学应与再狭窄形成过程相一致,因此,一个可控的药物释放系统是药物缓释支架构建过程中的重要组成部分。目前常用的可控给药系统包括扩散控制或聚合物降解和渗透压控制或离子交换等。基于支架的给药方法也有很多种,主要包括非聚合物药物涂层、药物共价附着(交联剂)、聚合物涂层药物浸泡、非吸收性或吸收性的聚合物载体[9]。采用生物可吸收性聚合物作为载体来运载药物通常可获得最佳的和持续的药物释放。将活性药物掺和到生物可降解药物载体基质聚合物中,实现将药物装载到支架上。生物可降解聚合物交联的程度提供了调控药物释放速度的一种方法。生物可降解载体基质形成互联孔隙,便于药物微小颗粒的溶解,实现药物从聚合物上可控的释放[10]。生物可降解聚合物降解的同时释放药物,而聚合物的降解物最终通过代谢途径排出机体[11]。支架的降解速度由聚合物链的水解作用决定,而药物的释放速度则由支架的降解速度决定。这样,通过调控支架的降解速度,便能控制药物的释放速度,支架的降解速度以及药物支架的药物释放特性应与愈合过程相一致[12]。
本研究构建的生物可降解雷帕霉素输尿管支架即采用将药物与载体基质掺和的方法实现药物装载。同时根据输尿管损伤或狭窄治疗中,输尿管支架管通常留置3个月左右的临床实际,本研究中构建的生物可降解药物输尿管支架预期降解时间为12周。支架有效药物释放量测定结果表明,随着支架的降解,药物可有效从支架上释放出来,前6周时释放的药物量占总药量的10%左右,后6周时释放的药物量占总药量的70%。由此可见,支架上的药物释放特征是早期缓慢释放,后期快速释放。药物的释放可以通过溶出、溶蚀及扩散等机制实现。本研究中,生物可降解支架载荷药物的释放是通过扩散机理和支架的不断降解溶蚀实现的。后期随着聚合物材料的降解加速,药物被快速释放出来。这种药物释放特性避免了早期药物突然释放对输尿管损伤处黏膜愈合的影响,同时后期药物快速释放可有效降低支架相关性上皮增生反应,从而降低输尿管再狭窄的发生。
此外,前期上尿路压力流率研究表明在支架植入后的输尿管,当排尿等动作引起膀胱内压增加时,其膀胱内压会直接传导至肾盂,因此长段输尿管支架,比如双J管可能会增加肾盂内压力,导致输尿管积水和膀胱输尿管返流。短段的支架构型会提供更好的抗返流效果。本研究构建的新型生物可降解药物输尿管支架采用短段构型,并未直接完全破坏肾盂及输尿管的蠕动和抗返流机制,可能会预防膀胱输尿管返流,但需进一步相应研究来证实。
由上可见,新型生物可降解药物输尿管支架采用具有良好生物相容性的聚乳酸为原料来构建支架平台和药物载体,不仅具有良好的机械性能及可自行降解避免二次手术取出等优点,还可有效持续释放药物,有望为输尿管损伤或狭窄的治疗提供一种新的简单有效的材料和微创方法。
[1]Chew BH,Duvdevani M,Denstedt JD.New developments in ureteral stent design,materials and coatings[J].Expert Rev Med Devices, 2006,3(3):395-403.
[2]Ozgur BC,Ekıcı M,Yuceturk CN,et al.Bacterial colonization of double J stents and bacteriuria frequency[J].Kaohsiung J Med Sci, 2013,29(12):658-661.
[3] Soria F,Morcillo E,Pamplona M,et al.Evaluation in an animal model of a hybrid covered metallic ureteral stent:a new design[J]. Urology,2013,81(2):458-463.
[4]Lange D,Chew BH.Update on ureteral stent technology[J].Ther Adv Urol,2009,1(3):143-148.
[5]Schurtz G,Delhaye C,Hurt C,et al.Biodegradable polymer Biolimus-eluting stent(Nobori®)for the treatment of coronary artery lesions:review of concept and clinical results[J].Med Devices (Auckl),2014,27(7):35-43.
[6]Kukreja N,Onuma Y,Daemen J,et al.The future of drug-eluting stents[J].Pharmacol Res,2008,57(3):171-180.
[7]Cutright DE,Perez B,Beasley JD,et al.Degradation rates of polymers and copolymers of polylactic and polyglycolic acids[J].Oral Surg Oral Med Oral Pathol,1974,37(1):142-152.
[8]Kulkarni RK,Pani KC,Neuman C,et al.Polylactic acid for surgical implants[J].Arch Surg,1966,93(5):839-843.
[9]Acharya G,Park K.Mechanisms of controlled drug release from drug-eluting stents[J].Adv Drug Deliv Rev,2006,58(3):387-401.
[10]Lewis AL,Willis SL,Small SA,et al.Drug loading and elution from a phosphorylcholine polymer-coated coronary stent does not affect long-term stability of the coating in vivo[J].Biomed Mater Eng,2004,14(4):355-370.
[11]Tesfamariam B.Drug release kinetics from stent device-based delivery systems[J].J Cardiovasc Pharmacol,2008,51(2):118-125.
[12]Wykrzykowska JJ,Onuma Y,Serruys PW.Advances in stent drug delivery:the future is in bioabsorbable stents[J].Expert Opin Drug Deliv,2009,6(2):113-126.
Construction and performance evaluation of a new biodegradable rapamycin-eluting ureteral stent.
WANG Zhong-xin1,2,TAN Hai-song2,CAO Lei2,XU Yong-de2,LI Gang3,FU Wei-jun1,2,WANG Xiao-xiong2.1.Department of Urology,Hainan Branch of Chinese PLA General Hospital,Sanya 572014,Hainan,CHINA;2.Department of Urology, Chinese PLA General Hospital,Beijing 100853,CHINA;3.Department of Urology,the 309thHospital of Chinese People's Liberation Army,Beijing 100091,CHINA
Objective To construct a new biodegradable rapamycin-eluting ureteral stent and to evaluate its mechanical property and drug-eluting characteristics.Methods Polylactic was selected as the stent material and dissolved by chloroform.The rapamycin powder was added into the solution.Then,a new helical biodegradable rapamycin-eluting ureteral stent was made by volatilization method.The mechanical property of the stent was measured by universal tension tester,while the drug-eluting characteristic was evaluated by chromatographic analysis machine.Results The new biodegradable rapamycin-eluting ureteral stent had good mechanical property with length in 50 mm,inner diameter in 8 mm,outer diameter in 1.4 mm,thickness in 200 μm and width in 1 mm.The stent can continuously release drug.The mean amount of rapamycin of the stent was 2 755 μg.After 3 weeks,the remained mean amount of rapamycin was 2 670 μg.At 6 weeks,it was 2 533 μg and 1 541 at 9 weeks.Eventually,it was decreased to 744 μg at 12 weeks.Conclusion The new biodegradable rapamycin-eluting ureteral stent made of polylactic acid not only has good mechanical property,but also can release drug efficiently,which may provide a new material for the treatment of ureteral strictures.
Biodegradable;Drug-eluting stent;Ureteral stent
R693
A
1003—6350(2014)18—2663—04
10.3969/j.issn.1003-6350.2014.18.1046
2014-07-01)
国家自然科学基金(编号:81070555);北京市自然科学基金资助项目(编号:7142145和2092029);军队临床高新技术重点项目(编号:413DG63J)
符伟军。E-mail:wangzx301@163.com
