卡培他滨联合奥沙利铂或顺铂一线治疗晚期胃癌临床观察
2013-10-17顾术东茅国新
顾术东 刘 艳 刘 凡 邵 棋 沈 浮 茅国新
南通大学附属医院肿瘤化疗科,江苏南通 226001
胃癌为我国常见消化道恶性肿瘤,由于早期临床症状缺乏特异性,较少能够得到早期诊断与治疗,在确诊时很多患者已属晚期,已无手术根治机会,化疗是晚期胃癌的主要治疗措施,对晚期胃癌患者进行全身化疗能缓解症状,延长生存时间[1-3]。氟尿嘧啶类和铂类药物联合组成的化疗方案是晚期胃癌化疗的常用方案之一,卡培他滨是新型氟尿嘧啶类口服化疗药物,口服后能够在肿瘤细胞内转化为5-氟尿嘧啶(5-Fu),具有高效低毒的优点,奥沙利铂为第三代铂类化疗药物,在胃癌的治疗中显示出了很好疗效,并且较顺铂不良反应更小[4-5]。本研究观察了卡培他滨联合奥沙利铂与卡培他滨联合顺铂一线治疗晚期胃癌的效果和不良反应,现将结果报道如下:
1 资料与方法
1.1 一般资料
收集南通大学附属医院2008年1月~2011年12月收治的晚期及术后复发转移胃癌患者共69例,所有病例均经组织病理学或细胞学诊断证实,根据AJCC第7版胃癌临床分期标准进行分期均为Ⅳ期。患者年龄为28~76岁,中位年龄57岁;男40例,女29例;病理类型包括:乳头状腺癌25例,管状腺癌17例,黏液腺癌18例,印戒细胞癌9例;功能状态评分(PS)≤2分,预计生存期大于3个月,重要脏器功能无明显异常,均为初治患者,有客观可测量病灶,患者临床病理特征见表1。
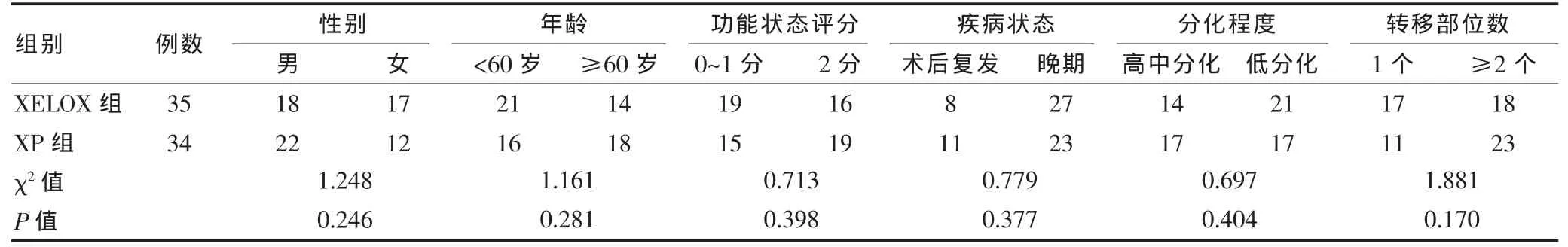
表1 69例晚期胃癌患者临床病理特征比较(例)
1.2 治疗方法
69例晚期胃癌患者分为两组,其中35例接受卡培他滨联合奥沙利铂方案化疗(XELOX组:卡培他滨1000 mg/m2,口服,每天2次,第1~14天;奥沙利铂130 mg/m2,静脉滴注2 h,第1天,3周为1个周期),34例接受卡培他滨联合顺铂方案化疗(XP组:卡培他滨1000 mg/m2,口服,每天2次,第 1~14 天;顺铂 25 mg/m2,静脉滴注,第 1~3 天),3 周为1个周期。所有患者化疗前常规予5-羟色胺受体拮抗剂及甲氧氯普胺止吐,顺铂组在用药期间常规水化利尿,化疗期间如出现3度以上骨髓抑制,给予粒细胞刺激因子对症治疗。所有患者至少接受2个周期化疗后评价疗效,患者出现病情进展或严重不良反应时停止化疗,最多化疗6个周期。随访采用住院治疗,门诊及电话随访相结合的方式,截至时间为2012年12月31日。
1.3 疗效及不良反应评价标准
按实体瘤疗效评价标准(RECIST)评定化疗疗效,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD),有效率(RR)为 CR+PR,疾病控制率(DCR)为 CR+PR+SD。不良反应按美国国立癌症研究所(NCI)的毒性反应分级标准判定。总生存期(overall survival,OS)是指从患者化疗疗时间始至患者死亡或最后一次随访的时间(失访患者),疾病进展时间(time to progression,TTP)指从治疗开始至肿瘤病灶出现进展的时间,计算中位生存期(median survival time,MST)和中位疾病进展时间(TTP)。
1.4 统计学方法
所有结果均采用SPSS 20.0统计软件包进行统计学分析处理。两组病例临床病理特征、化疗有效率、疾病控制率及化疗不良反应的比较采用χ2检验,生存分析使用Kaplan-Meier法,组间差异采用log-rank法检验,以P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效
69例患者共完成247个周期化疗,平均化疗3.6个周期,其中XELOX组35例患者完成化疗133个周期,平均化疗3.8个周期,XP组34例患者完成113个周期,平均化疗3.3个周期,69例患者均可评价疗效。XELOX组与XP组化疗RR分别为48.6%和41.2%,DCR分别为71.4%和67.6%,两组患者化疗RR及DCR经比较差异均无统计学意义(χ2=0.381,P=0.537,χ2=0.166,P=0.733)。 见表2。
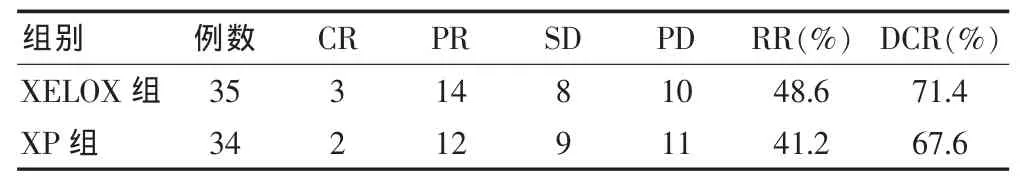
表2 两组晚期胃癌患者近期疗效比较(例)
2.2 远期疗效
截至末次随访时间XELOX组存活5例,XP组存活4例。XELOX组和XP组两组患者中位TTP分别5.9个月(95%可信区间4.548~7.252)和5.1个月(95%可信区间3.957~6.243),经检验差异无统计学意义(χ2=0.555,P=0.456,生存曲线见图1);两组患者MST分别为10.1个月(95%可信区间 7.550~12.650) 和 9.0个月(95%可信区间 6.571~11.429),经检验差异无统计学意义(χ2=0.463,P=0.496,生存曲线见图2)。

2.3 不良反应
69例患者均可评价不良反应,无治疗相关死亡。两组患者不良反应比较,XELOX组外周神经毒性发生率高于XP组(P<0.05),其他不良反应XELOX组的发生率均低于XP组,其中恶心呕吐的发生率差异有统计学意义(P<0.05),两组患者不良反应见表3。
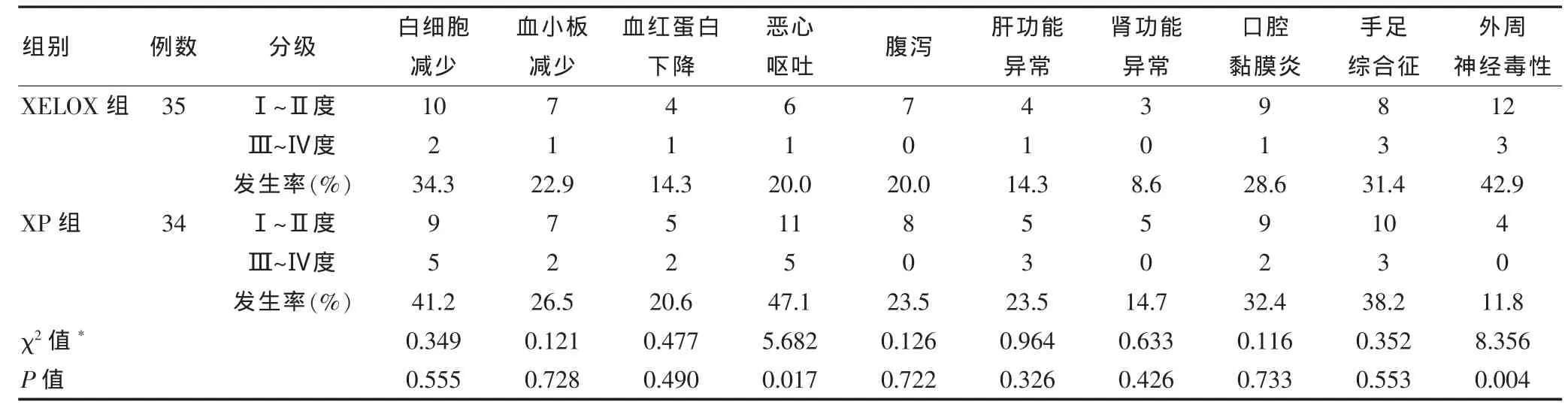
表3 两组晚期胃癌患者化疗后主要不良反应比较(例)
3 讨论
卡培他滨是新一代氟尿嘧啶类口服化疗药物,为5-FU的前体药物,口服后可迅速通过胃肠黏膜,在肿瘤细胞内经胸苷磷酸化酶催化转变为5-FU,由于肿瘤细胞中的胸苷磷酸化酶活性高于正常组织,使药物在肿瘤组织中具有更高活性,从而最大程度地降低5-FU对正常人体细胞的损害,提高疗效[4-6]。Kang等[7]在一项随机Ⅲ期临床研究中对卡培他滨与5-FU分别联合顺铂一线治疗晚期初治胃癌患者的疗效进行了评价,结果显示卡培他滨联合顺铂组与5-FU联合顺铂组RR分别为41%和29%,中位无进展生存期分别为5.6个月和5.0个月,总生存期分别为10.5个月和9.3个月,卡培他滨疗效略优于5-FU,但无统计学差异。Ma等[8]对卡培他滨和5-FU为基础的化疗方案治疗进展期胃癌的荟萃分析表明,与5-FU为基础的治疗方案相比较,卡培他滨方案的OS更长、RR更高,并且卡培他滨方案的不良反应发生率更低。
奥沙利铂为第三代铂类化疗药物,主要作用靶点为DNA,通过与细胞DNA结合,形成链内或链间DNA加合物,导致DNA损伤及复制障碍,从而引起细胞的凋亡,与顺铂相比其对DNA的抑制作用更强,并且与DNA结合的速率比顺铂快10倍以上,而且结合更牢靠,有着更强的细胞毒作用,并且不良反应尤其是肾毒性和血液学毒性较顺铂轻[9-10]。实验表明,奥沙利铂的抗癌谱较顺铂更广,与顺铂无交叉耐药,并且奥沙利铂与氟尿嘧啶类药物联合应用有协同作用[11-12]。Cunningham等[13]在一项非劣效性临床研究中对奥沙利铂和顺铂的临床疗效进行了比较,结果表明,对于初治患者奥沙利铂与顺铂相比较,在无进展生存期和RR上均无统计学差异,奥沙利铂的3或4级中性粒细胞减少、脱发、肾毒性和血栓栓塞发生率较顺铂低,但3或4级腹泻和神经病变发病率稍高。龚继芳等[14]在一项荟萃分析中对奥沙利铂与顺铂治疗进展期胃癌的临床疗效进行了比较,奥沙利铂方案的RR为46.3%,高于顺铂方案的40.6%(P=0.006),在1年生存率方面奥沙利铂(44.6%)亦高于顺铂(39.3%)(P=0.04),而在不良反应方面奥沙利铂除周围神经毒性发生率高于顺铂外,其他不良反应发生率均低于顺铂,认为在进展期胃癌的治疗中奥沙利铂方案与顺铂方案相比,有着更好的疗效和安全性。
氟尿嘧啶类与铂类联合组成的化疗方案,是晚期胃癌的常用化疗方案,文献报道RR在50%左右[15-16]。本研究对卡培他滨联合奥沙利铂与卡培他滨联合顺铂一线治疗晚期胃癌的疗效和安全性进行了比较,XELOX组与XP组化疗RR分别为48.6%和41.2%,DCR分别为71.4%和67.6%,中位TTP分别5.9个月和5.1个月,MST分别为10.1个月和9.0个月,XELOX组略优于XP组,但是两组之间差异无统计学意义(P>0.05);在不良反应方面,XELOX组除周围神经毒性外,其他不良反应发生率均低于XP组,尤其是胃肠道反应的发生率差异有统计学意义,并且XELOX组平均化疗周期数高于XP组,患者耐受性更好,在晚期胃癌的治疗中可以考虑给予奥沙利铂替代顺铂。本研究结果初步表明,XELOX方案与XP方案疗效相当甚至更优,不良反应发生率更低,患者耐受性更好,可考虑作为晚期胃癌的一线治疗方案。
[1]汤钊猷.现代肿瘤学[M].3版.上海:复旦大学出版社,2011:878-893.
[2]Oba K,Paoletti X,Bang YJ,et al.Role of chemotherapy for advanced/recurrent gastric cancer:an individual-patient-data meta-analysis[J].Eur J Cancer,2013,49(7):1565-1577.
[3]Cervantes A,Roda D,Tarazona N,et al.Current questions for the trea tment of advanced gastric cancer[J].Cancer Treat Rev,2013,39(1):60-67.
[4]Ajani J.Review of capecitabine as oral treatment of gastric,gastroesophageal,and esophageal cancers[J].Cancer,2006,107(2):221-231.
[5]Yamaguchi K,Sawaki A,Doi T,et al.Efficacy and safety of capecitabine plus cisplatin in Japanese patients with advanced or metastatic gastric cancer:subset analyses of the AVAGAST study and the ToGA study[J].Gastric Cancer,2013,16(2):175-182.
[6]Zhang C,Wang J,Gu H,et al.Capecitabine plus oxaliplatin compared with 5-fluorouracil plus oxaliplatin in metastatic colorectal cancer:Meta-analysis of randomized controlled trials[J].Oncol Lett,2012,3(4):831-838.
[7]Kang YK,Kang WK,Shin DB,et al.Capecitabine/cisplatin versus 5-fluorouracil/cisplatin as first-line therapy in patients with advanced gastric cancer:a randomised phase Ⅲ noninferiority trial[J].Ann Oncol,2009,20(4):666-673.
[8]Ma Y,Tang L,Wang HX,et al.Capecitabine for the treatment for advanced gastric cancer:efficacy,safety and ethnicity[J].J Clin Pharm Ther,2012,37(3):266-275.
[9]Kweekel DM,Gelderblom H,Guchelaar HJ.Pharmacology of oxaliplatin and the use of phamacogenomics to individualize therapy[J].Cancer Treat Rev,2005,31(2):90-105.
[10]Mowaka S,Ziehe M,Mohamed D,et al.Structures of oxaliplatinoligonucleotide adducts from DNA[J].J Mass Spectrom,2012,47(10):1282-1293.
[11]Cassidy J,Tabernero J,Twelves C,et al.XELOX(capecitabine plus oxaliplatin):active first-line therapy for patients with metastatic colorectal cancer[J].J Clin Oncol,2004,22(11):2084-2091.
[12]Ishitsuka H.Capecitabine:preclinical pharmacology studies[J].Invest New Drugs,2000,18(4):343-354.
[13]Cunningham D,Starling N,Rao S,et al.Capecitabine and oxaliplat in for advanced esophagogastric cancer[J].N Engl J Med,2008,358(1):36-46.
[14]龚继芳,沈琳.奥沙利铂对照顺铂治疗进展期胃癌的荟萃分析[J].中华医学杂志,2009,89(46):3261-3265.
[15]吕慧芳,张延新,韩黎丽,等.奥沙利铂联合替吉奥或卡培他滨治疗老年晚期胃癌的临床观察[J].中国医药导报,2012,9(23):61-63.
[16]王爱英,张毛讲.卡培他滨联合奥沙利铂治疗晚期胃癌的临床观察[J].中国医药导报,2012,9(6):58-59.
