熔盐电解还原二氧化碳制碳技术
2013-10-11王宝辉洪美花吴红军罗明检苑丹丹
王宝辉,洪美花,吴红军,罗明检,苑丹丹,董 维
(东北石油大学化学化工学院石油与天然气化工重点实验室,黑龙江 大庆 163318)
自工业革命以来,煤、石油、天然气等化石燃料已成为世界能源的主体,化石能源的大规模开发和利用在推动了人类社会向前发展的同时也带来了严重的生态环境问题。其中,由化石燃料燃烧释放的CO2是造成全球气候变暖的主要元凶之一,如何有效控制温室气体排放问题已成为全球诸多亟待解决的战略课题之一[1-4]。CO2是典型的直线型分子[5],化学性质极为稳定,对CO2的直接转化非常困难且耗能,因此,探索CO2的化学利用技术意义重大。
熔融盐是由盐类熔化形成的阴、阳离子所组成的离子熔体[6],具备许多水溶液无法具有的特性。其中,熔融碱金属碳酸盐由于具有热容量大、蓄热及传热能力佳、高温电导率高等优点已成为最具潜力的高温反应介质、电解质及储能热载体[7-8]。2010年,Licht等提出熔融碳酸锂可作为二氧化碳零排放的炼铁[9-12]及水泥生产[13]反应的高效媒介。对高温熔融碳酸盐作为电解质吸收并电解CO2的理论电解电势[14]的研究结果表明,一价碳酸盐中碳酸锂作为电解质时最有利于C的析出。但Li2CO3的熔点为723℃,且熔盐电解反应的温度通常要高于电解质的熔点50~100℃,则电解反应的温度过高,不仅对设备要求高、能耗大,且容易引起副反应。针对上述问题,本文作者采用高温熔融混合碳酸盐Li0.896Na0.625K0.479CO3作为电解质,与单一纯盐相比,混合熔盐的熔点大幅降低,拓宽了温度的使用范围。高温下,熔融混合碳酸盐被电解还原为C,并通过中间产物Li2O、Na2O、K2O吸收空气中CO2,使碳酸盐电解质再生,从而构筑一个完整的循环,最终表现为将CO2转化为C,反应机理如图1所示。
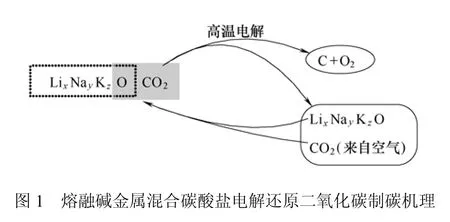
1 实验方法
1.1 实验试剂
无水碳酸钠、无水碳酸钾、无水碳酸锂、盐酸,均为分析纯试剂。
1.2 实验装置
本实验采用图2所示的电解装置,作为电解池的刚玉坩埚中盛放质量比1∶1∶1的Li2CO3、Na2CO3、K2CO3(Li0.896Na0.625K0.479CO3),并用陶瓷加热器(定制)加热至熔融。实验采用两电极体系,阴极分别采用Fe、Cu、304不锈钢,阳极采用Ni、W、304不锈钢。为避免电极表面氧化膜等杂质对体系稳定性及测试结果造成影响,电解前需对电极进行抛光,后将其浸没于油中待用,实验前再将电极表面油污除净,并将处理过的电极插入刚玉管中以防在电解过程中被氧化。整个实验过程均在高纯氩气保护下进行,待体系温度恒定后连接电化学工作站进行数据采集。
1.3 电化学性能测试
实验采用美国Pine公司的WaveNow电化学工作站对体系的循环伏安曲线、极化曲线进行测定,同时考察不同阴、阳极材质以及电解温度对反应结果的影响。
1.4 产物制备与表征
1.4.1 产物制备与提纯
相同电量下(均为1A·h)进行恒电流电解制备产物,电流值分别取0.5 A、1.0 A、2.0 A,相应电解时间分别为2.0 h、1.0 h、0.5 h。待电极冷却后收集阴极上析出的产物,并通过50%HCl溶解—→超生清洗30 min—→60℃水浴加热2~3 h—→抽滤—→洗涤—→干燥等步骤除去产物中残余的碳酸盐等杂质。
1.4.2 产物表征
将提纯后的产物进行SEM-EDS、TG/DTA、XRD分析。SEM表征采用德国Zeiss ΣIGMA场发射显微镜进行,Inlens二次电子检测器,工作电压5 kV,工作距离8.7 mm,放大倍数20000倍。EDS分析借助Oxford Instruments X-Max能谱仪进行,能谱分辨率123 eV,束斑影响区为1 μm。热重分析(TG/TDA)采用美国Perkin Elmer公司的Diamond型热重分析仪进行。空气氛围,初始温度30℃,最终温度800℃,升温速率15℃/min。X射线衍射分析(XRD)采用Rigaku D/MAX-2200型X射线衍射仪进行。测试参数如下:Cu阳极,石墨单色器;电压为40 kV;电流为20 mA;狭缝为DS=1°,SS=1°,RS=0.3 mm。X射线源为Al靶Kα射线(hυ=1486.6 eV),分析室真空度 6.7×10−7Pa。
1.5 电流效率计算
根据法拉第定律可计算电流效率,电流效率计算公式如式(1)、式(2)。

式中,q为电化当量,即单位电量下所获得的产物质量,kg/(A·h);法拉第单位用F表示,1 F=96500 C=26.8 A·h;n为电荷转移数,产物为C时n=4;G为电解时间内实际生成的产物质量,kg。
2 结果与讨论
2.1 电化学性能测试
2.1.1 循环伏安曲线
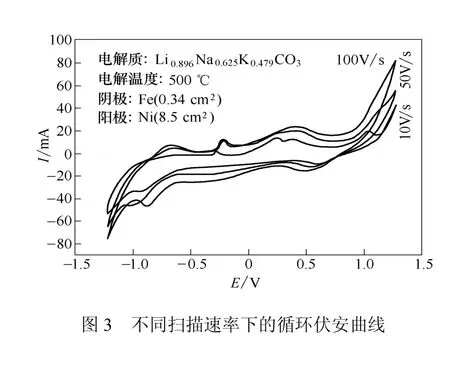
扫描速率分别为10 mV/s、50 mV/s、100 mV/s时的循环伏安曲线如图3所示。
由图3可知,在所测试区间内阴极电流密度与阳极电流密度基本对称,并且出现明显的氧化峰及碳生成的还原峰。随着扫描速率逐渐增大,氧化还原峰的形态基本保持不变,峰电流值逐渐上升,且峰电位随扫描速率的增大逐渐向正移动。
2.1.2 极化曲线
实验测得质量比1∶1∶1的Li-Na-K混合碳酸盐(Li0.896Na0.625K0.479CO3)的熔点为408℃,由于一般熔盐电解时选择的电解温度高于电解质的熔点50~100℃,因此,本实验分别在450℃、500℃、550℃、600℃等温度下进行电解,同时考察不同电极材质对反应结果的影响。测定阴极极化曲线时,为减小阳极极化对实验结果的影响,使阳极有效表面积大于阴极有效表面积10倍以上。同理,测定阳极极化曲线时,使阴极有效表面积大于阳极表面积10倍以上,结果如图4所示。
由图4可知,有电流通过电极时,电极电位偏离平衡位置,随电流密度的增大,阴极电位逐渐向负移,而阳极电位逐渐向正移动。相同阳极条件下,采用Cu或304不锈钢阴极时测得的电势值较接近,均高于Fe作阴极时的电势值[图4(a)],因此本实验采用Fe作阴极。
Fe作阴极时,进一步考察不同阳极材质对反应结果的影响,如图4(b)。电流密度较小时,3种不同阳极材质下的电势值差距较小,随着电流密度进一步加大,采用Ni电极时的电势值低于W和不锈钢。且Ni作阳极时的极化曲线相对平坦,金属钝化程度较小,稳定性较好,因此本实验采用Ni作阳极。Fe作阴极、Ni作阳极,不同温度下的阴、阳极极化曲线如图4(c)、图4(d)。由图可知,随着温度的升高,电势的绝对值逐渐降低。熔盐电解质中由离子导电,随着温度的升高,离子的运动速率加快,有利于电解质的传质与电荷转移,同时,高温降低了反应所需的活化能,因此电势值随之降低。由于O2在阳极一侧析出,温度越高阳极的腐蚀情况就会越严重,因此本实验宜在500~550℃范围内制备产物。
2.2 电压-时间曲线
相同电量(均为1A·h)、不同电流强度下进行恒电流电解,实验结果如图5所示。
由图5可知,1A·h的电量下,电流恒定为0.5A时的电势值维持在2.0~2.3 V;1.0 A时电势值为2.4~2.6 V;2.0 A时为3.1~3.4 V。电解产物在阴极析出,反应前后的Fe圈如图5所示。冷却的电极上还包含一部分碳酸盐等杂质,因此需将收集的产物按酸洗—→超声—→水浴加热—→抽滤—→洗涤—→干燥等步骤进行提纯,对提纯后的产物进行SEM-EDS、TG/DTA、XRD分析,结果如图6~图9所示。
2.3 产物表征
2.3.1 SEM-EDS分析
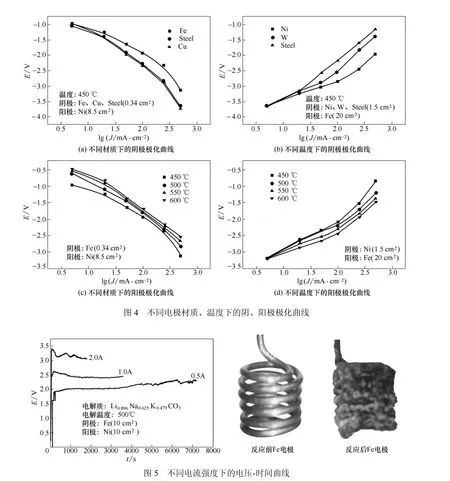

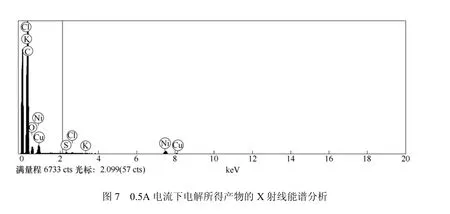
图6、图7分别为恒电流0.5A、电解2 h后所得产物(提纯后)的表面形貌(放大20000倍)与能谱分析结果。由图可知,产物表面粗糙,呈不规则颗粒状,并伴有团聚现象。能谱分析结果显示产物中含有C、O、S、Cl、K、Ni、Cu等元素,其中C元素的原子分数高达88.73%,可知产物以C为主。样品中含有的O可能是由于中间产物K2O未除净以及样品测试过程中使用的导热胶(含O、Cu、S)掺入其中所致。而Cl则是由提纯过程中使用的HCl引入到产物中,Ni则是阳极残留物未除净引起,但S、Cl、K、Ni、Cu等元素的含量均非常小。电流强度为1.0 A、2.0 A时的产物形貌、能谱分析结果均与此相似,仅元素含量上略有差别,3组产物的EDS元素分析结果见表1。
2.3.2 热重分析
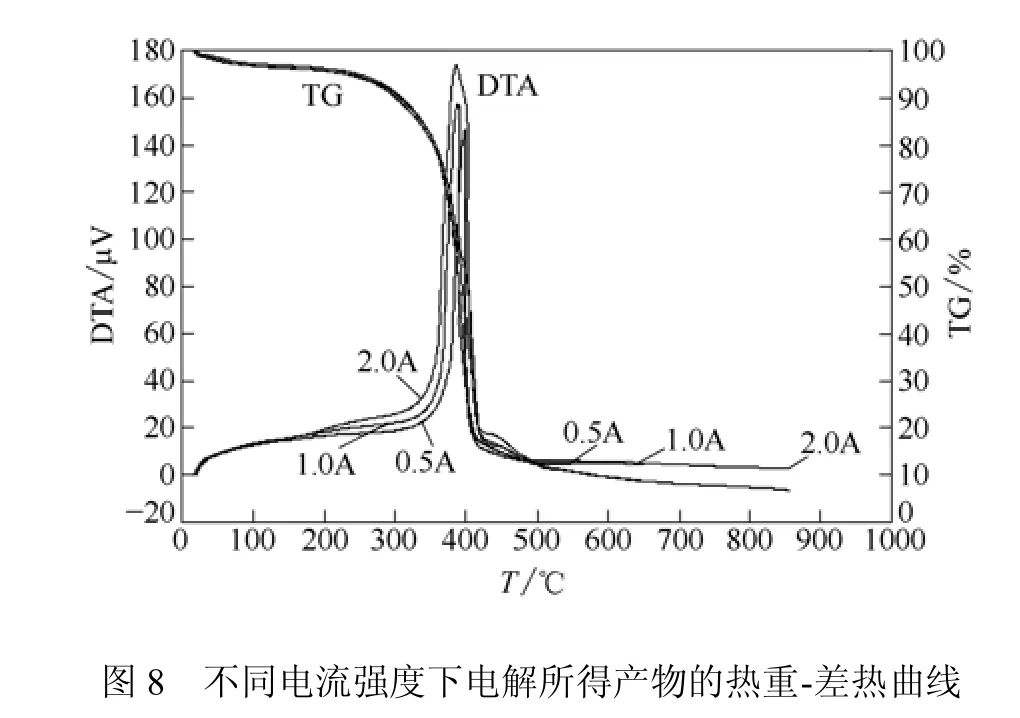

表1 不同电流强度电解所得产物EDS分析结果
图8为提纯后产物的热重分析结果,由图8可知,3组实验结果基本一致。TG曲线上,产物均从300℃开始发生明显失重,由SEM-EDS分析已知产物主要为碳,且不同形态的碳在空气中有不同的燃烧温度,而单一的无定形碳在300℃开始氧化[15-18]。此外,DTA曲线均只在350~400℃范围内出现一个明显的放热峰,吕德义等[19]对碳纳米管粗产品的TG-DTA曲线的研究结果表明,DTA曲线上峰温为357℃的尖锐放热峰为无定形碳的放热峰,与本实验结果基本吻合。因此,可进一步证明本实验中产物碳的形态为无定形碳。从TG曲线上还可看出,电流强度分别为0.5A、1.0A、2.0A时,无定形碳的失重量分别为83.68%、83.46%、84.98%。
2.3.3 XRD分析

图9为提纯后产物的XRD分析结果,2θ=44.5°、52°处为Ni衍射峰,2θ=37.2°、43.1°处为NiO的衍射峰。电流强度为0.5 A时产物中只出现Ni的特征峰,而电流强度增至1.0 A、2.0 A时产物中同时出现Ni和NiO的特征峰。原因可能在于电流增大时反应的电势值随之升高,从而促进了阳极Ni在高温电解过程中被氧化形成NiO。图中未出现明显的碳类特征峰,这是由于产物为无定形碳,由碳原子六角形环状平面形成的层状结构零乱而不规则,晶体形成有缺陷,且晶粒微小,因此在X光衍射图中的反射线模糊不清,从而难以精确定位其特征峰位置。
2.4 电流效率
本实验条件下,电流效率计算结果如表2所示。
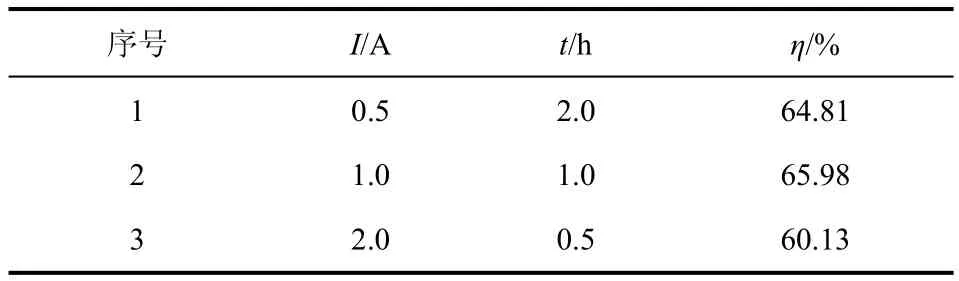
表2 电流效率计算结果
由表2可知,1A·h的电量下,电解电流为1.0A、电解时间为1.0 h时的电流效率较高。
3 结论
本实验采用熔盐电解法还原空气中CO2,实验结果表明以Li0.896Na0.625K0.479CO3混合碳酸盐为电解质吸收并电解CO2是可行的。Fe作阴极、Ni作阳极,于500℃下电解制取碳时,产物中无定形碳含量最高可达84.98%,电流效率最高可达65.98%。
[1]栾健,陈德珍.二氧化碳减排技术及趋势[J].能源研究与信息,2009,25(2):88-93.
[2]Lonngren K E,Bai Erwei.On the global warming problem due to carbon dioxide[J].Energy Policy,2008,36(4):1567-1568.
[3]Ambuj D S.Automobiles and global warming:Alternative fuels and other options for carbon dioxide emissions reduction[J].Environmental Impact Assessment Review,1995,15(3):241-274.
[4]Georgios A F,Paul C.Global warming and carbon dioxide through sciences[J].Environmental International,2009,35(2):390-401.
[5]Lagowski J J.Modern Inorganic Chemistry[M].New York:Marcel Dekker,1973:68-80.
[6]谢刚.熔融盐理论与应用[M].北京:冶金工业出版社,1998:6-40.
[7]吴耀明,苏明忠,杜森林.熔融盐研究进展[J].化工进展,1995,14(5):5-7.
[8]敖先权,王华,魏永刚.熔融碱金属碳酸盐特性及其在能源转化技术中的应用[J].化工进展,2007,26(10):1384-1390.
[9]Licht S,Wang B H.High solubility pathway for the carbon dioxide free production of iron[J].Chem.Commun.,2010,46:7004-7006.
[10]Licht S,Wu H J,Zhang Z H,et al.Chemical mechanism of the high solubility pathway for the carbon dioxide free production of iron[J].Chem.Commun.,2011,47:3081-3083.
[11]Licht S,Wu H J.Step iron,a chemistry of iron formation without CO2emission:Molten carbonate solubility and electrochemistry of iron ore impurities[J].Phys.Chem.C,2011,115:25138-25147.
[12]Licht S,Wang B H,Wu H J.Step-a solar chemical process to end anthropogenic global warmingⅡ:Experimental results[J].Phys.Chem.C,2011,115:11803-11821.
[13]Licht S,Wu H J,Hettige C,et al.Step cement:Solar thermal electrochemical production of CaO without CO2emission[J].Chem.Commun.,2012,48:6019-6021.
[14]王宝辉,苑丹丹,吴红军,等.太阳能驱动分解高温熔融碳酸盐电解电势的理论分析[J].大庆石油学院学报,2010,34(5):92-95.
[15]Kitiyanan B,Alvarez W E,Harwell J H,et al.Controlled production of single-wall carbon nanotubes by catalytic decomposition of CO on bimetallic Co–Mo catalysts[J].Chem.Phys.Lett.,2000,317:497-503.
[16]Herrera J E,Resasco D E.In situTPO/Raman to characterize single-walled carbon nanotubes[J].Chem.Phys.Lett.,2003,376:302-309.
[17]Shi Z J,Lian Y F,Liao F H,et al.Purification of single-wall carbon nanotubes[J].Solid State Communication,1999,112:35-37.
[18]孔令涌,罗文耀,欧阳增图,等.浅析碳纳米管纯度测定方法[J].材料导报,2006,20(s1):114-116.
[19]吕德义,徐丽萍,徐铸德,等.温度对CVD法制备碳纳米管的影响[J].化学物理学报,2002,15(2):118-122.
