肺结核即时诊断技术研究进展
2012-09-06隗慧林王书崎
胡 杰,王 琳,隗慧林,王书崎,徐 峰
肺结核即时诊断技术研究进展
胡 杰,王 琳,隗慧林,王书崎,徐 峰
肺结核给全球特别是发展中国家和地区的公共卫生健康带来严重危害。潜伏期、耐药性肺结核的检测,以及患者依从性差给全球肺结核的预防和控制提出了新的难题。WHO要求对结核病检测成本低廉、使用方便、快速可靠、无需设备,且普及性强。因此,本文总结了现有的基于免疫血清学和分子生物学开发的肺结核诊断产品,以及即时诊断(point-of-care testing,POCT)技术的最新研究进展,以期为将来开发新型高效的结核病POCT技术和产品提供思路。
结核,肺;诊断技术和方法;研究技术
肺结核(tuberculosis,TB)是由结核分枝杆菌(mycobacterium tuberculosis)引起的一种传染性疾病。它是影响全球人类健康的主要传染性疾病之一[1]。据世界卫生组织(WHO)的报告显示,2010年全球约有1200万肺结核患者,新增患者880万,死亡人数达145万[2]。其中超过50%的新增患者分布在亚洲(59%),而中国(12%)仅次于印度(26%),位居世界第二[2]。我国不仅是全球22个肺结核高负担国家之一,同时也是全球27个耐药肺结核流行严重的国家之一[2]。虽然肺结核可以治愈,且治疗成功率相当高,但由于目前很多国家存在着数目庞大而未确诊的病例[3],对肺结核的防控造成一定难度。因此,提高肺结核的诊断技术对已感染的个体和控制肺结核在人群中的传播都是十分必要的。
1 概述
目前,全球控制肺结核的重点是寻求更早、更有效的检测方法,并且扩大耐药性肺结核的诊断能力[2]。传统肺结核的检测手段为痰液涂片法,其检测灵敏度低,并且取决于患者依从性,因此检出率不高[1,3];金标准为痰液培养法,虽然灵敏度高,但对实验条件要求严格,并且检测时间过长[1,3];有些国家应用胸部X线诊断肺结核,该方法依赖于大型仪器,且特异性不够,因而难以推广和普及[3]。此外,肺结核检测还缺乏有效的生物标志物。虽然目前针对肺结核不同时期(潜伏期和活动期)及其耐药性均有相应的检测标志物,但它们的特异性和灵敏度不一,无法用来作为确诊的标志物[1,3]。传统检测方法的不足及其可靠的标志物的缺失都造成了目前肺结核在全球范围持续传播的局面。因此,亟需发现一种可确诊肺结核的有效标志物,并发展一种高效、简便、快捷、易推广的诊断技术[3-4]。
近年来,迅速发展的即时诊断(point-of-care testing,POCT)成为检验医学发展的一个新领域,并作为一种新检验手段[4]。POCT分析方法快速简单,可现场分析,减少了样品转送流程,具有快速、高通量、自动化、微型化、高灵敏度以及多参数同步分析等优点[5-6],将在今后肺结核诊断检测领域占据重要的地位[4]。同时,POCT检测内容也逐步向各个领域扩展(如生化、免疫、微生物、核酸等),故在传染性疾病临床检测领域有着广泛的发展前景。因此,本文总结了现有的基于免疫血清学和分子生物学开发的肺结核诊断产品,以及POCT技术的最新研究进展,以期为将来开发新型高效的肺结核POCT技术和产品提供思路。
2 POCT技术产品
2.1 基于血清学检测产品 目前,肺结核的血清学检测尽管未被国际指导方针推荐,但已经使用多年[7],并且基于酶联免疫吸附法和免疫层析色谱法开发出多种成熟的市场化产品[7]。但是,Steingart等[8-9]对68种肺内和21种肺外肺结核血清检测产品的性能进行了系统评估,发现它们的灵敏度和特异性不一致。WHO联合多家单位对19种肺结核肺内快速检测产品也进行实验评估,结果表明其灵敏度低,特异性也不一致[10],因而难以推广和普及。此外,γ-干扰素释放试验(IGRA)作为肺结核临床常规检测方法之一,在肺结核发生率低的欧美国家,已成为肺结核尤其是潜伏期肺结核和肺外结核的辅助诊断手段。然而其对活动期肺结核特异性较差,因此对于潜伏期肺结核较为流行的中低收入国家,WHO不建议使用[11]。市场上部分肺结核快速血清学检测产品[12-13]的性能比较见表1。
蛋白芯片技术作为一种高通量、高灵敏度、高特异性且微型化的蛋白质分析技术[14],目前也被应用于肺结核蛋白标志物的检测。现在市场上的结核蛋白芯片的特点是可对多种结核分枝杆菌抗原或抗体进行同时筛查,简便、快速、准确而又有较高的特异性与敏感性,以及检测成本低,该技术为临床诊断肺结核起到了积极的作用,在临床已得到广泛应用。对于痰涂片检查阴性、无痰、肺外结核病患者的检出更具优越性[15],但其对耐药性肺结核的高效、特异性检测仍存在一定的不足。
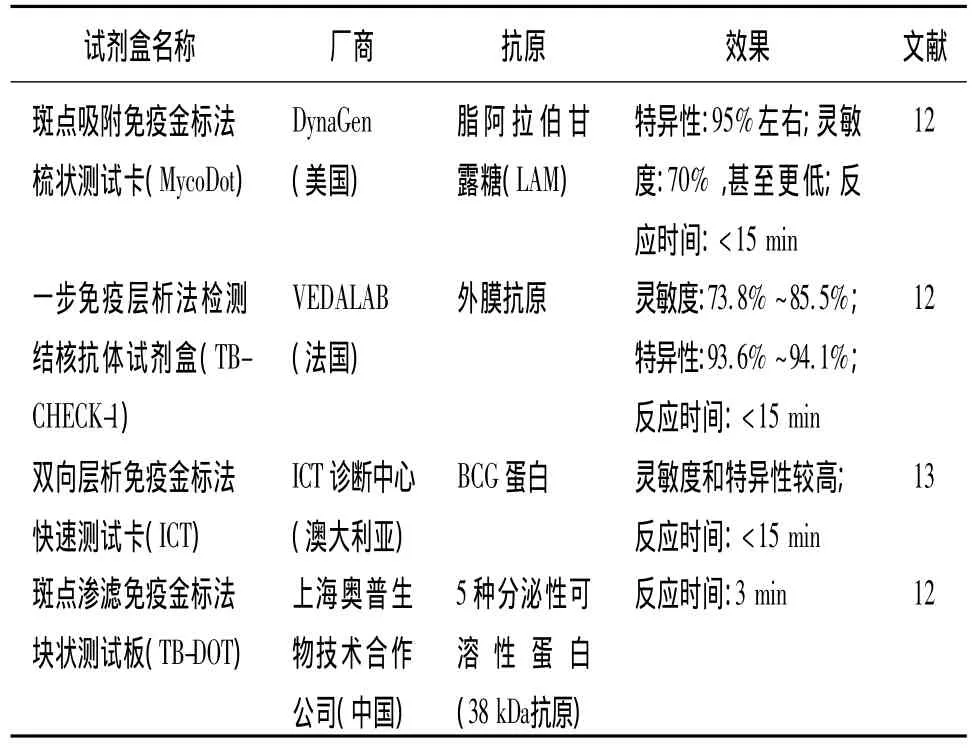
表1 部分肺结核快速血清学检测产品的性能比较
2.2 基于分子生物学检测产品 基于分子生物学技术的诊断方法越来越多的应用到日常的检测工作中,自核酸扩增试验(nucleic acid amplification tests,NAAT)应用到肺结核的早期诊断以来,就显示出其强大的优越性。因此,美国疾病预防控制中心(CDC)推荐将NAAT用于诊断活动期肺结核,并建议在第一次取痰时就应行涂片及NAAT检测。此外,核酸探针技术(DNA probe)、DNA指纹技术等因具备检测敏感性高、特异性强、简便、快速等特点,在肺结核的诊断中也较常用。
虽然NAAT技术较涂片法在精确度方面有了巨大的进步,较分枝杆菌培养法节省时间,但较高的投资及设备需求极大地限制了其在临床的应用。2010年美国Cepheid公司开发的GeneXpert MTB/RIF试剂盒可在2 h内直接从患者新鲜痰液或冻存痰液中检测是否含有结核分枝杆菌及对利福平的耐药性,整个过程都在一密闭环境中进行,手动时间短(≤5 min),对操作者和周围环境安全[16](图1)。但此方法仍需专门的GeneXpert仪器、健全的实验室基础设施和训练有素的实验人员的支持,因其高成本和复杂性限制了该方法在发展中国家的广泛使用[17]。
此外,市场上出现的基因芯片具有检测效率高、自动化程度高、检测靶分子种类多、结果可靠性高等优势,利于大规模推广应用[18]。在肺结核检测中主要用于分枝杆菌的菌种鉴定和耐药性检测等方面。黄明翔等[19]以BACTECMGIT 960收集了分离到的肺结核分枝杆菌阳性培养物,以传统分枝杆菌菌种鉴定方法为对照,应用DNA芯片技术进行菌种鉴定。结果表明,DNA芯片检测技术可以简便、快速、灵敏、特异地鉴定大多数分枝杆菌菌种。但该方法仍然存在着许多难以解决的问题,如技术复杂、成本昂贵、检测灵敏度较低、重复性差、分析范围较狭窄等,有待于进一步改进和完善。

图1 GeneXpert MTB/RIF试剂盒操作过程
总之,市场上现有的结核分枝杆菌检测产品还难以满足肺结核防控的需求,它们或灵敏度较低,或特异性不强,抑或只能满足部分患者,无法大规模应用。因此,世界范围内的组织、机构以及学者仍不断加入到对肺结核诊断技术的研究中,并为诊断技术的发展作出了贡献。
3 POCT诊断技术研究
从2007年开始,WHO推荐使用了一系列肺结核诊断技术[4]。到目前为止,虽然尚无批准的肺结核即时检测产品,但人们对其特性要求已经有所讨论[3]。新的肺结核诊断技术需具备以下特点:实惠(affordable)、灵敏(sensitive)、特异(specific)、友好(user-friendly)、快速而可靠(rapid and robust)、不依赖仪器(equipment-free)、易于配送(deliverable)[5]。本文将对在肺结核诊断技术发展中具有良好产业化前景的基于微流体技术的试纸检测、芯片检测技术平台进行详细介绍,并对新兴的手机医学在快速检测技术中的应用进行探讨。
3.1 试纸检测技术 试纸检测技术起源于20世纪50年代,早孕试纸获得巨大成功后,其思路被大家迅速采纳和运用。一个典型的试纸条由样品垫、结合垫、硝酸纤维素膜、吸水垫、支持垫以及外壳组成。一般检测时,取少量样品(如唾液、尿液、血液)滴于样品垫上,定性分析可简单地通过观察测试区的颜色变化而获得[20],在15 min内即可获得检测结果。市场商品化的基于抗体-抗原反应的肺结核脂阿拉伯甘露糖(LAM)试纸条见图2。试纸不仅可以基于抗体-抗原反应检测蛋白质标记物,还可以基于碱基对之间的杂交互补配对,检测特定的目的DNA或RNA片段(图3)。试纸条除了定性检测外,还可以实现多重检测[21]。Dineva等[22]在试纸条上同时实现了乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)和艾滋病病毒(HIV)核酸扩增的检测。除此之外,Martinez等[23]将微流体技术引入试纸中,赋予了试纸检测新的功能和用途,必将在包括肺结核在内的传染性疾病检测中发挥作用。
因此,基于新技术的引入,研究者尝试开发新型的肺结核核酸检测试纸:①基于传统定性检测试纸的基础上力求实现半定量甚至定量检测;②研发同时检测多个生物标记物的肺结核检测试纸,除了提高其检测特异性外,还可应用于耐药性肺结核的筛查;③为了提高试纸检测灵敏度,还可以利用纳米技术进行信号放大。

图2 蛋白检测试纸条

图3 核酸检测试纸条
3.2 芯片检测技术 新兴的芯片检测技术已经成为肺结核诊断的重要辅助手段。该技术由于具有检测指标集成度高、需样量少、省时等优势而迅速发展。目前,伴随着微纳制造技术的进步,推动着芯片检测技术向更新、更宽广的领域发展。它可以整合样品处理到样品检测等多个单元于一体,因而十分适用现场快速检测。
Lee等[24]报道了一种基于芯片的核磁共振系统,可实现多重定量快速检测。同时,利用磁性颗粒作为近距离传感器,能放大分子间的相互作用,从而能检测未经处理的生物样品(图4)。结果表明,该检测系统可实时检测细菌,鉴别部分细胞,同时检测一系列蛋白质标记物。随后,他们将其改造,用于卡介苗的检测中,在30 min中内痰液检测灵敏度为20 cfu/ml[25]。Fang 等[26]开发了一个整合环介导等温核酸扩增反应(LAMP)的手持式微芯片。该芯片实现了DNA快速释放,信号指数扩增,可肉眼读取单个或多重检测结果。研究人员将其用于结核分枝杆菌的检测中,检测限为 270 拷贝/μl。Kim 等[27]则开发了一个基于免疫荧光的微头传感器,可在25 min内检测痰液中结核分枝杆菌。该装置通过在微头上修饰特异性的抗体保证其特异性,而通过耦联流体循环和电场在微头表明聚集目标细菌以保证其灵敏度,最后通过免疫荧光检测捕获的细胞,其检测灵敏度为200 cfu/ml。LAMP手持式微芯片和免疫荧光微头传感器检测结果均与聚合酶链反应(PCR)检测结果相当。
目前,对于新型肺结核POCT核酸检测产品的研发,主要包括两个技术要点,一个是实现现场核酸扩增,另一个是实现扩增产物的快速检测。对于核酸扩增,除了PCR法,目前已开发出多种核酸等温扩增技术,为基于芯片的核酸扩增提供了便利,将其和试纸检测相结合,即可迅速获得检测结果。因此,利用日益成熟的微纳制造技术,可以将传统的大型仪器、精密仪器等所具备的功能移植于芯片甚至其一个小小的单元上,这样有望一步实现从样品到结果,大大缩短了检测周期和成本。
3.3 手机医学 随着新技术的发展,手机不仅用于通信联络和社交网络,在健康保健、环境检测和远程医学等领域的应用也很广泛。手机在电信系统中处于核心地位,又兼有成像功能,鉴于其应用的广泛性,近年来手机在发展中国家和资源有限地区的医学诊断、影像学检查领域中的应用价值备受关注。手机的拍照功能可以获得明场图片,而利用LED灯进行激发,也可以获得荧光图片,从而进行检测和分析[28]。此外,它还可以和显微镜、超声探头,以及微流体装置联用。而其自身还可以集成各种功能的软件,对采集的数据或图片进行处理。通过手机终端还能将数据发给医疗中心,由医务人员进行分析和处理,并将诊断结果反馈给用户。
Breslauer等[29]利用标准的、便宜的显微镜目镜和物镜(放大倍数和分辨率可由不同的物镜进行调节)开发出了手机-光学显微镜(图5)。他们在明场下对恶性疟原虫感染和镰刀形红细胞,并在LED激发的荧光下对结核分枝杆菌感染的痰标本进行成像。其上述所有情形的分辨率都超过了检测血细胞和微生物形态所需;对结核分枝杆菌样本,他们进一步利用数字相片,通过影像分析软件实现了自动细菌计数。Lee等[25]将其核磁共振芯片进一步改造,一方面通过增加一个自动化的负反馈系统跟踪并补偿温度漂移,提高了其在现实环境测量时的稳定性和可靠性,另一方面通过无线网络和手机共享数据,从而方便了系统控制[30]。

图5 手机-光学显微镜检测
目前,麻省理工学院(MIT)国际健康创新项目(innovations in international health,IIH)致力于将诊断试纸和手机通信相结合,以提高贫穷国家和地区的肺结核治疗。该项目组和合作者一起开发了一个简单的诊断试纸,它能够检测尿液中抗结核药物的代谢产物。当试纸和患者尿液接触后,代谢物和试纸上化学物质反应,反应揭示了一个密码,患者将其信息发给中心数据库,连续用药30 d的患者会获得手机话费的奖励。此方法在尼加拉瓜实地试验已经获得成功,并将在巴基斯坦开展更大规模的试验[31]。
因此,我们一方面可以利用手机进行肺结核检测技术的改进和完善,另一方面还可以利用其通讯网络,建立远程医疗监控,使手机在肺结核的诊断、治疗及患者依从性方面发挥作用。
4 前景展望
目前,我国肺结核疫情形势依然严峻,防控工作仍面临诸多挑战。提高我国肺结核的诊断能力,发展比常规方法快速、即时、准确且成本更低的诊断方法控制活动期肺结核是一种必然趋势,对我国控制肺结核流行有重要意义。POCT是检验医学发展的必然产物,是医学进步和科学技术发展推动产生的仪器小型化和操作程序简便化的结晶,是当代科技信息化的反映[32]。诊断装置小型化,操作简单化,结果报告即时化的POCT检验模式受到人们的青睐。目前,POCT虽集合了多个学科的新技术得到了快速的发展,但临床应用仍受到限制和制约。因此,POCT是否能够提供高质量、可信赖的检验结果则显得至关重要。此外,分子生物学技术的迅猛发展为疾病的诊断和治疗提供了广阔的应用前景。伴随结核分枝杆菌全部基因组测序工作的完成,医学诊断进入分子基因时代,基因研究也将进入后基因时代。
目前新的肺结核诊断技术是在现有检测方法基础上进行改进、拓宽,寻找特异性、敏感性高的生物标记物结合其他学科技术的发展,将多种检测方法联合应用,优势互补,从而提高检出率。因此,我们希望充分利用结核分枝杆菌基因组丰富的信息,运用一切分子生物学技术、微流控技术和其他技术手段,发展一种对结核杆菌(尤其是多药耐药性结核杆菌)进行快速、高敏核酸检测的POCT技术,开发一种价格低廉、便携、高灵敏度、高特异性的肺结核核酸诊断试剂盒。该类产品不仅可有效地诊断潜在的和结核杆菌检测阴性的肺结核,而且可对结核病耐药基因进行筛查等,为临床提供较传统方法更为快速灵敏的检测指标,该类POCT产品将在未来的临床检验中占有极为重要的地位。
[1]Walzl G,Ronacher K,Hanekom W.Immunological biomarkers of tuberculosis[J].Nat Rev Immunol,2011,11(5):343-354.
[2]World Health Organization.Global tuberculosis control:WHO report 2011[EB/OL].[2012-06-20].http://www.who.int/tb/publications/global_report/en/.
[3]McNerney R,Daley P.Towards a point-of-care test for active tuberculosis:obstacles and opportunities[J].Nat Rev Microbiol,2011,9(3):204-213.
[4]Wallis R S,Pai M,Menzies D.Biomarkers and diagnostics for tuberculosis:progress,needs,and translation intopractice[J].Lancet,2010,375(9729):1920-1937.
[5]Lee W G,Kim Y G,Chung B G.Nano/Microfluidics for diagnosis of infectious diseases in developing countries[J].Adv Drug Deliv Rev,2010,62(4-5):449-457.
[6]Wang S,Xu F,Demirci U.Advances in developing HIV-1 viral load assays for resource-limited settings[J].Biotechnol Adv,2010,28(6):770-781.
[7]Pinto L M,Grenier J,Schumacher S G.Immunodiagnosis of tuberculosis:state of the art[J].Med Princ Pract,2012,21(1):4-13.
[8]Steingart K R,Flores L L,Dendukuri N.Commercial serological tests for the diagnosis of active pulmonary and extrapulmonary tuberculosis:an updated systematic review and meta-analysis[J].PLoS Med,2011,8(8):e1001062.
[9]Steingart K R,Henry M,Laal S,et al.A systematic review of commercial serological antibody detection tests for the diagnosis of extrapulmonary tuberculosis[J].Thorax,2007,62(10):911-918.
[10]World Health Organization/TDR.Laboratory-based evaluation of 19 commercially-available rapid diagnos-tic tests for tuberculosis[EB/OL].[2012-06-21].http://www.who.int/tdr/publications/documents/diagnostic-evaluation-2.pdf.
[11]Denkinger C M,Dheda K,Pai M.Guidelines on interferon-gamma release assays for tuberculosis infection:concordance,discordance or confusion?[J].Clin Microbiol Infect,2011,17(6):806-814.
[12]贾震,王晓燕.当前常用结核抗体快速检测试剂盒临床使用的对比观察[J].检验医学,2004,19(3):180-184.
[13]费晓峰,吴建鸿,方明娟.ICT结核快速免疫色谱卡对结核病诊断价值探讨[J].中国防痨杂志,2000,22(4):58-59.
[14]Hillemann D,Galle J,Vollmer E.Real-time PCR assay for improved detection of mycobacterium tuberculosis complex in paraffin-embedded tissues[J].Int J Tuberc Lung Dis,2006,10(3):340-342.
[15]沈云华.蛋白芯片技术快速诊断结核病的临床应用[J].当代医学,2009,15(34):87-88.
[16]Boehme C C,Nabeta P,Hillemann D.Rapid molecular detection of tuberculosis and rifampin resistance[J].N Engl J Med,2010,363(11):1005-1015.
[17]He F,Zhao J,Zhang L,Su X.A rapid method for determining mycobacterium tuberculosis based on a bulk acoustic wave impedance biosensor[J].Talanta,2003,59(5):935-941.
[18]刘爱英,孙建方,尹跃平,等.基因芯片技术检测生殖器溃疡性性病病原体[J].中华皮肤科杂志,2004,37(5):19-21.
[19]黄明翔,王琳,张丽水,等.DNA芯片鉴定分枝杆菌的研究[J].中国人兽共患病学报,2010,26(6):555-557.
[20]Mao X,Ma Y,Zhang A,et al.Disposable nucleic acid biosensors based on gold nanoparticle probes and lateral flow strip[J].Anal Chem,2009,81(4):1660-1668.
[21]隗慧林,蒋法兴,徐峰,等.免疫层析法在性传播感染即时诊断中的应用[J].解放军医药杂志,2012,24(4):1-4.
[22]Dineva M A,Candotti D,Fletcher Brown F,et al.Simultaneous visual detection of multiple viral amplicons by dipstick assay[J].J Clin Microbiol,2005,43(8):4015-4021.
[23]Martinez A W,Phillips S T,Whitesides G M.Diagnostics for the developing world:microfluidic paper-based an alytical devices[J].Anal Chem,2010,82(1):3-10.
[24]Lee H,Sun E,Ham D,et al.Chip-NMR biosensor for detection and molecular analysis of cells[J].Nat Med,2008,14(8):869-874.
[25]Lee H,Yoon T J,Weissleder R.Ultrasensitive detection of bacteria using core-shell nanoparticles and an NMR-filter system[J].Angew Chem Int Ed Engl,2009,48(31):5657-5660.
[26]Fang X,Chen H,Xu L,et al.A portable and integrated nucleic acid amplification microfluidic chip for identifying bacteria[J].Lab Chip,2012,12(8):1495-1499.
[27]Kim J H,Yeo W H,Shu Z,et al.Immunosensor towards low-cost,rapid diagnosis of tuberculosis[J].Lab Chip,2012,12(8):1437-1440.
[28]Wang S,Zhao X,Khimji I.Integration of cell phone imaging with microchip ELISA to detect ovarian cancer HE4 biomarker in urine at the point-of-care[J].Lab Chip,2011,11(20):3411-3418.
[29]Breslauer D N,Maamari R N,Switz N A.Mobile phone based clinical microscopy for global health applications[J].PLoS One,2009,4(7):e6320.
[30]Issadore D,Min C,Liong M.Miniature magnetic resonance system for point-of-care diagnostics[J].Lab Chip,2011,11(13):2282-2287.
[31]Singer E.Take TB Meds,Get Mobile Minutes[EB/OL].[2012-06-26].http://www.techn ologyreview.com/news/411618/take-tb-meds-get-mobile-minutes/.
[32]黄祥芬.即时检验(POCT)发展现状与应用[J].中外医学研究,2011(25):154-156.
Progression in Point-of-Care Testing for Tuberculosis
HU Jie1,WANG Lin1,WEI Hui-lin2,WANG Shu-qi3,XU Feng1(1.School of Life Science and Technology,the Key Laboratory of Biomedical Information Engineering of Ministry of Education,Biomedical Engineering and Biomechanics Center,Xi'an Jiaotong University,Xi'an 710049,China;2.Lauren Biotechnology Ltd,Nanjing 210019,China;3.Brigham and Women's Hospital,Harvard Medical School,Cambridge 02139,U.S.A)
Tuberculosis(TB)has caused a significant medical threat to global health,especially in the developing countries.Latent infection,the spread of drug resistance TB strains and poor patient adherence exacerbate the prevention and control of TB around the world.To promote the use of rapid test for detection of infectious diseases,the World Health Organization(WHO)has released a set of guidelines for developing appropriate diagnostic tools,which are affordable,sensitive,specific,user-friendly,rapid and robust,equipment-free,and deliverable.Nevertheless,there is a lack of such diagnostic tools for TB diagnosis.Thus,we here review current research and development of point-of-care testing(POCT)for TB diagnostics to guide further development of TB rapid tests.
Tuberculosis,pulmonary;Diagnostic techniques and procedures;Investigative techniques
R521;R446-39
A
2095-140X(2012)08-0004-06
10.3969/j.issn.2095-140X.2012.08.002
2012-06-27)
国家杰出青年自然科学基金项目(10825210);国家重大国际(地区)合作研究项目(11120101002);国家自然科学基金海外青年学者合作研究基金(31050110125);高等学校学科创新引智计划项目(111计划,B06024);中央高校基本科研业务费专项资金资助
710049西安,西安交通大学生命科学与技术学院,生物医学信息工程教育部重点实验室,生物医学工程和生物力学中心(胡杰、王琳、徐峰);210019南京,罗润生物科技有限公司(隗慧林);02139 Cambridge,Brigham and Women's Hospital,Harvard Medical School.U.S.A(王书崎)
徐峰,E-mail:fengxu@mail.xjtu.edu.cn;王书崎,E-mail:shuqi.wang@cantab.net
