复方青花颗粒微生物限度检查方法的验证
2012-09-06杜凤霞刘峰群张诗龙周燕萍凌海慧
杜凤霞,刘峰群,张诗龙,周燕萍,周 旭,凌海慧
复方青花颗粒微生物限度检查方法的验证
杜凤霞,刘峰群,张诗龙,周燕萍,周 旭,凌海慧
目的 建立复方青花颗粒的微生物限度检查方法,并对其进行验证。方法 采用2010年版《中华人民共和国药典》(一部)附录“微生物限度检查法”项下相关内容进行方法学验证,采用培养基法。结果 试验组5株试验菌回收率均>70.00%,控制菌检查阳性菌生长良好,阴性对照组未检出大肠杆菌,符合验证要求。结论 复方青花颗粒微生物限度可以采用常规法检查。
复方青花颗粒;集落计数,微生物;阈限值
复方青花颗粒是我院抗流感特色中药复方制剂,其处方主要由大青叶、金银花、薄荷、甘草4味药材组成,具有清热解毒、宣肺利咽、散风祛邪的功能,主要适用于流行性感冒属风热毒邪者。其中,本品所含主要药味大青叶、金银花、薄荷和甘草对金黄色葡萄球菌、大肠杆菌、枯草芽孢杆菌等有一定的抑制作用[1-4]。为控制复方青花颗粒的质量,我们对本品的质量标准进行了研究[5],根据2010年版《中华人民共和国药典》的相关规定[6],为真实反映本品的污染情况,建立复方青花颗粒的微生物限度检查方法并对其进行验证。
1 仪器与试药
1.1 仪器 SFG电热恒温鼓风干燥箱(黄石市恒丰医疗器械有限公司);SPX-250B-Z型生化培养箱(上海博迅实业有限公司医疗设备厂);XG1UK脉动真空灭菌器(山东新华医疗器械股份有限公司);HZSH水浴振荡器(哈尔滨市东联电子技术开发有限公司)。
1.2 菌种 大肠埃希菌CMCC(B)44102,枯草芽孢杆菌CMCC(B)63501,金黄色葡萄球菌 CMCC(B)26003,黑曲霉 CMCC(F)98003,白色念珠菌CMCC(F)98001,均购于中国药品生物制品检定所。
1.3 培养基及稀释剂 营养琼脂培养基、营养肉汤培养基、玫瑰红钠琼脂培养基、改良马丁培养基、胆盐乳糖培养基(BL)、4-甲基伞形酮葡糖苷酸(MUG)培养基、改良马丁琼脂培养基、曙红亚甲蓝琼脂培养基(EMB)均购自中国药品生物制品检定所;pH 7.0无菌氯化钠-蛋白胨缓冲液,按2010年版《中华人民共和国药典》(一部)附录方法配制,0.9%无菌氯化钠溶液(10 ml/支、250 ml/袋,自302医院住院药房请领)。
1.4 供试品 复方青花颗粒(规格:5 g/袋,批号:090705、090706、090707,解放军 302 医院药学部制剂室),经外观、粒度、干燥失重、溶化性、装量差异等检查项目检查合格,并采用高效液相色谱法测定其绿原酸的含量在标准范围内。
2 细菌数、霉菌和酵母菌数测定方法的建立与验证
2.1 制备菌液 ①取经32~35℃培养24 h的金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌的营养肉汤培养物各1 ml,用0.9%氯化钠溶液10倍稀释至10-5~10-7,使其成含菌数为 50 ~100 cfu/ml的菌悬液,做活菌计数后备用。②取经25~28℃培养24 h的白色念珠菌的改良马丁培养物1 ml,用0.9%无菌氯化钠溶液10倍递增稀释成含菌数为50~100 cfu/ml的菌悬液,做活菌计数后备用。③取经25~28℃培养1周的黑曲霉的改良马丁琼脂斜面培养物,用0.9%氯化钠溶液5 ml洗下黑曲霉孢子,吸出孢子悬液1 ml,加0.9%无菌氯化钠溶液适量,稀释至与标准比浊管浊度相当的孢子悬液,取此孢子悬液1 ml,用0.9%无菌氯化钠溶液10倍递增稀释至10-4~10-5,使其成为含菌数为 50 ~100 cfu/ml的菌悬液,做活菌计数后备用[6]。④以上各菌悬液或孢子悬液同时各取2份分别注入琼脂培养基培养,采用平皿计数法计数活菌,结果见表1。
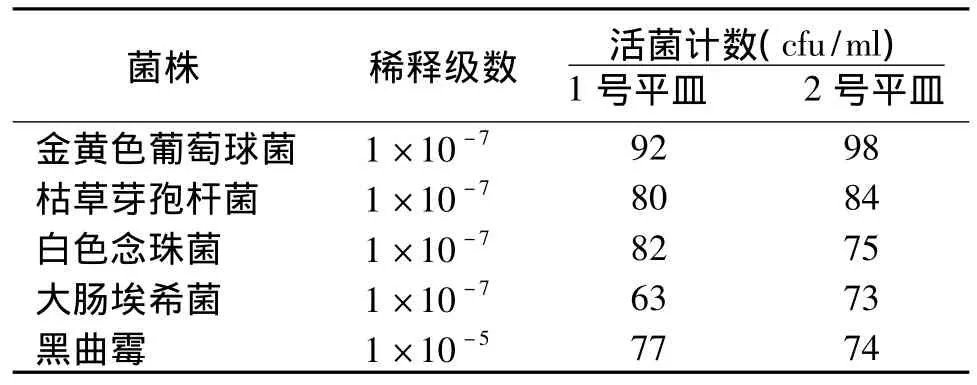
表1 各菌悬液或孢子悬液微生物检查活菌计数
2.2 制备供试液 随机抽取本样品10袋,将内容物研细,称取样品10 g,加入45℃ pH 7.0的无菌氯化钠-蛋白胨缓冲液100 ml,振摇,使其均匀分散,即得1∶10供试液,取此供试液1 ml,加pH 7.0的无菌氯化钠-蛋白胨缓冲液使其成10 ml,摇匀,即得1∶100供试液。
2.3 测定回收率 试验组:采用平皿法,各取供试液(1∶10)和实验菌液1 ml,分别平行注入2个平皿,立即加入相应培养基,待凝固后,置规定温度培养48~72 h,按菌落计数方法测定其菌落数。菌液组:测定每一种菌株所加的实验菌数。供试品对照组(常规法):取供试液(1∶10)1 ml注入平皿,立即加入规定的琼脂培养基,待凝固后,置规定温度培养24~72 h,逐日观察结果,作为供试品本底菌数。稀释剂对照组:用相应稀释剂代替供试液加入实验菌,使菌液的最终浓度为50~100 cfu/ml,按试验组方法进行菌落计数。试验组的加菌回收率(%)=(试验组的平均菌落数-供试品对照组平均菌落数)/菌液组的平均菌落数×100%。本研究供试品接种至5株阳性代表试验菌株,利用常规法测定,结果表明5株阳性试验菌的回收率均在70.00%以上(表2),提示本供试品无抑菌活性,故细菌、霉菌及酵母菌计数均可采用常规法进行测定。

表2 5株阳性试验菌活菌计数验证回收试验结果
2.4 控制菌检查方法的验证
2.4.1 选择菌种:复方青花颗粒属于不含药材原粉的中药口服固体颗粒制剂,按照2010年版《中华人民共和国药典》(一部)附录规定微生物限度检查法中有关控制菌检查方法[6],应检查大肠埃希菌。
2.4.2 制备菌液和供试液:菌液按2.1项下方法制备,菌数控制在10~100 cfu/ml。供试液按2.2项下方法制备。
2.4.3 验证方法和结果:取胆盐乳糖培养基100 ml各6份,2份分别加入10 ml供试液(1∶10)及1 ml 10~100 cfu/ml大肠埃希菌悬液作为实验组,2份分别加入1 ml 10~100 cfu/ml大肠埃希菌悬液作为阳性对照组,余2份分别加入稀释剂10 ml作为阴性对照组,均在33~35℃培养24 h。取上述各培养物0.2 ml,接种至含5 ml MUG培养基的试管内进行培养,分别于5、24 h时在波长366 nm的紫外光下观察,同时用未接种的MUG培养基作本底对照,依据参考文献[6]微生物限度检查方法进行判定,结果显示,控制菌检查阳性菌生长良好,阴性对照组未检出菌(表3)。

表3 各组控制菌检查方法验证结果
2.4.4 样品控制菌检查:3批供试品1∶10的供试液各10 ml,分别接种至100 ml胆盐乳糖培养基中;另取含大肠杆菌数为10~100 cfu/ml菌悬液1 ml、pH 7.0无菌氯化钠-蛋白胨缓冲液10 ml分别接种至同样培养基中作为阳性对照和阴性对照。按2.4.3项下方法操作,结果表明,3批供试品均未检出大肠杆菌,符合规定,而阳性对照组检出大肠杆菌。
3 讨论
通过以上验证,我们认为复方青花颗粒微生物限度检查方法可参考以下程序:取供试品10 g,加入45℃、pH 7.0无菌氯化钠-蛋白胨缓冲液100 ml,振摇,使其分散均匀,得1∶10供试液;取1∶10供试液1 ml,加pH 7.0无菌氯化钠-蛋白胨缓冲液使其成10 ml,摇匀,得1∶100供试液。采用常规法测定细菌、真菌及酵母菌总数;另取本品采用常规法检查控制菌。细菌、真菌及酵母菌数≤100 cfu/ml;金黄色葡萄球菌、铜绿假单胞菌应不得检出。
根据2010年版《中华人民共和国药典》收载的方法对常规法和培养基稀释法进行细菌、霉菌和酵母菌计数方法验证,结果表明按常规法和培养基稀释法测定的5种试验菌回收率均>70.00%,提示本品对细菌、霉菌和酵母菌无抑制作用,均符合2010年版《中华人民共和国药典》中方法学验证规定,因此,采用常规法检查复方青花颗粒微生物限度可行。
综上所述,在复方青花颗粒微生物限度检查中细菌、霉菌和酵母菌计数制备菌液尤其重要。菌液中含有菌落数的多少直接影响其检查误差。因此需要通过反复多次试验,摸索出接种环刮取菌苔的量及稀释菌液的经验方法,在菌液制备后,同时进行活菌计数和供试品的方法验证,这样才能将菌落数控制在50~100 cfu/ml。此外,在进行3次独立平行试验时,3次试验的菌原液浓度应尽量保持一致,除黑曲霉孢子悬液外,其他试验菌菌悬液最好现用现配,这样才能保证验证结果准确可靠。
[1]赵良忠,蒋贤育,段林东,等.金银花水溶性抗菌物质的提取及其抑菌效果研究[J].中国生物制品学杂志,2006,19(2):201-203.
[2]张连同,邱世翠,吕俊华,等.大青叶体外抑菌作用研究[J].时珍国医国药,2002,13(5):283-284.
[3]刘锐,莫倩美.薄荷水提取物抑菌活性的研究[J].农业机械,2011(10):166-169.
[4]丁长玲,邱世翠,宫照龙,等.甘草的体外抑菌作用研究[J].时珍国医国药,2002,13(9):518.
[5]杜凤霞,刘峰群,周旭,等.复方青花颗粒质量标准的研究[J].解放军药学学报,2010,26(4):304-306.
[6]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:79-88.
Verification of Microbial Limit in Testing Compound Recipe Qinghua Granule
DU Feng-xia,LIU Feng-qun,ZAHNG Shi-long,ZHOU Yan-ping,ZHOU Xu,LING Hai-hui(Department of Pharmacy,the 302ndHospital of PLA,Beijing 100039,China)
Objective To establish a testing method of microbial limit for compound recipe Qinghua granule and validate it.Methods The testing method was jerqued by culture media under the guidance of the microbial limit test,which is described in the appendix of China Pharmacopoeia(2010 edition,VolumeⅠ).Results The coefficient of recovery of the test organism in 5 stubs was higher than 70.00%,positive bacteria growed well in control bacteria,and no escherichiacoli was found in the negative control group.Conclusion Routine testing method is useful in microbial limit test for compound recipe Qinghua granule.
Compound recipe Qinghua granule;Colony count,microbial;Threshold limit values
R927.33
A
2095-140X(2012)08-0050-03
10.3969/j.issn.2095-140X.2012.08.015
2012-04-27 修回时间:2012-05-09)
100039北京,解放军302医院药学部
刘峰群,电话:13691157302
