“糖脂康”对大鼠天喂养实验研究
2012-05-08左绍远钱金栿
左绍远,钱金栿
(1.大理学院基础医学院,云南大理 671000;2.大理学院药学与化学学院,云南大理 671000)
左绍远1,钱金栿2
(1.大理学院基础医学院,云南大理 671000;2.大理学院药学与化学学院,云南大理 671000)
目的:观察功能性食品“糖脂康”的安全性。方法:选用健康断乳SD大鼠为受试对象,随机分为4组。分别以1 875、3 750、7 500 mg/kg.BW剂量的糖脂康样品掺入基础饲料中喂养,对照组则给予基础饲料,连续30 d后检测相应指标。结果:试验期间及实验结束时,各剂量组动物体重增长、食物利用率、血常规、血生化指标及脏体系数均在正常范围内,与对照组比较,差异均无显著性(P>0.05);病理组织学检查表明各实验组大鼠肝、肾、胃、肠、脾、睾丸和卵巢等组织均未见有病理改变。结论:糖脂康对大鼠的生长、发育、代谢及脏器无急性不良影响,在本实验剂量范围内,无短期毒副作用。
糖脂康;毒理学安全性评价;大鼠;30天喂养实验
糖脂康是大理学院研究开发的纯天然功能性食品,具有调节血糖、血脂,增强机体免疫力等功效〔1-4〕。为观察该产品的安全性,我们对糖脂康进行了大鼠30 d短期喂养实验研究,以期为该产品的安全性毒理学评价提供实验依据。
1 材料和方法
1.1 受试样品“糖脂康”,由大理学院“糖脂康”研究组提供,样品批号:20050520。样品性状:片剂,瓶装(0.3 g×50片/瓶)。人体推荐剂量为每天净含量4 500 mg(75 mg/kg.BW)。
1.2 试验动物与试验环境清洁级断乳SD大鼠,体重68.8~118.5 g,雌雄各半。由云南生物制药有限公司提供(合格证号:滇实动证第2004013号);饲料由云南生物制药有限公司提供(合格证号:SCXK(滇)2005—0007)。实验环境为温度18.01~23.65℃,相对湿度43.37%~59.35%〔5〕。
1.3 试验方法参照卫生部GB15193-2003“食品安全性毒理学评价程序和方法”及相关文献进行〔6-10〕。大鼠适应性喂养2 d后,按体重随机分为4组,每组20只。设空白对照组和糖脂康样品低、中、高3个剂量组。糖脂康样品受试剂量为1 875、3 750、7 500 mg/ kg.BW(相当于人体推荐剂量的25倍、50倍、100倍),采用掺入饲料法,以喂饲方式给予受试物。空白对照组则喂饲基础饲料。每只大鼠单笼喂养,自由摄食饮水,每周称一次体重,并根据体重调整给样品量,连续30 d,第31天处死动物,取血作血常规和生化指示检测,取主要脏器测定脏体系数及做病理组织学检查。实验结果用SPSS13.0统计软件进行方差分析,结果以表示。检验水准α=0.05。
2 观察及检测指标
2.1 大鼠生长状况、体重及食物利用率观察活动、进食饮水、大小便情况,计算体重、增重、进食量及食物利用率。
2.2 血液学及血液生化指标血红蛋白(Hb)、红细胞计数(RBC)、白细胞计数(WBC)及分类、血小板计数(PLT)。血糖(GLU)、甘油三酯(TG)、总胆固醇(TC)、总蛋白(TP)、白蛋白(ALB)、谷丙转氨酶(ALT)、谷草转氨酶(AST)、尿素氮(BUN)、肌酐(CRE)〔11〕。
2.3 主要脏器病理学检查肉眼观察试验动物主要脏器病理改变,并对肝、肾、脾、胃、十二指肠、结肠、睾丸、卵巢进行病理组织学切片检查;对肝、肾、脾、睾丸、卵巢进行脏体系数值测定,计算脏体系数(脏器/体重×100%)〔12〕。
3 实验结果
3.1 对一般状况、体重及食物利用率的影响结果表明:试验期间各组大鼠生长发育良好,行为活动、精神状况、毛色、进食饮水及大小便正常。在实验期间及实验30 d结束时,各剂量组与对照组之间、各剂量组之间比较,体重增长和食物利用率等差异无统计学意义(P>0.05)。见表1。
表1 糖脂康30d喂养对大鼠体重增长和食物利用率的影响(

表1 糖脂康30d喂养对大鼠体重增长和食物利用率的影响(
体重/g性别 剂量组/(mg/kg.BW)动物/ n 始 重 终体重 总增重量总进食量/g 食物利用率/ %雄雌0.0 1 875 3 750 7 500 0.0 1 875 3 750 7 500 20 96.75±11.36 257.62±28.23 160.87±26.42 639.60±92.24 25.20±2.38 20 98.08±12.66 268.63±27.61 170.55±21.30 620.24±67.50 25.41±1.25 20 97.32±12.02 263.46±31.15 162.14±28.20 646.78±72.85 24.81±2.25 20 97.79±12.18 259.58±45.37 161.79±39.54 625.77±98.66 26.06±4.54 20 91.63±10.42 190.70±18.17 99.07±14.21 563.60±41.84 17.62±2.48 20 91.39±7.82 181.92±13.84 90.53±18.47 546.67±38.28 16.66±3.88 20 90.47±6.80 188.08±14.37 97.61±11.13 580.54±52.37 16.84±1.49 20 90.91±8.13 190.00±16.36 99.75±18.42 550.66±41.20 18.13±3.28
3.2 对大鼠血常规的影响结果表明,各实验组Hb、RBC、WBC及分类(LYM:淋巴细胞,GRAN:中性粒细胞,MONO:单核细胞),与对照组比较,差异无统计学意义(P>0.05)。见表2。
表2 糖脂康30d喂养对大鼠血常规指标的影响(
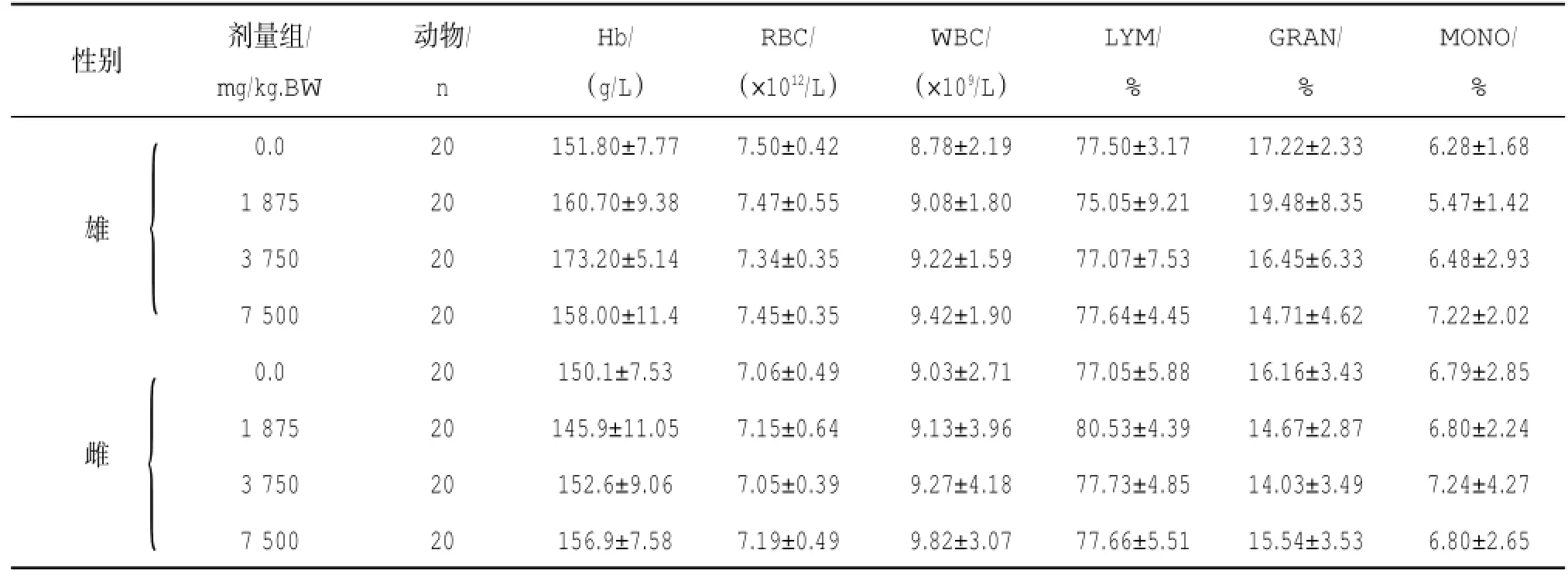
表2 糖脂康30d喂养对大鼠血常规指标的影响(
性别 动物/ n RBC/(×1012/L)WBC/(×109/L)LYM/ % GRAN/ %雄雌剂量组/ mg/kg.BW 0.0 1 875 3 750 7 500 0.0 1 875 3 750 7 500 MONO/ % 20 151.80±7.77 7.50±0.42 8.78±2.19 77.50±3.17 17.22±2.33 6.28±1.68 20 160.70±9.38 7.47±0.55 9.08±1.80 75.05±9.21 19.48±8.35 5.47±1.42 20 173.20±5.14 7.34±0.35 9.22±1.59 77.07±7.53 16.45±6.33 6.48±2.93 20 158.00±11.4 7.45±0.35 9.42±1.90 77.64±4.45 14.71±4.62 7.22±2.02 20 150.1±7.53 7.06±0.49 9.03±2.71 77.05±5.88 16.16±3.43 6.79±2.85 20 145.9±11.05 7.15±0.64 9.13±3.96 80.53±4.39 14.67±2.87 6.80±2.24 20 152.6±9.06 7.05±0.39 9.27±4.18 77.73±4.85 14.03±3.49 7.24±4.27 20 156.9±7.58 7.19±0.49 9.82±3.07 77.66±5.51 15.54±3.53 6.80±2.65 Hb/(g/L)
3.3 对大鼠血生化指标的影响见表3-1、表3-2。
表3-1 糖脂康30d喂养对大鼠血液生化指标的影响

表3-1 糖脂康30d喂养对大鼠血液生化指标的影响
性别 动物/ n ALT/(IU/L)剂量组/(mg/kg.BW)0.0 1 875 3 750 7 500 0.0 1 875 3 750 7 500 TP/(g/L)AST/(IU/L)Alb/(g/L)BUN/(mmol/L)雄雌Cr/(μmol/L)20 156.49±46.77 30.86±7.12 70.69±6.88 44.86±3.08 7.26±1.28 67.21±12.69 20 138.88±23.63 27.19±2.00 74.19±8.70 48.47±1.61 7.11±1.08 66.16±10.53 20 139.76±20.28 26.78±4.00 77.57±4.63 52.20±1.15 6.70±1.39 67.96±12.58 20 134.22±34.32 26.68±9.02 80.51±5.91 54.36±1.65 7.16±0.82 65.10±9.88 20 148.65±37.35 28.11±4.46 68.23±7.10 34.84±2.66 8.26±1.38 65.61±14.88 20 134.05±22.35 25.20±4.11 73.05±6.91 35.93±2.43 8.24±1.09 63.81±8.79 20 137.70±21.96 26.17±4.56 75.56±4.84 36.27±2.32 8.14±1.75 64.72±11.19 20 140.46±25.54 27.40±5.86 78.08±7.72 36.18±2.43 8.23±1.61 65.89±10.62
表3-2 糖脂康30d喂养对大鼠血液生化指标的影响

表3-2 糖脂康30d喂养对大鼠血液生化指标的影响
注:与对照组相比,*P<0.05。
性别 动物/ n TC/(mmol/L)雄雌剂量组/(mg/kg.BW)0.0 1 875 3 750 7 500 0.0 1 875 3 750 7 500 Glu/(mmol/L)20 0.56±0.14 2.26±0.33 5.64±0.52 20 0.54±0.16 1.41±0.31* 5.58±0.79 20 0.53±0.13 1.52±0.19* 5.36±0.78 20 0.52±0.11 1.42±0.24* 5.31±0.71* 20 0.57±0.09 2.15±0.69 5.63±0.44 20 0.55±0.18 1.63±0.41* 5.47±0.51 20 0.54±0.16 1.57±0.26* 5.32±0.55 20 0.53±0.09 1.55±0.42* 4.87±0.34* TG/(mmol/L)
从表3-1可见,与对照组相比,雄性、雌性的糖脂康高、中、低各剂量组的AST、ALT、TP、Alb、BUN、Cr等指标差异均无统计学意义(P>0.05)。而从表3-2可见,与对照组相比,雄性、雌性的糖脂康各剂量组的甘油三酯(TG)有所降低,但差异无统计意义(P>0.05)。而雄性、雌性的糖脂康各剂量组总胆固醇均低于对照组,差异有统计学意义(P<0.05),提示糖脂康可降低正常小鼠血清胆固醇含量,但无明显的剂量效应关系。雄性、雌性的糖脂康高剂量组的血糖含量低于对照组,差异有统计学意义(P<0.05),提示高剂量的糖脂康可能具有降低正常小鼠空腹血糖的作用。但中、低剂量组血糖含量与对照组相比差异无统计学意义(P>0.05)。
3.4 病理组织学检查对全部实验动物进行大体肉眼解剖检查,未发现异常,主要脏器肝、肾、脾、胃、十二指肠、结肠、睾丸、子宫、卵巢进行病理组织学切片检查,均未发现病变。
3.5 对大鼠主要脏器系数的影响各剂量肝体系数、肾体系数、脾体系数、睾体系数、卵体系数与阴性对照组比较,差异均无统计学意义(P>0.05)。见表4。
4 讨论
本实验以1 875、3 750、7 500 mg/kg.BW剂量(相当于人体推荐剂量的25、50、100倍)的糖脂康喂饲大鼠30 d,结果显示:受试物对动物体重增长、食物利用率无不良影响,各组动物生长发育良好。表明受试物对大鼠的正常生长发育和食物的吸收、代谢无明显影响。除糖脂康各剂量组总胆固醇明显低于对照组(P<0.05)、糖脂康高剂量组的血糖含量明显低于对照组外(P<0.05)外,其余各剂量组的血常规、血生化各项指标与对照组相比差异均无统计学意义,各剂量组动物脏体系数无异常,病理组织学检查,被检脏器均未见有病理改变。综上所述,30 d短期喂养实验结果表明:与阴性对照组相比,糖脂康对大鼠生长发育、代谢无不良影响。血常规、生化指标、脏体系数及病理检查均未见异常,表明在本实验剂量范围内,糖脂康对受试动物无短期毒副作用。有关糖脂康的经口急性毒性试验及Ames试验、小鼠骨髓微核试验、小鼠精子畸形试验研究将另文报道。
表4 糖脂康30d喂养对大鼠脏器系数的影响(

表4 糖脂康30d喂养对大鼠脏器系数的影响(
性别 动物/ n 肝体系数/% 脾体系数/% 肾体系数/% 睾体系数/% 卵体系数/%雄雌剂量组/(mg/kg.BW)0.0 1 875 3 750 7 500 0.0 1 875 3 750 7 500 20 3.06±0.90 0.25±0.05 0.74±0.09 1.04±0.09 -20 3.00±0.59 0.21±0.03 0.74±0.09 1.05±0.20 -20 2.99±1.13 0.27±0.08 0.72±0.05 1.07±0.09 -20 3.05±1.58 0.26±0.05 0.74±0.04 1.11±0.16 -20 3.01±0.60 0.25±0.05 0.72±0.09 - 0.058±0.02 20 3.16±0.42 0.27±0.06 0.75±0.07 - 0.054±0.03 20 3.13±0.38 0.28±0.07 0.77±0.07 - 0.056±0.03 20 3.11±0.59 0.25±0.04 0.76±0.08 - 0.062±0.06
本实验在云南省疾病预防控制中心协助下完成,特此致谢。
〔1〕熊伟,左绍远.“糖脂康”多糖对人乳腺癌Mcf-7细胞生长和细胞周期的影响〔J〕.大理学院学报,2010,9(6):19-21.
〔2〕左绍远,钱金栿.糖脂康抗糖尿病作用实验研究〔J〕.时珍国医国药,2011,22(9):2200-2201.
〔3〕左绍远,钱金栿,万顺康.螺旋藻多糖降血糖活性实验研究〔J〕.时珍国医国药,2000,11(8):677-678
〔4〕王芬,何华亮,刘铜华.抗糖尿病中药活性成分及其作用机制的研究进展〔J〕.时珍国医国药,2008,19(3):799-768.
〔5〕卫生部药政司.中药新药毒理学研究指南〔M〕.北京:人民卫生出版社,1993:75-79.
〔6〕中国国家标准汇编.GB15193-2003食品安全性毒理评价程序和方法〔S〕.北京:中国标准出版社,2004:17-55.
〔7〕中华人民共和国卫生部.GB15193.1保健食品检验与评价技术规范〔S〕.北京:中国标准出版社,2003:85-90.
〔8〕叶会呈,蔡宇.益髓胶囊的毒理安全性试验〔J〕.毒理学杂志,2009,23(2):173-174.
〔9〕邹文玮,张维民,夏芝璐,等.姜蒜精华素安全性实验研究〔J〕.2010,28(3):245-246.
〔10〕袁伯俊,王治乔.新药临床前安全性评价与实践〔M〕.北京:军事医学科学出版社,1997:78-107.
〔11〕李然,刘晓红,孔天,等.姜黄素的安全性毒理学评价〔J〕.卫生研究,2011(6):67-68.
〔12〕王茵,楼正清,来伟旗,等.SD大鼠血液生化指标正常参考值范围的探讨〔J〕.卫生毒理学杂志,2000(2):52-54.
(责任编辑 董 杰)
Study on 30-Days of Tangzhikang Tablets Feeding in SD Rats
ZUO Shaoyuan1,QIAN Jinfu2
(1.Pre-clinical College,Dali University,Dali,Yunnan 671000,China; 2.College of Pharmacy and Chemistry,Dali University,Dali,Yunnan 671000,China)
Objective:To observe the toxicological safety on functional food of Tangzhikang tablets.Methods:The SD ablactated rats were randomly divided into four groups.The control group was fed with basic diet.Three experimental groups were fed with basic diet mixed with Tangzhikang tablets with the dose of 1 875,3 750 and 7 500 mg/kg on body weight for 30 days,respectively.The corresponding indexes of each group were measured.Results:During and at the end of the experiment,the body weight,food utilization rate,full blood count,blood biochemistry,and organ/body weigh ratios had no significant differences among the four groups. Furthermore,the histopathological examination showed that there were no significant changes in liver,kidney,stomach,intestines, spleen,testicle and ovary among the 4 groups.Conclusion:Tangzhikang tablet has no acute toxic effect and is a safe functional food on rats'growth,development,metabolism and viscera organs.
Tangzhikang tablets;toxicological safety assessment;rat;30-day feeding study
R285.5
A
1672-2345(2012)06-0026-04
云南省科技厅科技计划基金资助项目(GX10-2004)
2012-04-30
左绍远,教授,主要从事生化药理学研究.
