偏瘫康胶囊的质量标准研究
2012-05-03江南
江南
(湖南衡阳市中医医院,湖南 衡阳421001)
偏瘫康胶囊的质量标准研究
江南
(湖南衡阳市中医医院,湖南 衡阳421001)
目的:建立偏瘫康胶囊的质量标准。方法:采用薄层色谱法(TLC)对处方中的石菖蒲、丹参、赤芍、郁金、冰片进行定性鉴别;采用高效液相色谱法测定制剂中丹参酮ⅡA和丹酚酸B的含量。结果:TLC法可检出石菖蒲、丹参、赤芍、郁金、冰片的特征斑点;丹参酮ⅡA的线性范围为0.032~0.32 μg(r=0.999 9),平均回收率为99.28%(RSD=1.37%,n=6);丹酚酸B的线性范围为0.56~5.6 μg(r=0.999 9),平均回收率为99.02%(RSD= 1.74%,n=6)。结论:该质量标准可有效控制偏瘫康胶囊的质量。
偏瘫康胶囊;质量标准;薄层色谱法;高效液相色谱法
偏瘫康胶囊是由石菖蒲、丹参、赤芍、郁金、冰片等9味中药制成的复方制剂,具有活血化痰、祛瘀通络的功效。用于缺血性中风后遗症,痰瘀阻络,症见肢体偏瘫、语言蹇涩、舌唇紫暗、苔滑腻等。为保证偏瘫康胶囊的质量,本研究采用薄层色谱法(TLC)对方中石菖蒲、丹参、赤芍、郁金、冰片进行了定性鉴别,并采用高效液相色谱法(HPLC)对方中丹参的主要有效成分丹参酮ⅡA和丹酚酸B进行了含量测定。
1 仪器与试药
1.1 仪器
LC-20AT高效液相色谱仪 (日本岛津公司),SPD-20AVP紫外检测器 (日本岛津公司),N2000色谱工作站(浙江大学智能信息工程研究所)。
1.2 试药
偏瘫康胶囊及阴性样品 (衡阳市中医医院制剂室);石菖蒲对照药材、丹参对照药材、赤芍对照药材、郁金对照药材、丹参酮ⅡA对照品、丹酚酸B对照品、芍药苷对照品、冰片对照品(原中国药品生物制品检定所);硅胶G(青岛海洋化工厂);甲醇、乙腈为色谱纯,水为重蒸馏水,其他试剂均为分析纯。
2 定性鉴别
2.1 石菖蒲的鉴别[1-3]
取偏瘫康胶囊(以下简称胶囊)内容物0.4 g,加石油醚(60~ 90℃)20 mL,加热回流1 h,滤过,滤液蒸干,残渣加石油醚(60~ 90℃)1 mL使溶解,作为供试品溶液。另取石菖蒲对照药材0.2 g,同法制成对照药材溶液。再取缺石菖蒲的阴性样品,同法制成阴性溶液。照TLC(中国药典2010年版一部附录ⅥB)试验,吸取上述3种溶液各2 μL,分别点于同一硅胶G薄层板上,以石油醚(60~ 90℃)-乙酸乙酯(4∶1)为展开剂,展开,取出,晾干,放置约 1 h,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性无干扰。见图1。

图1 石菖蒲薄层色谱1石菖蒲对照药材 2偏瘫康胶囊 3缺石菖蒲的阴性样品注:T,实验时外周环境的温度;RH,相对湿度(下同)
2.2 丹参的鉴别[1,4]
取胶囊内容物1 g,加乙酸乙酯20 mL,超声处理30 min,滤过,滤液蒸干,残渣加乙酸乙酯 1 mL使溶解,作为供试品溶液。另取丹参对照药材1 g,同法制成对照药材溶液。另取丹参酮ⅡA对照品,加乙酸乙酯制成每1 mL中含2 mg的溶液,作为对照品溶液。再取缺丹参的阴性样品,同法制成阴性溶液。照TLC(中国药典2010年版一部附录ⅥB)试验,吸取上述4种溶液各 5 μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯(19∶1)为展开剂,展开,取出,晾干。供试品色谱中,在与对照药材色谱及对照品色谱相应位置上,显相同颜色的斑点,阴性无干扰。见图2。
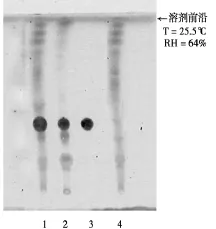
图2 丹参薄层色谱1偏瘫康胶囊 2丹参对照药材 3丹参酮ⅡA对照品 4缺丹参的阴性样品
2.3 赤芍的鉴别[1,4-5]
取胶囊内容物3g,加水20mL,超声处理10min,滤过,滤液加乙醚15 mL,振摇提取,弃去乙醚液,水液加水饱和的正丁醇15 mL,振摇提取,正丁醇液蒸干,残渣加乙醇 1 mL使溶解,作为供试品溶液。另取赤芍对照药材0.5 g,加乙醇10 mL,超声处理5 min,滤过,滤液蒸干,残渣加乙醇 1 mL使溶解,作为对照药材溶液。另取芍药苷对照品,加乙醇制成每 1 mL含 2 mg的溶液,作为对照品溶液。再取缺赤芍的阴性样品,同法制成阴性溶液。照TLC(中国药典2010年版一部附录ⅥB)试验,吸取上述4种溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以 5%香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照药材色谱及对照品色谱相应的位置上,显相同颜色的斑点,阴性无干扰。见图3。
2.4 郁金的鉴别[1-2]

图3 赤芍薄层色谱1芍药苷对照品2偏瘫康胶囊3赤芍对照药材4缺赤芍的阴性样品
取胶囊内容物 4 g,加无水乙醇 50 mL,超声处理 30 min,滤过,滤液蒸干,残渣加乙醇 1 mL使溶解,作为供试品溶液。另取郁金对照药材2 g,同法制成对照药材溶液。再取缺郁金的阴性样品,同法制成阴性溶液。照TLC(中国药典2010年版一部附录ⅥB)试验,吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以正己烷-乙酸乙酯 (17∶3)为展开剂,预饱和30 min,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应位置上,显相同颜色的斑点,阴性无干扰。见图4。
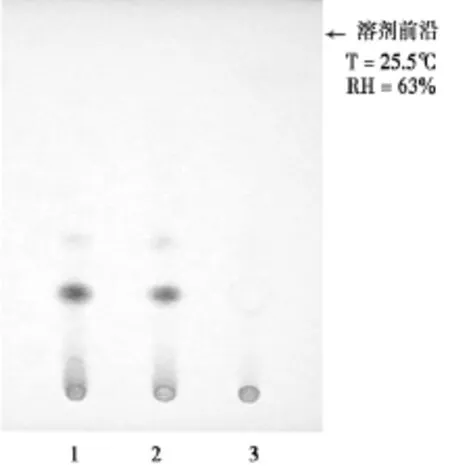
图4 郁金薄层色谱1偏瘫康胶囊 2郁金对照药材 3缺郁金的阴性样品
2.5 冰片的鉴别[1,6-7]
取胶囊内容物1 g,加乙醚15 mL,超声处理15 min,滤过,滤液挥干,残渣加乙酸乙酯2 mL使溶解,作为供试品溶液。另取冰片对照品,加乙酸乙酯制成每1 mL含2 mg的溶液,作为对照品溶液。再取缺冰片的阴性样品,同法制成阴性溶液。照TLC(中国药典2010年版一部附录ⅥB)试验,吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯(9∶1)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,阴性无干扰。见图5。

图5 冰片薄层色谱图1冰片对照品 2偏瘫康胶囊 3缺冰片的阴性样品
3 含量测定
3.1 色谱条件
3.1.1 丹参酮ⅡA色谱条件[8-10]色谱柱Kromasil C18(4.6 mm×150 mm,5 μm),柱温 25℃,流动相甲醇 -水 (75∶25),流速 1.0 mL/min,检测波长270 nm。理论板数按丹参酮ⅡA峰计算应不低于2 000。
3.1.2 丹酚酸B色谱条件[8-10]色谱柱Kromasil C18(4.6 mm×150 mm,5 μm),柱温 25℃,流动相甲醇-乙腈-甲酸-水(30∶10∶1∶59),流速 1.0 mL/min,检测波长286 nm。理论板数按丹酚酸B峰计算应不低于2 000。
3.2 对照品溶液的制备
3.2.1 丹参酮ⅡA对照品溶液的制备 取丹参酮ⅡA对照品适量,精密称定,置棕色量瓶中,加甲醇制成每1 mL含0.016 mg丹参酮ⅡA的溶液,即得。
3.2.2 丹酚酸B对照品溶液的制备 取丹酚酸B对照品适量,精密称定,加75%甲醇制成每1 mL含0.28 mg丹酚酸B的溶液,即得。
3.3 供试品溶液的制备
3.3.1 丹参酮ⅡA供试品溶液的制备 取胶囊内容物0.3 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定重量,加热回流1 h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
3.3.2 丹酚酸B供试品溶液的制备 取胶囊内容物 0.2 g,精密称定,置具塞锥形瓶中,精密加入75%甲醇50 mL,称定重量,加热回流1 h,放冷,再称定重量,用75%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
3.4 阴性溶液的制备
取缺丹参的阴性样品,分别按3.3.1和3.3.2项下方法制备,即得。
3.5 系统适用性实验
3.5.1 丹参酮ⅡA系统适用性试验 分别精密吸取丹参酮ⅡA对照品溶液、供试品溶液、阴性溶液各5 μL注入高效液相色谱仪,测定,见图6~8。丹参酮ⅡA保留时间约为32.5 min,与其他组分分离良好(分离度 >1.5),阴性溶液色谱图在丹参酮ⅡA峰位置无干扰。
3.5.2 丹酚酸B系统适用性实验 分别精密吸取丹酚酸B对照品溶液、供试品溶液、阴性溶液各10 μL注入高效液相色谱仪,测定,见图9~ 11。丹酚酸B保留时间约为22 min,与其他组分分离良好(分离度>1.5),阴性溶液色谱图在丹酚酸B峰位置无干扰。

图6 丹参酮ⅡA对照品色谱

图7 丹参酮供试品色谱

图8 缺丹参阴性色谱

图9 丹酚酸B对照品色谱

图10 丹酚酸B供试品色谱

图11 缺丹参阴性色谱
3.6 线性关系考察
3.6.1 丹参酮ⅡA线性关系考察 精密吸取丹参酮ⅡA对照品溶液 2、8、10、12、16、20 μL进样,按拟定色谱条件测定峰面积,以对照品进样量X(μg)为横坐标、峰面积值Y(mv)为纵坐标,进行线性回归,丹参酮ⅡA回归方程

r=0.999 9,线性范围为0.032~0.32 μg。
3.6.2 丹酚酸B线性关系考察 精密吸取丹酚酸B对照品溶液 2、8、10、12、16、20 μL进样,按拟定色谱条件测定峰面积,以对照品进样量X(μg)为横坐标、峰面积值 Y(mv)为纵坐标,进行线性回归,丹酚酸B回归方程

r=0.999 9,线性范围为0.56~5.6 μg。
3.7 精密度试验
3.7.1 丹参酮ⅡA精密度试验 精密吸取丹参酮ⅡA对照品溶液5 μL,连续重复进样6次,丹参酮ⅡA峰面积的RSD为0.82%(n=6),表明本测定方法精密度良好。
3.7.2 丹酚酸B精密度试验 精密吸取丹酚酸B对照品溶液10 μL,连续重复进样6次,丹酚酸B峰面积的RSD为0.95%(n=6),表明本测定方法精密度良好。
3.8 稳定性试验
分别取同一批(110815)丹参酮ⅡA供试品溶液和丹酚酸B供试品溶液,分别在0、2、4、6、8、10 h测定峰面积。结果,丹参酮ⅡA供试品溶液的RSD=0.88%(n=6),丹酚酸 B供试品溶液的RSD=0.83%(n=6),表明两个供试品溶液在10 h内稳定。
3.9 重复性试验
3.9.1 丹参酮ⅡA重复性试验 取同一批号样品(110815)6份,精密称定,按3.3.1项下方法制备,进样5 μL测定,测得丹参酮ⅡA 2.44 mg/g,RSD为1.46%(n=6),表明本测定方法具有良好的重复性。
3.9.2 丹酚酸B重复性试验 取同一批号样品(110815)6份,精密称定,按3.3.2项下方法制备,进样10 μL测定,测得丹酚酸B 65.4 mg/g,RSD为1.63%(n=6),表明本测定方法具有良好的重复性。
3.10 准确度试验
3.1 0.1丹参酮ⅡA准确度试验 采用加样回收法,取已知含量样品(110815),精密称定6份,每份0.15 g,分别置6个具塞锥形瓶中,精密加入含丹参酮ⅡA对照品0.366 mg/mL的混合对照品溶液1 mL,按3.3.1项下方法制备,进样5 μL测定,测得丹参酮ⅡA回收率 99.28%,RSD= 1.37%(n=6)。
3.1 0.2丹酚酸B准确度试验 采用加样回收法,取已知含量样品(110815),精密称定 6份,每份0.1 g,分别置6个具塞锥形瓶中,精密加入含丹酚酸B对照品6.54 mg/mL的混合对照品溶液1 mL,按3.3.2项下方法制备,进样10 μL测定,测得丹酚酸B回收率99.02%,RSD=1.74%(n=6)。
3.11 样品测定
3.1 1.1丹参酮ⅡA精密度试验 取3批样品(110815、110816、110917),按 3.3.1项下方法制备,分别精密吸取5 μL注入液相色谱仪,测定样品中丹参酮ⅡA含量。结果,3批样品的丹参酮ⅡA含量分别为2.44、2.47、2.42 mg/g。
3.1 1.2丹酚酸B精密度试验 取3批样品(110815、110816、110917),按 3.3.1项下方法制备,分别精密吸取10 μL注入液相色谱仪,测定样品中丹酚酸B含量。结果,3批样品的丹酚酸B含量分别为65.4、65.1、65.6 mg/g。
4 讨论
石菖蒲、丹参、赤芍、郁金和冰片的薄层色谱鉴别方法操作简便,结果准确,重现性好,斑点清晰,阴性无干扰。丹参占处方药量比例最大,为处方总量的1/4以上,因此,控制丹参的质量能确保偏瘫康胶囊的临床疗效。丹参药材按中国药典2010年版(一部)丹参含量测定项下检验,含丹参酮ⅡA 0.27%、丹酚酸B 7.2%。偏瘫康胶囊的规格为0.35 g/粒,处方1 000粒胶囊所含的丹参药材量为334 g,本研究测得胶囊内容物含丹参酮ⅡA 0.244%和丹酚酸B总量为6.54%,经过计算,与丹参药材 (含丹参酮ⅡA 0.27%、丹酚酸 B 7.2%)比较,丹参酮ⅡA和丹酚酸 B的转移率均为95%以上,说明胶囊中丹参酮ⅡA和丹酚酸B基本提取完全。实验结果表明,本研究测定丹参酮ⅡA和丹酚酸B含量的方法稳定性、重现性好,精密度、回收率都较满意,因此,能有效控制偏瘫康胶囊的质量。
[1] 国家药典委员会.中国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:70,85,136,147,193.
[2] 谢瑞萍,林常定,黎泽.益脑复智片的薄层色谱鉴别研究[J].云南中医中药杂志,2010,31(11):62-64.
[3] 左红香,金勇,张成义,等.孔枕益智片质量标准研究[J].北华大学学报(自然科学版),2010,11(5):420-423.
[4] 王孟良,赵佳丽,于慧娜.丹芍活血胶囊的薄层色谱鉴别[J].中国中医药咨讯,2011,3(16):275.
[5] 徐庆仪,徐济恒.清痤颗粒中赤芍、金银花、甘草的薄层色谱鉴别[J].内蒙古中医药,2011,30(5):87.
[6] 张宜凡,李瑾.牛黄解毒片中冰片的化学鉴别及薄层色谱鉴别[J].中医药导报,2011,17(6):95-96.
[7] 贾春燕,王萍,聂继红.消痔栓质量标准的研究[J].新疆中医药,2011,29(3):33-34。
[8] 武希桃,袁鲜云.HPLC法测定舒尔心胶囊中丹参酮ⅡA和丹酚酸B的含量[J].现代中医药,2010,30(5):97-98.
[9] 张永东,钟颖,谭鸿毅,等.高效液相色谱法测定复方丹参喷雾剂中丹酚酸 B和丹参酮ⅡA的含量 [J].中南药学,2010,8(6):435-437.
[10] 褚克丹,季国路,施红,等.高效液相色谱法测定参斛颗粒剂中丹参酮ⅡA和丹酚酸B的含量 [J].福建中医药大学学报,2011,21(1):30-32.
Study on the Quality Standards of Piantankang Capsules
Jiang Nan(Hospital of Traditional Chinese Medicine of Hengyang City,Hunan Hengyang 421001,China)
Objective:To establish the quality standards of Piantankang capsules.Methods:Acori Tatarinowii Rhizoma,Salviae Miltiorrhizae Radix Et Rhizoma,Paeoniae Radix Rubra,Curcumae Radix and Borneolum Syntheticum were identified by TLC.The contents of tanshinoneⅡA and salvianolic acid B in the preparation were determined by HPLC.Results:Acori Tatarinowii Rhizoma,Salviae Miltiorrhizae Radix Et Rhizoma,Paeoniae Radix Rubra,Curcumae Radix and Borneolum Syntheticum could be identified by TLC.The linear range of tanshinoneⅡA was 0.032-0.32 μg (r= 0.999 9),and the average recovery was 99.28% (RSD=1.37%,n=6).The linear range of salvianolic acid B was 0.56~5.6 μg (r=0.999 9),and the average recovery was 99.02% (RSD=1.74%,n= 6).Conclusion:The quality of piantankang capsules could be controlled effectively with the established quality standards.
Piantankang Capsules;Quality Standard;TLC;HPLC
10.3969/j.issn.1672-5433.2012.03.006
2011-11-18)
江南,男,主管药师。研究方向:质量标准和临床药学。E-mail:jiangnan_1977@163.com
