HPLC 波长切换法同时测定丹参酚酸提取物中5种成分
2012-01-26暴凤伟刘玉强胡丽萍张振秋侯学智谢剑琳
暴凤伟,刘玉强,胡丽萍,张振秋,侯学智,谢剑琳
(辽宁中医药大学,辽宁大连116600)
丹参为唇形科植物丹参Salvia miltiorrhizaBge.的干燥根及根茎,始于《神农本草经》,列为上品,是我国常用的传统中药。味苦,性微寒;归心、肝经;具有活血祛瘀,通经止痛,凉血消痈等功效;用于胸痹心痛,脘腹胁痛,癥瘕积聚,热痹疼痛,心烦不眠,月经不调,痛经经闭,疮疡肿痛[1]。丹参有效成分分为脂溶性成分和水溶性成分两大类[2],脂溶性成分主要有丹参酮ⅡA、丹参酮ⅡB、丹参酮Ⅰ、隐丹参酮Ⅰ等;水溶性成分主要有丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B等。有关丹参酚酸提取物的报道[3-6]多为药理作用和定量测定方法的研究,但同时测定丹参酚酸提取物中5种物质的报道较为少见。本实验采用HPLC波长切换技术[7-8]建立了同时测定丹参酚酸提取物中丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B等5种成分的分析方法,该方法简便、快速、准确,重复性好,为更好地控制丹参酚酸提取物的质量提供依据。
1 仪器与试药
1.1 仪器Agilent-1100型高效液相色谱仪(仪器编号:20041191 DE43607375),配置四元梯度泵、在线脱气机、VWD检测器;AS3120A超声提取器(天津奥特赛恩斯仪器有限公司);2140型电子分析天平(上海奥豪斯公司)、METTLER AB135-S十万分之一电子天平(瑞士);U-3010型紫外-可见分光光度计(日立公司)。
1.2 试药对照品丹参素钠(批号:110855-200809,纯度为100%),原儿茶醛(批号:110810-200205,纯度为98.6%),迷迭香酸(批号:111871-201001,纯度为98.8%)和丹酚酸B(批号:111562-201009,纯度为96.0%)均购于中国食品药品检定研究院。紫草酸(批号:110326,纯度为98.8%)购于四川省维克奇生物科技有限公司。本研究收集了来自于上海、浙江、河北、云南、北京、山东、辽宁7个不同来源的丹参药材,编号依次为1~7号,经辽宁中医药大学李峰教授鉴定均为正品药材。乙腈、甲醇为色谱纯(山东禹王化学试剂公司),水为重蒸馏水,磷酸为分析纯。
1.3 丹参酚酸提取物的制备取丹参药材,加水回流提取3次,每次2 h,第一次加12倍量,第二次加10倍量,第三次加10倍量,滤过,合并滤液,并浓缩,通过AB-8大孔吸附树脂柱,依次用水和50%的乙醇洗脱,收集50%乙醇洗脱液,回收乙醇,浓缩,干燥,即得。
2 方法与结果
2.1 色谱条件Phenomsil-C18色谱柱(250 mm×4.6 mm,5 μm);流动相为乙腈(A)-0.5%磷酸溶液(B),梯度洗脱(见表1);检测波长为280 nm(0~50 min,丹参素钠、原儿茶醛),330 nm(50~68 min,迷迭香酸),286 nm(68~90 min,紫草酸、丹酚酸B);体积流量1.0 mL/min;柱温30℃;进样量10 μL。

表1 流动相梯度洗脱程序Tab.1 Procedures of gradient elution
2.2 溶液的制备
2.2.1 混合对照品溶液的制备分别精密称取丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B等5个对照品,加甲醇制成每1 mL含丹参素钠0.566 0 mg、原儿茶醛0.830 mg、迷迭香酸0.525 0 mg、紫草酸0.614 0 mg、丹酚酸B1.300 mg的对照品贮备液,备用。分别精密量取上述5个对照品贮备液适量,加甲醇制成每1 mL含丹参素钠16.98 μg、原儿茶醛8.300 μg、迷迭香酸46.20 μg、紫草酸42.37 μg、丹酚酸B 650.0 μg的混合对照品溶液。
2.2.2 供试品溶液的制备取不同来源的丹参酚酸提取物约50 mg,精密称定,置具塞锥形瓶中,精密加入50%甲醇25 mL,密塞,称定质量,超声处理(功率25W,频率40 kHz)30 min,放冷,再称定质量,用50%甲醇补足损失的质量,摇匀,滤过,即得。
2.3 系统适应性试验按上述色谱条件,分别取混合对照品溶液和供试品溶液进样10 μL,记录色谱图。结果表明混合对照品溶液色谱图上,对照品色谱峰的理论塔板数均大于5 000,拖尾因子均在0.95~1.05之间;在供试品溶液的色谱图上,与对照品相对应的色谱峰与其临峰的分离度均大于1.5。混合对照品溶液及供试品溶液色谱图见图1。
2.4 方法学考察
2.4.1 线性关系的考察分别精密量取上述混合对照品溶液2、4、8、12、16、20 μL注入高效液相色谱仪,测定。以进样量为横坐标,峰面积为纵坐标,绘制标准曲线,计算回归方程,结果见表2。

图1 混合对照品溶液(A)和供试品溶液(5号)色谱图(B)Fig.1 Chromatograms of a m ixture of reference substances(A),sample(NO.5)(B)

表2 5种物质的标准曲线方程、相关系数和线性范围Tab.2 Regression equations、correlation coefficients and linear ranges of five constituents
2.4.2 精密度试验取丹参酚酸提取物(1号)约50 mg,精密称定。按2.2.2项下方法制备供试品溶液,在上述色谱条件下连续进样6次,测得丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B峰面积的RSD(n=6)分别为1.7%、1.2%、1.3%、1.5%、1.4%。结果表明,仪器精密度良好。
2.4.3 重复性试验取丹参酚酸提取物(1号)约50 mg共6份,精密称定。按2.2.2项下方法制备供试品溶液,在上述色谱条件下进样,测得丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B平均质量分数(n=6)分别为5.647、3.458、14.69、19.13、249.2 mg/g;RSD分别为1.5%、1.3%、1.5%、2.2%、1.2%。
2.4.4 稳定性试验取同一供试品溶液(1号),在室温下放置,分别于0、2、4、8、12、24 h在上述色谱条件下进样分析,测定峰面积。丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B峰面积的RSD(n=6)分别为1.7%、1.4%、1.6%、1.5%、1.4%。结果表明,供试品溶液中上述5种物质在24 h内稳定性良好。
2.4.5 加样回收率试验称取已知含有量(丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B的含有量分别为5.539、3.421、14.39、19.07、249.1 mg/g)的丹参酚酸提取物(上海)6份,每份约25 mg,精密称定。分别准确加入丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B的对照品贮备液0.24、0.1、0.68、0.77、3.8 mL,按2.2.2项下方法制备供试溶液,在上述色谱条件下进行测定,计算回收率。结果上述丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B等5种物质的平均回收率(n=6)分别为99.1%、99.2%、100.1%、99.7%、100.2%;RSD分别为2.2%、2.3%、1.9%、1.7%、2.0%。结果见表3。
2.5 样品测定取所收集的7个不同来源丹参药材的丹参酚酸提取物约50 mg,精密称定。按2.2.2项下方法制备供试品溶液,在上述色谱条件下进样测定,以外标法计算样品中丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B等5种物质,结果见表4。并对丹参酚酸提取物进行综合评分,设计丹参酚酸提取物中每种物质的含有量评分公式均为Y=(X-Xmin)/(Xmax-Xmin)×10(X为某物质的含有量,Y为计算分值),5种物质权重系数均定为0.2,最终综合评分结果公式为W=∑Y×0.2(W为综合评分值)分,结果见表5。
3 讨论
3.1 本实验建立的方法对7个不同来源的丹参药材的丹参酚酸提取物中5种成分进行了测定。结果表明7个来源的丹参酚酸提取物中丹参素钠的质量分数2.778~8.874 mg/g,原儿茶醛的质量分数2.596~4.482 mg/g,迷迭香酸的质量分数14.40~41.69 mg/g,紫草酸的质量分数16.59~23.24 mg/g,丹酚酸B的质量分数193.3~382.5 mg/g。
3.2 中药的药效是多种物质共同作用的结果,以单一物质的含有量来评价其质量的优劣不能够反映药物发挥作用的整体性。本实验同时测定丹参酚酸提取物中5种成分,采用综合评分法科学地评价丹参酚酸提取物的质量。最终评分结果表明来自于辽宁的丹参酚酸提取物质量最佳。

表3 丹参酚酸提取物中5种物质加样回收率试验结果Tab.3 Recovery test results of five constituents in Salvia m iltiorrhiza phenolic acids extract

表4 丹参酚酸提取物中5种成分的测定结果(n=3)Tab.4 Analytical results of five constituents in Salvia m iltiorrhiza phenolic acids extract(n=3)
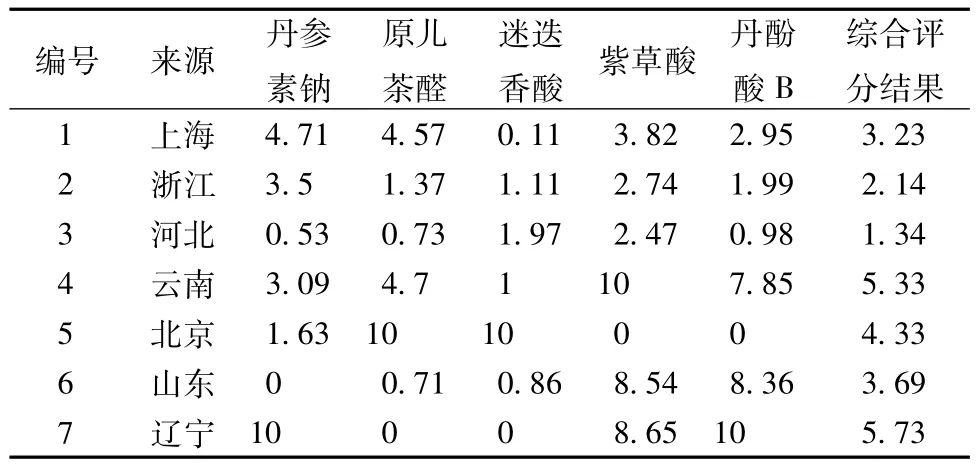
表5 不同产地丹参酚酸提取物综合评分结果表Tab.5 Assessment results of different origins Salvia m iltiorrorrhiza phenolic acids extract
3.3 目前有关丹参的文献报道[9-13],没有同时测定丹参酚酸提取物中丹参素钠、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B这5种成分。本实验建立了HPLC波长切换法同时测定丹参酚酸提取物中5种成分,并取得了比较满意的结果,该分析对丹参酚酸提取物的进一步研究、开发、利用和质量标准的制定提供了理论依据和科学参考。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:70.
[2]肖培根.新编中药志[M].北京:化学工业出版社,2001:184-200
[3]王卓,朱宝长,徐楠楠,等.丹参提取物对高血脂症地鼠糖脂代谢的影响[J].时珍国医国药,2008,19(12):2861-2863.
[4]尉萍萍,赵粼.HPLC测定丹参提取物中丹酚酸A含量[J].中国现代应用药学,2008,25(3):241-243.
[5]王洁,张均田.总丹酚酸抗脑缺血与抗血栓的关系[J].中国药理学通报,1999,15(3):237-239.
[6]杨英.丹参提取物对麻醉大鼠血流动力学的影响[J].中华医护杂志,2007,4(4):292-293.
[7]赵鸣舒,赵希贤.双波长高效液相色谱法测定丹参中多种成分的含量[J].中国药事,2010,24(8):804-806.
[8]王晖,张振秋.HPLC波长切换法同时测定迷迭香中咖啡酸、阿魏酸和迷迭香酸的含量[J].中国实验方剂学杂志,2011,17(5):116-118.
[9]潘英妮,袁丹,付文卫,等.HPLC法测定丹参类注射液中4种水溶性成分含量[J].沈阳药科大学学报,2004,21(3):196-200.
[10]韦英杰,李萍,李松林.高效液相二极管阵列检测法同时测定复方丹参制剂中7个成分的含量[J].分析化学研究报告,2006,34(12)1702-1706.
[11]潘雪梅,韦辉,刘毅,等.不同产丹参药材质量研究[J].中草药,2011,42(9):1833-1836.
[12]王伟,李焱,谢晓梅,等.高效液相色谱法同时测定丹参中四种酚酸类成分的含量[J].安徽医药,2010,14(11):1276-1277.
[13]张雪,褚文静,刘伟娜,等.高效液相色谱二极管阵列检测法同时测定丹参滴注液中四种水溶性成分的含量[J].分析化学学报,2010,26(1):109-111.
