醋五味子饮片质量标准研究
2012-01-26张莹毛春芹陆兔林黄玮苏桃蔡宝昌
张莹,毛春芹,陆兔林,2*,黄玮,苏桃,2,蔡宝昌,2
(1.南京中医药大学药学院,江苏南京210046;2.南京中医药大学江苏省中药炮制重点实验室,江苏南京210046)
五味子为木兰科植物五味子Schisandra chinensis(Turcz.)Baill.的干燥成熟果实,按醋蒸五味子生产工艺制备而得醋五味子饮片。主产于黑龙江、辽宁、吉林、河北等地。具有收敛固涩,益气生津,补肾宁心之功效,主要用于久嗽虚喘,梦遗滑精,遗尿尿频,久泻不止,自汗盗汗,津伤口渴,内热消渴,心悸失眠等症的治疗[1]。现代研究表明,五味子主要化学成分为木脂素、挥发油及有机酸等三类有效成分[2-3]。具有保护肝脏[4]、抗氧化[5-6]、抗肿瘤[7]、抗衰老[8-9]、增强免疫功能[10]等多方面活性。
《中国药典》2005年版一部44页五味子含量测定项下对五味子采用了五味子醇甲作为其质量控制的指标。根据文献研究及辽宁省主产地反馈的信息[11-12],未成熟五味子果实中五味子醇甲含有量高于成熟的果实,而临床上使用的是五味子成熟的果实。为了更好地科学地控制五味子的质量,故将五味子醇甲及五味子乙素共同作为指标性成分,对醋五味子饮片进行质量评价研究,为规范饮片质量、保证临床疗效提供科学依据。
1 仪器与试药
1.1 仪器Agilent1100 LC高效液相色谱仪(美国安捷伦公司);色谱柱为Hypersil ODS柱(250 mm×4.6 mm,5 μm)(大连依利特科技公司);AL104型电子天平(瑞士Mettler公司);KQ5200DB型数控超声波清洗器(昆山市超声仪器有限公司);TGL—16台式高速离心机(金坛市医疗仪器厂)。
1.2 试药五味子醇甲对照品(中国药品生物制品检定所,供含量测定用,批号:110857-200605);五味子乙素对照品(中国药品生物制品检定所,供含量测定用,批号:110765-200508)。甲醇(色谱纯,Tediacompany),水(超纯水),其余试剂均为分析纯。
1.3 饮片生五味子饮片,购自五味子主产地辽宁、黑龙江等地,经南京中医药大学药学院巢建国教授鉴定为木兰科植物五味子Schisandra chinensis(Turcz.)Baill.的干燥成熟果实,按醋蒸五味子生产工艺制备而得的醋五味子饮片。见表1。
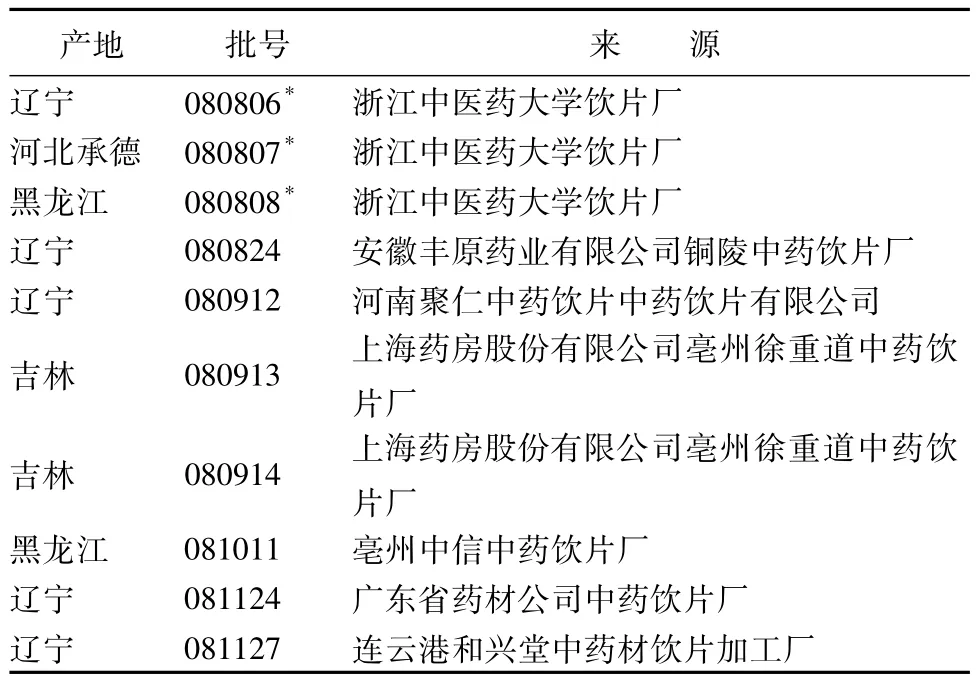
表1 样品来源及批次Tab.1 Sam p le sources and batches
2 薄层色谱鉴别
取醋五味子粉末1 g,加二氯甲烷20 mL,加热回流30 min,滤过,滤液蒸干,残渣加二氯甲烷1 mL使溶解,作为供试品溶液。另取醋五味子对照药材1 g,同法制成对照药材溶液。再取五味子甲素对照品,加二氯甲烷制成每1 mL含1 mg的溶液,作为对照品溶液。照薄层色谱法试验,吸取上述3种溶液各2 μL,分别点于同一硅胶GF254薄层板上,以展开系统1[石油醚(30~60℃)-甲酸乙酯-甲酸(15∶5∶1)]的上层溶液及展开系统2[正己烷-乙酸乙酯(8∶3)]为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。供试品色谱中,在与对照药材和对照品色谱相应的位置上,显相同颜色的斑点。比较薄层色谱的分离情况,最终确定将石油醚(30~60℃)-甲酸乙酯-甲酸(15∶5∶1)展开系统列入标准正文。见图1。

图1 醋五味子薄层色谱图Fig.1 TLC identification of Schisandra chinensis processed w ith vinegar
3 杂质、水分、灰分及浸出物检查
照《中国药典》2005年版一部杂质检查法(附录IXA)、水分测定法(附录ⅨH第二法)、灰分测定法(附录ⅨK法)、醇溶性浸出物测定法项下的热浸法(附录ⅩA)对10批次的醋五味子样品进行测定,计算结果见表2、表3。

表2 不同批次醋五味子中杂质、水分、灰分、浸出物Tab.2 Im purities,moisture,ash and extract contents of Schisandra chinensis processed w ith vinegar in different batches

表3 生五味子中杂质、水分、灰分、浸出物Tab.3 Im purities,moisture,ash and extract contents of Schisandra chinensis
4 样品测定
4.1 色谱条件Hypersil ODS色谱柱(250 mm×4.6 mm,5 μm);流动相为甲醇(A)-水(B)梯度洗脱,0~10 min(A为68%),10~13 min(A为68%~77%),13~30 min,(A为77%);柱温30℃;体积流量1.0 mL/min;测定波长250 nm;进样量10 μL。理论板数按五味子醇甲峰计算应不低于2 000。
4.2 对照品溶液的制备精密称取五味子醇甲及五味子乙素对照品适量置25 mL量瓶中,用甲醇溶解并稀释至刻度,摇匀,配制成含0.78 mg/mL五味子醇甲及0.956 mg/mL五味子乙素的混合对照品溶液。
4.3 供试品溶液的制备取醋五味子粉末(过三号筛)约0.2 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定质量,超声(500 W)提取30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过。
4.4 专属性试验分别取对照品、醋五味子样品、空白溶剂注入液相色谱仪中,按照上述色谱条件,进样10 μL,测定,结果见图2。

图2 对照品(A)、供试品(B)与空白溶液(C)HPLC色谱图Fig.2 HPLC chromatograms of reference substances(A),sample(B)and blank solution(C)
4.5 线性关系考察精密吸取上述对照品贮备液0.2、0.4、0.6、0.8、1.0、1.2、1.4 mL,分别置于5mL量瓶中,加甲醇稀释至刻度,摇匀,使五味子醇甲质量浓度分别为0.015 6、0.031 2、0.046 8、0.062 4、0.078、0.093 6、0.109 2 mg/mL;五味子乙素的质量浓度分别为0.007 648、0.015 296、0.022 944、0.030 592、0.038 24、0.045 888、0.053 536 mg/mL。各对照品液分别进样10 μL,重复2次,按上述色谱条件进行测定,以峰面积均值(Y)为纵坐标,进样浓度(X)为横坐标,绘制标准曲线。五味子醇甲回归方程、相关系数以及线性范围分别为:Y=20 247X+3.836,r=1.000 0;0.156~1.092 μg线性关系良好。五味子乙素回归方程、相关系数以及线性范围分别为:Y=16 538X-0.814,r=0.999 9;0.076 48~0.535 36 μg线性关系良好。
4.6 精密度试验取供试品溶液,按照上述色谱条件,连续进样6次,记录各自峰面积,RSD值分别为0.18%、0.36%。结果表明仪器精密性良好。
4.7 稳定性试验取供试品溶液,每隔2 h进样1次,记录五味子醇甲、五味子乙素18 h内的峰面积,RSD分别为0.20%,0.43%。结果表明样品在18 h内稳定性符合要求。
4.8 重复性试验取同一批号样品,平行称取6份,按4.3项下方法制备供试品溶液,照上述色谱条件测定五味子醇甲、五味子乙素,RSD分别为0.46%、0.37%,结果表明该方法具有较好的重复性。
4.9 加样回收率试验精密称取五味子醇甲质量分数为0.78%,五味子乙素质量分数为0.57%的五味子粉末0.1 g,平行9份,分别置于具塞锥形瓶中,分别加入0.8、1.0、1.2 mL五味子醇甲对照品液(0.780 mg/mL),及0.5、0.6、0.7 mL五味子乙素对照品液(0.956 mg/mL)各3份。按4.3项下方法制备供试品溶液,按上述色谱条件测定五味子醇甲、五味子乙素,计算准确度,见表4。结果表明,准确度良好,符合定量测定的要求。
4.10 样品测定取不同批次醋五味子粉末0.2 g,精密称定,每批样品平行称取2份,按照供试品溶液制备的方法制备,每一份样品进样2次进行测定。对10个批次的醋五味子样品进行测定,测定结果见表5、表6。
5 讨论
5.1 根据不同产地醋五味子饮片实验测定结果,按平均值的±20%作为限度制定幅度。暂定醋五味子饮片杂质不得过0.7%,水分不得过13.0%,灰分不得过6.0%,浸出物量不得低于28.0%,含五味子醇甲和五味子乙素的质量分数不得少于0.80%。

表4 加样回收试验结果Tab.4 Results of recovery tests

表5 醋五味子的测定结果Tab.5 Content determ ination results of Schisandra chinensis processed w ith vinegar

表6 五味子的测定结果Tab.6 Content determ ination results of Schisandra chinensis
5.2 分别采用不同体系、不同比例的流动相及不同色谱柱进行色谱分离,最终确定色谱条件为:Hypersil ODS柱色谱(250×4.6 mm,5μm);流动相为0~10 min,甲醇-水(68∶32),10~13 min,甲醇(68→77),13~30 min,甲醇-水(77∶23)。分离效果最佳。
5.3 醋五味子主要含有脂溶性成分,极性较小,故对其醇溶性浸出物进行研究,考虑到指标性成分的极性,最终选用95%的乙醇作为提取溶剂。此外,考虑到醇冷浸法时温度差异对结果影响较大,因此选用热浸法。
5.4 根据文献研究及辽宁省主产地反馈的信息,未成熟五味子果实中五味子醇甲含有量高于成熟的果实,而临床上使用的是五味子成熟果实,故在2005年版《中国药典》五味子含量测定项下对五味子醇甲作为其质量控制指标的基础上增加了五味子乙素共同作为定量控制的指标性成分,更好地科学地控制醋五味子的质量。
5.5 采用HPLC法测定不同产地醋五味子饮片中五味子醇甲、五味子乙素,结果显示,该法操作简便、结果可靠、重现性好、专属性强,可用于醋五味子中有效成分定量测定和质量控制。
[1]国家药典委员会.中华人民共和国药典:2005年版一部[S].北京:化学工业出版社,2005:44.
[2]葛会奇,贾天柱.HPLC测定五味子的最佳采收期及五味子醇甲在果实中的分布[J].中成药,2007,29(6):862-864.
[3]逄世峰,郑培和,许世泉.炮制对北五味子木脂素类成分的影响[J].中成药,2011,33(2):284-286.
[4]张明华,陈虹,李灵芝.五味子甲素和五味子醇甲对四氯化碳所致肝脏损伤的保护作用[J].武警医学,2002,13(7):395-396.
[5]谢宇,陈建光,孙新.4种五味子木脂素抗氧化作用实验研究[C]//第十届全国心血管药理学术会议2010(重庆)国际心血管疾病与药物高峰论坛,2010:151-153.
[6]商红军,孟宪军,李斌,等.北五味子乙素体外抗氧化及抑菌作用的研究[J].食品工业科技,2012,2(33):170-172.
[7]任丽佳,李林,殷放宙,等.五味子抗肿瘤活性成分及作用机制研究进展[J].中国药理学通报,2012,28(1):140-142.
[8]赵永德,崔惠玲,李娟.五味子的药理作用及临床应用[J].中华临床医药与护理,2005,3(6):41.
[9]孙文娟,吕文伟,于晓凤,等.北五味子粗多糖抗衰老作用的实验研究[J].中国老年学杂志,2001,21(11):54-455.
[10]苗明三,方晓艳.五味子多糖对正常小鼠免疫功能的影响[J].中国中医药科技,2003,10(2):100-108.
[11]李宝岩.五味子资源调查与品质评价[D].沈阳:辽宁中医药大学,2008.
[12]孙庆龙.北五味子种质资源及评价研究[D].哈尔滨:黑龙江中医药大学,2006.
