兰索拉唑在正常及溃疡模型家兔体内药代动力学研究*
2011-05-17潘桂玲张永文
韩 强,潘桂玲,张永文
徐州医学院附属医院药剂科,江苏 徐州 221002
兰索拉唑是由日本武田公司开发的H+/K+-ATP酶抑制剂,于1991年首次在法国上市,主要用于胃溃疡、十二指肠溃疡、吻合口溃疡及反流性食管炎、卓-艾综合征的治疗[1]。与奥美拉唑相比,由于兰索拉唑的吡啶环4-位引入了三氟乙氧基,使得其具有更好的疗效、较少的副作用和更强的稳定性[2]。在胃溃疡状态下,生理及病理上的变化,必将影响药物的药代动力学行为。现有的兰索拉唑的药代动力学研究报道,尚无在胃溃疡病家兔体内的药代动力学研究报道[3-5]。因此本实验建立了测定血浆中兰索拉唑的高效液相色谱法,并采用此方法研究了该药在正常及溃疡兔体内的药代动力学特征,为临床合理应用提供参考。
1 材料和方法
1.1 动物
家兔,体重(2.5±0.2)kg,雌雄各半,由徐州医学院实验动物中心提供(SYXK(苏)2001-0050)。
1.2 仪器
Shimadzu LC-10A高效液相色谱仪(日本岛津制作所),包括SCL-10Avp系统控制器,SPD-M20A二极管阵列检测器,LC-10ADvp两元泵,SIL-20A自动进样器,FCV-10Alvp四元低压梯度洗脱系统,DGU-20As在线脱气机,岛津Lcsolution色谱数据工作站。梅特勒托利多AE240电子天平(十万分之一,瑞士Mettler Toledo);台式高速冷冻离心机(5417R,德国 Eppendorf公司)。
1.3 药品与试剂
注射用兰索拉唑 (江苏奥赛康药业有限公司,批号:090501,规格:30 mg/支);兰索拉唑对照品(扬州市三药制药有限公司提供,批号:20080605,纯度>99.0%);奥美拉唑对照品(江苏奥赛康药业有限公司提供,批号:0908005,纯度>99.0%);甲醇、乙腈为色谱纯;二氯甲烷、乙酸乙酯、无水乙醚、无水碳酸钠为分析纯;水为去离子水。
1.4 供试样品及对照品溶液的制备
1.4.1 兰索拉唑注射液将30 mg/支注射用兰索拉唑用10 mL 0.9%氯化钠注射液稀释,取1 mL稀释液加入99 mL生理盐水中,备用。
1.4.2 对照品溶液精密称取兰索拉唑对照品5.16 mg置5 mL量瓶中,用甲醇溶解并稀释至刻度,配成1.03 mg·L-1的兰索拉唑对照品溶液。
1.4.3 兰索拉唑标准溶液精密称取兰索拉唑5.16 mg,置于5 mL量瓶中,加入甲醇溶解并稀释至刻度,摇匀,即得1.03 mg·L-1兰索拉唑的储备液。临用前用流动相 56%甲醇稀释成为 0.2、0.5、1.0、2.0、5.0、10.0、20.0 μg·mL-1的标准溶液,置冰箱 4℃冷藏保存,待用。
1.4.4 内标溶液精密称取奥美拉唑对照品5.18mg置5 mL量瓶中,用甲醇溶解并稀释至刻度,配成1.03mg·L-1的奥美拉唑储备液,并稀释成10.0μg·mL-1作为内标浓度。
1.5 动物实验方案及血浆样品处理方法
1.5.1 动物实验方案健康家兔12只,雌雄各半,体重(2.5±0.2)kg。禁食24 h后,其中6只绑于兔台上置于20℃水中,水量漫过兔的胸骨,8 h后取出吹干。待家兔可以自由活动后,耳缘静脉给药,控制在30 min左右滴注完毕,给药前及给药后5、10、15、20、30、45、60、75、90、120、150、210、270、390 min 颈总动脉取血2 mL,根据实际情况补充适量生理盐水。将全血置于肝素处理过的试管中3000 r·min-1离心10 min,分取血浆,-20℃冷冻保存,待测。
1.5.2 血浆样品处理方法精密量取离心后的血浆500 μL,至离心管中,精密加入 50 μL 10.0 μg·mL-1奥美拉唑内标溶液,混匀。加入200 μL 0.1 mol·L-1碳酸钠,涡旋混匀30 s,再加入2 mL乙腈,涡旋混匀2 min,于 4000 r·min-1离心 10 min。 取有机层 45℃下氮气流吹干,残渣用200 μL流动相溶解,于14000 r·min-14℃离心10 min。取上清液20 μL进样分析。
1.6 色谱条件
色谱柱为Kromasil C18柱 (大连依利特有限公司,250 mm×4.6 mm,5 μm);流动相:甲醇-水(56︰44,v/v);检测波长:284 nm;柱温:35℃;进样量 20 μL;流速 0.8 mL·min-1。
1.7 数据处理
药代动力学参数的估算按中国药理学会推荐的药代动力学程序“DAS2.0”对血药浓度-时间数据进行自动拟合,根据AIC进行房室模型判别,参数AUC(0-t)、AUC0-∞、t1/2、MRT(0-t)、CL、V 等分别作方差分析及双侧t检验。
2 结 果
2.1 方法学考察
2.1.1 专属性在上述色谱条件下检测空白血浆、模拟血浆样品和家兔给药后血浆样品,兰索拉唑的保留时间为19.9 min,内标奥美拉唑的保留时间为13.3 min。血浆中的内源性物质和代谢物不干扰兰索拉唑和内标的测定。色谱图见图1。
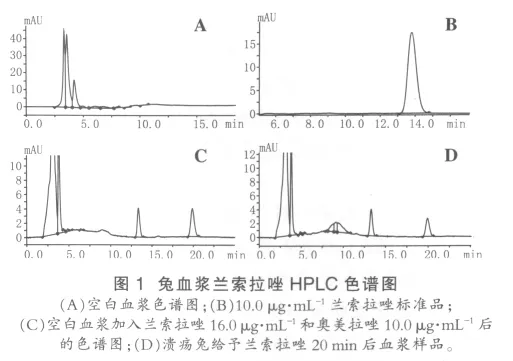
2.1.2 线性关系取兔空白血浆0.5 mL,精密加入7个不同质量浓度的兰索拉唑标准溶液50 μL,按“1.5.2”项血浆样品处理方法进行处理,使其含兰索拉唑浓度为 0.02、0.05、0.1、0.2、0.5、1.0、2.0 μg·mL-1的标准血浆,每种浓度做两份。在“1.6”项色谱条件下进样分析,记录色谱图、兰索拉唑峰面积(As)及内标奥美拉唑峰面积(Ar)。以兰索拉唑对奥美拉唑峰面积平均值的比值(As/Ar)对兰索拉唑血药浓度(C)作回归计算,得回归方程As/Ar=0.0016C+0.0438(权重系数 w=1/y)。结果表明,兰索拉唑在 0.02~2.0 μg·mL-1浓度范围内,其峰面积与内标奥美拉唑峰面积的比值与兰索拉唑浓度之间呈现良好的线性关系(r2=0.9981)。
2.1.3 定量下限本方法兰索拉唑的定量下限(LLOQ)为标准曲线最低浓度 0.02 μg·mL-1,且连续3次测定结果的准确度及精密度均符合生物样品测定方法的要求,见表1。
2.1.4 回收率考察
2.1.4.1 绝对回收率 精密量取不同浓度的兰索拉唑标准溶液100 μL,加入内标奥美拉唑100 μL,再加入200 μL流动相,涡旋混匀,配成含兰索拉唑浓度分别为低、中、高(0.1、0.5、1.6 μg·mL-1)的溶液,每种浓度各做3份样品,精密吸取20 μL上清液进样分析。记录色谱图,测定兰索拉唑与内标奥美拉唑的色谱峰面积(As与Ar)。
精密量取不同浓度的兰索拉唑标准溶液50 μL,加入空白血浆 0.5 mL, 制备 0.1、0.5、1.6 μg·mL-1的血浆,每种浓度各做3份样品。每份按“血浆样品的处理”项下“精密加入 50 μL 10.0 μg·mL-1奥美拉唑内标溶液”起操作。记录色谱图,测定兰索拉唑与内标奥美拉唑的色谱峰面积(As1与Ar1),对上述As1、Ar1与 As、Ar按 As1/As×100%计算,即为兰索拉唑的绝对回收率(R)。结果表明,兰索拉唑的高中低浓度回收率均大于75%。
2.1.4.2 相对回收率 对“绝对回收率”中得到的As1、Ar1与 As、Ar按(As1/Ar1)/(As/Ar)×100%计算,即得各浓度“血浆样品处理方法”的相对回收率,结果表明,兰索拉唑的高中低浓度相对回收率均大于80%。
2.1.5 精密度考察精密量取不同浓度的兰索拉唑标准溶液50 μL,加入空白血浆0.5 mL,制备0.1、0.5、1.6 μg·mL-1的血浆,每种浓度各做 5 份样品。每份按“血浆样品的处理”项下“精密加入50μL 10.0μg·mL-1奥美拉唑内标溶液”起操作。在批内和批间(连续5天)对每种浓度各做5份样品,记录色谱图,记下兰索拉唑峰面积(As)对奥美拉唑峰面积(Ar),用标准曲线计算兰索拉唑的浓度。求得批内和批间相对标准差,结果见表2,其表明血浆样品分析的精密度良好,RSD均小于10%。
表2 HPLC法的批内和批间变异 (±s,n=5)
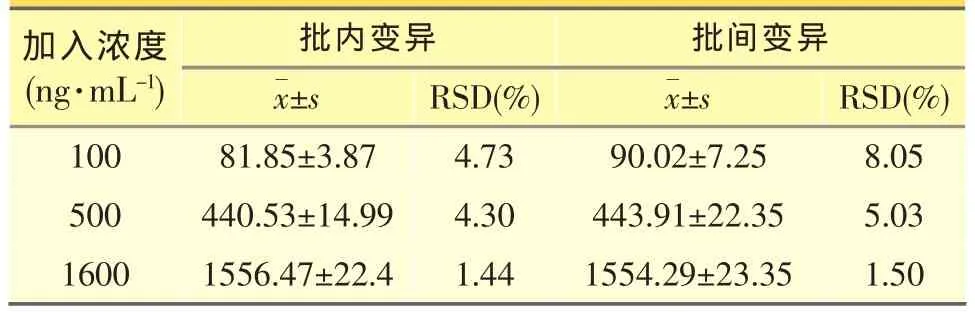
表2 HPLC法的批内和批间变异 (±s,n=5)
2.1.6 稳定性考察
血浆样品处理后室温放置稳定性 精密量取兰索拉唑标准溶液50 μL,加入空白血浆0.5 mL,制备低、中、高3个不同浓度水平的血浆样品,按“血浆样品处理”项下“精密加入 50 μL 10.0 μg·mL-1奥美拉唑内标溶液”起至 “于14000 r·min-14℃离心10 min”止操作后,各浓度每2份一组在室温下分别放置 0、12、24 h 后取上清液 20 μL 进样分析,测定各组分浓度,计算血药浓度变异系数。结果表明按实验方法处理后兰索拉唑血浆样品在室温下是稳定的,RSD均小于10%。
血浆样品冷藏放置稳定性 精密量取兰索拉唑标准溶液50μL,加入空白血浆0.5mL,制备低、中、高3个不同浓度水平的血浆样品,按“血浆样品处理”项下“精密加入50μL 10.0ng·mL-1奥美拉唑内标溶液”起至“于14000r·min-14℃离心10min”止操作后,各浓度每2份一组置4℃冰箱中保存,分别在0、4、7天后取20 μL进样。测定各组分浓度,计算血药浓度变异系数。结果表明按实验方法处理后兰索拉唑血浆样品在4℃下冷藏是稳定的,RSD均小于10%。
血浆样品冻融稳定性 精密量取兰索拉唑标准溶液50 μL,加入空白血浆0.5 mL,制备低、中、高3个不同浓度水平的血浆样品,每2份一组在-20℃下分别冻融1次、2次、3次后按“血浆样品处理”项下 “精密加入 50 μL 10.0 μg·mL-1奥美拉唑内标溶液”起操作。结果表明血浆中兰索拉唑在-20℃下反复冻融是稳定的,RSD均小于10%。
2.2 兰索拉唑在正常及溃疡模型家兔体内药代动力学研究
将兰索拉唑注射液分别给予正常及溃疡模型家兔耳缘静脉滴注,按“1.5.1”项下采血方案进行试验,血浆样本处理方法按“1.5.2”项下进行,血药浓度按照“2.1.2”项下标准曲线进行计算。结果见表3,兰索拉唑平均血药浓度对时间曲线见图2。
表3 正常及溃疡模型家兔静脉滴注兰索拉唑后血浆中的药物浓度(±s,n=6)
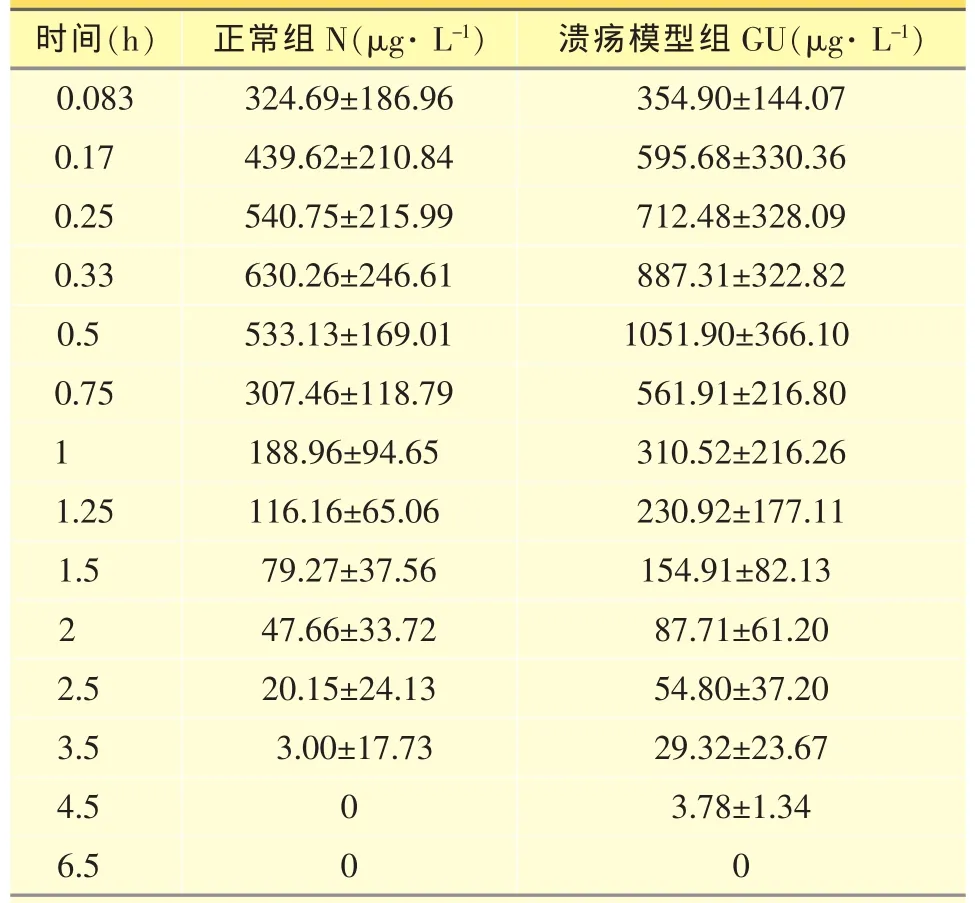
表3 正常及溃疡模型家兔静脉滴注兰索拉唑后血浆中的药物浓度(±s,n=6)
(注:0表示药物浓度低于最低检测限)
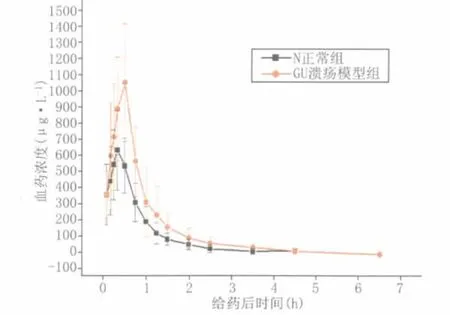
图2 正常及溃疡模型家兔静脉给予兰索拉唑后平均药时曲线
根据AIC进行房室模型判别,结果表明兰索拉唑在溃疡兔体内药代动力学行为符合二室模型,故采用“DAS2.0”软件按二室模型进行拟合,求得正常及溃疡兔静脉滴注兰索拉唑后的主要药代动力学参数,结果见表4(按矩量法求得)。
表4 正常及溃疡模型家兔静脉给予兰索拉唑后药代动力学参数 (±s,n=6)
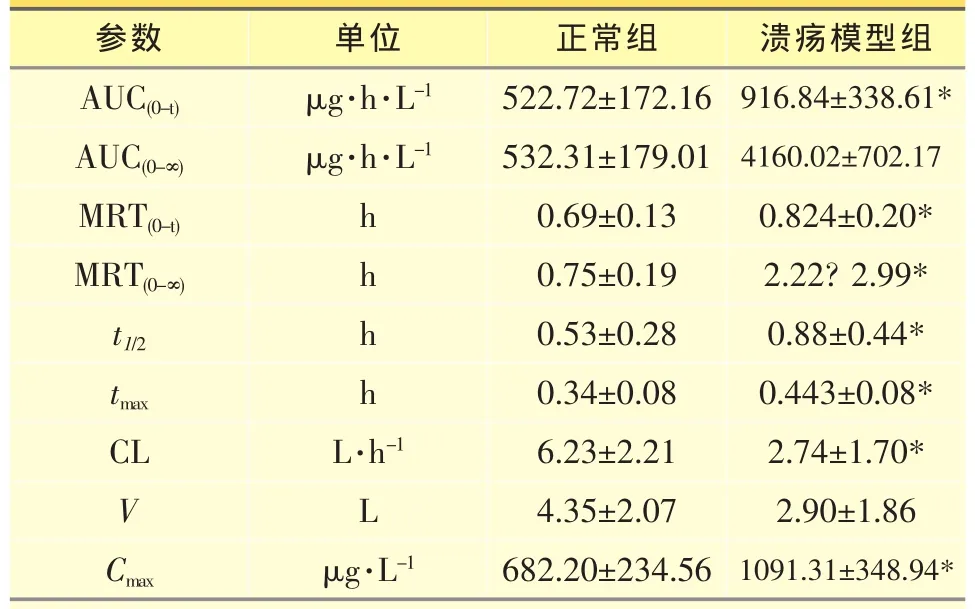
表4 正常及溃疡模型家兔静脉给予兰索拉唑后药代动力学参数 (±s,n=6)
(与正常组比较:*P<0.05)
由表4可见,分析时间内兰索拉唑在溃疡模型家兔体内AUC明显升高(P<0.05),兰索拉唑在溃疡模型家兔体内平均滞留时间延长,代谢速度减慢,血浆清除亦减慢(MRT(0-t)、t1/2、tmax、CL 及 Cmax和正常组比较P均<0.05),提示胃溃疡病理状态影响兰索拉唑的药代动力学行为。
3 讨 论
本实验发现,兰索拉唑在溃疡模型家兔体内过程发生了显著变化,其体内AUC(0-6.5)明显增加,体内平均滞留时间显著延长,血浆消除半衰期显著增大,血浆清除率显著减小,推测可能是在胃溃疡病状态下,体内肝药酶体系发生了改变,导致兰索拉唑代谢减慢。
本实验建立了HPLC法测定兰索拉唑兔血浆药物浓度的方法,样品前处理方法简单,分析方法的灵敏度、选择性、精密度和定量分析线性关系均良好,符合生物样品分析测定要求。应用本试验所建立的分离、检测方法测定正常及溃疡兔体内兰索拉唑的血药浓度,计算其主要药动学参数,阐明了兰索拉唑在体内的经时过程,为临床药物浓度监测提供了实验依据,提高用药的安全性。
[1] 沈海蓉,李中东,钟明康.新型抗真菌药兰索拉唑[J].中国新药与临床杂志,2004,23(5):3081.
[2] 刘学峰,蒋军荣,陈建军.兰索拉唑合成路线图解[J].中国医药工业杂志,2004,35(10):635-7.
[3] Dugger HA,Carlson JD,Henderson W,et al.Bioequivalence evaluation of lansoprazole 30-mg capsules(Lanfast and Lanzor)in healthy volunteers[J].Eur J Pharmacol Biopharm,2001,51(2):153-7.
[4] D.Vijaya Bharathi,Kishore Kumar Hotha.Simultaneous estimation of four proton pump inhibitors-lansoprazole,omeprazole,pantoprazole and rabeprazole:development of a novel generic HPLC-UV method and its application to clinical pharmacokinetic study[J].Biomed.Chromatogr,2009,23(9):732-9.
[5] 曾晓晖,石 磊,罗新根,等.反相高效液相色谱法测定人血浆中兰索拉唑的浓度[J]. 中国药师,2006,9(9):823.
