注射用哌拉西林/舒巴坦治疗呼吸和泌尿系统感染多中心临床研究
2011-05-17冒国光张道友吴彩玲周巧玲邓声莉胡成平苏晓丽张征宇邓桂兴吕华冲李苌清
冒国光 ,章 辉 ,张道友 ,吴彩玲 ,周巧玲 ,敖 翔 ,邓声莉 ,胡成平,孟 婕 ,苏晓丽 ,张征宇,施 毅 ,邓桂兴,吕华冲 ,李苌清 ,王 霆*
1皖南医学院弋矶山医院,芜湖 241001;2中南大学湘雅医院,长沙 410008;3解放军南京军区南京总医院,南京210002;4湘北威尔曼制药有限公司,长沙 410331
呼吸道和泌尿道是临床常见的感染部位,均位居医院和社区感染的前列。近年来,随着高效广谱抗菌药物大量应用于临床,呼吸道和泌尿道感染病原菌及其耐药性不断发生着变化,给临床治疗带来一定困难[1,2]。研究显示,临床病原菌对β-内酰胺类抗生素耐药最主要的机制是产生β-内酰胺酶,尤其是产超广谱 β-内酰胺酶(extended spectrum β-lactamases,ESBLs)。ESBLs的出现和流行使得青霉素类,第一、二、三代头孢菌素在临床中的应用受到严重限制[1,2]。文献显示,呼吸道和泌尿道感染中最主要病原菌如克雷伯菌属和大肠埃希菌产ESBLs的比率分别为48.5%和69.5%[3,4]。国内外已证实,克服此种耐药的有效途径之一是使用β-内酰胺类/酶抑制剂的复方制剂[5]。
1993年美国Lederle公司研发了哌拉西林/他唑巴坦(piperacillin-tazobactam,PIP/TAZ),通过联合应用β-内酰胺酶抑制剂他唑巴坦有效地解决了ESBLs引起的耐药问题。舒巴坦也是一个有效的β-内酰胺酶抑制剂,除本身具有一定的抑菌作用外,其化学成本仅为他唑巴坦的1/10[6]。鉴于此,国内研发出了具有自主知识产权(专利号为CN1167618A)的新型抗耐药菌抗生素——注射用哌拉西林舒巴坦(piperacillin-sulbactam,PIP/SBT)[7]。 处方中哌拉西林(piperacillin,PIP)是广谱青霉素,而舒巴坦钠对ESBLs可产生较强的抑制作用,两者合用时可增强PIP对产ESBLs菌的杀菌能力[8]。为了评价PIP/SBT治疗耐药菌所致呼吸和泌尿系统感染的临床疗效和安全性,皖南医学院弋矶山医院等多家医院以注射用PIP/TAZ作对照,进行多中心、随机、对照、双盲临床研究,现予以总结。
1 材料、对象与方法
1.1 试验设计
用多中心、随机、双盲、阳性药、平行对照试验方法。
1.2 病例选择标准
纳入标准:年龄18~65岁的住院或门诊患者;经临床和实验室确诊的中、重度急性细菌感染;未使用其他抗菌药物或使用3 d后确诊无效,且未发现对PIP/SBT耐药致病菌存在;受试者已签署知情同意书。
排除标准:对β-内酰胺类药物过敏者;严重心功能不全,肝肾功能损害(ALT、AST、Urea、Cr≥正常高限2倍者)者;有精神、神经疾患,晚期肿瘤及血液病患者;妊娠期和哺乳期妇女;依从性差或生命垂危,不能完成疗程者;必须联合应用其它抗菌药物的严重感染者。
剔除标准:试验期间加用或换用其他抗菌药物者;用药不足72 h或因故中断治疗,无法评价疗效者;因严重药物不良反应停药者不纳入疗效分析,但纳入药物不良反应统计;为达细菌培养阳性率80%以上,用药后3 d内,细菌培养阴性者可剔除。
停药标准:依从性差、不能按试验方案完成试验者;出现严重药物不良反应或化验值明显异常、不宜继续用药者;用药3~5 d病情无改善或有加重者;病人或家属要求停药者。
1.3 实验病种与菌种
呼吸系统感染:急性化脓性扁桃体炎、急性支气管炎、慢性支气管炎急性发作、支气管扩张合并肺部感染、肺炎及其他肺部感染。
泌尿系统感染:急性膀胱炎、肾盂肾炎、复杂性尿路感染等。
对PIP单方耐药,对PIP/SBT和PIP/TAZ敏感的产β-内酰胺酶的革兰阴性、阳性菌,如甲氧西林敏感金黄色葡萄球菌和凝固酶阴性葡萄球菌、卡他莫拉菌、肺炎链球菌、流感嗜血杆菌、化脓性链球菌、肠球菌、大肠埃希菌、克雷伯菌、肠杆菌属、不动杆菌、铜绿假单胞菌、阴沟肠杆菌、沙门菌、枸橼酸杆菌属、沙雷菌属、奇异变形杆菌、普通变形杆菌、摩根菌等。
1.4 药品
试验药:PIP/SBT (2︰1),粉针剂,1.5 g/瓶,批号:020501,由湘北威尔曼制药有限公司生产。
对照药:PIP/TAZ(8︰1),粉针剂,2.25 g/瓶,批号:20020801,由海南三洋德林药业有限公司生产。
1.5 给药方法
给予含PIP量相同的试验药和对照药,试验药每次6.0 g,对照药每次4.5 g,每日8︰00和20︰00各给药1次。溶于5%葡萄糖注射液500 mL中静滴,滴注时间 60~90 min,疗程 7~10 d。
1.6 观察指标
临床观察:试验期间每日详细观察患者症状、体征变化,并按观察表要求准确记录。
不良事件观察:试验中密切观察并记录患者出现的与治疗目的有关的各种反应,如发生时间、表现、程度、处理经过及转归。若出现严重药物不良反应致命、致残,需入院治疗或致住院时间延长等,必须立即通知临床试验负责单位、研制单位及卫生行政部门。
临床检验:血常规在用药前24 h内、用药后第4 d、停药后第1 d各查1次。肝、肾功能试验(ALT、AST、ALP、Urea、Cr),用药前及停药后各 1 次, 有异常者需追踪至正常。呼吸系统感染者,用药前及停药后各1次胸片检查。泌尿系统感染者,尿常规需在用药前、用药第4 d和用药后各查1次。
细菌学检查:细菌培养,用药前及停药后第1日各1次,用药前致病菌阳性率应达80%以上。各参研单位在分离出致病菌后,测定细菌对 PIP、PIP/SBT、PIP/TAZ、氨苄西林、氨苄西林/舒巴坦、头孢唑林纸片(中国药品生物制品检定所提供)的敏感性。菌种保留,集中将分离菌送至临床试验组长单位,用琼脂稀释法测定以上抗生素的MIC值,用Nitrocefin检测β-内酰胺酶。
1.7 疗效评价标准
临床疗效:依据《抗菌药物临床研究指导原则》分为痊愈、显效、进步、无效4级,痊愈与显效合计为有效,据此计算有效率。
细菌学疗效:按清除、部分清除、替换、再感染4级评定;细菌学疗效分析包括各种致病菌感染的有效率、细菌清除率,并根据CLSI2002标准测定MIC。
1.8 药物不良反应评价
评价不良反应和检验值异常与试验药物的关系;按肯定有关、很可能有关、可能有关、可能无关、无关5级进行评价,前3者入计为药物不良反应。
1.9 资料处理及统计学分析
临床试验资料经复核后输入电脑,对试验组与对照组一般资料进行统计,比较证实资料有可比性后,用统计软件NDST-Excel进行分析,用SAS 6.12软件进行复核。依资料属性进行分析。所有统计检验均采用双侧检验,P值≤0.05的为差别有统计学意义。计量资料采用均数±标准差进行统计描述,基础值比较采用配对t检验。两组治疗前后的变化采用方差分析和Wilcoxon秩和检验。多中心齐性采用CMH分析。计数资料采用频数(构成比)进行统计描述,两组治疗前后的变化采用χ2检验或非参数检验。
2 结 果
2.1 一般资料比较
试验组共进入临床试验病例105例,因不良反应中途退出4例,失访脱落1例,故临床有效病例100例;细菌学疗效评价93例,药物不良反应评价105例。对照组共进入临床试验病例105例,因不良反应中途退出1例,失访脱落1例,故临床有效病例103例;细菌学疗效评价83例,药物不良反应评价105例。
试验组与对照组入选病例的各参数,包括性别、年龄、体重、生命体征、病情、临床诊断、合并疾病、过敏病史和试验前用药、合并用药、依从性、用药程度、细菌阳性率及菌种的分布、治疗前病情总积分等,经统计分析,差异均无统计学意义(P>0.05),说明本项临床试验条件、病情程度与病例分配符合试验方案和统计分析要求。
2.2 临床疗效分析
PIP/SBT和PIP/TAZ治疗105例细菌性呼吸系统感染,两组有效率分别为92.3%和84.9%,其中痊愈率分别为46.2%和41.5%。治疗98例细菌性泌尿系统感染,两组有效率分别为97.9%和98.0%,其中痊愈率分别为81.2%和76.0%。将呼吸和泌尿系统感染病例合并,两组的痊愈率分别为63.0%和58.2%,有效率分别为95.0%和91.3%。经统计学检验,以上结果表明试验药和对照药间的差异均无统计学意义(P>0.05),见表 1。
2.3 细菌学疗效比较
两组细菌学阳性率分别为90.0%和78.6%,经PIP/SBT和PIP/TAZ治疗后,致病菌的总清除率分别为90.0%和95.1%。其中,PIP/SBT对革兰阳性菌和阴性菌的清除率分别为95.2%和88.1%,PIP/TAZ对革兰阳性菌和阴性菌的清除率分别为94.4%和95.1%。经统计分析,以上结果试验药和对照药间的差异均无统计学意义(P>0.05,见表2)
2.4 MIC测定结果
共检出15种致病菌共180株,以大肠埃希菌(28.3%)、表皮葡萄球菌(13.9%)、克雷伯菌(11.1%)、铜绿假单胞菌(8.3%)等为主,占61.7%。受试菌MIC测定结果见表3。由表3可见PIP/SBT对临床常见的革兰阳性和革兰阴性致病菌均具有较好的抗菌活性。
2.5 安全性评价
进行药物安全性评价的病例共210例,PIP/SBT组和PIP/TAZ组各105例。PIP/SBT组有皮疹和皮肤瘙痒各2例(停药消失),轻度恶心2例,ALT升高1例 (停药后逐渐恢复),不良反应发生率为6.8%。PIP/TAZ组出现皮疹和皮肤瘙痒各1例(停药消失),轻度恶心1例,ALT升高2例(停药后逐渐恢复),不良反应发生率为4.8%。经统计分析,两组不良反应发生率的差异无统计学意义(P>0.05)。
3 讨 论
本临床试验观察了湘北威尔曼制药有限公司生产的PIP/SBT(2︰1)治疗呼吸和泌尿系统中、重度细菌性感染共100例,取得了满意的临床疗效和细菌学疗效,有效率为95.0%,细菌清除率90.0%,药物不良反应发生率为6.8%,上述结果同对照药物PIP/TAZ(8︰1)无统计学差异。
国内多家研究机构对PIP/SBT的体内外活性进行了系统研究。宣天芝等[9]研究显示,PIP/SBT对临床常见5种致病菌(铜绿假单胞菌、大肠埃希菌、肺炎克雷伯菌、金葡球菌和粪肠球菌)的MIC和MBC非常接近,差异在0~2之间,表明PIP/SBT为杀菌剂。四川大学华西医院[10]、北京大学第一医院[11]、解放军总医院[12]等多个研究显示,PIP/SBT对临床分离需氧菌及兼性菌(包括金黄色葡萄球菌、表皮葡萄球菌、其它葡萄球菌、大肠埃希菌、肠杆菌属、克雷伯菌属、不动杆菌属、铜绿假单胞菌、其它假单胞菌、枸橼酸杆菌、肠球菌、变形杆菌、摩根菌、沙雷菌及其它革兰阴性菌)和厌氧菌(包括类杆菌属、梭形杆菌属、卟啉单胞菌、放线菌、口腔纤毛菌等)的体外抗菌活性较强,优于PIP。四川大学华西医院[13]用产酶的金黄色葡萄球菌、大肠埃希菌、肺炎克雷伯菌及铜绿假单胞菌建立感染动物模型,评价PIP/SBT对感染小鼠的保护作用,结果显示,PIP/SBT(2:1)的保护作用比PIP强1.8~3.6倍,也强于阿莫西林/舒巴坦(2:1)。本研究共检出15种致病菌共180株,以大肠埃希菌(28.3%)、表皮葡萄球菌(13.9%)、克雷伯菌(11.1%)、铜绿假单胞菌(8.3%)等为主,占61.7%,同文献报道一致[14,15]。结合PIP/SBT的体外抗菌谱和动物体内抗菌试验结果,本研究说明目前临床流行的常见致病菌均在PIP/SBT的抗菌谱内,也是PIP/SBT治疗呼吸、泌尿系统感染获得满意的有效率和细菌清除率的根本原因所在。
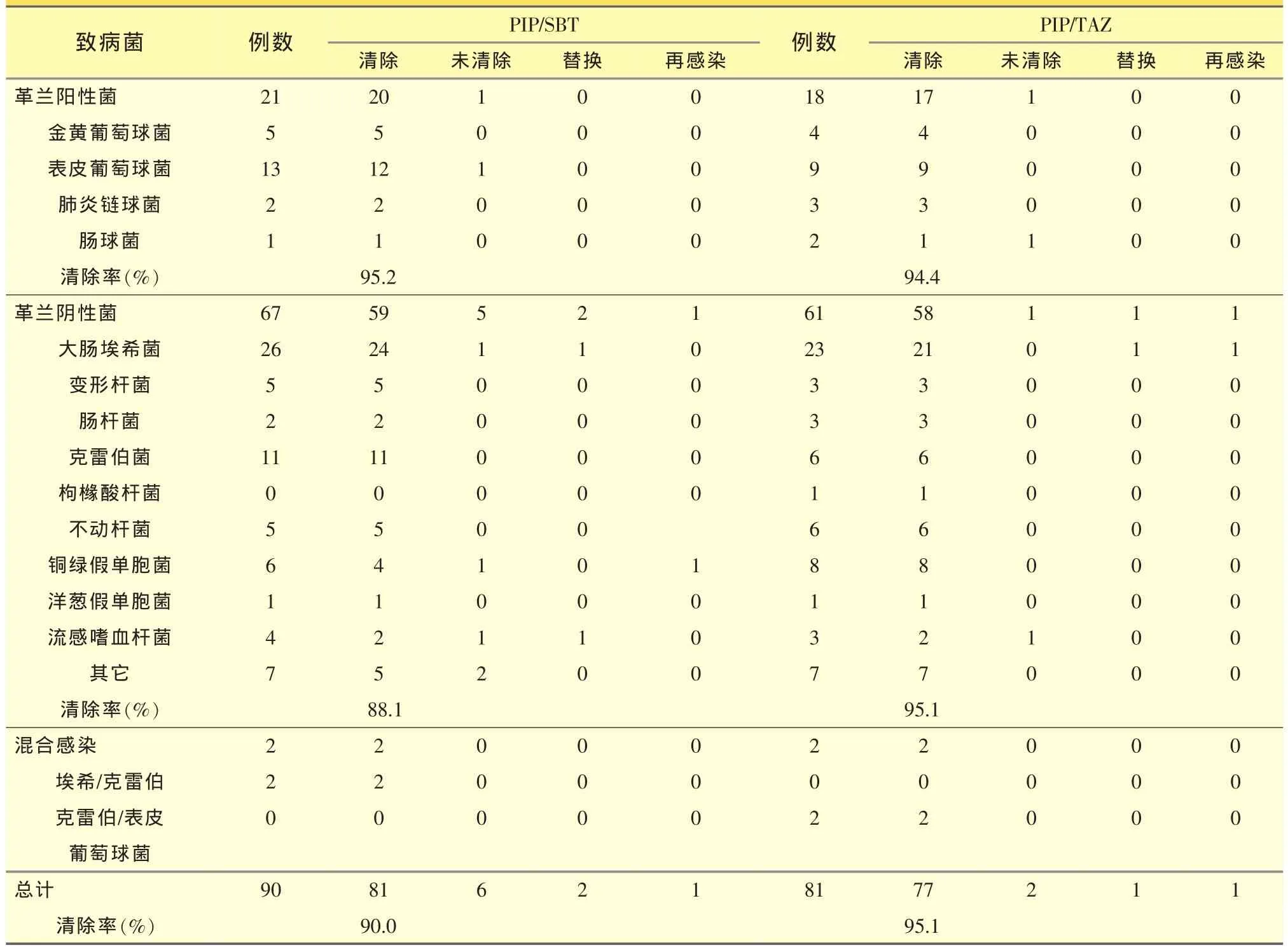
表2 PIP/SBT和PIP/TAZ治疗中、重度感染的细菌清除率

表3 临床致病菌对PIP、PIP/SBT、PIP/TAZ的MIC值(mg·L-1)
PIP/TAZ由美国Lederle公司于1993年研发上市,有效地解决了ESBLs引起的耐药问题,在全球获得了广泛应用。本研究证明,我国自主研发的PIP/SBT同PIP/TAZ具有相同的疗效和安全性,可广泛应用于临床。此外,由于舒巴坦比他唑巴坦合成的化学成本低,因此PIP/SBT比PIP/TAZ更经济。
总之,PIP/SBT明确针对目前临床细菌耐药产生机制,延长了PIP使用寿命,治疗目前医院流行的各种产酶菌所致中、重度感染效果显著,不良反应低,可作为急性细菌性感染治疗的一线药物。
[1] 巩玉梅.产超广谱β内酰胺酶病原菌的检测及耐药结果分析[J].中国现代药物应用,2010,4(7):107-8.
[2] 张兴艳,王 霆,李苌清,等.革兰阴性菌对哌拉西林耐药性的国内文献分析[J].药物流行病学杂志,2010,19(5):288-91.
[3] 刘小华,吕志英,陈数珍,等.大肠埃希菌、肺炎克雷伯菌产超广谱β-内酰胺酶检测及药敏分析 [J].中外医学研究,2010,8(5):20-1.
[4] 彭 俊,金 今,周喜桃,等.痰液及尿液中产超广谱β-内酰胺酶大肠埃希菌的耐药性分析 [J].检验医学与临床,2010,7(9):811-3.
[5] Wang FD,Lin ML,Lee WS,et al.In vitro activities of beta-lactam antibiotics alone and in combination with sulbactam against Gram-negative bacteria[J].Int J Antimicrob Agents,2004,23(6):590-5.
[6] 李小青,黄文祥.β-内酰胺酶抑制剂研究进展[J].现代医药卫生,2006,22(3):356-7.
[7] 孙明杰,吕华冲,王 霆.注射用哌拉西林钠/舒巴坦钠(2︰1)[J].中国新药杂志,2007,16(13):1061-4.
[8] Hung MN,Hsueh PR,Chang HT,et al.In vitro activities of various piperacillin and sulbactam combinations against bacterial pathogens isolated from Intensive Care Units in Taiwan:SMART 2004 programme data[J].Int J Antimicrob Agents,2007,29(2):145-52.
[9] 宣天芝,陶风荣,许宏涛,等.哌拉西林/舒巴坦对临床分离菌的体外抗菌作用 [J].中国抗生素杂志,2001,26(6):454-6,463.
[10] 冯 萍,吕晓菊,俞汝佳,等.哌拉西林/舒巴坦对临床分离菌的体外抗菌活性研究 [J].中国抗生素杂志,2002,27(8):479-84.
[11] 王 琪,刘 健,许 军,等.不同配比哌拉西林-舒巴坦对545株临床分离菌体外抗菌作用研究 [J].中国抗感染化疗杂志,2003,3(5):280-3.
[12] 李聪然,董 涛,梁蓓蓓,等.哌拉西林/舒巴坦等5种抗菌药物对常见致病菌体外抗菌活性的研究 [J].解放军药学学报,2007,23(1):25-9.
[13] 吕晓菊,俞汝佳,冯 萍,等.哌拉西林钠/舒巴坦钠体外、体内药效学研究[J].四川大学学报(医学版),2004,35(2):289-91.
[14] 刘焱斌,吕晓菊,杨 尧,等.哌拉西林钠/舒巴坦钠(4:1)治疗急性细菌性感染多中心随机单盲对照临床研究[J].中国临床药理学杂志,2005,32(6),403-6.
[15] 鲁 钢,周维春,李万志,等.哌拉西林/舒巴坦与美洛西林/舒巴坦治疗呼吸道感染的疗效比较[J].实用药物与临床,2005,8(1):24-6.
