在线固相萃取-HPLC法测定比格尔犬血浆中丹参素的含量
2011-05-15崔晓如窦颖辉杭太俊范国荣
王 丽,崔晓如,窦颖辉,闻 俊,杭太俊,范国荣*
(1.中国药科大学药学院药物分析学教研室,南京 210009;2.第二军医大学药学院药物分析学教研室,上海 200433)
丹参素(danshensu)又名D(+)-β-(3,4-二羟基苯基)-乳酸,是从唇形科植物丹参(Salvia miltiorrhiza Bge.)的根中提取分离的一种酚性芳香酸类化合物,是丹参的主要有效成分之一,具有保护心肌、抗血栓、抗炎、抗肿瘤等多种药理活性[1]。近年来,中药的药动学研究已经成为药学研究的一个热点,目前已有多篇以丹参素作为指标成分的药动学研究,不过这些文献中多采用 HPLC[2]、HPLC/MS/MS[3]、在线固相萃取-HPLC法[4]、在线固相萃取-HPLC/MS/MS法[5]、胶束毛细管电泳法[6]和荧光光谱法[7]等方法,上述方法中样品前处理较为复杂耗时,分析时间较长或检测限较高,不适于大量生物样品的分析。本研究在文献方法的基础上进行了优化,建立了一种简便、快速的新型在线固相萃取-HPLC法测定犬血浆中丹参素的浓度。
1 仪器、试药和动物
岛津超高效液相色谱仪:LC-20AD型泵,SIL-20A型自动进样器,CTO-20AC型柱温箱,SPD-20A型紫外可见检测器,DGU-20A3型脱气机,LV-306R型自动高压切换阀及LC-solution色谱工作站(日本岛津公司)。XW-80A型涡旋混合器(上海医科大学仪器厂),Thermo CR3i冷冻离心机(美国热电公司)。HA-202M电子天平(日本A&D公司)。丹参素对照品(含量103%,批号:20081103-2-1)由第二军医大学药学院新药研究中心提供;内标对羟基苯甲酸对照品(含量99%,批号:H0207)购自梯希爱(上海)化成工业发展有限公司。氯化钠注射液购自上海百特医疗用品有限公司,乙腈为色谱纯,其余试剂均为分析纯。比格尔犬6条,雌雄各半,犬龄6~8个月,体重9~10 kg,由上海新冈实验动物场提供,实验动物合格证号:SCXK(沪)2007-0009。
2 方法和结果
2.1 色谱条件 富集柱 Lichrospher C18柱(37 mm ×4.6 mm,25 μ m),分析柱 Ultimate XBC18柱 (50 mm ×4.6 mm,5 μ m);富集流动相:乙腈-10 mmol/L NaH2PO4(5∶95),流速 2 ml/min;分析流动相:乙腈-10 mmol/L NaH2PO4(11∶89),流速0.8 ml/min;切换时间0.2 min,切回时间3.0 min,分析时间 5 min;检测波长 285 nm;进样量 100 μ l。
2.2 溶液配制 (1)丹参素标准溶液 精密称取丹参素对照品10 mg,置于10 ml棕色量瓶中,用甲醇溶解并定容,制成浓度为1 mg/ml的丹参素对照品贮备液。以40%甲醇稀释该贮备液获得浓度依次为0.20、0.50、1.00、2.00、5.00、10.00、20.00 μ g/ml的丹参素系列浓度标准溶液,4℃冰箱中避光保存备用。(2)内标工作溶液 精密称取对羟基苯甲酸对照品10 mg,置于10 ml棕色量瓶中,用甲醇溶解并定容,制成浓度为1 mg/ml的内标贮备液。同样以40%甲醇稀释得1 μ g/ml的内标工作溶液,4℃冰箱中避光保存备用。
2.3 在线固相萃取过程 在线固相萃取系统示意图见图1[8]。在线固相萃取过程主要是通过一个切换阀来实现的。当切换阀在1号位时,样品先进入富集柱,经富集流动相冲洗,使血浆中的干扰大分子和其他水溶性杂质被冲掉,而被测物保留在柱子上。转动切换阀至0号位,此时富集柱和分析柱成串联状态,分析流动相把样品从富集柱上反冲进入分析柱,进行分离测定。最后切回切换阀至1号位,分析流动相继续对被测物进行分析,富集流动相冲洗并平衡富集柱,等待下次进样。
2.4 血浆样品预处理 取犬血浆样品0.1 ml,加入内标工作溶液 10 μ l,涡旋混匀,加入 6%高氯酸溶液80 μ l,涡旋混合3 min,2.125 5×104×g离心10 min,取上清液100 μ l进样分析。
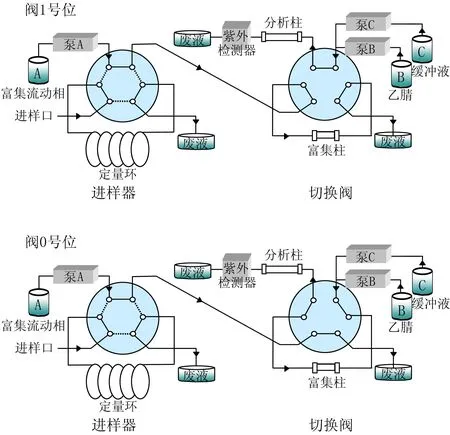
图1 在线固相萃取系统示意图[8]Figure 1 Schematic diagram of the on-line SPE system using a six-port switching valve(step 1,valve 1;step 2,valve0;step 3,valve 1)
2.5 标准曲线与线性范围 取比格尔犬空白血浆90 μ l,共7份,分别加入丹参素系列浓度标准溶液10 μ l,制得相当于丹参素浓度分别为 20、50、100、200、500、1000、2000 ng/ml标准含药血浆样品。按2.4项下操作,以丹参素浓度(c)为横坐标,丹参素与内标峰面积比值(Y)为纵坐标,用最小二乘法进行加权线性回归,得回归方程为Y=6.120×10-3c+6.907×10-3,r=0.999 6(n=7)。在20~2000 ng/ml浓度范围内血浆药物浓度与峰面积比值线性关系良好。定量下限为20 ng/ml。
2.6 方法专属性 以2.1项下色谱条件测得空白血浆、空白血浆标准添加丹参素和对羟基苯甲酸及给药后血浆样品的色谱图见图2。由图2可见,丹参素和对羟基苯甲酸的保留时间分别约为2.5、4.3 min,内源性物质均不干扰丹参素和对羟基苯甲酸的色谱分离。
2.7 精密度及相对回收率实验 取空白血浆15份分为3组,分别制备含50、200和 1 600 ng/ml 3种浓度的含药血浆样品,各5份。按2.4项下方法处理后1 d内连续进样,计算得日内 RSD分别为5.82%、2.40%、2.45%(n=5);连续测定3d,计算得日间 RSD分别为 6.35%、2.37%、6.06%(n=3)。3种浓度的丹参素含药血浆样品的相对回收率分别为(100.07±6.35)%、(106.86±2.54)%、(105.90±6.42)%(n=15)。
2.8 绝对回收率实验 同上配制低、中、高浓度的含药血浆样品,按2.4项下方法处理并测定,测得的丹参素峰面积与等浓度丹参素溶液直接进样所得峰面积作比,得3种浓度血浆样品的绝对回收率分别为80.05%、80.21%和84.89%(n=5)。
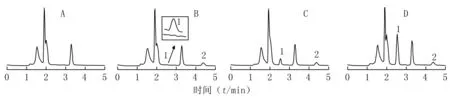
图2 比格尔犬血浆中丹参素的HPLC谱图Figure 2 HPLC photograms of danshensu in beagle dog plasma
2.9 稳定性实验 同上配制50、1 600 ng/ml的含药血浆样品,按2.4项下方法处理后分别进行稳定性实验。分别考察血浆样品在室温放置2 h、进样器放置10 h、冻融3次和-20℃冷冻放置20 d的稳定性。结果见表1。结果表明丹参素血浆样品在上述条件下稳定。
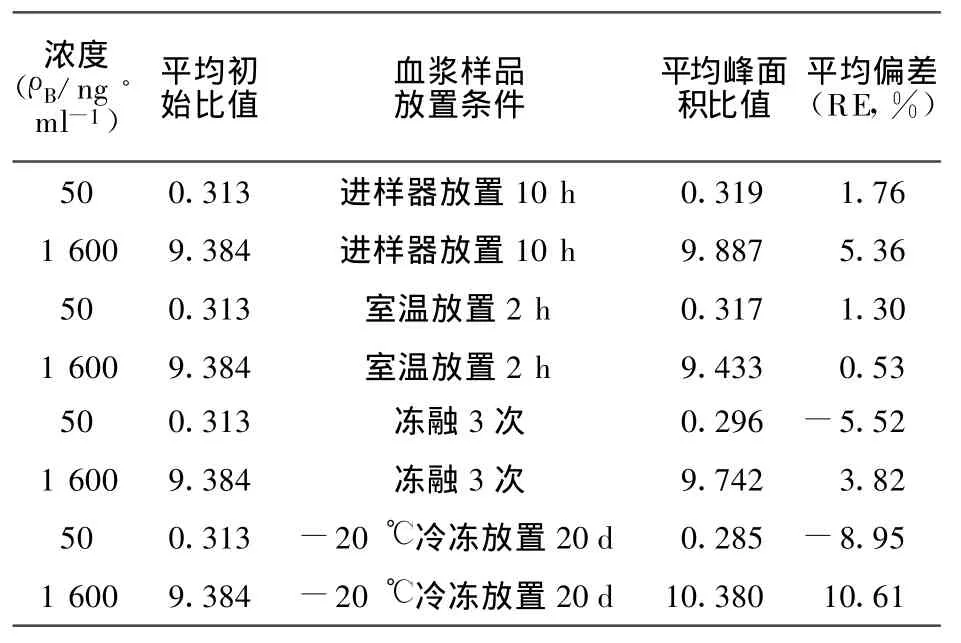
表1 丹参素血浆样品稳定性考察结果T able 1 Stability test results of danshensu in beagle dogplasma
2.10 稀释效应实验 静脉给药时部分血浆样品中药物浓度较高,部分犬血浆样品需要稀释,因此要考察丹参素血浆样品的稀释效应。由于血浆样品直接稀释到相应浓度会引起较大的操作误差,本实验以1/2、1/5为基数对血浆样品做相应的稀释。配制血浆标准曲线样品和血浆质量控制样品,并配制稀释至1/2、1/5、1/10、1/100后的中浓度和高浓度血浆质量控制样品各5份,按2.4项下方法处理后分别进样,计算得血浆样品经过稀释后,其相对偏差值均<6%,符合生物样品分析测定要求,说明高浓度血浆样品经稀释后测定结果不影响其实际血药浓度。
2.11 比格尔犬体内血药浓度测定 健康成年比格尔犬6只,雌雄各半,依次称重,按10 mg/kg的剂量静脉注射丹参素氯化钠注射液,分别于给药前及给药后0、2、5、10、20 、40 min,以及 1、1.5 、2、3、4、6、8、12 h在比格尔犬一侧后肢静脉取血2 ml,置肝素钠抗凝离心管中,离心(4.555×103×g)10 min,分取上层血浆,-80℃避光保存。取血浆样品,按2.4项下方法处理并测定,按标准曲线方程计算各时间点血浆药物浓度,结果见图3。
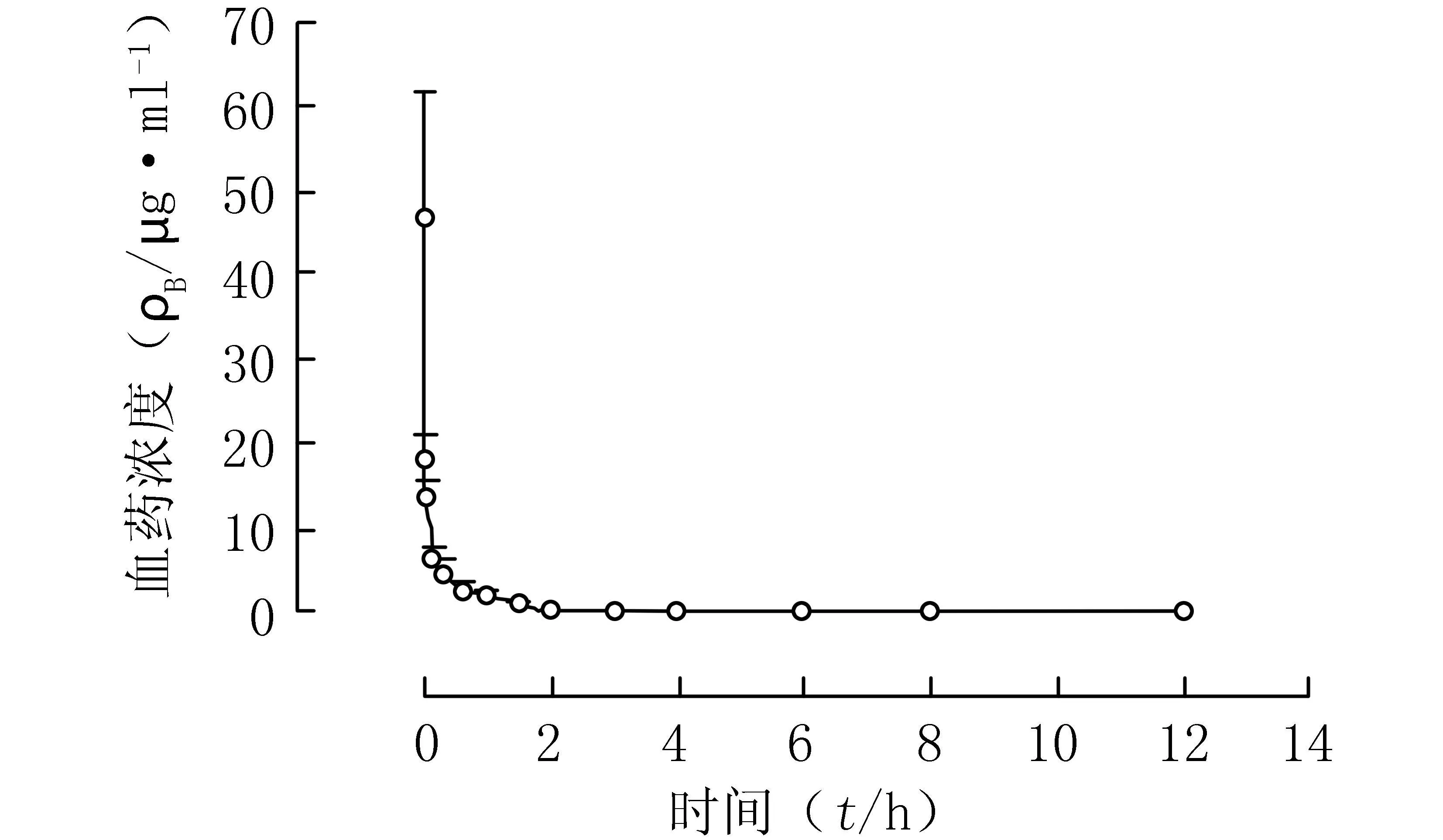
图3 比格尔犬单剂量静注10 mg/kg丹参素后的药-时曲线Figure3Mean drug plasma concentration-time curve of danshensu after single intravenous dose of 10 mg/kg in beagle dogs;n=6
3 讨 论
3.1 富集流动相的选择 富集流动相常以水溶性溶液为主,以除去部分蛋白质及其他内源性水溶性杂质并使被测组分保留在富集柱上。但由于犬血浆样品中干扰物质较多,故在富集流动相中加入低比例乙腈,更有利于除去血浆中的干扰物质。
3.2 预处理方法的选择 在线固相萃取技术允许血浆样品直接进样,但血浆样品内大量蛋白质及内源性杂质会使柱子阻塞、柱压升高,影响柱子的柱效并减少柱子的使用寿命。因此在实际操作过程中,通常用沉淀法除去血浆样品中的部分蛋白质后再进样分析,既提高分离效果,又延长柱子使用寿命。
3.3 切换时间和切回时间的选择 在线固相萃取时切换时间较短,富集流动相的流速较大,以有利于在短时间内冲掉大部分蛋白质并使被测物保留在富集柱上。选择合适的切回时间,有利于被测物完全转移至分析柱并有充足的时间平衡富集柱。因此选择0.2 min作为切换时间,3.0 min作为切回时间,整个分析时间5 min。
3.4 富集柱的选择 富集柱的长度应适宜,防止高流速时两根柱子串联造成极高的柱压;富集柱填料的粒径应适宜,既利于冲掉大分子蛋白质,又利于保留被测物。因此选择了自制 Lichrospher C18柱(37 mm×4.6 mm,25 μ m)作为富集柱。
本研究采用在线固相萃取-HPLC法测定比格尔犬血浆样品中丹参素的浓度,使样品的纯化、富集与分析同步进行,操作简单,提取效率高,分析时间短,适于大量生物样品的分析。
[1] 李艳杰,孙玉华.丹参素药理作用研究进展[J].延边大学医学学报,2006,29(1):73-74.Li YanJie,Sun YuHua.Advances in research on pharmacological effects of danshensu[J].J Med Sci Yanbian Univ,2006,29(1):73-74.Chinese.
[2] Li Xiao Li,Li Xiao Rong,Wang LiJuan,et al.Simultaneous determination of danshensu,ferulic acid,cry ptotanshinone and tanshinoneⅡA in rabbit plasma by HPLC and their pharmacokinetic application in danxiongfang[J].J Pharm Biomed Anal,2007,44(5):1106-1112.
[3] Liu Yun,Li XiaoRong,Li YuHang,et al.Simultaneous determination of danshensu,rosmarinic acid,cryptotanshinone,tanshinoneⅡA,tanshinoneⅠand dihydrotanshinoneⅠ by liquid chromatographic-mass spectrometry and the application to pharmacokinetics in rats[J].J Pharm Biomed Anal,2010,53(3):698-704.
[4] 赵新峰,祝忠民,刘爱芳,等.柱切换法在复方丹参滴丸中丹参素药代动力学研究中的应用[J].中成药,2004,26(6):490-492.Zhao XinFeng,Zhu ZhongMin,Liu AiFang,et al.Qualitative and quantitative analysis of Compound Danshen Dripping Pills by CS-HPLC[J].Chin T radit Pat M ed,2004,26(6):490-492.Chinese with abstract in English.
[5] Pei WeiJing,Zhao XinFeng,Zhu ZhongMin,et al.Study of the determination and pharmacokinetics of compound Danshen dripping pills in human serum by column switching liquid chromatography electrospray ion trap mass spectrometry[J].J Chromatogr B Analyt T echnol Biomed Life Sci,2004,809(2):237-242.
[6] 杨 燕,杨 荣,卫引茂,等.胶束毛细管电泳法测定家兔体内的丹参素及药代动力学和组织分布[J].药物分析杂志,2008,28(3):362-366.Yang Yan,Yang Rong,Wei YinM ao,et al.MEKC determination of pharmacokinetic and tissue distribution study of Danshensu in rabbits[J].Chin J Pharm Anal,2008,28(3):362-366.Chinese with abstract in English.
[7] 何怀冰,王 蓓,陈 沄,等.荧光光谱法测定家兔中丹参素血浓度及其药物动力学参数[J].上海第一医学院学报,1983,10(4):295-300.He HuaiBing,Wang Bei,Chen Yun,et al.Spectrofluorometric determination of rabbit plasma level and pharmacokinetic parameters of“Dan-shen-su”[J].Acta Acad Med Primae Shanghai,1983,10(4):295-300.Chinese with abstract in English.
[8] Xie Rui,Wen Jun,Wei Hua,et al.Hig h-throughput determination of faropenem in human plasma and urine by on-line solid-phase extraction coupled to high-performance liquid chromatography with UV detection and its application to the pharmacokinetic study[J].J Pharm Biomed Anal,2010,52(1):114-121.
