pH值及金属离子对樟树果实红色素吸收光谱的影响
2011-01-24田春莲文赤夫
田春莲,文赤夫
(吉首大学林产化工工程湖南省重点实验室,湖南张家界 427000)
近年来,人们发现合成色素多数有慢性毒性和致癌作用,已意识到它对人体健康的威胁,各国开始限制合成色素的使用[1],而实用天然色素却以每年10%的销售额递增[2],对天然色素研究也愈为深入 ;樟树〔Cinnam om um cam phora(L.)Presl〕属樟科樟属的常绿乔木,是我国特有的园林绿化树种,但因大量落果对城市环境造成污染[3],目前,虽对樟树果实有一定利用和研究,如樟树果实红色素抑菌作用、提取工艺及稳定性[4-6],但未涉及 pH值、金属离子、热稳定性因子等对樟树果实红色素吸收光谱的研究。因此,本实验研究红色素吸收光谱,旨在为综合开发樟树资源提供理论依据。
1 材料与方法
1.1 材料
樟树果实采自吉首大学张家界校区校园内,紫红色,果实经去核、干燥、粉碎过 24目筛,冷藏备用。
1.2 仪器与试剂
1.2.1 主要仪器与设备
UV-160紫外可见分光光度计,日本岛津;BS-220恒温水浴锅,北京长安科学仪器厂;HM-60V酸度计,上海虹益仪器有限公司;格兰仕微波炉;CD5-2A离心机,北京;R-215旋转蒸发仪,瑞士BUCHE公司。
1.2.2 试剂
所用试剂均为国产分析纯。
1.3 实验方法
1.3.1 樟树果实色素提取纯化
樟树果实干粉→加水浸提,柠檬酸调 pH至 1~2,低火力微波辅助提取 4次,提取时间分别为 1 min、45 s、30 s、20 s,得紫红色溶液 ,过滤残渣 ,同等条件重复提取,合并滤液,4 000 r/min离心 20 min,过滤,浓缩,树脂纯化,得纯品色素。
从各相关系数来看,与南京河流表层沉积物中APA最具相关性的是有机质质量百分数(r=0.763),极显著正相关(p=0.006);其次是总磷(r=0.703),显著正相关(p=0.016);再次为可交换态氮,与硝酸盐氮、铵态氮均显著正相关。表明表层沉积物营养成分充足情况下,使各种微生物保持旺盛的新陈代谢,则APA相对较高。各种磷形态中TP与APA的相关性最好,OP其次。APA与OP相关性较好,为正相关(r=0.576)。这一现象说明调查区域沉积物的有机磷经碱性磷酸酶作用产生的无机磷为沉积物中生物所利用。可交换态氮与APA的相关性好于凯氏氮,进一步印证了上述结论。
1.3.2 樟树果实红色素最大吸收波长的测定
取樟树果实红色素原液用水稀释成色素试验液,用 UV-160紫外分光光度计在 800~400 nm波长范围内进行光谱扫描,得最大吸收波长为517 nm。
1.3.3 pH值对樟树果实红色素吸收光谱的影响
取 3 mL樟树果实红色素溶液,分别用 pH值为2.6~8.6的系列缓冲液定容至 25 mL,暗处放置1 h,以缓冲液作参比,在紫外分光光度计上自动扫描。
1.3.4 热稳定因子对樟树果实红色素吸收光谱的影响
取 2 mL红色素溶液 7份置于试管,在 100℃分别处理 0、5、10、20、30、60、120 min,冰水冷却后在800~400 nm扫描。再取 2 mL红色素溶液 9份置于试管中 ,分别于 0、30、40、50、60、70、80、90、100℃加热 30 min,冰水冷却后紫外扫描。
1.3.5 光照对樟树果实红色素吸收光谱的影响
取红色素 8 mL置于 250 mL的锥形瓶分两组置于室内和暗处,每隔 30 min取样 10 mL,在 517 nm处紫外检测。
取红色素溶液各 1 mL,分别用浓度为 0.001%、0.05%、0.01%、0.1%、1%的 NaCl、KCl、MgCl2、CaCl2、AlCl3·6H2O、FeCl3盐溶液定容至 25 mL,于暗处放置 1 h、4 h、24 h后在紫外分光光度计从 800~400 nm扫描检测。
2 结果与讨论
2.1 pH值对樟树果实红色素吸收光谱的影响
从图1可知,樟树果实红色素在 pH为 3.6~8.6的缓冲溶液中光谱吸收特性变化不一,pH为2.6~3.6的强酸性环境中,红色素在 517 nm处有吸收高峰且光谱特性稳定,说明色素在强酸性条件下稳定易保存;pH为 8.6时,最大吸收峰漂移到402 nm处,此时吸光值为 1.403,说明樟树果实红色素在碱性条件下其结构发生变化,此结论与前人研究一致[5]。
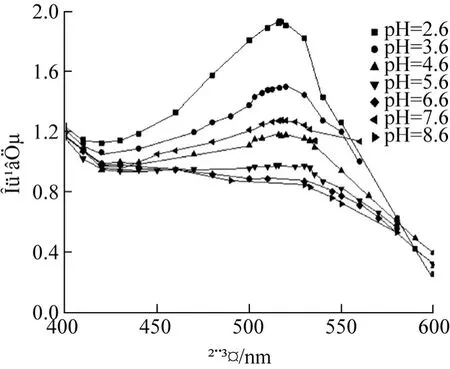
图1 pH值对红色素吸收光谱的影响
2.2 热稳定因子对樟树果实红色素吸收光谱的影响

表1 温度对红色素吸光值的影响 (λmax=517 nm)

表2 加热时间对红色素吸光值的影响 (λmax=517 nm)
表1得出:温度对樟树果实红色素吸收光谱影响较小,色素性质稳定。0~100℃内,红色素最大吸收峰在 517 nm处,,吸光值在 1.321~1.412之间;表2看出:红色素耐短时高温,随加热时间延长,吸收光谱发生变化,100℃加热 60 min以内,红色素性质稳定,517 nm处吸光值范围是 1.318~1.479,但加热 120 min时,红色素最大吸收峰移至512.5 nm,且吸光值下降至 1.189。从而判定长时间高温加热,红色素结构发生变化。
2.3 光照对樟树果实红色素吸收光谱的影响
樟树果实红色素对光的耐受性较好,光照时间对其吸收光谱无明显影响。从图2可见,随光照时间的延长,在自然光照射下,红色素吸光值随光照时间呈正态分布现象,90~120 min时,吸光值上升0.127,随后吸光值随光照时间延长而下降,避光下红色素吸光值持续平稳。因此,红色素在避光条件下易于保存。

图2 光照对红色素吸收光谱的影响
2.4 金属离子对樟树果实红色素吸收光谱的影响
2.4.1 Na+、K+处理后红色素的吸收光谱
总体来说,加入 Na+、K+的色素溶液吸收光谱无明显变化,该色素的最大吸收波长为 517 nm。但处理 4 h时,由图3得出:加入 0.1%Na+的红色素溶液吸收光谱在 517 nm后持续平稳,从 517~600 nm吸光值仅降低 0.099;24 h后,图4显示,加入0.05%K+的红色素溶液吸收光变化明显,其最大吸收波长是 477 nm,随后吸光值急剧下降;其他浓度下,当波长由 517 nm~530 nm时,吸光值呈负相关,以 0.01%K+的下降幅度最大,吸光值减少0.543。所以,在色素应用过程中也应避免长时间的Na+、K+干扰。
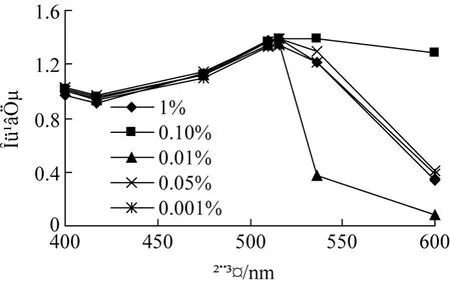
图3 Na+对红色素吸收光谱的影响(4 h)

图4 K+对红色素吸收光谱的影响 (24 h)
2.4.2 Mg2+、Ca2+对红色素吸收光谱的影响

图5 Mg2+对红色素吸收光谱的影响(1 h)
图5~10表明:加入 Mg2+、Ca2+后的红色素吸收光谱呈正态分布,但加入Mg2+后随处理时间延长至 24 h时,最大吸收波长漂移至 512 nm处;不同的Mg2+浓度对樟树果实红色素吸收光谱影响较为明显,从 400~517 nm,浓度高的上升幅度大,517~600 nm,浓度越大下降幅度越大,1%和 0.001%的吸光值分别下降 1.154与 0.897。

图6 Mg2+对红色素吸收光谱的影响 (4 h)

图7 Mg2+对红色素吸收光谱的影响 (24 h)
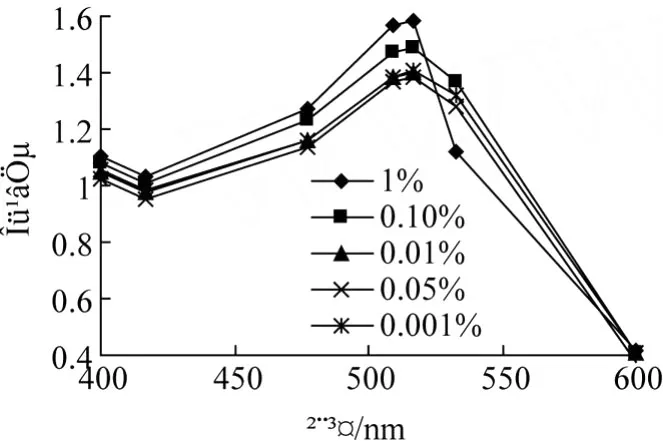
图8 Ca2+对红色素吸收光谱的影响(1 h)

图9 Ca2+对红色素吸收光谱的影响 (4 h)

图10 Ca2+对红色素吸收光谱的影响(24 h)
2.4.3 加入 Fe3+后樟树果实红色素的吸收光谱
Fe3+对樟树果实红色素吸收光谱影响最大,不同浓度和处理时间均产生明显变化。图11~13结果表明:1 h后,由于 Fe3+与色素发生了反应,红色素颜色产生变化,0.01%、0.05%产生红褐色沉淀,1%和 0.1%使色素溶液变为深褐色及浅褐色,这与前人报道的 Fe3+使花色苷颜色变褐、对色素的结构有不良影响相一致[5,7];就吸光值来说,Fe3+浓度 >0.01%,在 400~500 nm之间吸光值达到 1.8,500 nm以上,吸光值与波长成反比;从 Fe3+浓度<0.01%,吸光值随波长增加呈现下降 -上升 -再下降的趋势。因此,在该色素制取、使用和储运过程中应尽量避开铁质容器。

图11 Fe3+对红色素吸收光谱的影响 (1 h)

图12 Fe3+对红色素吸收光谱的影响(4 h)
2.4.4 加入Al3+的樟树果实红色素的吸收光谱
Al3+对樟树果实红色素吸收光谱影响显著程度介于 Fe3+和其他金属离子之间。如图所示,最大吸收波长在 517 nm,400~448 nm,吸光值随波长增加而下降,448~517 nm,吸光值与波长成正相关,517 nm后下降;不同浓度和处理时间变化幅度不同,1~4 h,0.01%~1%吸光值的变化幅度大于低浓度条件下,当处理 24 h后,以 0.05%的 Al3+处理变化最小。所以,该色素使用过程中尽量避免与铝器接触。
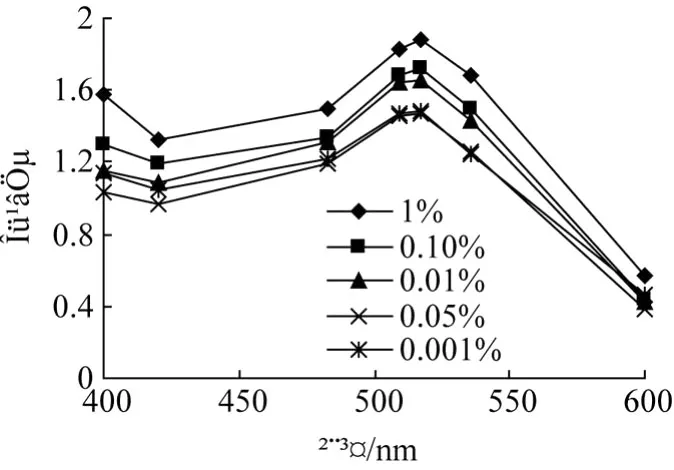
图14 Al3+对红色素吸收光谱的影响 (1 h)

图15 Al3+对红色素吸收光谱的影响 (4 h)

图16 Al3+对红色素吸收光谱的影响 (24 h)
3 结 论
(1)樟树果实色素主要成分为花色苷色素,具有一般花色苷类色素的共同特性,其吸收光谱和颜色稳定性受多种因素的影响。pH为 3.6~6.6的缓冲溶液对光谱吸收特性无明显变化,λmax是 517 nm,色素在强酸性条件下稳定易保存;pH为 8.6的碱性环境下吸收峰漂移至 402 nm,说明红色素在碱性条件下结构发生变化。
(2)温度对该色素吸收光谱影响较小,100℃以内,色素性质稳定,该色素耐短时高温,随加热时间延长,吸收光谱发生变化,100℃加热 120 min,最大吸收峰移至 512.5 nm;红色素对光的耐受性较好,自然光照射 90~120 min时,吸光值上升 0.127,避光下该色素稳定性好。提取加工及保藏中要尽量避光。
(3)大多数金属离子对樟树果实红色素吸收光谱无明显影响,但 Fe3+使红色素短时间内变色,产生沉淀,吸收光谱发生漂移,Fe3+浓度越高影响越大,吸收光谱随之改变,所以,生产中应避免接触铁、铝容器;当加入Mg2+时间延长至 24 h,最大吸收峰由 517 nm漂移至 512 nm,随 Mg2+浓度升高,从 400~517 nm及从 517~600 nm的上升或下降幅度越大。其他金属离子和氧化剂对樟树果实红色素吸收光谱的影响有待于进一步研究。
[1] 赵桂红,姚凤莲.蓝靛果天然色素提取条件研究[J].食品研究与开发,2005,26(3):106-107.
[2] 周国立.食用天然色素及其提取应用[M].济南:山东科技出版社,1993:44.
[3] 许莉勇.樟树籽的开发利用[J].浙江万里学院学报,2000,13(4):19-20.
[4] 文赤夫,曾超文,黄造成,等.樟树果实红色素的抑菌活性[J].食品与发酵工业,2007,33(4):23-25.
[5] 文赤夫,赵虹桥,田春莲,等.樟树熟果红色素提取工艺及稳定性研究[J],食品科学,2006,27(4):157-160.
[6] 蒋益花,蒋新龙.樟树果实红色素的提取及性质研究[J].生物质化学工程,2006,40(6):29-33.
[7] 吕晓玲,范辉,马淑青,等.1次和 2次精制紫甘薯色素理化特性的比较[J].食品与发酵工业,2009,35(2):7-11.
