离子液体磷钨酸盐合成及在酯化反应中的应用
2011-01-16张彦佳吕振波桂建舟江海英孟祥巍林赛燕
张彦佳, 吕振波, 刘 丹, 桂建舟, 江海英,许 敏, 孟祥巍, 林赛燕
(辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001)
酯是一种重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,其合成技术一直受到国内外广大学者的重视[1-2]。浓硫酸是酯化反应的常用催化剂,但腐蚀设备,污染环境[3]。随着对催化剂的广泛研究,发展绿色化学及环境友好催化剂日益受到人们的关注。目前出现了固体超强酸、杂多酸、强酸性阳离子交换树脂等多种酯化催化剂[4-6],但是这些催化剂的制备过程往往比较复杂,或是重复利用比较困难,存在一定的局限性。
近年来,利用离子液体作为有机反应催化剂的报道已经有很多,其中以酯化反应为热点[7-8]。离子液体用于催化酯化反应,其具有良好的催化活性。离子液体具有优异的特性,对热稳定、不挥发、不可燃、不氧化、不爆炸、低毒性,用于合成反应对环境友好[9]。在环境问题日益引起重视的今天,开发环境友好的酯化催化剂显得更为重要[10-11]。
本研究利用不含卤素原子、成本较低廉的酸性离子液体与磷钨酸反应,生成磷钨酸盐催化剂,研究其在酯化反应中的应用,得到很好的催化效果,反应结束后产物易于分离且催化剂可重复使用。
1 实验部分
1.1 原料及仪器
原料:乙醇(分析纯,国药化学试剂有限公司);乙酸(分析纯,沈阳化学试剂厂);1-甲基咪唑(分析纯,百灵威进口);1,3-丙烷磺内酯(分析纯,山东瀛寰化工有限公司);磷钨酸(分析纯,国药化学试剂有限公司)。以上试剂均为分析纯或化学纯试剂,没有特殊说明的均未进一步提纯。
仪器:日本理学D/max-RB X射线衍射仪;美国Perkin-Elmer SPECTRUM GXIII型红外谱仪(KBr压片);美国Pyris 1TGA热重分析仪;循环水式真空泵(巩义市予华仪器有限责任公司);85-1型磁力搅拌器(山东鄄城华鲁电热仪器有限公司);PE Q-Mass 910GC/MS气质联用仪。
1.2 催化剂的合成和表征
1.2.1 离子液体的合成 在100mL圆底烧瓶中加入1-甲基咪唑(31.6mL,0.4mol)和1,3-丙烷磺内酯(48.8g,0.4mol)室温搅拌3d,可得到白色固体,用乙醚(80mL乙醚洗涤5次)洗涤,除去非离子残余物并进行真空干燥得到高纯度的两性盐。
1.2.2 催化剂的合成 将H3PW12O40(约0.01 mol)溶于100mL去离子水中制得溶液,然后将上述制得的离子液(约0.03mol)加入到H3PW12O40水溶液中,室温搅拌24h,得到白色溶液,反应完全后再将溶液经过减压蒸馏除去溶液中的水分,得到白色固体,在真空干燥箱内80℃干燥为白色粉末,得到离子液体磷钨杂多酸盐(见式(1),简写为[MIMPS]3PW12O40)。

[MIMPS]3PW12O40:13C NMR(DMSO)δ:2 6.13,35.71,47.27,47.72,122.29,123.56,136.78;1H-NMR(DMSO)δ:2.09(m,2H,CH2),2.44(s,2H,CH2),3.85(s,3H,CH3),4.30(s,2H,CH2),7.70(s,H,CH),7.78(s,H,CH),9.10(s,H,CH)。
1.2.3 催化剂的表征 核磁共振实验在Varian公司的Varian Mercury-plus 300BB核磁共振光谱仪上进行,对所合成的化合物进行1H-NMR和13C-NMR测试,溶剂选用氘代二甲基亚砜(DMSO),内标物选用四甲基硅烷(TMS)。
热重实验在美国Pyris 1TGA热重分析仪上进行,温度范围为室温至800℃,程序升温速度为10℃/min,以氮气作为保护气且气氛流速为20mL/min。
X射线粉末衍射实验在日本理学D/Max-RBX型X射线衍射仪上进行,使用Cu靶Kα射线,射线管电压:30kV,管电流:100mA。
红外检测实验在NICOLET公司的NESUS670傅里叶变化红外光谱仪GE/KBr分束器DTGS检测器上进行。测试条件:样品及100~200倍的特殊处理过的KBr,经充分研磨使粒度小于2.5μm,压制成直径为13mm厚度约为0.5mm的透明薄片,中红外DTG检测器检测范围:4 000~400cm-1,扫描次数为16次,分辨率为4cm-1。
1.3 酯化反应
在25mL圆底烧瓶中依次加入乙醇1.975g(4.3×10-2mol),离子液体磷钨杂多酸盐1g(2.867×10-4mol),乙酸0.515g(8.6×10-3mol),在磁力搅拌器上加热至60℃并持续4h,反应结束后,产物和催化剂分层,通过简单的过滤即可分离产物和催化剂,催化剂在100℃干燥后即可重复利用。
1.4 定性及定量分析
本实验利用质谱进行定性分析,结果表明无副反应产生。
本实验采用酸碱滴定的方法来测定反应的收率。以乙醇溶液作为溶剂,经标定后浓度为0.05 mol/L的KOH溶液作为滴定溶液,质量分数1%酚酞溶液作为指示剂,氢氧化钾-乙醇标准溶液滴定试样直到出现粉红色并保持30s不褪色即为滴定终点。
2 结果与讨论
2.1 反应时间
在催化剂物质的量为0.286mmol,n(催化剂)/n(乙酸)/n(乙醇)=1∶30∶150,反应温度为60℃的条件下,考察不同反应时间对酯化反应的影响,结果见图1。从图1中可以看出,延长反应时间能够提高酯化反应的收率,当达到4h时,收率达到最大,再增加反应时间,酯化反应的收率变化不大,说明酯化已达到平衡,因此,反应时间4h为最佳反应条件。

Fig.1 Esterification results under different reaction time图1 不同反应时间下酯化反应结果
2.2 反应温度
在催化剂物质的量为0.286mmol,n(催化剂)/n(乙酸)/n(乙醇)=1∶30∶150,反应时间为4h的条件下,控制加热温度,考察不同反应温度对酯化反应的影响,结果见图2。从图2中可以看出,升高温度酯化反应的收率不断的上升,当温度达到60℃时,催化剂的活性和选择性都非常高,但再提高温度收率并无提高且有略下降,因此酯化反应的最佳反应温度为60℃,在此温度下既有好的收率又有高的选择性,并节约能耗。
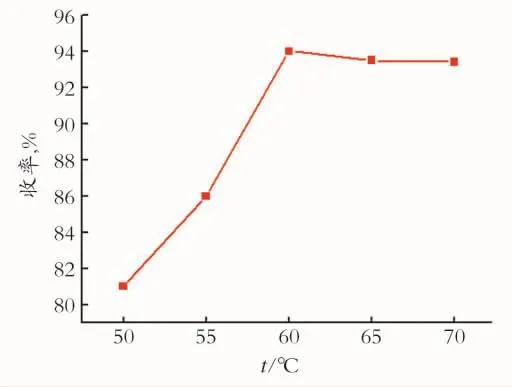
Fig.2 Esterification results under different temperature图2 不同反应温度下酯化反应结果
2.3 催化剂用量
其他条件不变(反应温度60℃,n(乙酸)/n(乙醇)=1∶5,反应时间为4h)的情况下,考察不同催化剂用量对酯化反应的影响。图3给出了不同用量的催化剂对酯化反应的影响。从图3中可以看出提高催化剂的用量,酯化反应的收率稳步上升,说明催化剂具有非常高效的催化性能。当n(催化剂)/n(乙酸)=1∶30时,酯化反应的收率为94%,再增加催化剂用量,收率提高很小。因此,n(催化剂)/n(乙酸)=1∶30为最佳反应条件。
2.4 反应酸醇物质的量比
其他条件不变(催化剂物质的量为0.286 mmol,n(催化剂)/n(乙酸)=1∶30,反应时间为4 h)的情况下,考察不同酸醇物质的量比对酯化反应的影响,结果见图4。由图4中可以明显看出,随着原料nCH3COOH/nCH3CH2OH的不断减小,酯化反应的收率逐渐提高,当酸醇物质的量比为1∶5时,酯化反应的收率达到最高。为了使酯化反应更为完全,乙醇应过量。但若乙醇的量太少,反应不完全;若乙醇的量过多,造成乙酸在反应体系中相对浓度降低,减少了反应物分子碰撞的机会,对收率产生影响,因此酸醇物质的量比为1∶5为最佳反应条件。

Fig.3 Esterification results under different amount of catalyst图3 不同催化剂用量下酯化反应结果

Fig.4 Esterification results under different ratio of raw materials图4 不同原料配比下酯化反应结果
2.5 产物分离和催化剂的循环使用
由于生成的酯不溶于催化剂,反应时体系为均相,反应结束后,产物和催化剂分层,通过简单的过滤即可分离产物和催化剂。除去产物后,将催化剂干燥(100℃)4h,催化剂可重复使用4次,结果见表1。由表1可见,收率分别为9 4%,9 1.3%,87.6%,85.1%。催化剂催化4次后,催化活性变化不大。
从表1可以看出,反应4次后催化剂的活性有所下降,原因可能由于催化剂在每次的过滤过程中略有损失,以上结果表明此催化剂用于酯化反应可重复使用。本催化剂用于酯化反应具有以下优点:(1)具有很高的收率和选择性;(2)成本较低,对环境污染小;(3)产物和催化剂容易分离;(4)经过简单处理就可重复使用。

表1 催化剂的循环使用Table 1 Recycle of[MIMPS]3PW12O40
2.6 催化剂的表征
2.6.1 催化剂的热重表征 图5为磷钨酸盐[MIMPS]3PW12O40的热重曲线。由图5可知,催化剂的失重过程包含了两个过程:100~310℃,310~720℃。在第一阶段的重量损失主要是由于少量水的存在。第二阶段的重量损失可能是由于化合物中阳离子MIMPS+的分解,其次是与有机阳离子相连的Keggin阳离子发生分解。

Fig.5 The TG curve of[MIMPS]3PW12O40图5 [MIMPS]3PW12O40的热重曲线
2.6.2 反应前后催化剂的XRD表征 图6给出了催化剂反应前后的XRD谱图。从图6中可以看出,反应前后催化剂在2θ为9.4°,18.9°,25.8°,31.9°,34.4°时均出现主要特征峰,反应前后没有发生明显变化,这说明催化剂[MIMPS]3PW12O40结构稳定。由此可见,反应前后催化剂的结构未发生明显变化,催化剂活性变化不大,催化剂可重复使用。

Fig.6 XRD patterns for[MIMPS]3PW12O40 before and after reaction图6 [MIMPS]3PW12O40反应前后的XRD谱图
2.6.3 反应前后催化剂的IR表征 图7给出了催化剂反应前后的IR谱图。由图7可以看出,反应前后的催化剂在801,896,977,1 079cm-1处均出现特征峰,其归属于阴离子[PW12040]3-中的ν(W-Oc-W),ν(W-Ob-W),ν(W-Od)和ν(P-Oa)振动;而在520cm-1和1 169~3 150cm-1有特征峰出现,可归属为阳离子1-甲基咪唑产生。由图7可知,催化剂反应前后IR谱图基本一致,说明反应前后催化剂的结构基本无明显的变化。

Fig.7 IR spectra of[MIMPS]3PW12O40 before and after the reaction图7 反应前后[MIMPS]3PW12O40的IR谱图
[1] 吴如春,童张法,谢涛,等.金属离子负载修饰阳离子树脂在酯化反应中的研究[J].离子交换与吸附,2003,19(1):83-87.
[2] Larock R C.Comprehensive organic transformation[M].New York:John wiley and sons inc,1999.
[3] 许胜先,胡国强.杂多酸催化合成戊二酸双丁酯[J].石油化工高等学校学报,1998,11(2):18-21.
[4] 陈静,孙蕊,韩梅,等.MCM-41负载S2O2-8/TiO2固体超强酸的制备和酯化性能研究[J].无机化学学报,2006,22(3):421-425.
[5] Verhoef M J,Kooyman P J,Peters J A,et al.A study on the stability of MCM-41-supported heteropoly acids under liquid-phase and gas-phase esterification conditions[J].Micropor mesopor mat.,1999,27(2-3):365-371.
[6] Blagov S,Parada S,Bailer O,et al.Influence of ion-exchange resin catalysts on side reactions of the esterification of n-butanol with acetic acid[J].Chem.eng.sci.,2006,61(2):753-765.
[7] Song C E,Jung D,Choung S Y,et al.Dramatic enhancement of catalytic activity in an ionic liquid:highly practical friedel-crafts alkenylation of arenes with alkynes catalyzed by metal triflates[J].Angew.chem.,2004,116(45):6309-6311.
[8] Gui J,Cong X,Liu D,et al.Novel brøsted acidic ionic liquid as efficient and reusable catalyst system for esterification[J].Catal.commun.,2004,5(9):473-477.
[9] 宋永波,赵文军,苏建玲,等.酯化反应技术进展[J].化学推进剂与高分子材料,2006,4(2):23-26;31.
[10] Peng G,Wang Y H,Hua C W,et al.Heteropolyoxometalates which are included in microporous silica,CsxH3-xPMol2O40/SiO2and CsyH5-yPMo10V2O40/SiO2,as insoluble solid bifunctional catalysts:Synthesis and selective oxidation of benzyl alcohol in liquid-solid systems[J].Appl.catal.A,2001,218(1-2):91-99.
[11] Chaudhari M P,Sawant S B.Kinetics of heterogeneous oxidation of benzyl alcohol with hydrogen peroxide[J].J.chem.eng.,2005,106(2):111-118.
