尿素在ZnO()表面的吸附
2010-12-05唐文东高阳艳孙予罕
唐文东 高阳艳 魏 伟 孙予罕
(1中国科学院山西煤炭化学研究所,太原 030001; 2中国科学院研究生院,北京 100049; 3中国科学院上海高等研究院低碳能源研究中心,上海 201203)
唐文东1,2高阳艳1,2魏 伟1,*孙予罕1,3,*
(1中国科学院山西煤炭化学研究所,太原 030001;2中国科学院研究生院,北京 100049;3中国科学院上海高等研究院低碳能源研究中心,上海 201203)
运用VASP(Vienna ab-initio simulation package),采用基于密度泛函理论(DFT)的第一原理计算,研究了尿素在ZnO(101¯0)表面的吸附行为.计算结果表明:尿素分子在ZnO(101¯0)表面主要发生分子吸附,稳定的吸附产物通过尿素分子中的氮原子或氧原子与表面锌原子之间的键合作用而形成,吸附能分别为-1.48和-1.41 eV;表面吸附的尿素分子也可以发生解离,生成表面吸附的异氰酸根、氨气和一个表面羟基,吸附能为-1.66 eV.
吸附;尿素;ZnO;碳酸二甲酯;VASP
近年来,人们为了克服合成碳酸二甲酯传统工艺的缺点,如有毒性、易爆炸性、反应工艺复杂和低转化率等,发展了一种满足“绿色化学”要求[1]的新型合成方法,即以尿素和甲醇为原料合成碳酸二甲酯[2-5](图1).
为了提高反应的转化率,人们研究了包括碱、有机锡化合物、金属氧化物、含锌化合物在内的一系列催化剂[2,6-15],结果表明,在这一系列催化剂中,ZnO由于其低毒性,高催化活性和易于分离的优点而被认为是最具潜力的催化剂[2,16].为了对该尿素甲醇化反应有一个清晰的认识,人们设计了许多实验来研究反应的机理,并且提出了几种机理模型[2,17-18].Wang等[2]认为,ZnO对第二步反应具有很高的活性,并且把这种高活性归因于氧化锌的酸碱性质.祁增忠等[17]则认为,在反应过程中,首先是氧化锌吸附甲醇,吸附的甲醇再与尿素作用生成中间产物氨基甲酸甲酯,该中间产物再和另一分子的甲醇反应生成终产物碳酸二甲酯.Zhao等[18]则做了更进一步的研究:他们比较了分别从尿素和氨基甲酸甲酯为原料合成碳酸二甲酯的醇解反应,发现氧化锌对第二条路线即氨基甲酸甲酯和甲醇合成碳酸二甲酯几乎没有催化活性,而它却是第一条路线的决速步骤.因此,他们认为氧化锌只是催化剂的前驱体,真正的催化剂是由氧化锌转变成的另外一种物质.通过对该物质的提取和表征,他们建议该物质的化学式为Zn(NH3)2(NCO)2,该物质通过三步过程生成:尿素首先分解成HNCO和NH3,接着HNCO和ZnO作用生成Zn(NCO)2,该物质再和NH3通过配合作用生成Zn(NH3)2(NCO)2.然而整个反应的机理仍然没有搞清楚.
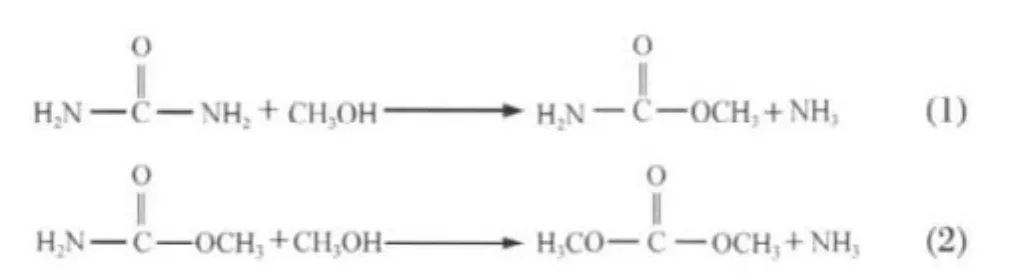
图1 尿素和甲醇合成碳酸二甲酯的反应方程式Fig.1 Reactions of dimethyl carbonate(DMC) synthesis from urea and methanol
要认识非均相反应的机理,首先要认识非均相催化剂在反应过程中的催化行为,而考察反应分子在催化剂表面的吸附则是第一步.对于我们的反应体系,反应物为尿素和甲醇,催化剂为氧化锌,由于Raj等[19]对甲醇在氧化锌表面的吸附行为已做了相关研究,因此本文工作主要研究尿素在氧化锌表面的吸附行为.这对认识整个反应过程的反应机理具有很重要的意义.
1 计算方法和模型
本文中的所有计算都是通过VASP(Vienna abinitio simulation package)[24]完成的.采用由Blöchl[25], Kresse和Joubert[26]发展的缀加投影波函数(PAW)方法来描述电子-离子的相互作用(electron-ion interactions),交换相关能采用广义梯度函数(GGA) PW91[27]进行计算,紧束缚芯电子采用PAW-GGA赝势进行描述.所有计算中平面波截断能(planewave basis cutoff energy)和布里渊区k点分别设置为350 eV和2×2×1,除了在模拟尿素时采用了5×5×5的布里渊区k点设置.经过结构优化的氧化锌元胞的晶格参数为a=b=0.32493 nm,c=0.52054 nm,该结果和Sawada等[28]的实验值,a=b=0.32490 nm,c= 0.52052 nm,非常吻合.表1中还列出了其他一些理论计算结果[29-32],均表明我们的结果与实验值符合得比较好.
2 结果与讨论
尿素可以在ZnO(101¯0)表面发生分子吸附和解离吸附.我们首先设计了尿素分子在氧化锌表面发生分子吸附的可能构型,进行结构优化以确定最稳定的分子吸附模型,然后再以最稳定的分子吸附模型出发,进一步研究解离吸附.
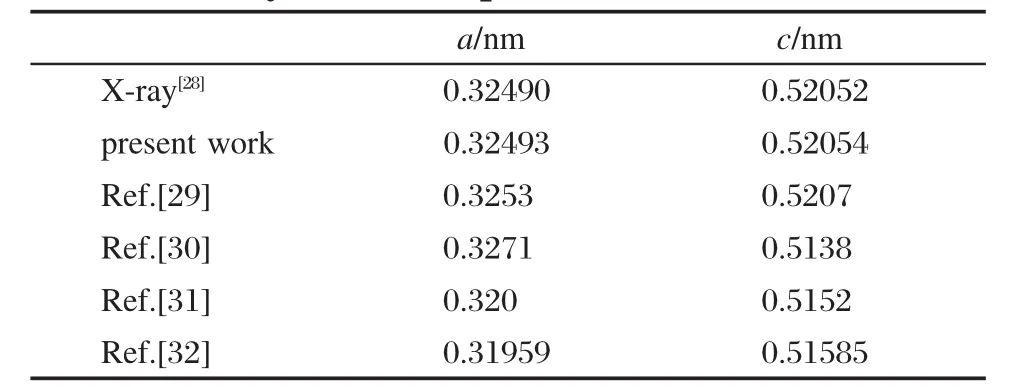
表1 ZnO元胞的晶格参数Table 1 Crystal lattice parameters of ZnO unit cell
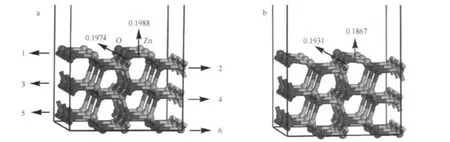
图2 ZnO(1010)表面的超晶胞模型Fig.2 Supercell models of the ZnO(1010)surface(a)unrelaxed surface structure,(b)relaxed surface structure;The numbers 1 to 6 in Fig.1(a)represent the atomic layers 1 to 6,respectively. bond length in nm
本文中我们只计算了各种可能吸附构型的吸附能,以此来确定最稳定的吸附构型,并且期望能从中得到一些关于催化行为的信息.所有的吸附能由以下公式计算所得:
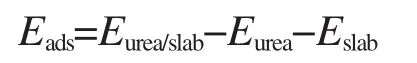
其中,Eurea/slab表示吸附复合物的总能,Eurea表示尿素分子的总能,Eslab则表示表面所在的超晶胞的总能.Eads为负值时就表明该吸附是一放热过程.
2.1 分子吸附
所有可能的分子吸附构型的优化结构和其相应的吸附能列于图3中.
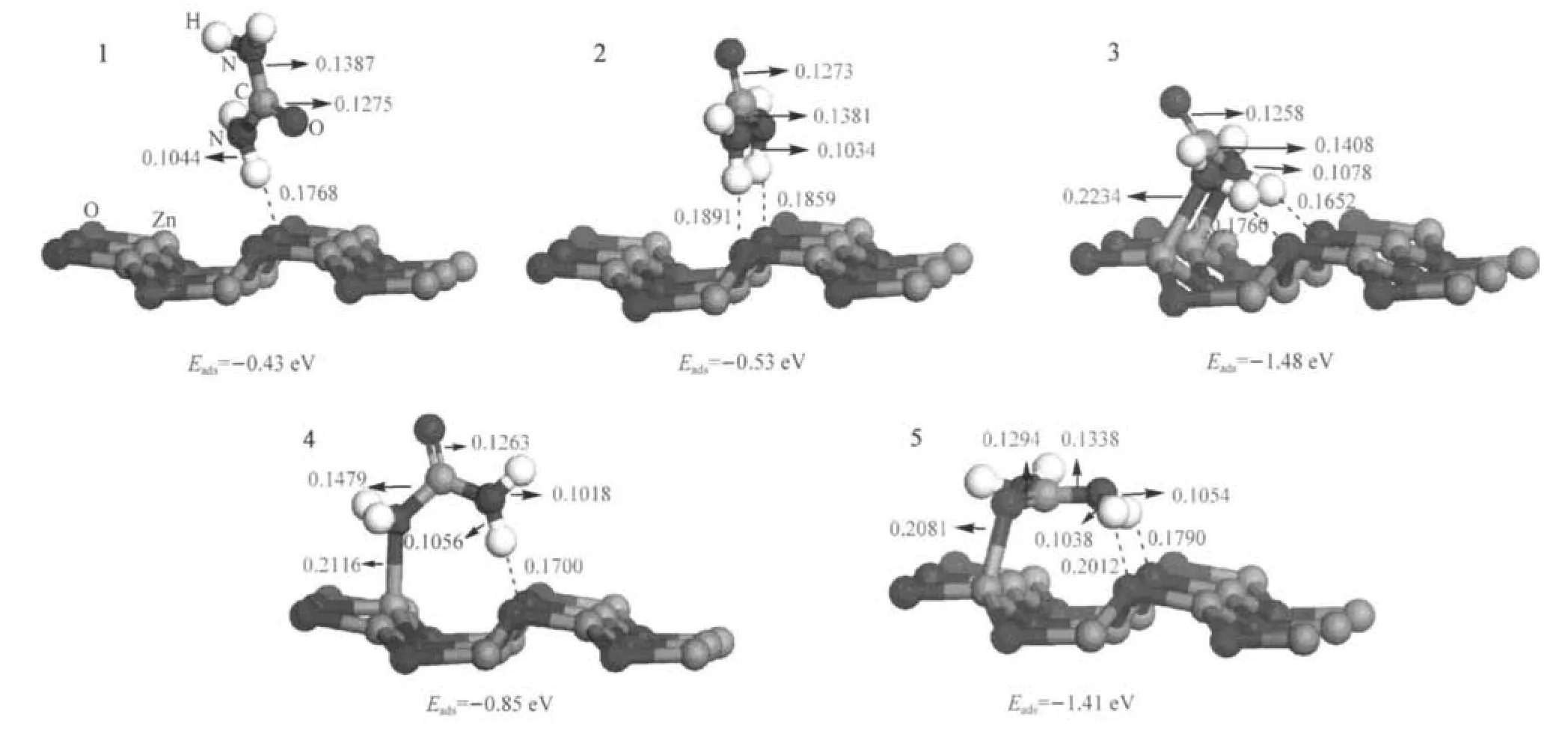
图3 尿素在ZnO(1010)表面发生分子吸附的优化构型及其相应的吸附能Fig.3 Optimized structures and adsorption energies of the molecular adsorption modes of urea on the ZnO(1010)surfaceWe used the top two layers of the ZnO(1010)supercell for short.bond length in nm
计算结果指出,尿素分子倾向于通过其氮原子和表面的锌原子发生键合作用而形成相对比较稳定的吸附复合物(图3,构型3和4).在这两种吸附构型中,和表面锌原子发生作用的氮原子所在的C— N键变长,C=O键变短;构型3新形成两个N—Zn键和两个氢键;构型4中则只形成一个N—Zn和一个氢键.吸附的发生也使表面结构发生了变化,在这两种构型中,表面的O1—Zn1和O2—Zn1键都有明显的增长(此处的Zn1原子是表示和氮原子相连接的锌原子),使得表面的锌原子有从表面离开的趋势.构型3中两个N—Zn键和两个氢键的形成使其比构型4更稳定,二者的吸附能分别为-1.48和-0.85 eV.
另一种比较稳定的吸附构型是尿素分子通过其羰基中的氧原子和表面锌原子发生键合作用的情况.O—Zn键的生成减弱了C=O键的作用,C=O键键长变长;两个氢键的形成也减弱相应的N—H键的作用,键长变长;表面结构也因吸附作用的发生而发生改变,表面的O1—Zn1和O2—Zn1都有所增长.在该构型中,由于分子和表面之间形成了一个O—Zn键和两个氢键,使得该吸附构型也相对比较稳定,吸附能高达-1.41 eV.
从我们的计算结果来看,所有的分子吸附过程都是放热反应.这表明,它们都是热力学上有利的吸附构型,吸附能绝对值越大,其相应的吸附复合物就越稳定.因此,这些吸附复合物的稳定性和被吸附的机会具有相同的顺序:即3>5>4>2>1.如果把吸附能作为产率的粗略近似,根据吸附能Eads之间较大的差异,通过假设平衡的粗略估算可以得知,在ZnO(101¯0)表面上,吸附复合物1、2和4几乎不会存在,而吸附复合物3和5则是最多的.这就意味着在整个分子吸附过程中,吸附复合物3和5是主要的分子吸附产物.
2.2 解离吸附
在表面原子的作用下,表面吸附的分子可以发生解离作用.我们以2.1节中得到的两种主要分子吸附产物为起始点,进一步研究尿素在表面的解离吸附情况.解离吸附的优化构型及相应的吸附能列于图4中.
在我们的结果中只得到了一种解离吸附复合物,来源于分子吸附复合物3.我们用同样的符号标记解离吸附复合物以表明它们的来源(即分子吸附复合物).该解离吸附复合物来自于尿素分子中的N—H键的断裂,形成了一个表面羟基和一个H2NCONH自由基,该自由基的两个氮原子和表面的锌原子键合在一起.通过对吸附能的比较,我们发现,解离吸附复合物没有其相应的分子吸附复合物稳定.解离吸附复合物的吸附能为-1.37 eV,而其相应的分子吸附复合物的吸附能为-1.48 eV,解离需吸热0.11 eV.这表明,尿素分子在ZnO(101¯0)表面倾向于发生分子吸附.
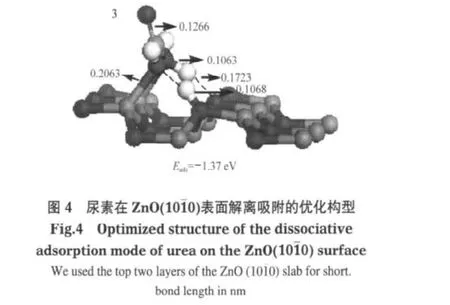

研究发现,初次解离吸附产物可以发生进一步的解离.计算结果表明,解离吸附复合物3可以通过C—N键的断裂,生成表面吸附的氨气、异氰酸根和一个表面羟基,形成更稳定的二次解离吸附复合物3(Eads=-1.66 eV),放出0.29 eV的能量(图5).
3 结论
致谢: 感谢中国科学院山西煤炭化学研究所霍春芳副研究员的有益讨论和帮助.
1 Tundo,P.;Selva,M.Accounts Chem.Res.,2002,35(9):706
2 Wang,M.H.;Zhao,N.;Wei,W.;Sun,Y.H.Ind.Eng.Chem.Res., 2005,44(19):7596
3 Yang,B.L.;Wang,D.P.;Lin,H.Y.;Sun,J.J.;Wang,X.P.Catal. Commun.,2006,7(7):472
4 Wang,M.H.;Wang,H.;Zhao,N.;Wei,W.;Sun,Y.H.Catal. Commun.,2006,7(1):6
5 Sun,J.J.;Yang,B.L.;Wang,X.P.;Wang,D.P.;Lin,H.Y. J.Mol.Catal.A-Chem.,2005,239(1-2):82
6 Cho,T.;Tamura,T.;Cho,T.;Suzuki,K.Process for preparing dialkyl carbonates:US,5534649[P].1996-10-15
7 Lin,H.Y.;Yang,B.L.;Sun,J.J.;Wang,X.P.;Wang,D.P. Chem.Eng.J.,2004,103(1-3):21
8 Saleh,R.Y.;Michaelson,R.C.;Suciu,E.N.;Kuhlmann,B. Process for manufacturing dialkyl carbonate from urea and alcohol: US,5565603[P].1996-10-15
9 Ryu,J.Y.;Gelbein,A.P.Process and catalyst for making dialkyl carbonates:US,6392078[P].2002-05-21
10 Wu,C.C.;Zhao,X.Q.;Wang,Y.J.Catal.Commun.,2005,6(10): 694
11 Bhanage,B.M.;Fujita,S.;Ikushima,Y.;Arai,M.Green Chem., 2003,5(4):429
12 Li,Q.B.;Zhang,W.Y.;Zhao,N.;Wei,W.;Sun,Y.H.Catal. Today,2006,115(1-4):111
13 Zhao,X.Q.;Zhang,Y.;Wang,Y.J.Ind.Eng.Chem.Res.,2004, 43(15):4038
14 Suciu,E.N.;Kuhlmann,B.;Knudsen,G.A.;Michaelson,R.C. J.Organomet.Chem.,1998,556(1-2):41
15 Wang,D.P.;Yang,B.L.;Zhai,X.W.;Zhou,L.G.Fuel Process. Technol.,2007,88(8):807
16 Zhao,W.B.;Wang,F.;Peng,W.C.;Zhao,N.;Li,J.P.;Xiao,F. K.;Wei,W.;Sun,Y.H.Ind.Eng.Chem.Res.,2008,47(16):5913
17 Qi,Z.Z.;Wang,H.B.;Xia,D.K.Industrial Catalysis,2006,14 (1):26 [祁增忠,王洪波,夏代宽.工业催化,2006,14(1):26]
18 Zhao,W.B.;Peng,W.C.;Wang,D.F.;Zhao,N.;Li,J.P.;Xiao,F. K.;Wei,W.;Sun,Y.H.Catal.Commun.,2009,10(5):655
19 Raj,G.S.P.;Horia,M.J.Catal.,2008,254(2):325
20 Jan,W.;Jacek,P.Solid State Commun.,2008,146(7-8):324
21 Gay,R.R.;Nodine,M.H.;Henrich,V.E.;Zeiger,H.J.;Solomon, E.I.J.Am.Chem.Soc.,1980,102(22):6752
22 Marana,N.L.;Longo,V.M.;Longo,E.;Martins,J.B.L.; Sambrano,J.R.J.Phys.Chem.A,2008,112(38):8958
23 Sarano,D.;Spoto,G.;Bordiga,S.;Zecchina,A.;Lamberti,C.Surf. Sci.,1992,276(1-3):281
24 Kresse,G.;Furthmuller,J.Comput.Mater.Sci.,1996,6(1):15
25 Blöchl,P.E.Phys.Rev.B,1994,50(24):17953
26 Kresse,G.;Joubert,D.Phys.Rev.B,1999,59(3):1758
27 Perdew,J.P.;Chevary,J.A.;Vosko,S.H.;Jackson,K.A.; Pederson,M.R.;Singh,D.J.;Fiolhais,C.Phys.Rev.B,1992,46 (11):6671
28 Sawada,H.;Wang,R.P.;Sleight,A.W.J.Solid State Chem., 1996,122(1):148
29 Beltran,A.;Andres,J.;Calatayud,M.;Martins,J.B.L.Chem. Phys.Lett.,2001,338(4-6):224
30 Binks,D.J.;Grimes,R.W.J.Am.Ceram.Soc.,1993,76(9):2370
31 Gopal,P.;Spaldin,N.A.J.Electron.Mater.,2006,35(4):538
32 Cooke,D.J.;Arnaud,M.;Stephen,C.P.J.Phys.Chem.B,2006, 110(15):7985
33 Nyberg,M.;Nygren,M.A.;Pettersson,L.G.M.;David,H.G.; Rohl,A.L.J.Phys.Chem.,1996,100(21):9054
34 Wander,A.;Harrison,N.M.Surf.Sci.,2000,457(1-2):342
October 19,2009;Revised:February 5,2010;Published on Web:March 19,2010.
Adsorption of Urea onto a ZnO()Surface
TANG Wen-Dong1,2GAO Yang-Yan1,2WEI Wei1,*SUN Yu-Han1,3,*
(1Institute of Coal Chemistry,Chinese Academy of Sciences,Taiyuan 030001,P.R.China;2Graduate University of Chinese Academy of Sciences,Beijing 100049,P.R.China;3Low Carbon Energy Center,Shanghai Advanced Research Institute,Chinese Academy of Sciences,Shanghai 201203,P.R.China)
First-principles calculations based on density functional theory(DFT)were used to investigate the adsorption of urea onto a nonpolar ZnO(101¯0)surface with the VASP(Vienna ab-initio simulation package)code.The calculation results indicated that urea was favorably adsorbed onto the ZnO(101¯0)surface molecularly,and that stable adsorption products were formed through the reaction between nitrogen atom or oxygen atom from urea and zinc atom on the surface.The adsorption energy was-1.48 and-1.41 eV,respectively.The adsorbed urea can dissociate to form an isocyanic radical,an ammonia molecule,and a surface hydroxyl,all of which adsorb onto the surface.The adsorption energy was-1.66 eV.
Adsorption;Urea;ZnO;Dimethyl carbonate;VASP
[Article] www.whxb.pku.edu.cn
*Corresponding authors.Email:weiwei@sxicc.ac.cn,yhsun@sxicc.ac.cn;Tel:+86-351-4053801.
The project was supported by the Key Technology R&D Program for 11th Five-Year Plan,China(07ZCU11691)and the Key Project of Knowledge Innovation Program of Chinese Academy of Sciences(08YCA21691).
“十一五”国家科技支撑计划重大项目(07ZCU11691)和中国科学院知识创新重要方向性项目(08YCA21691)资助
O641
