水热法制备TiO2纳米线薄膜的光生阴极保护性能
2010-11-06朱燕峰杜荣归漆海清林昌健
朱燕峰 杜荣归 李 静 漆海清 林昌健
(厦门大学化学化工学院化学系,固体表面物理化学国家重点实验室,福建厦门 361005)
水热法制备TiO2纳米线薄膜的光生阴极保护性能
朱燕峰 杜荣归*李 静 漆海清 林昌健
(厦门大学化学化工学院化学系,固体表面物理化学国家重点实验室,福建厦门 361005)
应用水热法在钛箔表面制备TiO2纳米线薄膜,采用场发射扫描电子显微镜、X射线衍射和紫外-可见分光光度法对薄膜进行表征,用电极电位和电化学阻抗谱考察TiO2光生阴极保护性能.结果表明:薄膜由纵横交错的锐钛矿型TiO2纳米线组成,纳米线的直径约10 nm.在150℃下反应6 h生成的TiO2纳米线薄膜在0.3 mol·L-1Na2SO4溶液和0.3 mol·L-1Na2SO4+0.5 mol·L-1HCOOH混合溶液中对与TiO2薄膜耦连的403不锈钢均有良好的阴极保护效应.TiO2膜所在溶液中含有HCOOH时,可使耦连的403不锈钢在0.5 mol·L-1NaCl溶液中电极电位负移约545 mV,界面反应电阻显著变小,表明电解质溶液加入HCOOH可以增强TiO2纳米线薄膜对403不锈钢的光生阴极保护效应.
水热法;TiO2纳米线薄膜;光生阴极保护;403不锈钢
纳米二氧化钛半导体以其优越的光电性能引起了人们的广泛关注,并成功应用于光催化降解有机物[1-2]、光解水[3-4]、太阳能电池[5-6]﹑气敏传感器[7-8]和生物医用材料[9-10]等领域.例如,Wen等[11]采用溶胶凝胶的方法制备了I-F共掺杂的TiO2涂层,应用于亚甲基蓝(MB)的降解,结果表明共掺杂的TiO2膜比纯TiO2有更高的光催化活性.Uchida等[12]利用水热法合成了TiO2纳米管,并表明制备的纳米管与未处理前的粉末相比拥有更大的比表面积,可以吸附更多的染料,提高光转换率.李海龙等[13]研究了贵金属Ag对TiO2涂层性能的影响,发现Ag修饰的TiO2纳米管(Ag/TNTs)在可见光区域有较好的吸收,光催化降解甲基橙表明Ag/TNTs的光催化活性显著高于纯的TNTs.近年来,人们发现TiO2涂层在金属腐蚀保护方面也有光明的应用前景[14-16].光照时,TiO2价带电子就会被激发到导带,在价带上产生相应的空穴,当TiO2薄膜与某种金属相连时,导带的电子进入金属,使金属的腐蚀电位降低,从而抑制或减少该金属的溶解.将纳米TiO2半导体材料的光电特性应用于金属的保护,相当于起到了一种阴极保护效应,也就是光生阴极保护作用.与牺牲阳极保护法不同的是[17],TiO2膜在产生阴极保护过程中本身并不发生溶解,有益于实现资源的可持续利用.Ohko等[18]采用喷雾热解法在304不锈钢表面制备TiO2半导体薄膜,发现紫外光照射时,304不锈钢耐蚀性能提高;Zhou等[19]采用溶胶-凝胶法在304不锈钢表面构筑了TiO2-WO3的纳米复合涂层,提高了不锈钢在NaCl溶液中的耐蚀性;Li等[20]应用阳极氧化法在钛箔表面制备N掺杂的TiO2纳米阵列在太阳光照射下对316L不锈钢具有一定的阴极保护作用.
虽然TiO2薄膜光生阴极保护性能的发现和研究已有多年,但相关的报道仍较少.存在的主要问题是如何提高TiO2薄膜光生阴极保护性能(重要指标是被保护金属电极电位降低的数值).为此,人们一般采用改进制备方法[18-20],或对TiO2薄膜进行改性[19-20],以增强其阴极保护效果.目前,制备TiO2膜层往往成本较高、或可能造成环境污染,有时膜层易出现缺陷.本工作应用环境友好的水热法于钛箔表面制备网状TiO2纳米线薄膜,并对薄膜形貌、结构、光电性能进行表征.通过电化学测试,重点考察TiO2薄膜光生阳极对耦连的403不锈钢电极的光生阴极保护效应及其薄膜所处的电解质溶液的影响作用.
1 实验部分
1.1 TiO2纳米线薄膜制备
制备TiO2纳米线薄膜的基体材料为厚度0.1 mm,纯度>99.9%的钛箔,由厦门达真磁记录有限公司提供;用于测试TiO2膜层光生阴极保护效应的金属材料是厚度为2 mm的403不锈钢(即1Cr13)板,天津元浩腾飞公司供应;所用试剂均为分析纯;实验用水为二次去离子水.
TiO2纳米膜制备方法.钛箔于室温下经10%(w) HNO3+1%(w)HF溶液刻蚀处理1 min后,冲洗,再依次用丙酮、无水乙醇、去离子水超声波清洗.处理后的钛箔放入容积为40 mL的聚四氟乙烯反应釜中,加入20 mL 10 mol·L-1NaOH溶液,于150℃下反应一定时间,再自然冷却至室温.取出钛箔试样,去离子水清洗,然后在0.1 mol·L-1HNO3溶液中浸泡8 h.取出后用去离子水清洗,最后于450℃下煅烧2 h.
403不锈钢电极的制备方法.先把钢板加工成2 cm×1 cm的长方形试样,其表面依次用400#-1500#的水磨砂纸逐级打磨,再用1.0 μm的抛光粉抛光至镜面,依次在丙酮、无水乙醇、去离子水中超声波清洗30 min,最后存放在干燥器中备用.
1.2 TiO2纳米线薄膜的表征
采用日本日立公司Hitachi S-4800场发射扫描电子显微镜(SEM)观察TiO2纳米线薄膜的形貌和测试其膜厚;利用荷兰Philips公司的panalytical X′pert转靶X射线粉末衍射仪(XRD)测试膜层TiO2的晶型;应用美国Varian公司生产的Cary5000型紫外-可见-近红外分光光度计(UV-Vis-NIR spectrophotometer)测试膜层的光吸收性能.
1.3 TiO2纳米线薄膜光生阴极保护性能的测试
TiO2薄膜光生阴极保护性能的测试采用光生电解池和腐蚀测试电解池组成的双电解池联用系统.表面有TiO2薄膜的Ti箔试样为光生阳极,处于光生电解池中,其中的电解质为0.3 mol·L-1Na2SO4或0.3 mol·L-1Na2SO4+0.5 mol·L-1HCOOH溶液.腐蚀测试电解池为三电极体系,工作电极为403不锈钢,辅助电极为Pt电极,参比电极为饱和甘汞电极(SCE),以0.5 mol·L-1NaCl为电解质溶液.TiO2膜光生阳极与403不锈钢电极通过导线连接,光生电解池与腐蚀测试电解池通过盐桥连接.测试TiO2纳米薄膜对403不锈钢的阴极保护效应时,分为暗态与光照两种条件.光照时以150 W高压Xe灯作为白光光源,直接照射于光生电解池中TiO2纳米薄膜表面.采用Autolab PGSTAT30电化学工作站测试不锈钢的腐蚀电化学参数.电化学阻抗(EIS)测试在腐蚀电位或光生电位下进行,激励信号为正弦,扰动电压10 mV,频率范围为105-10-2Hz.测试均在室温下进行.

图1 150℃水热反应不同时间制备的TiO2纳米线薄膜的SEM图Fig.1 SEM images of the TiO2nanowire films prepared at 150℃for different hydrothermal reaction time(a)2 h,(b)4 h,(c)6 h;(d)cross-sectional view for the film prepared for 6 h
2 结果与讨论
2.1 TiO2薄膜的表征
图1为150℃NaOH溶液中不同反应时间在Ti箔表面上制备的TiO2薄膜的SEM图,可以看出,当反应时间为2 h时,膜表面呈现出由纳米线组成的鸟巢状的结构,线条没有一定的取向性,处于纵横交错(图1(a)).仔细观察,可以发现这些纳米线的表面并不是光滑的,而是由一些颗粒组成,纳米线形状类似糖葫芦[21].反应时间为4 h时,Ti表面膜鸟巢状结构中的孔洞减小,表面的纳米线增多,其表面也较光滑(图1(b)),表面膜也完全形成.反应达到6 h后,钛箔表面形成了完整的纳米线薄膜(图1(c)),其中纳米线直径约为10 nm,相应的侧面图显示膜层厚度约3.13 μm(图1(d)).因此,水热法制备TiO2纳米线薄膜的反应时间应选择6 h,以获得稳定的结果.

图2 150℃水热反应不同时间制备的TiO2纳米线薄膜的XRD谱Fig.2 XRD patterns of the TiO2nanowire films prepared at 150℃for different hydrothermal reaction time
图2 为TiO2纳米线薄膜的XRD谱图.可以看出,图中存在着锐钛矿型TiO2和纯钛的两种特征谱峰,表明纳米线主要成分是锐钛矿型TiO2.水热反应时间为4 h对应的TiO2膜的特征峰位置与2 h比较并没有发生变化,只是强度增大,这是因为随着反应时间的延长,表面的纳米线逐渐增多,这与SEM图显示的结果一致;当反应时间增至6 h时,TiO2膜的特征峰同样不变,而且与4 h的谱峰比较,其强度也几乎不变.这表明当反应时间达到4 h后,纳米线薄膜已在Ti箔表面完全形成,正如上述SEM图所显示的反应时间为4和6 h时,TiO2膜的形貌基本相同.

图3 150℃水热反应不同时间制备的TiO2纳米线薄膜的紫外-可见吸收光谱Fig.3 UV-Vis absorption spectra of the TiO2nanowire films prepared at 150℃for different hydrothermal reaction time(a)2 h;(b)4 h;(c)6 h
图3 显示了不同反应时间制备的纳米线薄膜的紫外-可见吸收光谱.可以看出,TiO2膜的主要吸收波长为小于400 nm的紫外光,对应于锐钛矿型TiO2的本征吸收.水热反应4 h时生成的TiO2纳米膜的吸收边与2 h时比较有了显著的红移,但仍然主要吸收紫外光.反应时间为6 h制备的纳米膜的吸收边与4 h的情况几乎相同.这是因为随着反应时间的延长,钛箔表面的TiO2纳米线逐渐增多(如图1所示),有效表面积增大,因此对入射光的吸收就增强;此外,对于网状结构的纳米线薄膜,光还可以在其内部产生散射,提高薄膜对光的吸收率[21-22],由于薄膜对光的吸收增强,其相应的光谱就表现为吸收边红移.
2.2 TiO2纳米线薄膜光生阴极保护性能
2.2.1 光生电位及其变化

图4 403不锈钢耦连电极在0.5 mol·L-1NaCl溶液中电极电位随时间变化Fig.4 Time evolution of the potentials of 403 stainless steel in 0.5 mol·L-1NaCl coupled to TiO2film electrode in different solutions(a)0.3 mol·L-1Na2SO4;(b)0.3 mol·L-1Na2SO4+ 0.5 mol·L-1HCOOH
为考察TiO2纳米线薄膜对金属的光生阴极保护效应,把表面有TiO2纳米线薄膜Ti箔与403不锈钢耦连后,测量403不锈钢的电极电位E,也即测试薄膜光生阳极在暗态和光照条件下对应耦连的不锈钢的光生电位Eph及其变化.图4为403不锈钢在0.5 mol·L-1NaCl溶液中与水热反应时间为6 h制得的处于不同介质中的TiO2纳米线薄膜电极耦连后电极电位随时间的变化曲线.图中曲线(a)显示,光生电解池中介质为0.3 mol·L-1Na2SO4溶液时,用白光照射TiO2薄膜时,不锈钢电极电位由原来的开路电位(腐蚀电位)15 mV迅速降低至约-370 mV,随后保持基本稳定,这就表明TiO2薄膜使403不锈钢的电极电位显著降低,起到了光生阴极保护作用.产生这种现象的原因是由于光照射于TiO2薄膜时, TiO2半导体价带的电子被激发到导带,导带中的电子通过导线传到403不锈钢的表面,产生光生电子,使不锈钢的电极电位降低[23].当不锈钢表面电子数目基本不变时,光生电位就达到基本稳定,不再随时间变化.如果TiO2薄膜所处介质为0.3 mol·L-1Na2SO4+0.5 mol·L-1HCOOH的混合溶液,光照后, 403不锈钢电极电位也迅速降低,并且降低的数值更大,然后稳定在约-530 mV.可见,与0.3 mol·L-1Na2SO4电解质溶液比较,光生电解池的介质为混合溶液时,可使相应的403不锈钢产生的光生电位更负,表明此种情形TiO2纳米线薄膜对不锈钢的光生阴极保护效果更好.产生这种效果的原因可解释为电解质溶液中的甲酸不但作为空穴捕获剂降低了TiO2纳米薄膜中电子和空穴的复合几率,而且甲酸还具有电流加倍效应以及在电极表面有较强的吸附[24].这样,TiO2纳米薄膜就可以向耦连的不锈钢提供更多的电子,产生更负的光生电位,达到更佳的阴极保护作用.
2.2.2 电化学阻抗谱

图5 403不锈钢在0.5 mol·L-1NaCl溶液中与TiO2膜电极耦连前后的Nyquist图Fig.5 Nyquist plots of 403 stainless steel in 0.5 mol·L-1NaCl solution under different conditions(a)no coupling;(b)coupled to the TiO2film in 0.3 mol·L-1Na2SO4solution under illumination;(c)coupled to the TiO2film in 0.3 mol·L-1Na2SO4+0.5 mol·L-1HCOOH under illumination
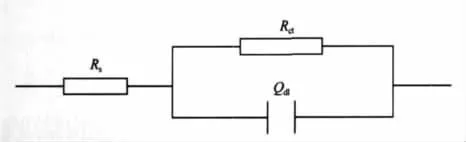
图6 403不锈钢在0.5 mol·L-1NaCl溶液中的电极过程等效电路图Fig.6 Equivalent circuit of 403 stainless steel in 0.5 mol·L-1NaCl solutionRs:electrolyte solution resistance,Rct:charge transfer resistance, Qdl:double-layer capacitance
图5 为403不锈钢在0.5 mol·L-1NaCl溶液中与受光照的TiO2纳米薄膜耦连前后的电化学阻抗谱.从Nyquist谱图可看出,其阻抗谱曲线只有一个半圆弧,根据此特征可采用图6的等效电路进行拟合.其中,Rs代表溶液电阻;Rct代表不锈钢/溶液界面电荷转移电阻,其值大小反应了上述界面反应的趋势;Qdl为空间电荷层电容.从图中可以看出,两种情况下Nyquist图谱的形状基本上无变化,但阻抗值的大小差别显著.根据等效电路对阻抗谱进行拟合,获得了403不锈钢电极耦连前的界面电荷转移电阻Rct为37.7 kΩ·cm2,而与TiO2膜光生阳极耦连后光生电解池电解质分别为0.3 mol·L-1Na2SO4溶液和0.3 mol·L-1Na2SO4+0.5 mol·L-1HCOOH混合溶液时的Rct分别为9.35 kΩ·cm2和3.53 kΩ·cm2.可以看出,403不锈钢与TiO2膜光生阳极相连后, Rct值减小了约1个数量级.这是因为光照时,TiO2光生阳极产生的电子注入到403不锈钢的表面,使体系的总电流增大,使不锈钢/溶液界面电荷转移速度增大,表现为电荷转移电阻降低,阻抗值变小, Nyquist图中圆弧半径也就变小,而此时不锈钢表面处于阴极保护状态,其阳极溶解过程受到抑制.当光生电解池中电解质溶液中增加了HCOOH后,如上所述,使电子在单位时间内从TiO2膜转移到不锈钢表面的数量增加,相当于光生电解池和腐蚀测试电解池之间的短路电流增加,即电极反应速度更快,因此界面电荷转移电阻更小,表现在Nyquist谱图的圆弧半径也就更小.因此,介质为0.3 mol·L-1Na2SO4+ 0.5 mol·L-1HCOOH混合溶液时,TiO2纳米薄膜对金属具有更好的阴极保护效应.
3 结论
应用水热法在钛箔表面构筑了网状锐钛矿型的TiO2纳米线薄膜.当水热反应时间达到6 h后,TiO2膜完整覆盖了钛箔表面,其纳米线直径约10 nm,膜厚约3.13 μm.紫外-可见吸收光谱测试结果表明, 403不锈钢在0.5 mol·L-1NaCl溶液与作为光生阳极的Ti-TiO2纳米线薄膜耦连后,在白光照射薄膜条件下,403不锈钢电极电位显著负移,界面电荷转移电阻降低约1个数量级,具有良好的阴极保护效应.特别是当Ti-TiO2纳米线薄膜所在的Na2SO4溶液中加入HCOOH后,可以使耦连的不锈钢的电极电位负移约545 mV,比电解质为单一Na2SO4溶液时负移值多了160 mV,表明介质中的甲酸对TiO2纳米线薄膜的阴极保护效应具有显著的增强作用.
1 Srimala,S.;Roshanorlyza,H.;Zainovia,L.Thin Solid Films, 2009,518(1-2):16
2 Zhuang,H.F.;Lin,C.J.;Lai,Y.K.;Sun,L.;Li,J.Environ.Sci. Technol.,2007,41(13):4735
3 Chatterjee,D.Catal.Commun.,2010,11(5):336
4 Shaban,Y.A.;Khan,S.U.M.Int.J.Hydrogen.Energ.,2008,33 (4):1118
5 Lee,C.Y.;Hupp,J.T.Langmuir,2010,26(5):3760
6 Wang,H.F.;Su,W.N.;Hwang,B.J.Electrochem.Commun., 2009,11(8):1647
7 Park,J.A.;Moon,J.;Lee,S.J.Kim,S.H.;Zyung,T.;Chu,H.Y. Mater.Lett.,2010,64(3):255
8 Seo,M.H.;Yussa,M.;Kida,T.;Huh,J.S.Shimanoe,K.; Yamazoe,N.Sensor.Actuat.B-Chem.,2009,137(2):513
9 Brammer,K.S.;Oh,S.;Cobb,C.J.;Bjursten,L.M.;van der Heyde,H.;Jin,S.Acta Biomater.,2009,5(8):3215
10 Peng,L.;Eltgroth,M.L.;LaTempa,T.J.Grimes,C.A.;Desai,T. A.Biomaterials,2009,30(7):1268
11 Wen,C.;Zhu,Y.J.;Kanbara,T.;Zhu,H.Z.;Xiao,C.F. Desalination,2009,249(2):621
12 Uchida,S.;Chiba,R.;Tomiba,M.Electrochemistry,2002,70(6):418
13 Li,H.L.;Luo,W.L.;Chen,T.Acta Phys.-Chim.Sin.,2008,24 (8):1383 [李海龙,罗武林,陈 涛.物理化学学报,2008,24 (8):1383]
14 Tatsuma,T.;Saitoh,S.Ohko,Y.;Fujishima,A.Chem.Mater., 2001,13(9):2838
15 Shen,G.X.;Chen,Y.C.;Lin,C.J.Thin Solid Films,2005,489 (1-2):130
16 Shen,G.X.;Chen,Y.C.;Lin,L.;Lin,C.J.Electrochim.Acta, 2005,50(25-26):5083
17 Park,H.;Kim,K.Y.;Choi,W.Chem.Commun.,2001,(3):281
18 Ohko,Y.;Saitoh,S.;Tatsuma,T.;Fujishima,A.J.Electrochen. Soc.,2001,148(1):B24
19 Zhou,M.J.;Zeng,Z.O.;Zhong,L.Corrosion Sci.,2009,51(6): 1386
20 Li,J.;Yun,H.;Lin,C.J.J.Electrochem.Soc.,2007,154(11): C631
21 Dong,X.;Tao,J.;Li,Y.Y.;Wang,T.;Zhu,H.Acta Phys.-Chim. Sin.,2009,25(9):1874 [董 祥,陶 杰,李莹滢,汪 涛,朱宏.物理化学学报,2009,25(9):1874]
22 Fujita,K.;Konishi,J.;Nakanishi,K.Sci.Technol.Adv.Mater., 2006,7(6):511
23 Park,H.;Kim,K.Y.;Choi,W.J.Phys.Chem.B,2002,106(18): 4775
24 Leng,W.H.;Liu,D.P.;Cheng,X.F.;Zhu,W.C.;Zhang,J.Q.; Cao,C.N.Acta Metall.Sin.,2007,43(7):764 [冷文华,刘东坡,程小芳,朱文彩,张鉴清,曹楚南.金属学报,2007,43(7):764]
Photogenerated Cathodic Protection Properties of a TiO2Nanowire Film Prepared by a Hydrothermal Method
ZHU Yan-Feng DU Rong-Gui*LI Jing QI Hai-Qing LIN Chang-Jian
(State Key Laboratory for Physical Chemistry of Solid Surfaces,Department of Chemistry,College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,Fujian Province,P.R.China)
A TiO2film was synthesized on the surface of a Ti substrate by a hydrothermal method,followed by acid treatment and calcination.The properties of the TiO2film were characterized by scanning electron microscopy,X-ray diffraction,and ultraviolet-visible spectrophotometry.The photogenerated cathodic protection properties of the TiO2film were investigated by electrochemical techniques.The corrosion performance of 403 stainless steel coupled to a TiO2film photoanode in different solutions was evaluated by photogenerated potential and electrochemical impedance spectroscopy.The results showed that the TiO2film was composed of many randomly-oriented anatase nanowires of about 10 nm in diameter.The TiO2nanowire film prepared by the hydrothermal reaction at 150℃for 6 h was used for the photogenerated cathodic protection of 403 stainless steel.When we coupled the steel in a 0.5 mol·L-1NaCl solution to the TiO2film photoanode in a mixed solution containing 0.3 mol·L-1Na2SO4and 0.5 mol·L-1HCOOH,its potential decreased by 545 mV.Additionally,the charge transfer resistance of the electrode reaction process for the coupled steel decreased considerably.The results also indicated that the HCOOH in the mixed solution improved the photogenerated cathodic protection of the TiO2film photoanode.
Hydrothermal method;TiO2nanowire film;Photogenerated cathodic protection; 403 stainless steel
O646
Received:April 16,2010;Revised:May 28,2010;Published on Web:July 13,2010.
*Corresponding author.Email:rgdu@xmu.edu.cn;Tel:+86-592-2189192.
The project was supported by the National High Technology Research and Development Program of China(2009AA03Z327)and National Key Technology R&D Program of China(2007BAB27B04).
国家高技术研究发展专项(2009AA03Z327),国家科技支撑计划项目(2007BAB27B04)资助
ⒸEditorial office of Acta Physico-Chimica Sinica
