TiO2纳米管阵列光电极的电化学阻抗及动力学特性分析
2010-10-14张知宇桑丽霞张晓敏马重芳
张知宇 桑丽霞 孙 彪 张晓敏 马重芳
(北京工业大学环境与能源工程学院,传热强化与过程节能教育部重点实验室及传热与能源利用北京市重点实验室,北京 100124)
TiO2纳米管阵列光电极的电化学阻抗及动力学特性分析
张知宇 桑丽霞*孙 彪 张晓敏 马重芳
(北京工业大学环境与能源工程学院,传热强化与过程节能教育部重点实验室及传热与能源利用北京市重点实验室,北京 100124)
采用声电化学阳极氧化法,在无机溶剂(H3PO4+NaF水溶液)和有机溶剂(NH4F+水+乙二醇)体系电解液中加20 V直流电压制得TiO2纳米管(TNT)阵列,其中无机溶剂样品(记为TNT-A)的管长为650 nm,有机溶剂样品(记为TNT-E)的管长为2 μm.基于X射线衍射(XRD)图谱、场发射扫描电子显微镜图(FESEM)、紫外-可见漫反射光谱(UV-Vis DRS)的表征和电流-时间(I-t)曲线、Mott-Schottky图和电化学阻抗谱(EIS)的分析可知,在空气中经500℃煅烧后,TNT-E的吸光性能明显好于TNT-A的吸光性能.在紫外光((365±15)nm)辐照下,测得TNT-E的平均光电流密度与TNT-A的仅差0.05 mA·cm-2,这是由于管长的增长增大了电荷转移电阻,并使得传质路径增长,增大了反应所需克服的势垒,降低了电极的反应速率,两者的电荷载流子密度分别为5.31×1020与9.86×1020cm-3.
TiO2纳米管阵列; 电荷转移电阻; 动力学特性; 电荷载流子密度
Abstract:The 2 μm and 650 nm TiO2nanotube(TNT)arrays were fabricated by sonoelectrochemical anodic oxidation in ethylene glycol(TNT-E)and in aqueous solution(TNT-A)electrolytes at 20 V direct voltage.X-ray diffraction(XRD)and field emission scanning electron microscopy(FESEM)were used to characterize the crystal phase and surface morphology of the resulting oxide films.UV-Vis diffuse reflectance spectra (UV-Vis DRS),current-time (I-t)curves,Mott-Schottky plots and electrochemical impedance spectroscopy(EIS)were used to investigate their kinetics properties and their electrochemical impedance behavior.The 2 μm nanotubes of TNT-E can help to harvest more light and provide more surface active sites than the 650 nm nanotubes of TNT-A.We found that TNT-E had stronger light absorption than TNT-A after calcination in air at 500℃,but the photocurrent density differences between TNT-E and TNT-A was only about 0.05 mA·cm2under UV illumination((365±15)nm).Since the longer TNT-E tubes can increase the charge transport resistance and decrease the concentration of the reactants on the electrode surface,TNT-E needs to overcome a larger energy barrier and it has a low charge carrier density of 5.31×1020cm-3.TNT-A with relatively shorter tubes showed a better kinetics property and had a charge carrier density of 9.86×1020cm-3.
Key Words: TiO2nanotube array;Charge transport resistance;Kinetics property;Charge carrier density
TiO2纳米管具有良好的化学稳定性和绿色环保性,且比一般体相材料有更高比表面积和更好的吸附能力,使其在光催化分解水制氢、环境净化、太阳能电池和气敏传感器等领域展现出良好的应用潜力[1-6].2001年,Grimes等[7]利用电化学阳极氧化法成功制备出TiO2纳米管阵列.相对模板法和水热合成法,电化学阳极氧化法制备成本低,操作简单,且制备的TiO2纳米管分布均匀,以整齐的阵列形式排列,纳米管与金属钛导电基底直接相连,可直接用作光催化反应的工作电极.随后该小组[8]通过阳极氧化法制备出6 μm的TiO2纳米管阵列,以AM1.5太阳光模拟器为光源,其能量转化效率要高于较短管长的TiO2纳米管阵列电极.Mohapatra等[9]研究证明在阳极氧化过程中加入超声场的声电化学法是一种快速合成高度有序TiO2纳米管的方法,此种方法生成TiO2纳米管阵列的速度比未加超声场的阳极氧化法快几乎两倍.这是由于超声场的空化效应能够加速传质过程,使得溶液中的F-和H+可以更快地迁移到管底部,促进F-和氧化膜层的化学反应,并有利于[TiF6]2-在管内的排出,因而使得氧化过程加速.Liu等[10]利用声电化学法以5%(w)HF为电解液制备出管长280 nm的TiO2纳米管阵列电极,比管长为430 nm的TiO2纳米管阵列电极的降解效率高21%.上述研究表明,在不同体系制得的不同管长的TiO2纳米管阵列在不同的应用体系中具有显著不同的光电特性.而单一电解液体系制备出的不同管长的TiO2纳米管阵列的光电特性与有效的电荷转移机制相关[11].本项研究则采用声电化学阳极氧化法在有机溶剂体系和无机溶剂体系中制备出不同管长的TiO2纳米管阵列,利用扫描电子显微镜(SEM)对 TiO2纳米管阵列的形貌进行表征,并通过UVVis DRS图,电流-时间曲线,Mott-Schottky图及电化学阻抗谱图(EIS),考察了不同电解液阳极氧化对所制纳米管阵列电极光敏性,并着重分析了TiO2纳米管阵列电极表面传质及电荷转移机理对电极光电特性的影响.
1 实验部分
1.1 TiO2纳米管阵列电极的制备和表征
实验采用的钛箔(厚度为0.2 mm,纯度为99.6%,STREM CHEMICAL,美国),裁剪成 6.5 cm×1.8 cm的电极样品,依次经机械抛光,丙酮超声除油30 min,乙醇清洗,去离子水超声清洗5 min,去离子水冲洗待用.室温下,用铂片电极做对电极,无机电解液体系为 0.50 mol·L-1H3PO4+0.14 mol·L-1NaF,有机电解液体系为0.5%(w)NH4F+10%(w)水+乙二醇(均为北京化学试剂公司产品,分析纯),外加20 V直流电压进行阳极氧化,氧化时间为1 h,整个氧化过程在超声波场(100 W,40 kHz,昆山超声仪器有限公司KQ-100DE)中进行.反应完成后,经超声去离子水清洗后,在500℃5%H2/N2气氛煅烧4 h,其升温速率5℃·min-1,再自然冷却至室温,得到TiO2纳米管阵列,分别记为TNT-A(无机溶液体系样品)和TNTE(有机溶液体系样品).用扫描电子显微镜(S4300 Hitachi,日本)观察所制样品的形貌,采用X射线衍射仪(D8 ADVANCE BRUKER/AXS,美国)表征所制样品的晶相结构.紫外分光光度计(Shimadzu,日本,UV-2450,带IRS-2200积分球)用来测量材料的UVVis DRS光谱.
1.2 TiO2纳米管阵列电极的光电化学特性测试
光电化学特性测试是在具有三电极系统的石英电解池(8 cm×6 cm×8 cm)中进行.用银胶及环氧树脂对所制TiO2纳米管阵列进行封装得到工作电极(面积为1 cm2),辅助电极为Pt网电极(3 cm×2 cm),Ag/AgCl电极为参比电极,文中所述电位均相对于此电极.以1 mol·L-1KOH为光电化学特性测试时的电解液,全部溶液均用分析纯试剂及去离子水配置.测试均在室温条件下进行,外照光源为300 W Xe灯(北京畅拓科技有限公司,PLS-SXE-300型号:输出波长320-780 nm).加(365±15)nm滤波片后,用UV-A型紫外辐照计(北京师范大学光电化学仪器厂)测得在电极位置处的辐照度为12.7 mW·cm2.用CHI614C型电化学分析仪(上海辰华仪器有限公司)进行电化学分析数据采集.电流-时间曲线在不加外部偏压情况下测得,电化学阻抗谱测试的电位扰动为5 mV,信号频率范围为104-10-1Hz.
2 结果与讨论
2.1 TiO2纳米管阵列的形貌
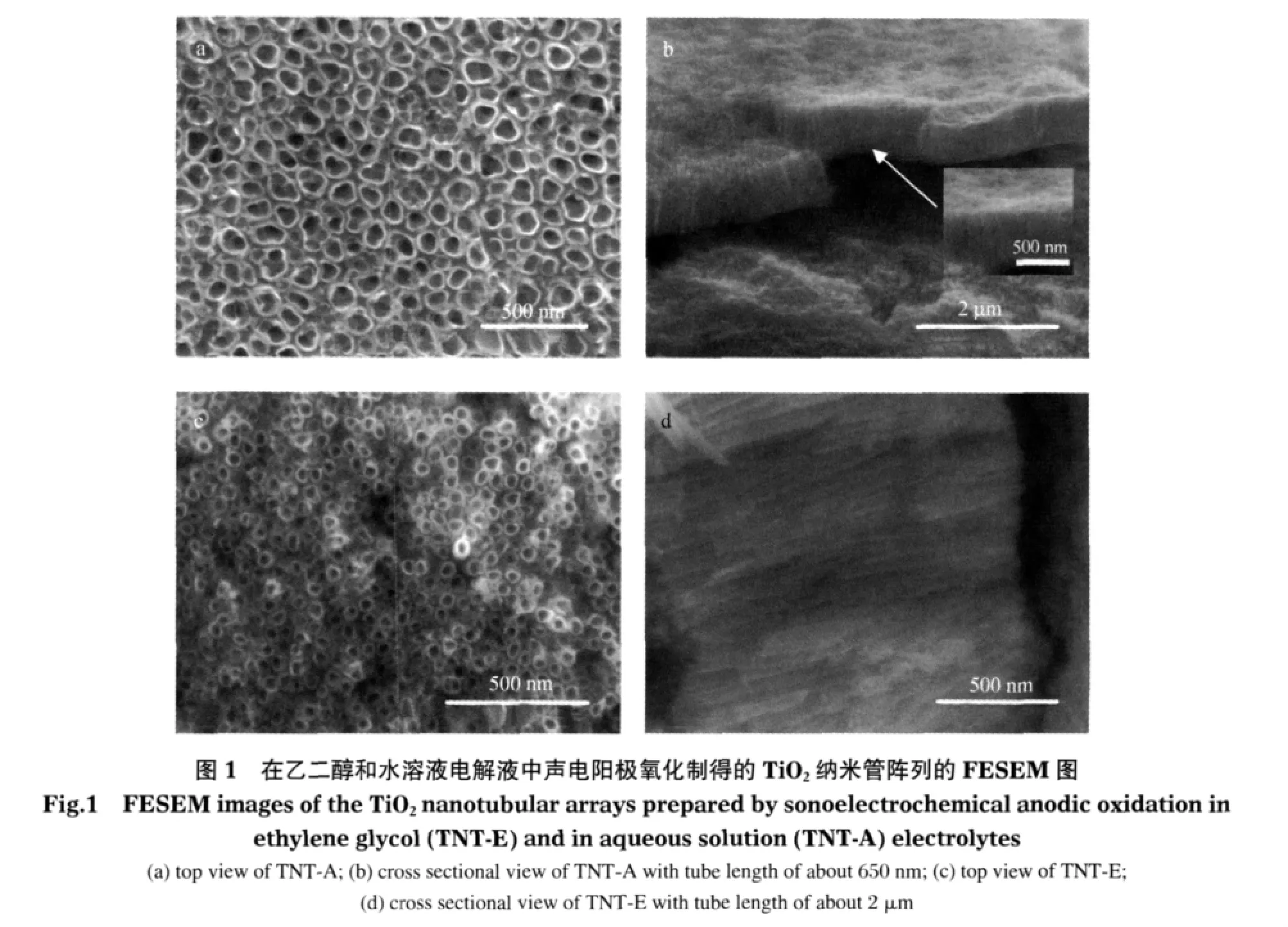
图1为采用声电化学阳极氧化法在无机溶液体系(TNT-A,图1(a,b))和有机溶液体系(TNT-E,图1(c,d))制备的TiO2纳米管阵列正面和侧面的扫描电镜照片.从正面图(图1(a,c))中可以看出,通过阳极氧化在纯Ti箔表面上自组织生长了一层多孔状氧化膜,且孔与孔间存在空隙,相互独立.由侧面图(图1(b,d))中可以看出,自组织的氧化膜是呈管状阵列结构,并可分为纳米管层,致密的阻挡层及钛金属基底.在TNT-A的纳米管内径约100 nm,管壁厚约为15 nm,管长约600 nm;而在TNT-E的纳米管内径约50 nm,管壁厚约为15 nm,管长约2 μm.产生这种结果的原因主要取决于pH值,F-浓度与溶剂的黏度.溶液的pH值越低,F-浓度越高,则TiO2化学溶解越剧烈,小孔形成后能够快速拓宽,产生大管径的TiO2纳米管.另一方面,虽然提高F-浓度有助于促进阻挡层的化学溶解,加速了离子迁移,使得阻挡层/金属界面快速移动,降低阻挡层的厚度,有利于管的生长,但低的pH值和高的F-浓度也会导致管壁的溶解而阻碍管长的增加.溶剂的黏度决定了离子的扩散速率,有机溶剂的黏度较大使得F-、H+的扩散速率降低,从而降低了管壁的溶解速率[12],增长了管壁的存在时间,使得管长增加.
在Ti基底上阳极氧化得到的TiO2纳米管阵列为无定形,经热处理后TiO2纳米管阵列得以晶化.图2为在5%H2/N2气氛中经500℃煅烧4 h后所制TiO2纳米管阵列的XRD图.由图2可知,两种不同溶剂体系阳极氧化1 h所得样品均为锐钛矿型晶相结构,未出现金红石晶型.且乙二醇溶液体系中形成的样品的锐钛矿晶型特征衍射峰的强度要明显高于水溶液体系中的样品.这是由于在相同晶化条件下,在乙二醇溶液体系中形成TiO2纳米管阵列的长度要远大于水溶液体系中生成的长度.
2.2 TiO2纳米管阵列的光电特性
图3是两种溶液体系制备TiO2纳米管阵列的UV-Vis DRS图.由图3可知,在未经热处理前,TNT-E的紫外光吸收强度明显高于TNT-A,而两者在可见区的光吸收特性近似相同.其紫外光吸收特性的差异可能与样品的管长有关,这是由于光吸收主要在材料表面的1 μm范围内[13],而TNT-E和TNTA的管长分别为2 μm和600 nm.在进行热处理后,两者在500-700 nm波段间的光吸收有明显的加强.有文献报道[14],Ti4+中心捕获电子出现的光吸收在500-700 nm范围内,因此可以认为在无氧气氛中煅烧使得样品产生了氧空位,部分Ti4+在还原性气氛中被还原,而导致样品有Ti3+形成的TiO2的出现[15].而TNT-E样品在380-500 nm附近出现一个较大的肩峰,这可能是由于TNT-E形成TiO2-xCx[16].进一步分析TNT-E在Ar离子刻蚀后的XPS图可知,样品中存在明显的C元素的特征峰,且在287 eV左右存在一个较小的肩峰,证明样品内存在C—O键,从而使材料的光吸收带边红移.
对于半导体材料电极,大于半导体禁带宽度能量的光可激发半导体产生光生电子-空穴对,并促使其分离,扩散至溶液/电极之间的界面形成双电层,从而产生开路电压.在光激发的瞬间,由于光诱导电子由价带跃迁到导带立即产生一个阴极光电流信号,信号的强弱反映了半导体薄膜内部电导的大小,说明半导体内部自由载流子的多少.图4是两种溶液体系制备TiO2纳米管阵列的电流-时间曲线.由图可知,在320-780 nm的光辐照下,TNT-E和TNT-A产生的光电流(0 V vs Ag/AgCl)分别为1.96和1.48 mA·cm-2,两者之间的光电流差值远大于加(365±15)nm滤波片时产生的光电流0.55 mA·cm-2与 0.50 mA·cm-2之间的差值,这也符合图 3中TNT-E可见光吸收要高于TNT-A.而在加(365±15)nm滤波片后,TNT-E光电流与TNT-A差别较小,这可能是因为TNT-E的纳米管长要大于TNT-A,从而增大光吸收的表面积并增加了电极的表面活性位;但管长增加同样导致了光生电子-空穴复合机率的提高和电荷的传输阻力的增大,并引起载流子浓度的降低.这将在图5、图6中给出进一步分析.
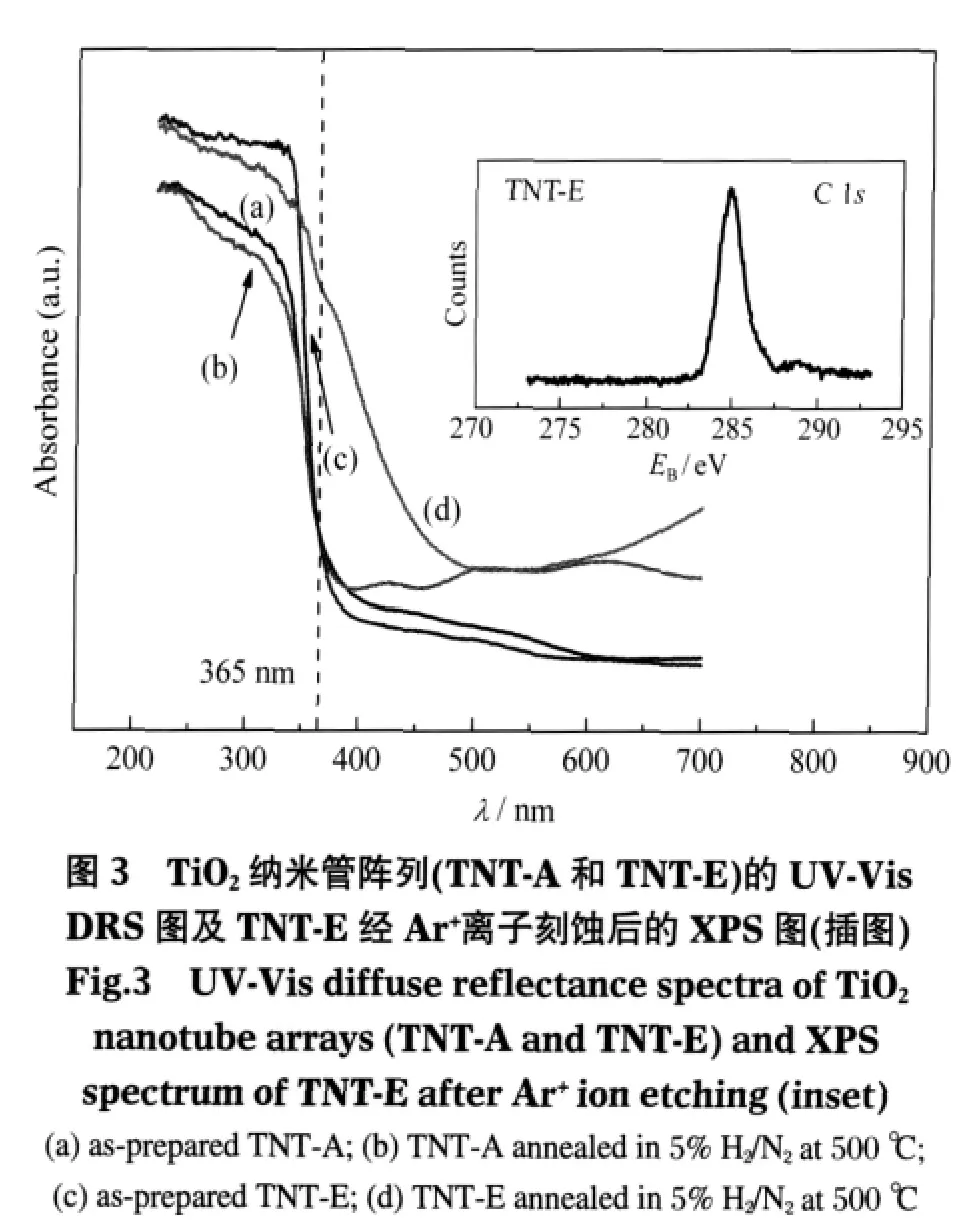

图5所示为光照时不同溶剂体系氧化所制TiO2纳米管阵列电极的 Mott-Schottky图.利用Mott-Schottky图可分析半导体的平带电势以及电荷载流子密度大小[17].当对半导体电极施加外电压时,就会改变其费米能级,从而引起能带弯曲.平带电势Ufb的值等于在某一外电压下,正好使得半导体内的电场为零时的外电压值.在Mott-Schottky图中,对于理想半导体平带电势Ufb的值等于Mott-Schottky曲线线形部分切线与电位轴的交点,由图5可知,在相同的反应条件下,TNT-A的平带电势比TNT-E更负,其平带电势分别为-0.75和-0.73 V.平带电势越正,能带弯曲越大,意味着电极在反应过程中需要克服的势垒越大.在光电体系中,由于光照使体系产生一个外加的光电压,从而使得半导体的空间电荷电容充电,空间电荷区的电荷量改变而影响电极的电荷载流子密度ND,对于理想半导体符合公式:
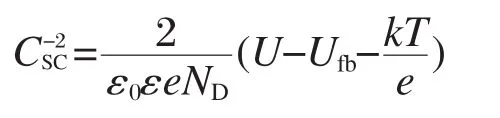
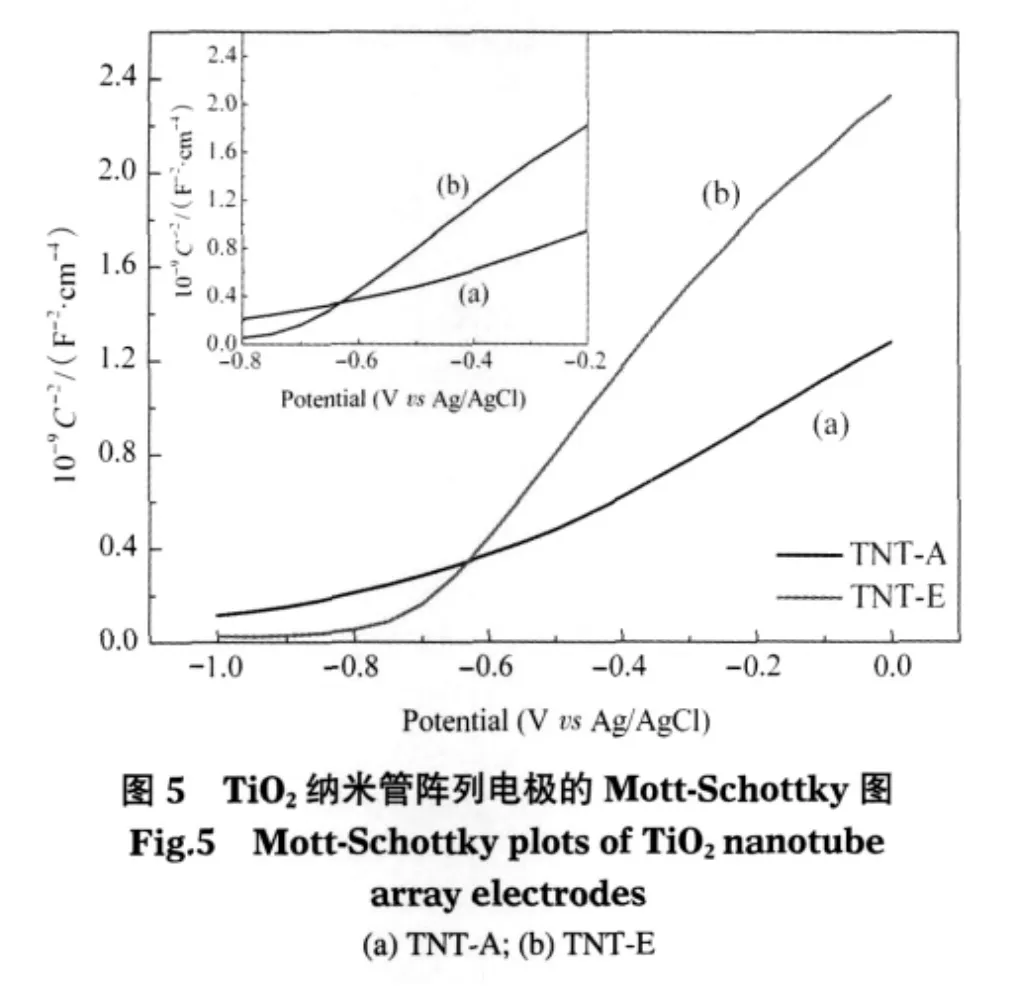
其中Csc为电极的空间电荷层电容,ε0为真空的介电常数,ε为氧化膜层的相对介电常数,k为玻尔兹曼常数(1.38×10-23J·K-1),T为温度,在常温下,kT/e值很小可以忽略.由图5可知,TNT-E的电荷载流子密度约为5.31×1020cm-3,而TNT-A的电荷载流子密度为9.86×1020cm-3.这可能是由于TNT-E的管长较长,在反应中电荷传递电阻较大,而降低了其电荷转移的能力.
图6为不同溶剂体系氧化所制TiO2纳米管阵列电极的电化学阻抗图,由图可知,在无光照的情况下,Nyquist图在测量频率(104-10-1Hz)范围内接近于一条直线,证明这时主要是扩散控制电极过程的特征,且有机溶剂样品的实部阻抗值大于无机溶剂样品,这也证明了管长的增加会导致材料电荷转移电阻的升高.而在光照条件下,样品的阻抗实部值基本没有发生变化,说明光照对电荷转移电阻基本不产生影响.在光照下无机溶剂样品的Nyquist图只出现了一个未封闭半圆弧,即证明在此频率范围内光催化反应速率主要受动力学控制,即电荷转移的影响,而扩散传质对其影响不大,浓差极化现象可以忽略;有机溶剂样品在中高频段也为未封闭半圆弧,而在低频段下偏离了半圆,即此时电极反应过程由动力学和扩散过程共同控制,这也反映了管长的增加使得传质路径的增长,同时管径的减小也降低了传质的能力.由于扩散传质对光照下的电极影响较小,因此可以把光照下的阻抗特性由电化学动力学步骤控制的阻抗方程描述:
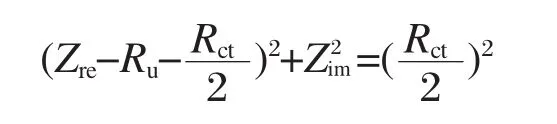

其中ZRe是电极阻抗的实部,ZIm是电极阻抗的虚部,Ru是体系的欧姆电阻,Rct是体系的电荷传递电阻.由图可知,两种溶液体系的Ru值基本相同,都接近于0.TNT-E的阻抗半径要大于TNT-A的,由于测量频率相同,证明在该时间常数上,TNT-E产生的电荷传递电阻值大,光生电荷与空穴的分离速率较慢[18].从电化学反应角度讲,就意味着有机溶剂体系制备的电极更难发生反应,电极反应时需克服的势垒更大;且电极反应速率较慢,参加电极反应的反应物的浓度较小.这可能也是由于有机溶剂体系制备的TiO2纳米管阵列电极的管长较长而增大了反应时的电荷传输阻力,降低了其电荷转移的能力,从而降低了其光催化反应中的反应速率,这也与Mott-Schottky曲线得出的结论一致.
3 结 论
采用声电化学阳极氧化法在钛箔上制备了垂直导向、排列规则的TiO2纳米管阵列,相对于无机溶剂体系的TiO2纳米管阵列(TNT-A),有机溶剂体系的样品(TNT-E)其管径较小,但有更长的管长.相比TNT-A,TNT-E光吸收性更好,但在(365±15)nm光下,其光电流密度差值仅有0.05 mA·cm-2,这是由于TiO2-xCx的形成和纳米管阵列管长的增长增强了光的吸收性,增加了材料的表面活性位;同时管长的增长增大了电荷转移电阻,并使得传质路径增长.TNT-A的平带电势要比TNT-E更负,反应中需克服的能垒较小,阻抗图中的阻抗半径较小,有着较快的光催化反应速率,两者的电荷载流子密度分别为9.86×1020cm-3与 5.31×1020cm-3.
1 Mor,G.K.;Shankar,K.;Paulose,M.;Varghese,O.K.;Grimes,C.A.Nano.Lett.,2005,5:191
2 Paulose,M.;Shankar,K.;Varghese,O.K.;Mor,G.K.;Hardin,B.;Grimes,C.A.Nanotechnology,2006,17:1446
3 Zhai,X.H.;Long,H.J.;Dong,J.Z.;Cao,Y.A.Acta Phys.-Chim.Sin.,2010,26:663 [翟晓辉,龙绘锦,董江舟,曹亚安.物理化学学报,2010,26:663]
4 Quan,X.;Yang,S.G.;Ruan,X.L.;Zhao,H.M.Environ.Sci.Technol.,2005,39:3770
5 Varghese,O.K.;Gong,D.;Paulose,M.;Ong,K.G.;Dickey,E.C.;Grimes,C.A.Adv.Mater.,2003,15:624
6 Mor,G.K.;Shankar,K.;Paulose,M.;Varghese,O.K.;Grimes,C.A.Nano Lett.,2006,6:215
7 Gong,D.;Grimes,C.A.;Varghese,O.K.;Hu,W.;Singh,R.S.;Chen,Z.;Dicky,E.C.J.Mater.Res.,2001,16:3331
8 Paulose,M.;Mor,G.K.;Varghese,O.K.;Shankar,K.;Grimes,C.A.J.Photochem.Photobio.A,2006,178:8
9 Mohapatra,S.K.;Misra,M.;Mahajan,V.K.;Raja,K.S.J.Catal.,2007,246:362
10 Liu,Y.B.;Zhou,B.X.;Li,J.H.;Gan,X.J.;Bai,J.;Cai,W.M.Appl.Catal,B,2009,92:326
11 Zhang,Z.Y.;Sang,L.X.;Lu,L.P.;Bai,G.M.;Du,C.X.;Ma,C.F.J.Inorg.Mater.,2010,in press [张知宇,桑丽霞,鲁理平,白广梅,杜春旭,马重芳.无机材料学报,2010,印刷中]
12 Mor,G.K.;Varghese,O.K.;Paulose,M.;Shankar,K.;Grimes,C.A.Sol.Energy Mater.Sol.Cells,2006,90:2011
13 Nowotny,J.;Bak,T.;Nowotny,M.K.;Sheppard,L.R.Int.J.Hydrog.Energy,2007,32:2609
14 Zhuang,H.F.;Lin,C.J.;Lai,Y.K.;Sun,L.;Li,J.Environ.Sci.Technol.,2007,41:4735
15 Macak,J.M.;Gong,B.G.;Hueppe,M.;Schmuki,P.Adv.Mater.,2007,19:3027
16 Khan,S.U.M.;Al-Shahry,M.;Ingler Jr.,W.B.Science,2002,297:2243
17 John,S.E.;Mohapatra,S.K.;Misra,M.Langmuir,2009,25:8240 18 Liu,H.;Wu,M.;Wu,H.J.;Sun,F.X.;Zheng,Y.;Li,W.Z.Acta Phys.-Chim.Sin.,2001,17:286 [刘 鸿,吴 鸣,吴合进,孙福侠,郑 云,李文钊.物理化学学报,2001,17:286]
Kinetics and Electrochemical Impedance Properties of TiO2Nanotube Array Photoelectrode
ZHANG Zhi-Yu SANG Li-Xia*SUN Biao ZHANG Xiao-Min MA Chong-Fang
(Key Laboratory of Enhanced Heat Transfer and Energy Conservation,Ministry of Education and Key Laboratory of Heat Transfer and Energy Conversion,Beijing Municipality,College of Environmental and Energy Engineering,Beijing University of Technology,Beijing 100124,P.R.China)
O649
Received:June 1,2010;Revised:August 5,2010;Published on Web:October 13,2010.
*Corresponding author.Email:sanglixia@bjut.edu.cn;Tel:+86-10-67391612-8045.
The project was supported by the National Natural Science Foundation of China(50806003)and Beijing Natural Science Foundation,China(3093018).
国家自然科学基金(50806003)和北京市自然科学基金(3093018)资助项目
