SARS-CoV-2 mRNA疫苗免疫血清抗体水平检测方法的比较
2024-01-02吴小红赵丹华刘欣玉杨立宏李玉华曹守春
吴小红,赵丹华,刘欣玉,杨立宏,李玉华,曹守春
中国食品药品检定研究院虫媒病毒疫苗室,北京 102629
SARS-CoV-2疫苗的研发及应急使用有效遏制了COVID-19疫情的扩散及特殊人群危重症病例的发生。mRNA 疫苗作为新技术平台疫苗,免疫后可激活人体细胞及体液免疫。研究发现,SARS-CoV-2 的有效清除主要依赖于T 细胞免疫[1-4],而中和抗体可中和SARS-CoV-2,从而阻断病毒进入细胞内增殖,对防控SARS-CoV-2感染引起的疾病具有重要作用[5-6],是公认的保护性抗体。另外,抗体水平与SARS-CoV-2 感染者症状严重程度之间也具有一定相关性[2,5]。
中和抗体水平的检测方法主要包括需采用活病毒的噬斑减少中和试验(plaque reduction neutralization test,PRNT)、微量细胞病变中和试验(micro-cytopathic effect neutralization test,MCPENT)及假病毒中和试验(pseudo virus-based neutralization assay,PBNA)[7-8]。国内外研究机构陆续开发了针对SARS-CoV-2 S1 蛋白中受体结合域(receptor binding domain,RBD)及N-末端域(N-terminal domain,NTD)单抗原表位或多抗原表位的酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)进行抗体检测,与中和抗体检测结果相关性较好[9-12]。目前,国内外虽然尚未建议在疫情防控中对大规模SARS-CoV-2 疫苗接种后人群开展抗体监测[13-14],但免疫后中和抗体水平仍是疫苗研发和临床评价过程中的重要参考指标。本研究通过ELISA、MCPENT及PBNA 3种方法对SARS-CoV-2 mRNA疫苗免疫前后的健康人血清进行检测,评价采用ELISA 及PBNA 法代替MCPENT 法用于疫苗免疫原性评价的可能性,为SARS-CoV-2疫苗的临床研究提供安全、快捷、有效的检测手段,以期加快变异株疫苗的研发,快速应对不断出现的变异毒株带来的风险。
1 材料与方法
1.1 血清 40 名健康人(18 ~ 59 岁)免疫前及免疫SARS-CoV-2 mRNA 原型株疫苗2剂(间隔28 d)后15及28 d 的血清,共120 份,均由树兰(杭州)医院提供,56 ℃水浴灭活30 min,≤-20 ℃保存。本研究经伦理委员会批准,文件号为:2020伦审(31)号。
1.2 病毒及细胞 SARS-CoV-2 临床分离原型株(1×106CCID50/mL)由军事医学科学院微生物流行病研究所提供;SARS-CoV-2 原型株假病毒及Vero 细胞均由中国食品药品检定研究院艾滋病疫苗室提供。
1.3 主要试剂及仪器 DMEM、胎牛血清、胰酶、HEPES、青-链霉素均购自美国Gibco公司;SARS-CoV-2 RBD IgG抗体检测试剂盒购自北京万泰生物药业股份有限公司;荧光素酶检测试剂、Promega GloMax 96孔板及化学发光检测仪(Glomax navigator)均购自美国Promega公司。
1.4 检测方法
1.4.1 ELISA法 将120 份血清用样品稀释液(试剂盒自带)经1∶40 稀释后再2 倍系列稀释至1∶2 560(未至阳性临界值可继续进行2倍稀释),每份样品设2 个复孔,按SARS-CoV-2 RBD IgG 抗体检测试剂盒说明书操作,采用酶标仪检测A450/630。A450/630≥0.10判为阳性,以阳性血清最大稀释倍数按下式计算IgG抗体滴度及几何平均滴度(geometric mean titer,GMT),IgG抗体滴度≥40时判为阳性,<40判为阴性。

1.4.2 PBNA法 于96孔板中将120份血清用DMEM完全培养基(含10%FBS、1%双抗、25 mmol/L Hepes的DMEM高糖培养基)3倍系列稀释至1∶7 290(高滴度抗体血清可继续进行3 倍稀释),每份样品设2 个复孔,100 μL/孔,加入SARS-CoV-2 原型株假病毒,50 μL/孔,于37 ℃中和1 h;加入Vero 细胞(2 ×105个/mL),100 μL/孔,于37 ℃,5%CO2细胞培养箱培养22~28 h;同时设细胞对照(仅加入细胞)及病毒对照(仅加入细胞和病毒),均设6个复孔;弃上清,加入荧光素酶检测试剂,100 μL/孔,室温避光反应2 min;反复吹吸6~8次,每孔吸出100 μL液体,加入对应Promega GloMax 96 孔板中,置化学发光检测仪读取发光值,并按下式计算中和抑制率,采用Reed Muench法计算EC50,从而得到抗体滴度,并计算GMT。血清抗体滴度≥30判为阳性,<30判为阴性[15-16]。

1.4.3 MCPENT法 于96孔板中用DMEM完全培养基对血清进行2倍系列稀释(1∶4~1∶1 024,高效价血清样本可先经10倍预稀释后,再进行2倍系列稀释),加入SARS-CoV-2 临床分离原型株病毒液,50 μL/孔,于37 ℃,5%CO2细胞培养箱中和1 h;加入Vero细胞(1.5×105个/mL),100 μL/孔,继续培养5 d;同时设阴性血清对照(加入内控阴性血清及病毒和细胞)、病毒对照(仅加入病毒及细胞)及细胞对照(仅加入细胞)。Karber法计算中和终点,能保护50%细胞不受100 CCID50病毒感染的血清最高稀释度即为血清中和抗体滴度,并计算GMT。抗体滴度≥4判为阳性,<4判为阴性。
1.5 统计学分析 应用SPSS19.0软件及GraphPadPrism 8.0 软件进行统计学分析。采用Kappa系数对3 种不同方法进行一致性分析,以P<0.05表示不同方法之间有一致性,Kappa值在0.6~0.8之间表明一致性较高;在0.8~1.0之间表明一致性极高。3种方法检测的样本阳性率比较采用卡方检验,免疫后血清抗体滴度比较采用t检验,均以P<0.05 为差异有统计学意义。将3 种方法检测的阳性血清抗体滴度经对数(Log)转换后,进行Pearson相关系数(r)及线性回归分析,采用Origin 2021软件绘制线性拟合图。
2 结果
2.1 3种方法检测结果的一致性 MCPENT、PBNA和ELISA 法检测40 份免疫前血清均为阴性;检测80 份疫苗免疫后血清,结果为阳性分别为71、65及75份,阳性率分别为88.8%(71/80)、81.2%(65/80)及93.8%(75/80),阳性率差异无统计学意义(χ2=6.390,P>0.05)。3 种方法检测120 份血清的符合率均达90%以上,Kappa系数均>0.7,P均<0.01,见表1。表明3种方法一致性较强。

表1 3种方法检测120份血清结果的一致性Tab.1 Consistency analysis of 120 serum samples detected by three methods
2.2 3种方法检测免疫后血清抗体滴度的比较 MCPENT、PBNA 和ELISA 法检测80 份免疫后血清的抗体滴度分别为6~2 048、35~79 347、55~42 168,GMT分别为110、282、1 393,MCPENT与PBNA、PBNA与ELISA法检测抗体滴度结果差异均无统计学意义(t分别为1.565、0.850,P分别为0.120、0.397),ELISA 与MCPENT法差异有统计学意义(t=4.921,P<0.001)。
2.3 3种方法检测抗体滴度的相关性 PBNA与MCPENT、ELISA 与MCPENT、ELISA 与PBNA 法阳性血清抗体滴度检测结果r分别为0.902、0.846 及0.825,P均<0.01,见图1。表明3 种方法检测抗体滴度结果具有良好的相关性。
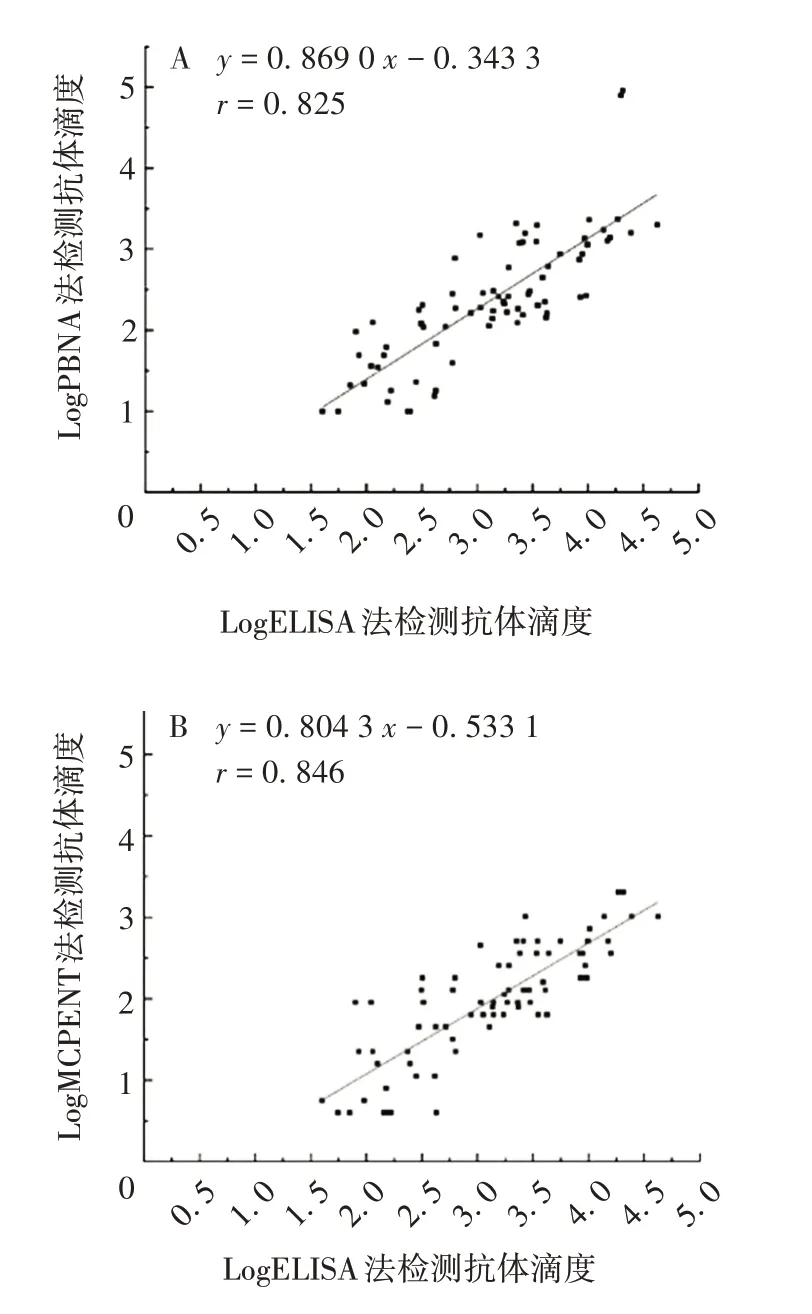
图1 3种方法检测阳性血清抗体滴度的线性拟合图Fig.1 Linear fitting diagram of antibody titers in positive serum detected by three methods
3 讨论
对病毒感染的保护性研究数据是疫苗研发和有效性评价的关键[17-18],疫苗免疫后抗体的阳转率及抗体滴度可用于评价疫苗的免疫原性[19-20],为疫苗上市审批提供数据支持。检测SARS-CoV-2 中和抗体水平的PRNT 及MCPENT 法均涉及活病毒操作,仅能在生物安全防护三级实验室(biological safety protection third-level laboratory,BSL3)中进行,给疫苗临床评价带来了一定困难。PBNA法更快速、操作更简便,与活病毒法具有良好的相关性,已广泛应用于SARS-CoV-2 疫苗的临床研究评价[21-22]。由于SARSCoV-2变异株不断出现,病毒抗原表位的变异也在不断变化,迄今为止尚未建立标准的中和抗体试验法及公认的检测用标准病毒株[23]。目前用于疫苗临床评价及疫苗效力评价的各种试验方法之间存在一定差异,需进行科学的分析和评估。针对疫苗免疫后的抗体水平监测应开发更简便、有效的检测方法[24]。
本研究收集的免疫前血清采自经严格筛选进入临床研究的健康人群血清,3种方法检测SARS-CoV-2疫苗免疫前SARS-CoV-2 抗体均为阴性,排除血清本底等干扰因素,使免疫后血清检测结果更可靠。本研究采用MCPENT、PBNA、ELISA 3 种不同方法检测免疫后80 份血清,抗体阳性率分别为88.8%、81.2%及93.8%,差异无统计学意义(P> 0.05)。3 种方法检测120 份血清样品的抗体符合率达90%以上,阳性抗体滴度结果进行Log 转换后比较,3 种方法之间具有良好的相关性,PBNA 与MCPENT、ELISA 与MCPENT、ELISA与PBNA法抗体滴度检测结果r分别为0.902、0.846及0.825(P均<0.001);抗体滴度检测结果经t检验,MCPENT 与PBNA、PBNA 与ELISA法差异均无统计学意义(P均>0.05),ELISA与MCPENT法差异有统计学意义(P<0.001)。TOLAN 等[25]利用Roche 的ELISA 试剂对美国Moderna 公司的SARSCoV-2 mRNA 疫苗mRNA-1273 和美国辉瑞公司的BNT162b2 疫苗进行免疫后血清检测,结果显示,ELISA 与PBNA 的相关性良好,r均≥0.85,与本研究结果相符。蒋国润等[26]建立的ELISA 与MCPENT 法检测抗体滴度的r为0.494。因此,ELISA 法检测试剂中对于中和表位的选择必须具有良好的代表性,需与活病毒检测具有良好的相关性方可用于疫苗评价或疫苗免疫后抗体监测。
本研究采用的3 种方法均可检测到疫苗免疫后不同滴度的抗体。PBNA、ELISA 法用于检测SARSCoV-2 疫苗免疫后的抗体阳性率与MCPENT 法差异无统计学意义(P>0.05),抗体滴度结果与MCPENT法有较强的相关性(P均<0.001),可用于临床研究中SARS-CoV-2 mRNA 疫苗的免疫原性评价及疫苗免疫后抗体监测。
