宁波市第一医院药品不良反应1 020例分析
2023-11-01孙雨
孙雨
药品不良反应(ADR)指合格药品在正常用法用量下出现的与用药目的无关的有害反应。ADR监测作为药物上市后评价的重要组成部分,可弥补相关药物在上市前研究的局限性,为患者提供药学服务。ADR监测的开展可有效保证患者用药安全、经济、有效、合理。随着ADR工作的稳步推进,其对患者产生的危害,已日益受到医务人员的重视,对相关数据进行评价与分析,有利于更好地发挥ADR监测的作用。
中国医院药物警戒系统(CHPS)通过与医院信息部门进行接口对接,与院内电子病历、检验系统、药库系统等原有系统进行衔接,可实现ADR主动监测(关注品种监测、ADR病历监测、ADR专项监测、自动监测计划)和辅助报告相结合的模式,改善原有ADR以被动监测为主的局面,简化上报流程,提升上报效率,打通原有的信息壁垒,改善现有上报模式实行过程中存在的漏报率高等问题。该模式可全面收集信息,具有针对性较强、准确性较高的优点。
宁波市第一医院作为国家药品不良反应监测哨点医院,于2020年底全面使用CHPS进行ADR的上报。2021年上报至国家药品不良反应监测中心的ADR 1 020例,相较于2020年的733例增加了39.15%。本文通过对1 020例ADR进行汇总、统计分析,为临床合理用药提供参考,保障患者用药安全。现报道如下。
1 资料与方法
收集宁波市第一医院2021年上报的ADR 1 020例。回顾性分析患者性别、年龄、ADR报告类型、上报人职业、药品类别、累及器官/系统、给药途径,分类依据为《药品不良反应报告和监测管理办法》《WHO药品不良反应术语集》等,利用Excel软件对上述信息进行数据汇总分析。
2 结 果
2.1 患者特征分布 1 020例ADR报告中,男474例,女546例,男女比为1∶1.15,女性略多于男性。年龄以≥65岁占比最高为34.61%,0~14岁患者占比最少,仅为0.98%,见表1。
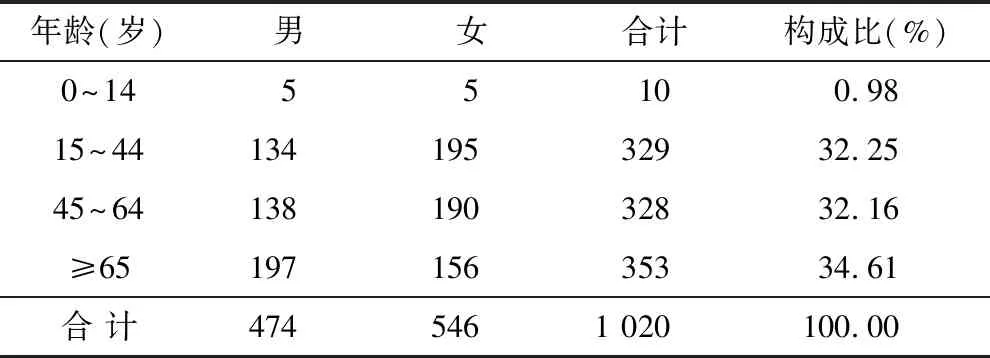
表1 ADR患者性别与年龄分布 (例)
2.2 ADR报告类型 ADR报告类型中,新的严重的、新的一般的及严重的ADR 588例,合计占57.65%,而一般的ADR报告类型占42.35%,见表2。
2.3 ADR上报人职业 ADR上报人职业以护士为主,占比为54.21%,而医师上报的报告占比最低为11.18%,见表3。
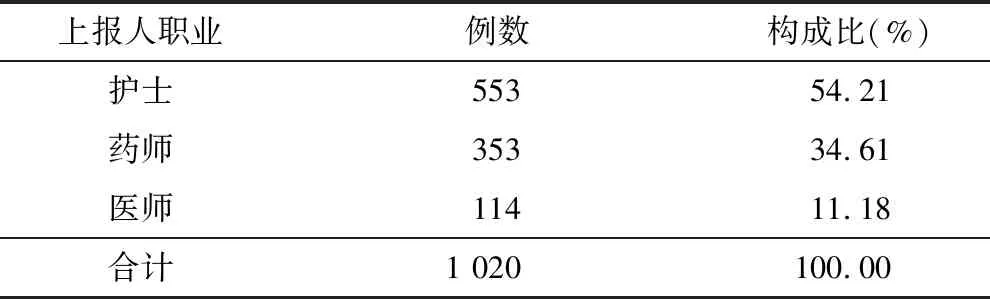
表3 ADR上报人职业
2.4 ADR药品类别 ADR涉及药品类别最多的为抗感染药、心血管系统用药及抗肿瘤用药,分别占52.31%、10.61%和9.16%。见表4。
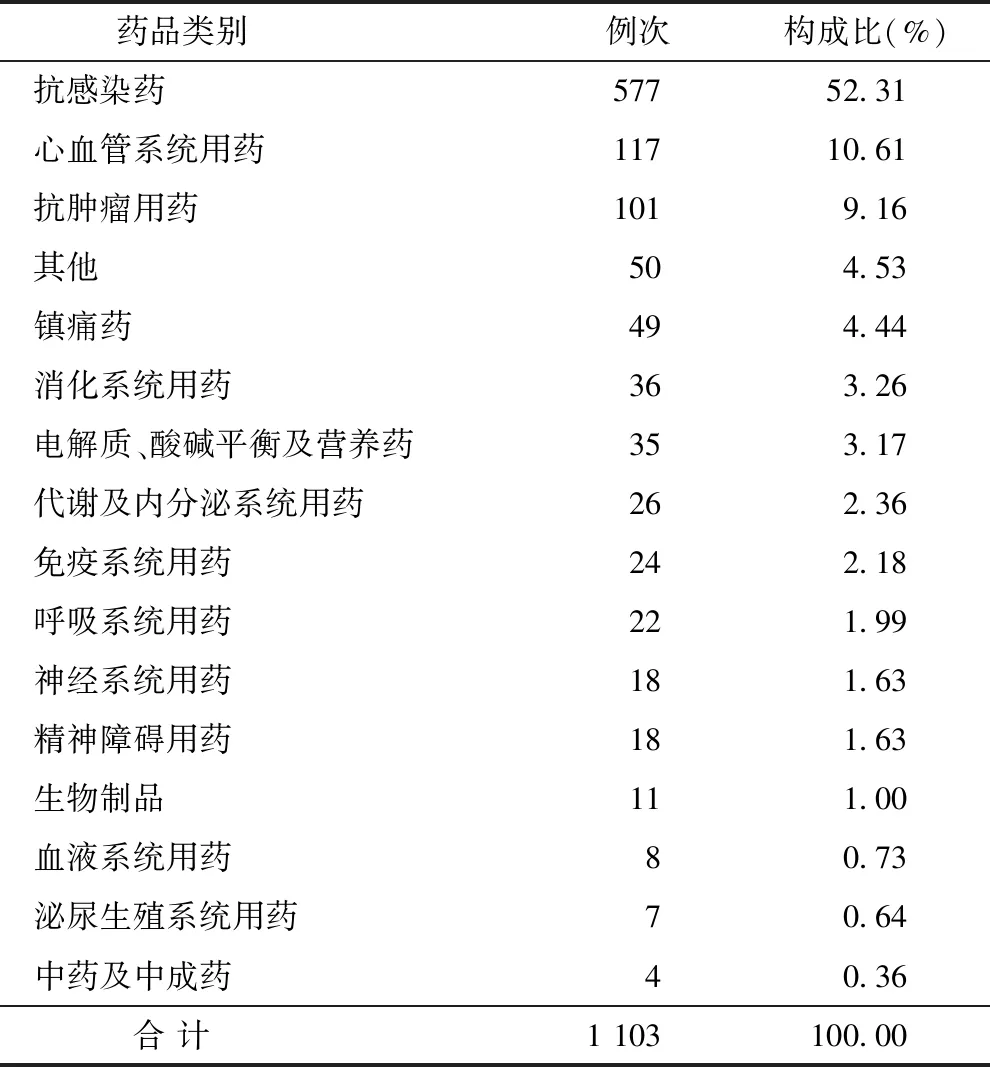
表4 ADR药品类别
2.4.1 抗感染药物相关ADR:ADR发生频次排名前3位抗菌药物为乳酸左氧氟沙星氯化钠注射液、注射用哌拉西林钠他唑巴坦钠、注射用头孢曲松钠,见表5。
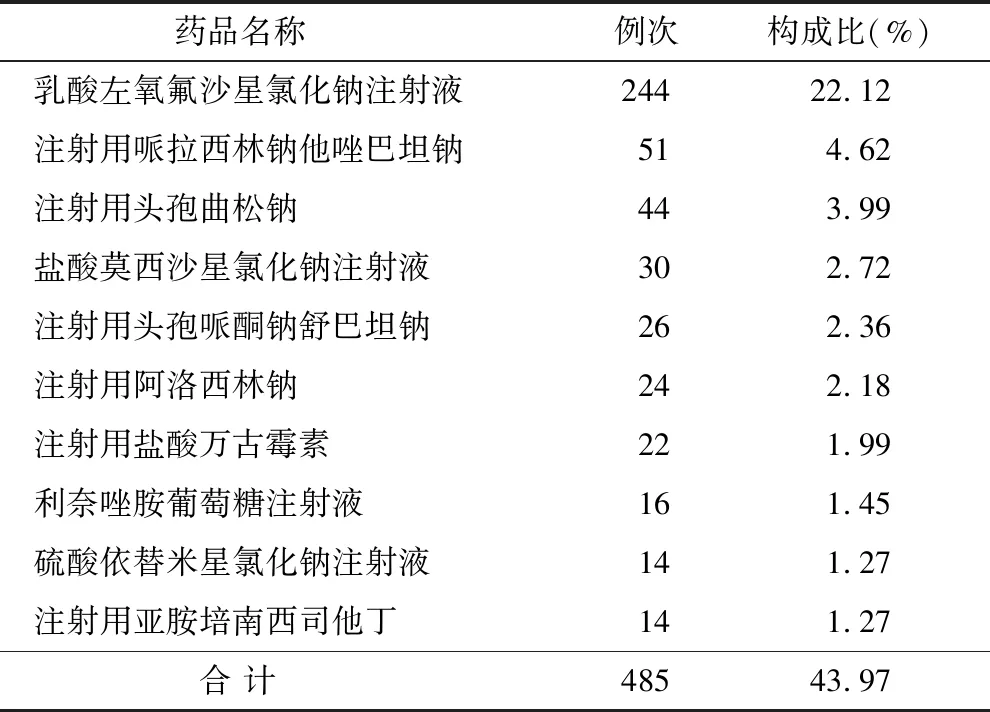
表5 ADR发生频次排名前10位抗菌药物
2.4.2 新型抗肿瘤药物相关ADR:新型抗肿瘤药物中以注射用卡瑞利珠单抗上报例数最多,不良反应表现为白斑病、骨髓抑制、重症肌无力样综合征、发热、寒战、发冷、肝功能异常,见表6。
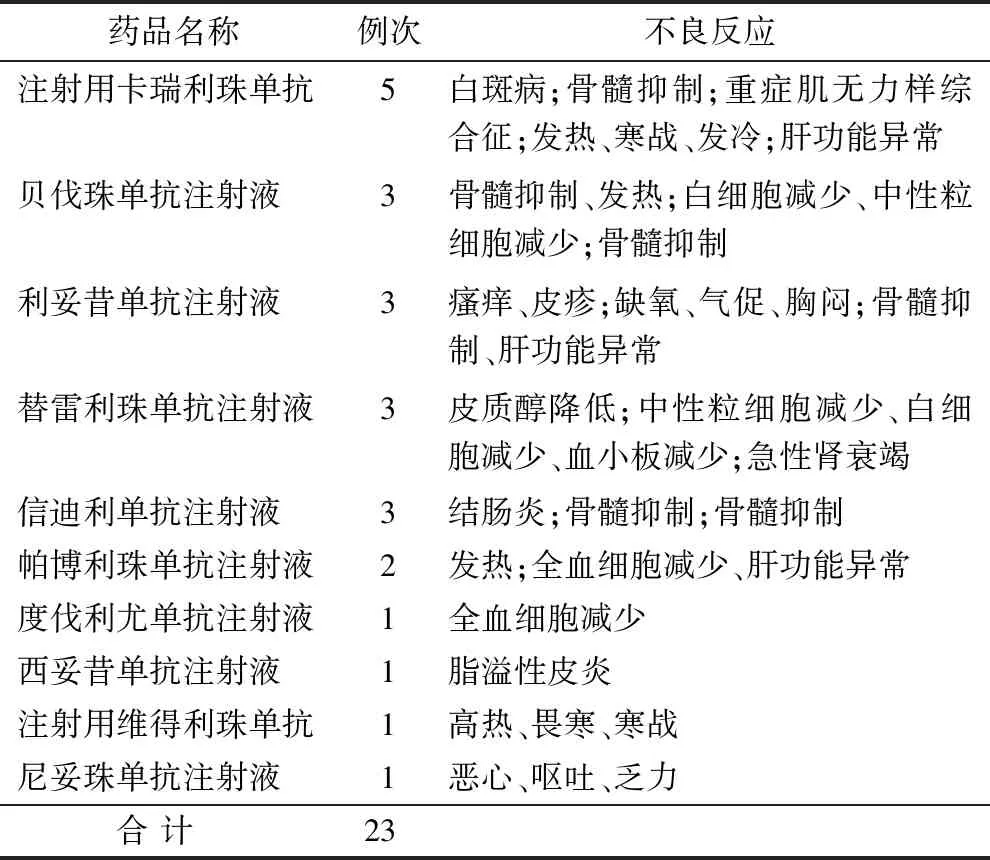
表6 新型抗肿瘤药物相关ADR
2.5 ADR累及器官/系统分布 ADR累及器官/系统中,以皮肤及其附件损害占比最高为36.57%,其次为消化系统损害占20.72%,排名第3位的为全身性损害占8.64%,见表7。
2.6 给药途径 1 020例ADR涉及多种给药途径,以注射给药为主,注射给药中以静脉滴注为主,共726例,占65.11%,见表8。
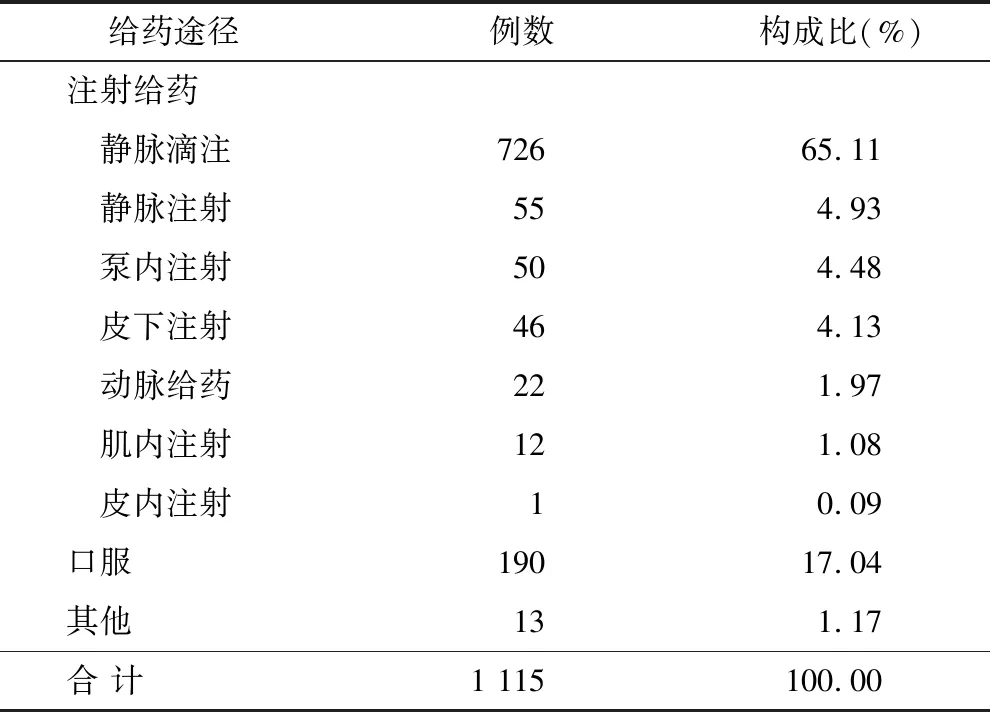
表8 给药途径
3 讨 论
为加强ADR的监测和报告工作的管理力度,我院2013年初将ADR监测工作作为一项全院的日常工作,纳入《科室质量控制目标考核评分细则》,有效推动了我院ADR监测工作的开展。从2016年开始,我院又将ADR上报情况作为各临床科室行政查房反馈的内容之一及各科室年终考核的指标之一,进一步推动了ADR监测工作在我院的开展。我院还建立了由分管院长任组长,医务部、药学部和护理部负责人为成员的ADR监测工作领导小组,药学部指定专职临床药师担任本院药品不良反应监测员。目前我院已建立一支覆盖各临床科室的人员相对稳定的药品不良反应监测员队伍,原则上每个病区各有1名临床医师和1名护理人员作为药品不良反应监测员。
通过对报告数据和结构的定期分析可见,我院2021年ADR报告数量有较大增加,这得益于我院业务量的增加及CHPS系统的应用[1]。往年由于部分医护人员觉得上报过程较复杂,或上报相关不良反应会引起医疗纠纷、医嘱医师处分等错误认知,导致ADR漏报率较高、报告上报不及时等问题,而CHPS系统的引入进一步简化了ADR上报流程,增加了医护人员的上报例数。此外,利用CHPS系统主动监测模块内容,通过对病历进行关键词(不良反应、药物性皮炎等)检索等方式,可进一步增加上报率。
我院在院内局域网上开辟药物警戒专栏,及时将国家药品不良反应中心发布的ADR信息通报及FDA、NMPA等药物警戒快讯在院内网上进行公布,使全体医务人员及时获知最新的药品不良反应相关信息,提高ADR的认识水平及鉴别能力。
3.1 患者性别与年龄分布 由本文分析可知,女性发生ADR的概率略高于男性,这可能与女性体内药动学特点、生理因素有关[2]。使用绝大多数药物后,女性体内具有更高的血药浓度和更长的消除时间[3]。与男性相比,女性肾小球滤过率相对较低,因此药物的肾脏清除率降低。女性的胃排空时间较慢,胃pH值较低等因素,均会影响药代动力学。此外,与男性相比,女性更有可能同时合用多种药物,这同样增加女性发生ADR的风险。
而从年龄分布来看,≥65岁的老年人更易发生不良反应,这与老年人合并基础疾病较多、器官老化、药代动力学发生改变、对药物的敏感性发生变化有关。老年人患高血压、糖尿病、高脂血症等慢性疾病风险较高,且老年患者对用药交代的接受程度和用药依从性较低,例如擅自停用普萘洛尔等药物会导致反跳现象,使ADR发生频率增加。老年患者发生药源性肾损伤等特定ADR风险较高,目前药源性肾损伤暂无有效的治疗手段,应以预防为主,并及时识别相关不良反应并进行停用可疑药物处理。在临床上针对老年人制定用药方案时,需要对患者的基本情况进行统筹考虑,并结合患者基础用药及既往不良反应史,严格遵守相关说明书中对于老年人的用法用量,作好老年人用药宣教,保障老年人安全用药[4]。
3.2 ADR报告类型和上报人职业 在2021年度我院上报的ADR中,一般的仅占42.35%,说明我院医务人员能较好地对新的和严重的ADR进行识别和上报,侧面反映我院临床药师对医护人员进行相关ADR知识的培训,可减少患者由于药物引起的损害。
但2021年我院上报的新的和严重的不良反应比例较2020年有明显下降,因此下一步将在全院继续进行ADR识别相关的培训,同时针对一些重点科室和部门进行专项培训,进一步提升临床医务人员对新的和严重的不良反应的识别能力,增加我院ADR的上报质量。例如通过增加临床药师覆盖科室,及时发现并上报相关ADR。通过实时查看医院的检验之星等软件,对检验异常值进行重点关注,结合电子病历系统,必要时深入临床了解具体的病情,从而发现严重的、新的严重的、罕见的ADR。2022年度我院拟加大对临床医务人员ADR相关知识的培训力度,增加对医务人员进行ADR应知应会的现场考核,尽量使每一位医务人员都知晓ADR的基本概念和上报ADR流程。
上报人职业以护士为主,医师占比最少。发现药品相关不良反应的途径包括门诊接诊、药房退药、病房查房、注射室输液等,医师在临床诊疗过程中,具有作为第一发现人的客观条件,且具备对药物与不良反应的关联性及对新的、严重的不良反应进行识别、评价、分析的能力。因此,未来需尽力提升医师上报的积极性,通过科室将问题反馈给各科室科主任、ADR监测员,提升医师上报的积极性。
3.3 发生ADR的药品类别 ADR药品类别排名前3位的分别是抗感染药、心血管系统用药及肿瘤用药。在抗感染药中,排名前3位的抗菌药物分别是乳酸左氧氟沙星氯化钠注射液、注射用哌拉西林钠他唑巴坦钠、注射用头孢曲松钠,这3种抗菌药物在我院抗感染药物中的使用一直位居前列,并不代表上述药物不良反应发生率较其他抗菌药物高。在患者使用相关抗菌药物之前,需特别关注患者的既往过敏史和ADR史,尽量避免使用同类怀疑药物[4]。特殊使用级抗菌药物中万古霉素、利奈唑胺、亚胺培南西司他丁钠的不良反应发生例次较多。万古霉素、利奈唑胺引起的严重的不良反应包括肝肾功能异常、白细胞减少、中性粒细胞减少、凝血时间延长等。而亚胺培南西司他丁钠引起严重的不良反应包括幻视、兴奋、失眠、血小板增多等。特殊使用级别抗菌药物,临床使用中需严格把握适应证和禁忌证,除进行专档管理外,用药前建议进行药敏试验,并根据细菌培养结果进行抗菌药物的选择,且应通过使用级抗菌药物会诊专家小组审核。
实施血药浓度检测、基因检测等个体化用药检测手段可有效提升抗菌药物使用的安全性。2022年我院可以检测血药浓度的抗菌药物包括伏立康唑、泊沙康唑、利奈唑胺、替考拉宁、伊马替尼,其中泊沙康唑、伊马替尼为2021年开展的新项目,借助药学部血药浓度检测契机,可及时对相关药物引起的不良反应进行监测和干预,并通过在医院内网公布相关的安全用药建议,例如《血药浓度监测:关于泊沙康唑的安全用药建议》,为安全用药保驾护航。
由于靶向性高、不良反应较少等优势,包括PD-1/PD-L1抑制剂在内的新型抗肿瘤药物在临床应用日益广泛。日前,国家颁布《新型抗肿瘤药物临床应用指导原则(2020年版)》,因此在ADR上报中,对此类药物相关不良反应需要进行格外关注,及时做好预防和预后。国家规定新药监测期内的药品应报告该药品发生的所有不良反应,新型抗肿瘤药物多为上市5年内的新药,应对所有的不良反应进行监测并上报。在抗肿瘤用药中,新型抗肿瘤药物相关ADR共计23例,涵盖注射用卡瑞利珠单抗、贝伐珠单抗注射液、利妥昔单抗注射液、替雷利珠单抗注射液、信迪利单抗注射液、帕博利珠单抗注射液、度伐利尤单抗注射液、西妥昔单抗注射液、注射用维得利珠单抗、尼妥珠单抗注射液,充实了该类药品的安全用药知识。
3.4 ADR累及器官/系统 ADR累及器官/系统中,以皮肤及其附件损害为主,主要表现为瘙痒、皮疹,该类不良反应表现明显,其次为消化系统损害,上述不良反应较易被医务人员识别,但需要与病毒感染、湿疹、胃炎等患者原患疾病进行区分[5]。在累及皮肤的不良反应中,较严重的不良反应有重症多形红斑型药疹,该类药品不良反应致死率较高,是临床发生最多的严重药疹[6],需尽快识别并停用可疑药物[7],并及时进行对症处理。
较为复杂且症状不明显的ADR,例如血液系统损害、肝脏系统、肾脏系统损害等,需引起临床重视,必要时请专科会诊,避免遗漏可疑药物引起的损害,对患者造成不良后果[8]。例如药物性肝损害的诱因复杂,临床表现缺乏特异性,临床医师需减少误诊及漏诊,并引起对药物性肝损害的重视。
3.5 给药途径 在所有给药途径中,占比最大的分别为静脉滴注、口服、静脉注射。静脉滴注给药不良反应的发生例数远高于口服给药,这与静脉滴注给药均在医疗机构内部进行,相关不良反应较易识别和上报相关。其次,静脉滴注给药相较于口服等其他给药途径,药物能快速进入血液循环系统,发挥药效[9],并易受到热原、配置过程、并用药物、溶媒等因素影响[10]。因此,应进一步加强静脉输液管理,我院已取消门诊输液,在患者病情允许的条件下,应尽量避免使用静脉滴注的药物。
综上所述,我院2021年通过CHPS系统大幅度提升了ADR上报的数量和质量,通过对患者信息、累及器官/系统、药品信息、类型、上报人信息进行分析后可知,医护药在药物选择、用法用量、不良反应处置等方面需开展紧密合作,共同保障患者用药安全。
利益冲突:所有作者声明无利益冲突。
