颞骨轴位高分辨CT在人工耳蜗植入中的指导作用及术后评估价值研究
2022-10-18刘永刚魏璐璐
刘永刚 魏璐璐
郑州大学附属医院南阳市中心医院耳鼻喉科 (河南 南阳 473000)
人工耳蜗植入(cochlear implants,CI)是一种利用特殊声-电转换电子装置替代原有耳蜗功能的术式,可将环境中机械声信号转化为电信号,并经电极传入耳蜗,刺激残存听觉神经元,让患者产生听觉,是当前重度或极重度感音神经性耳聋(sensorineural hearing loss,SNHL)唯一有效治疗方式[1]。CI手术重点在于将电极完全植入耳蜗内,同时避免耳蜗损伤,但耳蜗位于颞骨深部,其解剖结构精细、形态复杂,且存在较大个体差异,如何精确显示内耳解剖结构是保障手术安全、有效进行以及评价手术效果的关键[2]。近些年来,随着CT影像技术发展,高分辨率CT(high-resolution CT,HRCT)因成像质量高、清楚显示耳蜗解剖、评价耳蜗鼓阶同人工耳蜗关系等,在CI术前及术后评估应用越来越多[3]。本研究将颞骨轴位HRCT用于人工耳蜗植入中,旨在分析其对患者术前指导及术后评估价值,为提高CI手术效果及安全性提供参考。
1 资料与方法
1.1 一般资料选取2018年5月至2020年5月86例(108患耳)行CI治疗的SNHL患者,纳入标准:经听性脑干反应、声导抗、前庭功能等检查明确SNHL诊断,佩戴助听器、行常规训练无法改善,拟行CI手术,家属或患者签署知情同意;排除标准:既往外耳道或内耳损伤、手术史,合并中枢性耳聋,存在耳蜗未发育、神经纤维瘤、急性化脓性中耳炎、Michel畸形等手术绝对禁忌症。86例患者男49例,女37例,年龄1~33岁,平均(10.85±4.07)岁,患耳右侧36例,左侧28例,双侧22例。
1.2 方法采用GE Lightspeed 64排多层螺旋CT,于术前、术后行颞骨轴位扫描,扫描范围:以上眶耳线为基线,自外耳孔下缘到岩骨上缘,涵盖整个中耳、内耳。对无法配合的患儿检查前予以10%水合氯醛灌肠,小儿患者检查时均加穿铅防护服保护。参数设置:管电压140kV,管电流300mA,扫描层厚0.625mm,层间距0.625mm,螺距0.562:1,扫描完成后,采用骨加算法重建,完成MPR、CPR、MIP、VRT重建。将图像质量分为4级,差:伪影明显,细微结构难以分辨,无法观察;一般:存在小片状伪影,细微结构显示欠轻,尚可诊断;良:有少许线状伪影,细微结构显示较轻,但不影响诊断;优:无伪影,细微结构显示清晰,方便诊断,统计优良率;观察耳蜗、前庭、上外侧半规管等结构,测量面神经至前庭窗、蜗窗距离,面神经隐窝到前庭窗、蜗窗水平截面距离。患者手术及术中测量由同一医师完成;术后行HRCT观察电极位置、形态等。HRCT结果由具有丰富的经验1名手术医师、2名的放射科医师共同评估后达成一致。
1.3 统计学分析采用SPSS 19.0软件,计数资料用n(%)描述,行χ2检验或Fisher精确概率法,计量资料用均数±标准差()描述,行配对样本t检验;P<0.05为差异有统计学意义。
2 结 果
2.1 HRCT术前及术后重组图像质量评分情况86例患者术前HRCT图像质量评级中,差0例,一般2例(2.33%),良5例(5.81%),优79例(91.86%),优良率达97.67%;术后图像质量评分中,差0例,一般3例(3.49%),良5例(5.81%),优78例(90.70%)优良率达96.51%;术前、术后HRCT图像质量均可满足诊断需求。
2.2 HRCT术前内耳发育畸形检出情况术前颞骨轴位HRCT结果显示,86例(108耳)患者52例(68耳)存在内耳畸形,其中前庭导水管扩大28耳(见图1);耳蜗畸形共16耳,其中耳蜗发育不全7耳(见图2),不完全分隔型5耳,共腔畸形4耳;半规管发育畸形11耳(见图3);耳蜗神经发育不良8例;内听耳道畸形5例(见图4)。
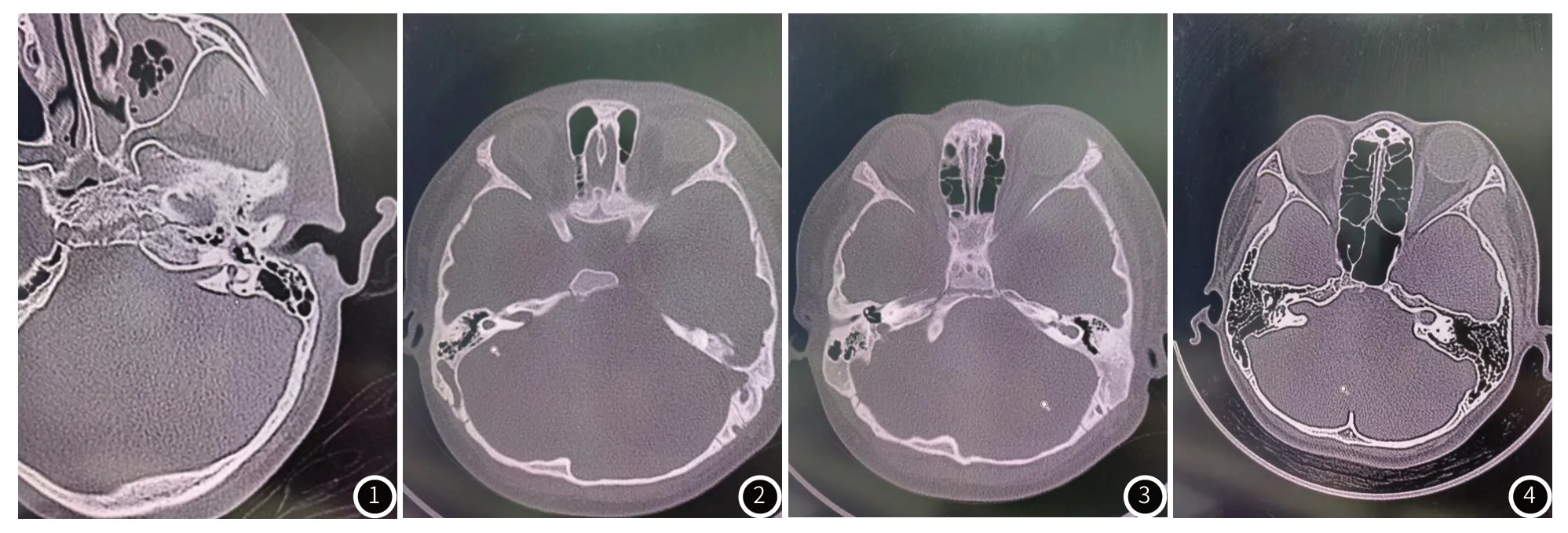
图1 患儿3岁,男,HRCT提示前庭导水管扩大。图2 患儿4岁,女,HRCT提示耳蜗发育不全。图3 患儿5岁,男,HRCT提示前庭半规管发育畸形。图4 患儿4岁,男,HRCT提示内耳道扩大。
2.3 HRCT术前检查与术中实测结果比较HRCT术前所测面神经到前庭窗、蜗窗距离及面神经隐窝到前庭窗、蜗窗水平截面距离与术中实测结果比较差异均无统计学意义(P>0.05)。
2.4 人工耳蜗植入术后电极植入异常情况86例108患耳人工耳蜗植入术后,经HRCT检查,共12例(11.11%)电极植入异常,其中不伴内耳畸形植入异常发生率2.50%,明显低于伴内耳畸形的16.18%(P<0.05)。
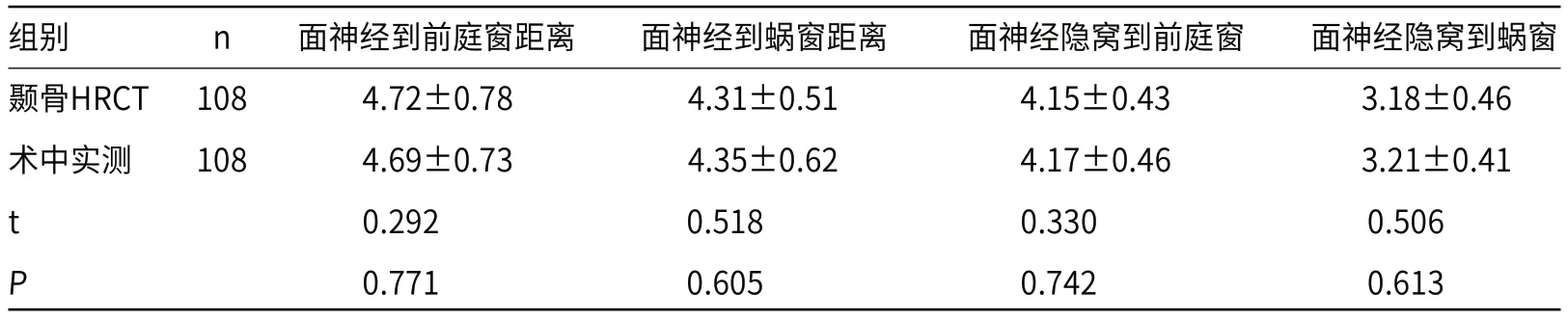
表1 HRCT术前检查与术中实测结果比较(mm)
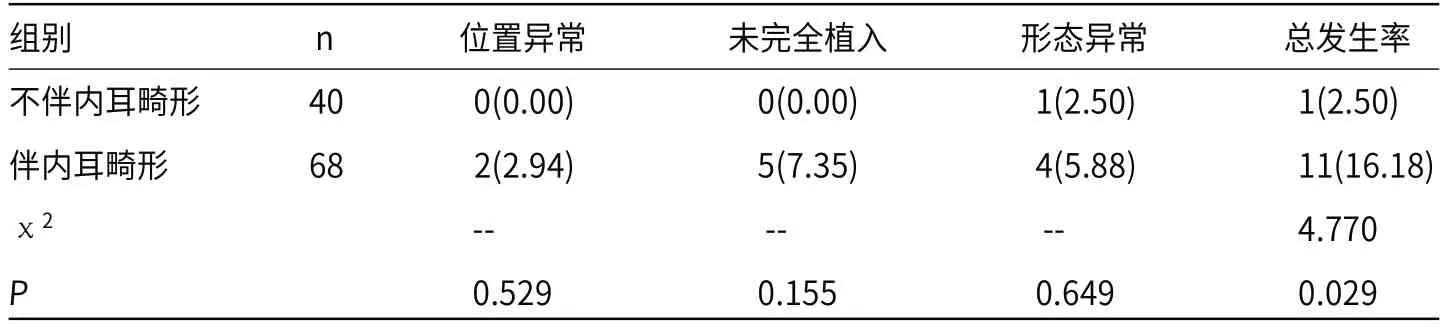
表2 人工耳蜗植入术后电极植入异常情况[n(%)]
3 讨 论
CI自上世纪70年代问世以来,让无数SNHL患者听觉或听力获得不同程度恢复,尤其对于小儿患者,其应用使得其语言能力得以继续发展,对患者人生影响重大[4]。CI最经典的术式主要步骤包括行后鼓室入路,开放面神经隐窝,将圆窗龛与圆窗膜暴露,最后开放内耳鼓阶、将电极植入,但在实际操作中,因患者内耳发育情况及个体解剖差异较大,手术医师常面临面神经隐窝及圆窗暴露困难问题,使得手术难度及术中神经损伤风险增加,因此准确进行术前评估,评价患者手术可行性、难易程度及手术风险,并以此制定合适手术方案及应急预案十分重要[5]。
既往X线在CI术前及术后评估中有一定应用,但其对颞骨解剖、深部耳蜗等重要结构显像差,已逐步为成像质量更好的CT、MRI等检查替代[6]。HRCT是CT技术的进一步发展,其可在较短的扫描时间内,获得良好空间分辨率,能清楚显示细微结构,在骨骼检查、眼耳鼻喉检查、胸部检查等方面展现出了良好应用前景[7]。将HRCT用于CI术前及术后检查,主要有以下优势:(1)图像层厚薄(一般1mm内),经后期三维重建可提高空间分辨率;(2)图像为断层显像,能清晰显示骨迷路及其他细微解剖结构;(3)综合应用多种三维重建模式,能从多角度、多方面显示细微解剖,了解内耳发育情况及病变;(4)可通过影像测量面神经到前庭窗、蜗窗等距离,为术中推测面隐窝可开放大小提供依据;(5)术后检查可直接显示电极植入长度、形态及在耳蜗内位置,了解手术效果;(6)CI以小儿多见,而HRCT因扫描时间短,较常规CT扫描提高了小儿配合度[8]。本研究将HRCT用于CI术前及术后评估中,结果显示,患者术前、术后获得的HRCT图像质量均可满足诊断需求,且优良率分别达97.67%、96.51%,提示HRCT适用于CI术前及术后评估。
SNHL发病与先天性内耳畸形密切相关,对先天性内耳畸形的准确诊断及分类有助于评估CI手术可行性、难易程度及并发症风险等,从而为临床精准化、个体化治疗提供参考[9]。本研究86例患者中,有52例(68耳)存在内耳畸形,其中前庭导水管扩大28耳,耳蜗畸形16耳,半规管发育畸形11耳,耳蜗神经发育不良8例,内听耳道畸形5例,这些内耳畸形的检出对指导手术进行具有重要意义。以前庭导水管扩大为例,患者耳蜗水管相比正常内耳解剖患者宽度明显增加,且常伴有不完全分隔畸形,术中出现脑脊液“井喷”风险升高,而脑脊液“井喷”会增加电极植入难度及颅内感染风险,因此术前评估需重视其发生可能性,做好以下应急准备:首先,对该类患者术中将面神经隐窝充分暴露;再者,如遇到“井喷”时,可适当将圆窗或耳蜗开窗口扩大,在鼓阶打开后,可不必将电极急于植入,而应等脑脊液涌出压力稳定后,再将电极缓慢植入,最后用少许肌肉组织将圆窗和鼓阶严密封闭,耐心观察约10min确认封闭可靠,进而降低术后脑脊液漏及颅内感染风险[10]。本研究对比HRCT术前所测面神经到前庭窗、蜗窗距离及面神经隐窝到前庭窗、蜗窗水平截面距离与术中实测结果,发现二者之间比较差异均无统计学意义,提示术前HRCT检查可内耳解剖形态可精确显示,可供术中面隐窝开放大小等参考,有利于提高手术精确性、降低面神经等损伤风险,与魏璐璐等[11]发现类似。人工耳蜗电极准确植入是CI手术成功的关键,理想状态下电极应位于鼓阶内,可使得电极更接近听神经,并可提示手术为对骨螺旋板、基底膜等完整性造成损害,若发现异常,应及时处理[12]。本研究显示,86例108患耳人工耳蜗植入术后,有12例存在电极植入异常,且不伴内耳畸形植入异常发生率2.50%,明显低于伴内耳畸形的16.18%,说明HRCT对术后电极植入异常有检测作用,且对于术前伴内耳畸形者,且检测尤为必要。
综上所述,HRCT检查用于CI患者术前、术后评估,具有图像质量好、能客观显示内耳发育情况及解剖结构特点,可有效评估患者术前内耳发育情况及术后电极植入效果,利于手术指导及术后评估,值得临床应用。
