症状性颅内粥样硬化患者前循环低灌注与缺血性卒中复发相关性的定量研究
2022-05-20任舒静沈子祯苏春秋吴蓉蓉施海彬鲁珊珊洪汛宁
任舒静,沈子祯,苏春秋,吴蓉蓉,施海彬,鲁珊珊,洪汛宁
南京医科大学第一附属医院放射科,江苏 南京 210029
颅内动脉粥样硬化性疾病(intracranial athero⁃sclerotic disease,ICAD)是亚洲缺血性卒中的主要病因[1],具有致死、致残、复发率高的特点。据报道,我国约有46.6%的急性缺血性卒中由ICAD 引起。即使是经过规范的临床治疗,ICAD相关的脑血管事件每年复发率仍高达17.1%~38.2%,尤其是症状性ICAD 患者,第1 年复发率高达17.6%~23.0%[2]。缺血性卒中复发造成的脑功能损害及疾病负担均明显大于首次发作,因此早期预测复发风险高的患者,在首次发病后进行更积极的干预治疗,有重要的临床意义。
既往研究表明,ICAD狭窄血管下游低灌注与脑卒中复发存在一定相关性[3-6],但多采用分水岭梗死作为评估低灌注的定性指标。本研究采用不同残余功能达峰时间(time to maximum of the residual function,Tmax)阈值对低灌注进行定量化研究,探讨不同阈值下低灌注体积与缺血性卒中复发的相关性,并与传统的指标对照,明确预警缺血性卒中复发的有效影像学标志物。
1 对象和方法
1.1 对象
本横断面研究回顾性分析了2016 年11 月—2021年5月期间南京医科大学第一附属医院完成头颅磁共振检查进行颅内血管病变评估的ICAD 患者,包括三维时间飞跃磁共振脑血管造影(three⁃di⁃mensional time⁃of⁃flight magnetic resonance angiogra⁃phy,3D⁃TOF⁃MRA),弥散加权成像(diffusion weight⁃ed imaging,DWI)和动态磁敏感对比增强灌注加权成像(dynamic susceptibility contrast⁃perfusion weight⁃ed imaging,DSC⁃PWI)。本研究符合伦理学标准,经院伦理审查委员会批准。
具体纳入标准如下:①患者表现为急性期(症状发作<4 周)及亚急性期(症状发作4~8 周)脑梗死,即DWI 图像可见高信号梗死灶;或短暂性脑缺血发作(transient ischemic attack,TIA);②责任血管为大脑中动脉(middle cerebral artery,MCA);③有完整的临床及实验室检查资料;④有高血压、高血脂、糖尿病、吸烟等1 个及以上动脉粥样硬化危险因素。排除标准如下:①有夹层、动脉瘤、烟雾病、心源性栓子等非动脉粥样硬化性血管病;②后循环或大脑前动脉供血区缺血性卒中患者;③慢性脑卒中患者(梗死时间>8 周);④MCA 供血区大面积软化灶;⑤MRA 或颈动脉超声图像示同侧颈内动脉(in⁃ternal carotid artery,ICA)狭窄程度>30%;⑥高分辨血管壁成像或颈动脉超声图像示同侧颈内动脉存在不稳定斑块;⑦图像质量差,无法分析。
复发性脑血管事件定义为:在首次发生的缺血性卒中责任血管供血区域,再次发生1 次及以上急性/亚急性梗死,或与受累供血区相对应的TIA 症状。据此将所有入组患者分为初发组及复发组。
1.2 方法
1.2.1 临床资料
收集患者的性别、年龄、动脉粥样硬化高危因素(高血压、糖尿病、高脂血症病史及吸烟史)、临床用药情况(阿司匹林、氯吡格雷及他汀类药物)及低密度脂蛋白(low density lipoprotein,LDL)水平。
1.2.2 图像采集
采用德国西门子公司3.0T MR、20 通道头线圈进行扫描。多模态MRI序列包括:①3D⁃TOF⁃MRA:重复时间/回波时间(repetition time/echo time,TR/TE)=22 ms/3.6 ms,翻转角=18°,视野(field of view,FOV)=210 mm×190 mm,分辨率=0.55 mm×0.55 mm×0.55 mm;②DWI:b 值=0 或1 000 mm2/s,FOV=230 mm×230 mm,矩阵=192×192,层厚=5 mm;③DSC⁃PWI:使用单次激发梯度回波⁃平面回波成像序列,TR=1 400 ms、TE=32 ms,FOV=230 mm×230 mm,矩阵=128×128,层数=18,层厚=5 mm,间隔=1.25 mm;静脉团注对比剂钆喷替酸普甲胺(Gd⁃DTPA)0.1 mmol/kg,注射速率4.5 mL/s,共采集50 个动态期相。总扫描时间为6 min 25 s。
1.2.3 图像分析
由2名分别有10年和4年工作经验的神经影像医师独立评估所有患者的3D⁃TOF⁃MRA、DWI 及DSC⁃PWI 图像。评估内容如下:①血管狭窄率:根据3D⁃TOF⁃MRA 图像,狭窄率=(1-最狭窄处血管直径/参照血管直径)×100%[7]。参照血管选择狭窄近端正常血管,如果选择困难(如长段病变),可选用对侧正常血管作为参照血管;②分水岭梗死评估:依据DWI图像分为分水岭梗死型(内分水岭、皮层分水岭梗死)及非分水岭梗死型(软脑膜动脉供血区及穿支动脉供血区梗死)[3];③定量低灌注体积:将DWI 及DSC⁃PWI 原始数据导入NeuBrain⁃CARE软件(v1.1.10,沈阳东软医疗),自动设置动脉及静脉输入函数,通过去卷积算法,计算得到灌注参数图Tmax。采用时间阈值Tmax>4 s 及Tmax>6 s,分别自动计算卒中同侧低灌注体积,并利用软件分割的功能,对低灌注区进行可视化。为了避免评估时观察者之间的差异,意见不一致时由1 名有多年工作经验的高年资神经系统影像医师协助评估,确保结果的准确性。
1.3 统计学方法
采用SPSS22.0 统计软件进行统计学分析。采用Shapiro⁃Wilk 检验计量资料是否符合正态分布,符合即用均数±标准差()表示,否则用中位数(四分位数)[M(P25,P75)]表示;计数资料用频数及百分比表示。采用Kappa 值或组内相关系数(intra⁃class correlation coefficient,ICC)评估两名医师对分水岭梗死、血管狭窄率评估结果的一致性:<0.40 为一致性较差;0.40~0.75为一致性中等;>0.75为一致性较好。
将初发组与复发组的临床及灌注指标进行对比分析,计量资料的比较采用独立样本t检验或非参数检验,计数资料的比较采用卡方检验、Fisher精确概率法。进一步将与缺血性卒中复发可能相关的临床及灌注指标进行单因素Logistic回归分析,单因素分析中有意义(P<0.1)的因素,纳入多因素Lo⁃gistic回归分析(逐步退后法),进一步探讨缺血性卒中复发相关的独立危险因素,P<0.05 为差异有统计学意义,计算OR 值及95%可信区间(confidence interval,CI),采用受试者工作特征曲线(receiver op⁃erating characteristic curve,ROC)分析,计算cutoff值、灵敏度、特异度及曲线下面积(area under ROC curve,AUC)。
2 结果
2.1 临床基线资料比较
本研究共纳入130 例缺血性脑卒中患者,其中初发组92例,复发组38例。临床资料结果如表1所示。两组中患者性别、年龄及危险因素(糖尿病、高脂血症及吸烟)的差异均无统计学意义(P均>0.05)。同初发组患者比较,复发组患者高血压的患病率更高(81.6%vs.63.0%,P=0.039),患者服用阿司匹林、氯吡格雷及他汀类3 种药物的比例更高(P<0.001),LDL水平也更低(P=0.001)。
2.2 低灌注指标与缺血性卒中复发的相关性
两名医生对狭窄率、分水岭梗死的评估一致性较好(ICC=0.826,Kappa=0.787)。与初发组患者比较,复发组患者的血管狭窄率更高(81.4%±19.8%vs.69.5%±20.8%,P=0.003)、分水岭梗死的发生比例更高(65.8%vs.45.7%,P=0.037)、Tmax>6 s 及Tmax>4 s的低灌注体积均更高(P均<0.001,表1)。初发及复发组的典型病例如图1、2所示。

图1 初发组代表性病例Figure 1 The representative patient with the first episode of acute ischemic stroke/TIA

表1 两组患者临床及影像学指标对比Table 1 Comparisons between two groups in terms of clinical characteristics and imaging markers
单因素Logistic 回归分析表明,血管狭窄率、分水岭梗死、Tmax>6 s及Tmax>4 s 的低灌注体积均与缺血性卒中复发相关(P均<0.05)。为了避免危险因素的多重共线性,采用逐步退后法进行多因素Lo⁃gistic 回归分析,结果表明,基于时间阈值Tmax>4 s量化的低灌注体积,是与前循环缺血性卒中复发相关的独立危险因素(OR=1.120,低灌注体积每增加10 mL,95% CI:1.051~1.194,P<0.001,表2),AUC 为0.756(95%CI:0.672~0.839),cutoff 值为32.2 mL,灵敏度为76.3%,特异度为63.0%(图3)。

图3 Tmax>4 s低灌注体积评估缺血性卒中复发风险的价值Figure 3 The predictive value of hypoperfusion volume based on Tmax>4 s for recurrent ischemic stroke
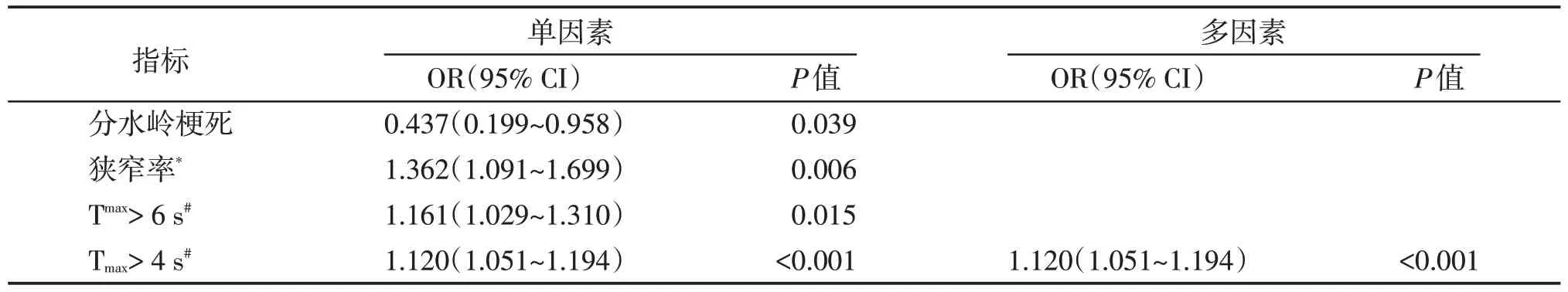
表2 低灌注指标与缺血性卒中复发的相关性Table 2 The relationship between hypoperfusion and ischemic stroke recurrence
3 讨论
ICAD是导致缺血性卒中的首要病因,且复发率高,多次复发患者往往预后差,早期预警缺血性卒中复发有重要的临床意义。既往研究表明,积极的药物治疗对于稳定ICAD斑块和降低动脉⁃动脉栓塞的风险是有效的[8-9],但是也有研究认为单纯的药物治疗不能使血管狭窄伴有下游显著低灌注的患者获益,卒中复发风险依然存在[10-13]。本研究中,同初发组比,复发组患者接受阿司匹林、氯吡格雷、他汀类药物内科治疗的比例更高,血LDL水平更低,这表明即使药物治疗可以稳定斑块,卒中复发的风险仍不能完全避免。缺血性卒中发生的病理生理机制同时涉及斑块(不稳定斑块破裂、血栓形成、动脉⁃动脉栓塞)及低灌注损伤[14]。因此,基于影像学探讨有效的低灌注指标,对预警卒中复发具有重要的临床价值。
分水岭梗死是狭窄血管下游灌注受损的标志,Wabnitz 等[3]的研究表明,同非分水岭梗死患者比较,这类患者卒中复发的风险更高。本研究中复发组患者分水岭梗死比例(65.8%)显著高于初发组(45.7%),与其结果一致。但分水岭梗死的评估具有主观性,这也造成了既往研究结论的不一致性[15]。Sacchetti 等[16]曾探索了定量化的低灌注指标,发现基于Tmax>6 s 量化的低灌注体积与梗死核心之间的不匹配体积大于15 mL 有助于预测ICAD 患者的卒中复发,这与Yaghi等[17]的结论一致。Lyu等[18]采用动脉自旋标记(arterial spin labelling,ASL)灌注成像研究前循环灌注与复发的相关性,发现不同标记后延迟时间(1.5 s 及2.5 s)的脑血流量图差值>50%,可能有助于判断卒中复发风险。但ASL 成像受标记后延迟时间影响较大,容易低估缺血性卒中患者侧支循环,且难以准确计算低灌注体积。
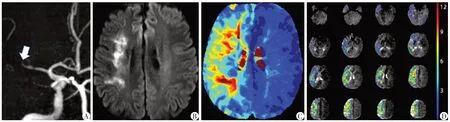
图2 复发组代表性病例Figure 2 The representative patient with recurrent acute ischemic stroke/TIA
本研究中,采用Tmax参数图对低灌注体积进行绝对定量,该参数图基于自动化灌注后处理软件可以快速获得,并且在CT、MRI模态中的可重复性高,目前被认为是最优的组织窗评价指标[19]。Takasawa等[20]曾将Tmax不同阈值与金标准PET半暗带范围进行对比,发现Tmax值在4~6 s之间可以最好地识别缺血半暗带。因此本研究中,我们探讨了这两个不同的Tmax时间阈值,结果发现复发组患者Tmax>6 s 及Tmax>4 s的低灌注体积均较初发组更高,与传统的定性指标(分水岭梗死)相比,Tmax>4 s的低灌注体积是缺血性卒中复发相关的唯一独立危险因素,低灌注体积每增加10 mL,缺血性卒中复发风险提高1.12倍。这一结果可能提示,对于下游灌注受损严重的患者,积极的内科治疗可能不能显著改善低灌注,这类患者需要积极行血管重建术,以改善脑组织灌注状态,降低卒中复发风险。
本研究存在一些不足:①本研究为单中心的回顾性研究,样本量较小,今后需要多中心、前瞻性、大样本研究来评估定量化低灌注体积对缺血性卒中复发风险的预测价值;②研究仅探讨了低灌注这一因素,后续研究需要整合斑块特征及低灌注体积,进一步提高对卒中复发风险预警的准确性。
综上所述,基于时间阈值Tmax>4 s量化的低灌注体积,是与前循环缺血性卒中复发相关的唯一独立危险因素,有望成为预警缺血性卒中复发的有效影像学标志物。
