国内常用全血白细胞滤器应用性评价研究*
2022-02-21陈显,姜健
陈 显,姜 健
(1.江苏省血液中心,江苏 南京 210042;2.无锡市中心血站,江苏 无锡 214000)
血液制剂不滤白进行临床输注可引起非溶血性发热、血小板输注无效、免疫抑制,甚至病毒感染等一系列临床输血反应。目前,国内多家采供血机构已开展了血液滤白操作,尤其是江苏省所有采供血机构已将血液滤白比例需要达到99%以上作为血站3年一度周期评审验收标准,要求除却制备手工浓缩血小板等特殊血液制剂外所有全血必须经滤白才可投入临床使用,从而进一步保证用血安全。
血液滤白有多种方法,使用全血白细胞滤器进行滤白作为最便捷的方式已广泛用于全国各大采供血机构。目前,市场上使用的全血白细胞滤器基本为第3代产品,主要是采用聚酯纤维无纺布作滤膜,并在纤维中添加了特殊的高分子聚合材料,通过拦截过滤和细胞黏附等方式,可以滤除全血中99.9%的白细胞,使过滤后残余白细胞的数值达到国标甚至欧标的效果。本研究调研了市场上常见的几种全血白细胞滤器,通过测试比较了不同滤器的滤白效果及滤器在血液制备流程中对部分血液制剂成分的影响,旨在为各家采供血机构选择合适的滤器提供数据支持。
1 资料与方法
1.1资料
1.1.1标本来源 血液样品采集在江苏省血液中心流动献血车上进行,体采科按照《GB18467-2011献血者健康检查要求》对献血者健康征询、初筛检测后进行全方位评估,完全合格者方可献血,采集后的400 mL全血需满足2019版《血站技术操作规程》和《GB18469-2012全血及成分血质量要求》,采集时间需小于13 min,全血肉眼观察无色泽异常、溶血、凝块、气泡及重度乳糜等情况。2020年3月共采集160份(血袋厂家:山东威高集团医用高分子制品股份有限公司,保存液为ACD,批号:202002)。采集后全程冷链至成分制备科完成血液交接,将全血充分混匀,使用无菌接驳设备和全自动成分血分离机将该全血均匀分为2份,每份200 mL。对其中一份(对照组)全血不经白细胞滤器直接离心分离速冻后制备成新鲜冰冻血浆(FFP),另一份(研究组)则使用目前国内常用的4种全血白细胞滤器(即A、B、C、D组,A、B组为国产硬壳滤器,C组为进口软壳滤器,D组为进口硬壳滤器)进行滤白后截取少量全血,剩余部分离心分离后速冻制备成FFP。
1.1.2仪器 SEPAMTIC-SL(Ⅲ)全自动成分血分离机(德国LMB公司),MBF-21速冻机(卢森堡多美达公司)、TSCDⅡ无菌接驳机(日本泰尔茂比司特公司)、残余白细胞计数器Adam-rWBC(韩国NanoEnTeK公司)、ACL7000血凝仪(德国贝克曼公司)、西斯美康XP-100(日本西斯美康公司)等。
1.1.3试剂 白细胞计数试剂盒(NanoEntek公司,批号3RW16303)、游离血红蛋白(Hb)测定试剂盒(北京瑞尔达生物科技有限公司,批号200409)、Ⅷ因子试剂盒(Hemosil公司,批号495571)等。
1.2方法
1.2.1残余白细胞计数 4组截取的少量全血充分混匀后使用Adam-rWBC系统进行残余白细胞计数,并同《GB18469-2012全血及成分血质量要求》中滤过后白细胞残余量进行比对,计算合格率。按照《GB18469-2012全血及成分血质量要求》白细胞残留量应≤2.5×106个/U,根据2019版《血站技术操作规程》,75%的抽检结果应落在质量控制指标范围内。
1.2.2滤器吸附量 对4种滤器滤前、滤后进行称重,计算滤器的全血吸附量。
1.2.3储存期末溶血率 将滤白后全血在6 h内分离制备成1 U去白细胞悬浮红细胞和FFP,使用西斯美康XP-100测量去白细胞悬浮红细胞中血红蛋白(Hb)含量和血细胞比容(Hct),应用血浆游离Hb测定试剂盒 (Trinder法) 检测上清液游离Hb浓度,根据公式(1- Hct)×游离Hb浓度/Hb浓度×1 000×100%计算储存期末溶血率。按照《GB18469-2012全血及成分血质量要求》储存期末溶血率小于红细胞总量的0.8%。
1.2.4FFP中Ⅷ因子含量 将待测FFP置于37 ℃水浴箱中迅速融化,使用ACL7000血凝仪检测2组全血6 h内分离制备的FFP中Ⅷ因子含量。
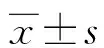
2 结 果
2.14组全血滤白后残余白细胞合格率和滤器吸附量比较 A组全血滤白后残余白细胞合格率未达到要求,与B、C、D组比较,差异均有统计学意义(P<0.05)。见表1。

表1 4组全血滤白后残余白细胞合格率和滤器吸附量比较
2.24组全血滤白后去白细胞悬浮红细胞中Hb含量、Hct、35 d储存期末溶血率比较 4组全血滤白后均达到要求。C、D组全血滤白后储存期末溶血率略优于A、B组,差异均有统计学意义(P<0.05)。见表2。
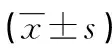
表2 4组全血滤白后去白细胞悬浮红细胞中Hb含量、Hc储存期末溶血率比较
2.34组全血滤白前后对FFP中Ⅷ因子含量的影响比较 A、B、D组全血滤白前后FFP中Ⅷ因子含量比较,差异均有统计学意义(P<0.05)。见表3。

表3 4组全血滤白后对FFP中Ⅷ因子含量的影响比较
3 讨 论
血液中含有的白细胞是人体免疫系统中重要的组成成分,不仅是导致临床非溶血性发热反应的元凶,也是经血传播病原体在血液中的主要载体,还能引起免疫抑制、同种免疫等一系列输血反应,危及受血者生命安全。另外,全血若不滤白进行储存,白细胞易崩解后产生白细胞介素、肿瘤坏死因子等一系列生物活性分子,同样也会引起临床输血过敏等反应。自20世纪60年代开始研发全血白细胞滤器,发展至今已是第3代滤器,通过拦截过滤和细胞黏附去除全血中白细胞,可去除99.9%以上的白细胞,并使残留白细胞≤2.5×106个/U,极大地提升了白细胞清除率,同时,血小板在过滤过程中也能黏附在滤膜上,从而促进白细胞的进一步黏附,进一步提升过滤效率,从而进一步保证临床用血的安全性。
本研究采用4种国内常用的全血白细胞滤器验证了其实用性。白细胞滤器关键指标是滤过后白细胞残留量符合《GB18469-2012全血及成分血质量要求》。从表1可见,A组全血滤白后残余白细胞合格率仅为60.0%,B、C、D组全血滤白后残余白细胞合格率均在97.5%。由于本中心对冷沉淀凝血因子的需求量较大,血液采集后需及时送往本中心成分制备科开展FFP制备。所以,多数血液自采集开始到成分科交接时血液的储存时间还不满3 h,血液自身温度很难达到2~6 ℃,存在热血过滤的情况较多,不同温度的血液过滤对白细胞的清除是有区别的[1-5],尤其是热血过滤,对滤器自身的质量要求较高。本研究结果显示,B、C、D组全血经热血过滤后白细胞可达到国家标准,而A组40%没有达到国标,若将A组血液温度降至2~6 ℃再进行过滤,滤白合格率可提升至80.0%。但由于全血降温所需时间较长,会影响本中心后续FFP的制备效率,建议需要制备较大量FFP的采供血机构可以选择B、C、D组可以承受热血过滤的白细胞滤器,保证滤白质量。另外,本研究结果显示,4组滤器吸附量差异不大,提示4组滤器对全血的吸附程度相当。
本研究随后针对滤白后的去白细胞悬浮红细胞进行了Hb、Hct及储存期末溶血率(35 d)检测,结果显示,4组全血滤白后去白细胞悬浮红细胞中Hb、Hct均达到国标要求。影响白细胞滤器实用性的另一个质量问题是溶血[6-8]。从本研究结果来看,4组35 d储存期末溶血率在全血滤白后均达到<0.8%的标准,但C、D组全血滤白后期末溶血率略优于A、B组,差异均有统计学意义(P<0.05)。
FFP和冷沉淀凝血因子的质量一直是关注的重点,影响Ⅷ因子的因素很多,滤器的质量也是其中之一。滤器作为外源性生物材料,主要通过物理拦截和细胞黏附等方式对白细胞进行过滤清除[9]。据文献报道,滤白同时会引起血液中部分凝血因子活性的变化,从而对后续血液制剂质量造成影响[10-13]。所以,为探讨滤器对FFP中Ⅷ因子活性有无影响,本研究对4组全血滤白前后FFP中Ⅷ因子含量进行了统计分析,结果显示,A、B、D组全血滤白后Ⅷ因子含量明显降低,差异均有统计学意义(P<0.05),而C组则无明显差异。证明了不同材质滤器确实可以影响凝血因子的变化,也同时为血站选择合适滤器从而提高成分制备产品尤其是FFP、冷沉淀凝血因子的质量提供了数据支持。
