基于蛋白质、多糖混合体系的食品凝胶结构设计策略
2021-07-29李安琪李前进郭玉蓉
李安琪,尚 静,李前进,郭 绰,杨 曦,郭玉蓉,*
(1.陕西师范大学食品工程与营养科学学院,陕西 西安 710119;2.洛川县苹果产业研发中心,陕西 延安 727400)
凝胶是指空间三维网络结构和束缚在网络内部的水分子共同够成的一大类软物质体系[1]。很多食品以凝胶的形式存在,例如果冻、果酱等,简称为凝胶食品或食品凝胶。凝胶食品口感独特、热量较低、易于吞咽,适合开发成为针对老年人等特殊人群的功能食品。多糖和蛋白质是食品中广为存在的天然高分子,是食品中主要的结构性功能物质。例如多糖具有显著的增稠、胶凝、乳化、分散等特性,在食品领域作为质构改良剂已得到广泛应用[2-7]。与多糖相比,蛋白质的增稠和胶凝能力相对不足,凝胶时通常需要更高的质量分数。然而,蛋白质具有优良的界面活性,在食品加工中可作为乳化剂、泡沫稳定剂,赋予食品体系更加独特的质构特点[8-12]。
虽然多糖和蛋白质种类繁多、结构各异、理化性质差别也较大,然而单一体系往往流变学特性也较为单一,实际应用中难以满足凝胶食品结构的精细调控。近年来,将两种或两种以上的多糖或蛋白质结合使用已成为食品凝胶结构设计的热点方向[3-4,13-20]。其中,双相混合聚合物体系是最基本、最简单的混合聚合物体系。然而,即使双相聚合物体系仅包括两种聚合物,也能产生复杂的流变学性质和凝胶结构[21-22]。简而言之,当两种聚合物存在足够强的分子间引力时,可能会形成沉淀或者发生凝胶化,这取决于两种聚合物的质量分数和分子间聚集速率。若两种聚合物不存在明显的分子间吸引作用,在低质量分数下,两种聚合物以均一相的形式存在,当质量分数升高时,聚合物分子彼此排斥,导致相分离[23]。显然,双相混合聚合物的存在状态是影响凝胶结构的主导因素。
目前,有关混合聚合物体系在凝胶食品结构设计方面的报道日益增多,且大多集中在基于双相聚合物体系的凝胶结构设计方面,有关多元混合聚合物体系的研究十分匮乏。尽管如此,双相混合体系也包括多糖混合体系、蛋白质混合体系以及多糖和蛋白质混合体系3 种情况。与前两种混合体系相比,多糖和蛋白质混合体系在食品凝胶结构设计方面更具前景。例如通过引入蛋白质和多糖的混合体系可构建多尺度、多梯度层次的复合凝胶结构[24-29]。此外,由于蛋白质本质上是天然两亲性大分子,因此引入蛋白质后,可进一步构建包含亲脂性成分的食品凝胶结构[30]。本文通过综述多糖和蛋白质双相混合体系在凝胶结构设计方面的基本理论、总结二者在凝胶结构设计中的基本原则,旨在为凝胶食品质构调控和新型凝胶食品开发提供理论依据和技术参考,同时也为促进多糖和蛋白质在食品领域的应用提供新思路。
1 多糖和蛋白质混合体系的相行为
当溶质溶于水中时会产生混合焓,一般而言,混合焓越高越易形成单相体系。通常,混合焓和溶液中溶质分子的数目密切相关,与溶液中溶质的质量分数无关。因此,与多糖或蛋白质这类大分子物质相比,小分子溶质具有很高的混合焓,有利于形成单一相溶液。当多糖和蛋白质混合时,若分子间存在较强的吸引力,例如多糖和蛋白质携带相反电荷时,两种聚合物倾向于形成单一相的凝胶结构或沉淀。若多糖和蛋白质不存在分子间吸引力时,两种聚合物分子倾向于互相排斥,这种现象称为聚合物的热力学不兼容性[31]。对于热力学不兼容的混合多糖和蛋白质体系,当总聚合物质量分数较低时,多糖和蛋白质分子彼此间距较大、排斥力较低,因此分子排斥效应不明显,容易形成均一相溶液;当总聚合物质量分数增加时,多糖分子间的间距减小,分子间斥力增大,导致多糖和蛋白质分离为两相,每一相中富含一种聚合物,形成“水包水”型乳液。此时,溶液体系中质量分数较高的一种聚合物作为连续相,质量分数较低的一种聚合物作为分散相。当继续增加聚合物质量分数时,多糖相和蛋白质相逐渐分离,最终形成层次分明的两层体系,上层富集一种聚合物,下层富集另一种聚合物,这种现象称为相分离,是不兼容混合聚合物体系中的典型情况[32]。
1.1 多糖和蛋白质分子间引力及影响因素
1.1.1 多糖和蛋白质静电引力
对于多糖和蛋白质,分子间引力主要包括静电引力、氢键、疏水相互作用等[23]。其中,静电引力是最主要的分子间引力形式[33]。当阴离子多糖和处在等电点以下的蛋白质混合时,即构成典型的聚阴离子-聚阳离子体系,此时分子间静电引力显著存在,导致多糖和蛋白质互相聚集。在静电引力的作用下,多糖和蛋白质发生电性中和,形成静电聚集体。因此,静电聚集体的形成是多糖和蛋白质电荷中和的结果[23]。若蛋白质和多糖电性中和不完全,聚集体仍然携带一定数目的电荷,此时聚集体仍然是可溶的,混合体系以均一相形式存在;若蛋白质和多糖电性中和程度较高,即静电聚集体本身携带的电荷密度很低,则其倾向于进一步聚集形成团聚物,此时混合体系形成分离的两相,一相富集团聚物,另一相富集溶剂分子(水),出现相分离。不难看出,聚集体形成和团聚是两个分离的步骤,聚集体形成不必然导致团聚。
从热力学角度而言,多糖和蛋白质聚集体或团聚物是否形成主要受热动力学驱使,本质上取决于混合体系中总吉布斯自由能变(ΔG)[34]。当体系中总吉布斯自由能变降低时(即ΔG<0),多糖和蛋白质聚集体可自发形成,反之,聚集体不能自发形成。一般地,ΔG主要由两部分组成,包括熵变(ΔS)和热焓变(ΔH),其中ΔG=ΔH-TΔS(T为体系温度)。因此,ΔG是否大于0或小于0取决于ΔS和ΔH两者间的平衡。简而言之,体系熵增大(ΔS>0)或焓减小(ΔH<0,即放热反应)均有利于多糖和蛋白质混合体系形成聚集体或团聚物。研究表明,多糖和蛋白质混合体系中,熵增(ΔS>0)主要来自于聚合物对阳离子的释放以及由于聚合物分子构象变化而导致的溶剂分子释放[34];ΔH则主要反映混合体系中总的热量变化,包括多糖和蛋白质混合过程中产生的混合热、由于聚合物稀释效应产生的热、溶剂分子重排产生的热、聚集体界面由于非共价键作用产生的结合热等。此外,需要注意的是,熵变和焓变的过程并非是独立的,两者常相互影响。例如,由于熵是评估体系混乱程度的度量(体系混乱程度越高,熵越大),因此当焓变有利于多糖和蛋白质形成聚集体时(ΔH>0),体系趋于规整、有序,此时体系的熵趋于降低。虽然影响和决定多糖和蛋白质混合体系是否发生分子聚集或团聚的因素众多,但当前较为普遍的观点是,多糖和蛋白质聚集体或团聚物形成主要取决于ΔS,其中多糖和蛋白质静电相互作用是影响聚集体形成的主要因素[23,35]。
因此,混合体系中多糖和蛋白质的电荷密度和电荷中性程度是决定两者以均一相存在还是出现相分离的关键因素[35]。由于不同类型的多糖和蛋白质分子结构各异,所以它们的电荷特性也不同。此外,外界环境因素也会导致混合体系中多糖和蛋白质电荷密度发生变化,最终改变两种聚合物的静电作用强度。理论上,所有能够引起多糖和蛋白质电荷特性发生变化的因素均能影响多糖和蛋白质的电荷中和过程及团聚现象,这些因素包括pH值、盐离子类型和质量分数、聚合物混合比例、总聚合物质量分数、温度、机械剪切等。此外,多糖和蛋白质自身的电荷密度和分子质量也对团聚现象有一定影响。
1.1.2 静电引力影响因素
通常,pH值能够改变阴离子多糖一元弱酸基团的解离程度,进而引起多糖电荷密度变化。同理,蛋白质作为两性电荷大分子,pH值变化也能改变蛋白质的电荷特性及电荷密度。因此,当多糖和蛋白质混合体系的pH值发生变化时,两者间静电作用力也会发生变化。当缓慢降低多糖和蛋白质混合体系的pH值时,可得到两个关键的pH值参数,即pHc和pHØ[23]。pHc代表体系中形成第一个多糖和蛋白质聚集体形成时所对应的pH值,pHØ代表体系发生宏观相分离时(团聚)所对应的pH值。测定pHc和pHØ的重要意义在于预测多糖和蛋白质混合体系中聚集体或团聚物的形成情况。例如,当体系pH值分别对应pHc以上、pHØ以下、pHc和pHØ之间时,体系中静电聚集体的形成显然不同。此外,对于每一个阴离子多糖和蛋白质双相混合体系,总是存在一个pH值,在此条件下多糖和蛋白质所携带电荷数目相等但属性相反,因此静电引力最强,静电聚集体形成程度也最高,该pH值定义为电荷等效pH值(electrical equivalence pH,EEP)[36]。通常,对于多糖和蛋白质的混合体系,有pHØ<EEP<pHc。
盐离子对多糖和蛋白质静电作用的影响主要在于两方面。其一,盐离子能够屏蔽多糖携带的负电荷,降低多糖电荷密度,从而减弱多糖和蛋白质之间的静电引力。其二,当盐离子质量分数升高时,聚合物释放盐离子的特性被削弱,不利于体系熵增加,因此也抑制了多糖和蛋白质静电聚集体的形成。再者,当混合多糖和蛋白质体系中盐离子质量分数提高时,溶剂介电常数发生改变,同样也不利于产生静电相互作用。与一价阳离子相比,由于二价阳离子具有更高的电荷,因此在更低的质量分数下就能抑制静电聚集体的形成。然而,混合体系稀释后,可一定程度抵消由阳离子质量分数升高引起的静电作用抑制,这是因为稀释后,阳离子质量分数降低,再次有利于静电聚集体形成[23]。
此外,多糖和蛋白质混合比例及总聚合物质量分数也是影响多糖和蛋白质静电聚集作用的重要因素。在特定的pH值和离子环境中,多糖和蛋白质电荷密度几乎恒定,因此总是存在一个最佳的混合比例,此时多糖和蛋白质电荷中性程度最高,静电聚集体和团聚物生成也最显著[37]。需要注意的是,当混合体系总聚合物质量分数增加时,虽然多糖和蛋白质静电聚集体形成数目增多,但二者静电聚集作用可能受到轻微抑制,因为聚合物质量分数较高时,分子相互接触,流动性降低,形成静电聚集体的熵优势也随之减弱,不利于静电聚集作用发生。
1.1.3 其他影响因素
除上述影响因素外,温度、机械剪切、聚合物分子结构(分子质量、关键基团)等因素也对多糖和蛋白质静电聚集作用有一定影响。就温度而言,较低的温度利于形成氢键,较高的温度利于增强疏水相互作用。根据上文所述ΔG=ΔH-TΔS,改变温度(T)显然能够改变ΔG,进而影响多糖和蛋白质混合体系中静电聚集体的形成。例如有报道称,降低温度能够轻微增加多糖和蛋白质混合体系的pHØ,表明当氢键作用增强时,需要更少的静电相互作用即可诱导体系发生宏观相分离(团聚物形成)[38]。此外,温度升高时,体系中疏水相互作用加强,当疏水作用力足够强时,可能导致静电相互作用不能发生[39]。再者,温度改变时,多糖和蛋白质的分子构象也会发生变化,从而影响两者的结合。如有研究表明,对于牛血清白蛋白和海藻酸钠的混合体系(pH 6.8、0.1 mol/L NaCl),当温度在35~70 ℃之间时,没有聚集体形成,但当温度高于70 ℃时,形成了明显的聚集体[23]。原因可能是温度升高时,牛血清白蛋白解旋,暴露了更多的疏水基团,加强了疏水相互作用,导致聚集体形成。
由于混合多糖和蛋白质时常涉及机械搅动,因此有研究表明,机械搅动也能影响多糖和蛋白质静电聚集体的形成[23]。由于机械搅动并不影响蛋白质和多糖本身的分子结构,因此施加机械剪切力时,多糖和蛋白质的静电结合几乎不受影响,但团聚物形成过程会受到较大影响[39]。通常,机械搅动速率越大,团聚物尺寸越小。但也有研究表明,适当的搅动速率能够增加团聚物尺寸,原因可能是,一方面适度的机械搅动利于多糖和蛋白质静电聚集体团聚;另一方面搅动速率不至于过高,因此不会导致团聚物碎裂[40]。
此外,多糖、蛋白质分子质量和所含官能团类型也是影响两者静电聚集作用的重要因素。一般而言,含有羧基官能团的阴离子多糖电荷密度低于含有硫酸基团或磷酸基团的阴离子多糖。因此,含有硫酸基团的多糖能够和蛋白质发生更紧密的静电聚集。同等条件下,多糖和蛋白质分子质量越高,流体力学体积也越大,更容易彼此接触发生静电聚集。
1.2 分子间排斥与相不兼容
当多糖和蛋白质双相体系中不存在分子间引力时,低质量分数下多糖和蛋白质以均一相形式存在,高质量分数下两者分离为不连续的两相,或形成“水包水”型乳液,或形成分离的两层,称为相分离或排斥相分离。相分离是混合聚合物体系中的常见现象,也是构建多重凝胶结构的主要理论基础。通常,多糖和蛋白质混合体系发生相分离的临界质量分数差异较大,主要受多糖和蛋白质分子结构特征和外部环境因素的影响。尽管影响因素较多,但它们影响相分离临界浓度的本质在于影响多糖和蛋白质分子的流体力学体积[32]。对于特定的多糖和蛋白质混合体系,当外界因素有利于降低多糖或蛋白质的流体力学体积时,相分离所对应的临界质量分数相应增加,反之,相分离临界浓度则减小。这是由于流体力学体积越大,多糖和蛋白质分子间距越小,彼此之间的排斥力也越大,越容易诱导相分离。本文以相分离前后多糖和蛋白质的混合体系为例,简单阐述两者的相行为。
1.2.1 均一相溶液中的分子间排斥
当混合体系中总的多糖和蛋白质浓度低于相分离临界浓度时,多糖和蛋白质以均一相的形式存在。尽管如此,分子间排斥作用仍然对混合体系的物理性质有显著影响。有些多糖,例如琼脂糖、结冷胶等典型的凝胶多糖,能够以无规卷曲构象和螺旋构象两种状态存在,与蛋白质混合后,在分子间排斥力的作用下,多糖分子将优先以更为紧密的螺旋构象形式存在。因此,在这类混合体系中,分子间排斥作用能够促进凝胶多糖从无规卷曲构象向螺旋构象转变,从而促进多糖凝胶化[41]。同理,分子间斥力也可能促进蛋白质的凝胶化。值得一提的是,这种情况下,混合体系仅表现出凝胶强度的轻微增加,几乎不能形成多重结构的凝胶。
1.2.2 相分离状态下的分子间排斥
当多糖和蛋白质总浓度高于相分离临界浓度时,相分离随即发生。为了更清楚地阐释多糖和蛋白质相分离的相关理论,本文引入有关多糖和蛋白质双相混合体系相分离的机制示意图[42]。
如图1A所示,曲线表示多糖和蛋白质混合体系的浊点线,当多糖和蛋白质总质量分数位于浊点线以下时,混合体系以均一相的形式存在。当多糖和蛋白质总质量分数位于浊点线以上时,相分离发生,其中一相富集多糖且蛋白质量分数较少(多糖相),另一相富集蛋白质且多糖含量较少(蛋白质相)。浊点线上的两个实心圆圈处分别表示多糖相、蛋白质相中多糖和蛋白质各自的质量分数,连接两个实心圆圈后获得一条直线(tie line),当多糖和蛋白质总质量分数位于直线上任意一点时,均会产生分离的两相,且这两相中多糖和蛋白质各自的质量分数分别和两个实心圆圈所对应的多糖和蛋白质量分数一致。然而,由于位于这条直线上的多糖和蛋白质总质量分数不同,因此相分离后多糖相和蛋白质相的相对体积也不同[32]。
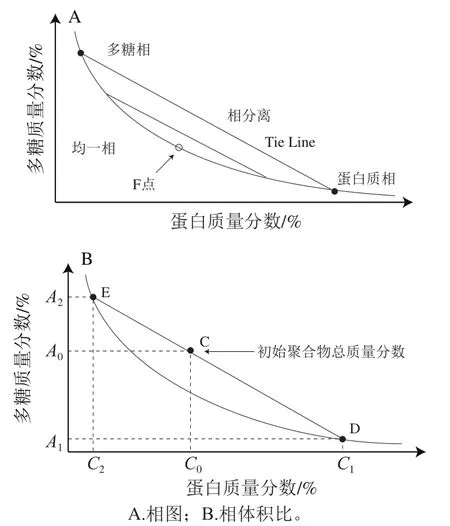
图1 多糖和蛋白质双相混合体系相分离机制示意图[42]Fig. 1 Schematic diagram of phase separation of mixed polysaccharide and protein systems[42]
如图1B所示,如果将蛋白质相的体积分数记为φ1,且蛋白质相中多糖质量分数记为A1,蛋白质量分数记为C1;同时,将多糖相的体积分数记为φ2,且多糖相中多糖质量分数记为A2,蛋白质量分数记为C2,则混合体系中多糖和蛋白质各自的总质量分数分别如式(1)、(2)所示。

式中:A0和C0分别是混合体系中多糖和蛋白质各自的总质量分数。
对于整个混合体系,有φ1+φ2=1,因此,式(1)和式(2)可以进一步改写成式(3)、(4)。
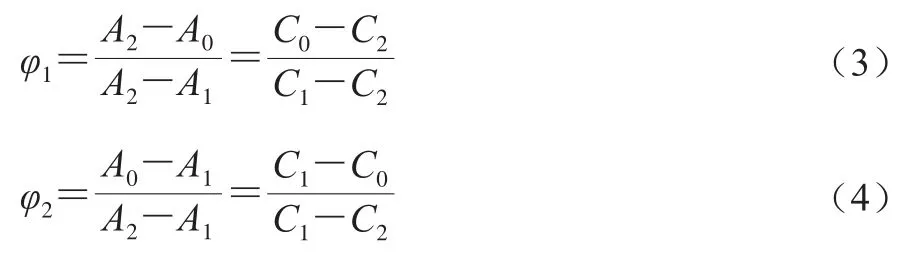
则φ1和φ2之比如式(5)所示。

由图1B可知,当混合体系中多糖和蛋白质总质量分数位于直线上(tie line)不同位置时,它们总质量分数之和是不同的,但产生相分离后,多糖相和蛋白质相中多糖和蛋白质的质量分数均不变,即A1、A2和C1、C2不变,只有A0和C0变化。因此,φ1和φ2之比也随之改变。
1.2.3 相逆转
当多糖和蛋白质总质量分数位于相分离临界浓度以上时,混合体系将产生相分离,导致3 种情况:1)形成“水包水”型乳液。此时,混合体系中体积分数较小的一相作为分散相,体积分数较大的一相则作为连续相。2)当连续相中的聚合物质量分数增加时,“水包水”型乳液破乳,导致混合体系分离为两层,一层富含多糖,另一层富含蛋白质。通常,由于蛋白质的流体力学体积总体上低于多糖,因此,富含蛋白质的一相常处在下层,而富含多糖的一相常位于上层。3)当连续相质量分数继续增加时,可诱导最初的连续相转变为分散相,而开始时的分散相转变为连续相,称为相逆转[43]。相分离的3 种存在状态是调控多糖和蛋白质双相混合物凝胶结构的重要途径。
2 双相凝胶微观结构调控原则
上文简要概括了多糖和蛋白质双相混合体系相行为的基本概念和理论,本节将阐述多糖和蛋白质混合体系相行为和双相凝胶微观结构的内在关联。
2.1 单一相混合体系的凝胶化
当多糖和蛋白质以均一相形式存在时,不产生明显的相分离。这种情况下,混合体系发生凝胶化的前提是多糖和蛋白质至少其中之一具有胶凝能力。该情况又分为两种类型:1)多糖和蛋白质存在分子间引力时,会形成可溶的静电聚集体,随后在改变外界环境因素的作用下诱导静电聚集体发生凝胶化,从而产生凝胶[44];2)多糖和蛋白质不存在分子间静电引力时,在分子排斥效应的作用下,凝胶性聚合物的分子构象以更紧密的形式存在,因此促进了该聚合物的凝胶化。这一情况和1.2.1节中描述的情况相同。
2.2 相分离状态下混合体系的凝胶化
当多糖和蛋白质混合体系形成“水包水”型乳液后,通过诱导连续相发生凝胶化,而分散相不发生凝胶化,可得到乳液凝胶。其中,分散相以液相的形式存在,作为“乳滴”分散于凝胶化的连续相中。此时,分散相的强度远低于连续相的凝胶强度,因此分散相的存在削弱了整个凝胶体系的强度。当施加一定剪切应力时,分散相更容易发生形变,因此连续相和分散相表现出同等的应变程度,称之为“等应变”条件[42]。此时,整个体系的模量可由式(6)表示。

式中:G是整个混合体系的模量;G1和G2分别是连续相和分散相的模量;φ1和φ2分别是连续相和分散相的体积分数。
相反,通过诱导分散相发生凝胶化,而连续相不发生凝胶化则会产生分散于液体连续相中的凝胶小珠。此外,还有一种情况是分散相和连续相均发生凝胶化,此时若分散相凝胶强度低于连续相凝胶强度,整个体系仍然表现出“等应变”条件下的模量变化规律。然而,当连续相凝胶强度低于分散相时,分散相的存在能够加强整个凝胶体系的强度,当施加一定应力时,分散相表现出比连续相凝胶更低的形变,此时整个凝胶体系表现出“等应力”条件下的特性,即整个体系的柔量(J=1/G)关系如式(7)。

对式(7)进行转换,得到式(8)。

显然,只需要得到混合体系中分散相和连续相各自的模量,就可以通过公式(7)、(8)预测双相凝胶体系整体的模量。此外,值得一提的是,当混合多糖和蛋白质体系处在特定的质量分数范围内时,两者均以连续相的方式存在,在这种情况下,混合体系的凝胶强度将位于“等应变条件”条件和“等应力条件”之间,具体是表现出更倾向于“等应变条件”还是更倾向于“等应力条件”,则取决于两种聚合物的相对相体积[26,43]。
2.3 其他考虑因素
对于多糖和蛋白质混合体系形成双相凝胶的相关理论,在实际构建双相凝胶时仍然会存在一些问题。首先,本文所讨论的多糖和蛋白质混合体系的相行为是在假设混合体系所处外界环境不变的情况下推导得出的。然而,实际制备凝胶时,外界环境因素总会发生变化,可能导致多糖和蛋白质分子间作用力变化,进而影响混合体系的相行为。例如,当添加阳离子诱导多糖或蛋白质形成凝胶时,多糖或蛋白质发生凝胶化,促成它们与另一种聚合物的不兼容性,可能导致临界相分离浓度质量分数降低。其次,实际制备凝胶时,选用的多糖和蛋白质可能均具有胶凝能力,因此当诱导混合体系形成凝胶时,相分离和凝胶化可能同时发生。这种情况下,最终的凝胶结构主要取决于凝胶化发生时混合体系的相行为。最后,当两种聚合物具有不同的凝胶速率且凝胶速率差异较大时,凝胶速率较快的聚合物发生凝胶化时几乎不受另一种聚合物的影响,但另一种聚合物凝胶时受第一种聚合物的影响较大。因此,实际制备凝胶时,常改变两种聚合物的凝胶化次序以获得不同的凝胶结构和凝胶特性[45]。
尽管混合凝胶的发展还处在起步阶段,但这样的凝胶结构在食品领域具有较好的应用前景。例如,当不兼容的两种聚合物形成“水包水”型乳液时,通过诱导连续相形成凝胶同时使分散相保持溶液状态,可以得到充满囊泡的凝胶体系;在非凝胶化的分散相中添加风味物质,可以制备得到新型凝胶食品;再者,由于水胶体溶液具有比凝胶更好的风味释放特性,因此当制备这种类型的凝胶食品时,可以减少风味物质和食盐的添加量,利于减少人体对食盐的摄入。
3 乳清蛋白和食品多糖双相混合体系在凝胶结构设计中的应用
当前,很多类型的多糖和蛋白质都在食品工业中得到应用,但就双相凝胶设计而言,仅有一小部分蛋白质被报道,包括乳清蛋白[43,46]、明胶[47-48]、酪蛋白[49-50]、大豆分离蛋白[51-52]、其他植物或动物蛋白[53-55]等。其中,乳清蛋白由于具有优良的胶凝能力,因此是研究多糖和蛋白质混合凝胶的理想蛋白。乳清蛋白是从牛奶中提取获得的一种优质蛋白质资源,具有易消化吸收、含有多种活性成分等特点,而且是公认的高营养价值蛋白质[56]。乳清蛋白可在加热、阳离子或酸性诱导的条件下发生凝胶化,因此是一类具有胶凝能力的食品蛋白质。近年来,乳清蛋白已作为一种模型蛋白质和各类食品多糖混合,用以构建不同结构特点的双相凝胶。因此,本文以乳清蛋白和食品多糖的混合体系为例,列举多糖和蛋白质双相混合体系在设计凝胶结构中的应用实例。表1中整理了有关乳清蛋白和多糖混合体系在构建双相凝胶结构方面的主要研究,并总结了不同凝胶构建参数对双相凝胶微观结构的影响。

表1 基于乳清蛋白和食品多糖混合体系的双相凝胶形成条件及凝胶特性Table 1 Fabrication conditions and gel properties of binary gels based on whey protein isolate and food polysaccharides
由表1可知,乳清蛋白分散于水溶液后在高温下加热,蛋白质发生解折叠,形成乳清蛋白聚集体溶液,进一步和多糖溶液混合后,即可得到双相混合体系。随后,可采用两种策略诱导混合体系发生凝胶化:1)再次加热混合体系,诱导乳清蛋白聚集体发生热凝胶化,之后冷却混合体系,获得双相凝胶;2)在混合体系中添加酸化剂或阳离子,诱导乳清蛋白聚集体凝胶化。依赖于多糖的物理性质和凝胶形成条件,最终获得的双相凝胶也表现出各异的结构特点和物理特性。需要注意的是,尽管近年来有很多关于乳清蛋白和多糖混合体系在双相凝胶结构设计中的实例,但该混合体系在凝胶结构设计方面的研究仍然处在初步阶段,需要进一步完善。例如,Berg等[43]虽然研究了刺槐豆胶、高甲氧基果胶、结冷胶和乳清蛋白混合体系的凝胶化作用,并观察到这3 种多糖对乳清蛋白凝胶结构的调控作用,但由于该研究中所使用的多糖质量浓度较低,不足以发生多糖凝胶化;因此该研究并未涉及多糖凝胶化对乳清蛋白凝胶结构的影响。此外,有研究表明,乳清蛋白和淀粉的混合体系可产生不同于乳清蛋白和其他多糖混合体系的凝胶结构,原因在于淀粉具有糊化作用,高温下淀粉颗粒能够吸水膨胀,从而和乳清蛋白凝胶网络发生物理挤压[46]。Lavoisier等[46]研究了马铃薯淀粉和乳清蛋白混合体系的凝胶化作用,发现低质量浓度的淀粉能削弱混合凝胶的结构强度,但高质量浓度的淀粉显著增强了凝胶结构,原因可能是高质量浓度的淀粉糊化后,自身也形成了网络结构,和原有的乳清蛋白网络互相穿插,增加了整个凝胶网络的密度。
4 结 语
多糖和蛋白质的双相混合体系可表现出各异的相行为,最终影响混合凝胶的微观结构和物理性质。通过制备合适的多糖和蛋白质混合体系,并优化凝胶形成条件,可获得物理性质更为优良、凝胶结构更加独特的混合凝胶。此外,多糖和蛋白质混合凝胶不仅具有独特的结构特性,也具有蛋白质的营养功能,对于功能性凝胶食品设计意义重大。然而,当前有关多糖和蛋白质混合凝胶的研究还处在初步阶段,相关报道仍然较少。鉴于此,本文重点综述了多糖和蛋白质双相混合体系的相行为,总结了双相凝胶设计的基本原则,以期为国内凝胶食品的设计和开发提供理论参考。
