新型神经氨酸酶抑制剂的设计合成及抗流感病毒活性
2020-10-16尤义鹏刘晋彪丰亚辉
尤义鹏,聂 林,刘晋彪,丰亚辉,鲁 桂
(中山大学药学院,广州 510006)
流感严重威胁人类健康,目前主要通过流感疫苗和药物对流感进行预防和治疗.流感病毒亚型较多,容易发生变异,疫苗的开发与生产需要时间较长.因此,防治流感的药物的研究、开发受到全球范围的高度重视.神经氨酸酶是流感病毒的重要糖蛋白,在流感病毒复制和传播中发挥着重要作用,也是设计抗流感病毒药物的重要靶点[1,2].目前,已有4个神经氨酸酶抑制剂药物上市,分别是葛兰素史克公司的扎那米韦(Zanamivir)[3,4]、罗氏公司的奥司他韦(Oseltamivir)[5,6]、日本的帕拉米 韦(Peramivir)[7,8]和拉尼米韦(Laninamivir).这些药物通过模拟唾液酸在神经氨酸酶中的氧鎓离子中间体设计并经结构修饰得到,尽管母环结构有所不同,但均含有羧基、乙酰氨基、氨基或胍基、脂肪侧链等官能团,均以相似的方式与神经氨酸酶结合.Scheme 1示出了上述4种药物及扎那米韦前体药4-氨基-2,4-脱氧-2,3-脱氢-N-乙酰基神经氨酸(4-氨基DANA)的结构.
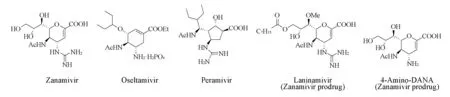
Scheme 1 Structures of known neuraminidase inhibitors
神经氨酸酶的活性中心可以分成5个区域,其中S2,S4和S5区域存在一个较大的疏水口袋[9].Fang等[10,11]发现,将扎那米韦和奥司他韦的羧基换成磷酸类基团可获得活性更优的化合物,且化合物的口服利用度得到显著提高.
本文对上市药物扎那米韦、奥司他韦和帕拉米韦进行了结构修饰,将化合物相应的氨基进行磷酰化,设计合成了新衍生物I-1~I-10(Scheme 2).研究了其合成方法,并在激酶水平与细胞水平考察了新化合物的抗病毒活性.
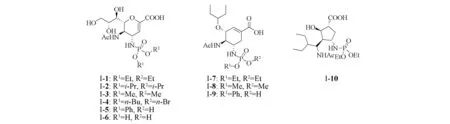
Scheme 2 Structures of designed new phosphorylated derivatives
1 实验部分
1.1 试剂与仪器
唾液酸(纯度98%)、氯化亚砜(SOCl2,纯度99.5%)、碳酸氢钠(NaHCO3,纯度99.8%)、亚磷酸二乙酯(纯度99%)、亚磷酸二异丙酯(纯度98%)和亚磷酸二苯酯(纯度80%)购于上海阿拉丁生化科技股份有限公司;4-二甲氨基吡啶(DMAP,纯度99%)购于Alfa Aesar公司;叠氮磷酸二苯酯(DPPA,纯度97%)和亚磷酸二丁酯(纯度96%)购于Sigma Aldrich公司;1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU,纯度98%)购于北京百灵威科技有限公司;奥司他韦(纯度97%)购于上海毕得医药科技有限公司;硫酸(质量分数98%)购于广州泽元贸易有限公司.所用溶剂均为分析纯,试剂除特殊说明外均未经纯化直接使用,溶剂按常规方法处理纯化.硅胶(200~300目),青岛海洋化工公司;C18硅胶,北京慧德易科技有限责任公司;HSGF254型薄层层析(TLC)硅胶板,烟台江友硅胶开发有限公司;用紫外灯、碘缸、高锰酸钾显色剂和2,4-二硝基苯肼(DNP)显色剂等检测.
Bruker Avance 400型核磁共振波谱(NMR)仪,德国Bruker公司,除特殊说明外,以四甲基硅烷(TMS)为内标;岛津LCMS-IT-TOF型离子阱飞行时间质谱仪,日本岛津公司;Agilent 6120型液相色谱-质谱联用(LC-MS)仪,美国Agilent公司;Perkin Elmer 341型自动旋光仪,美国Perkin Elmer公司.
1.2 实验过程
扎那米韦前体A及其C4位氨基磷酰化化合物I-1~I-6、奥司他韦C5位氨基磷酰化化合物I-7~I-9和帕拉米韦前体C4位氨基磷酰化化合物I-10的合成路线见Scheme 3~Scheme 6.
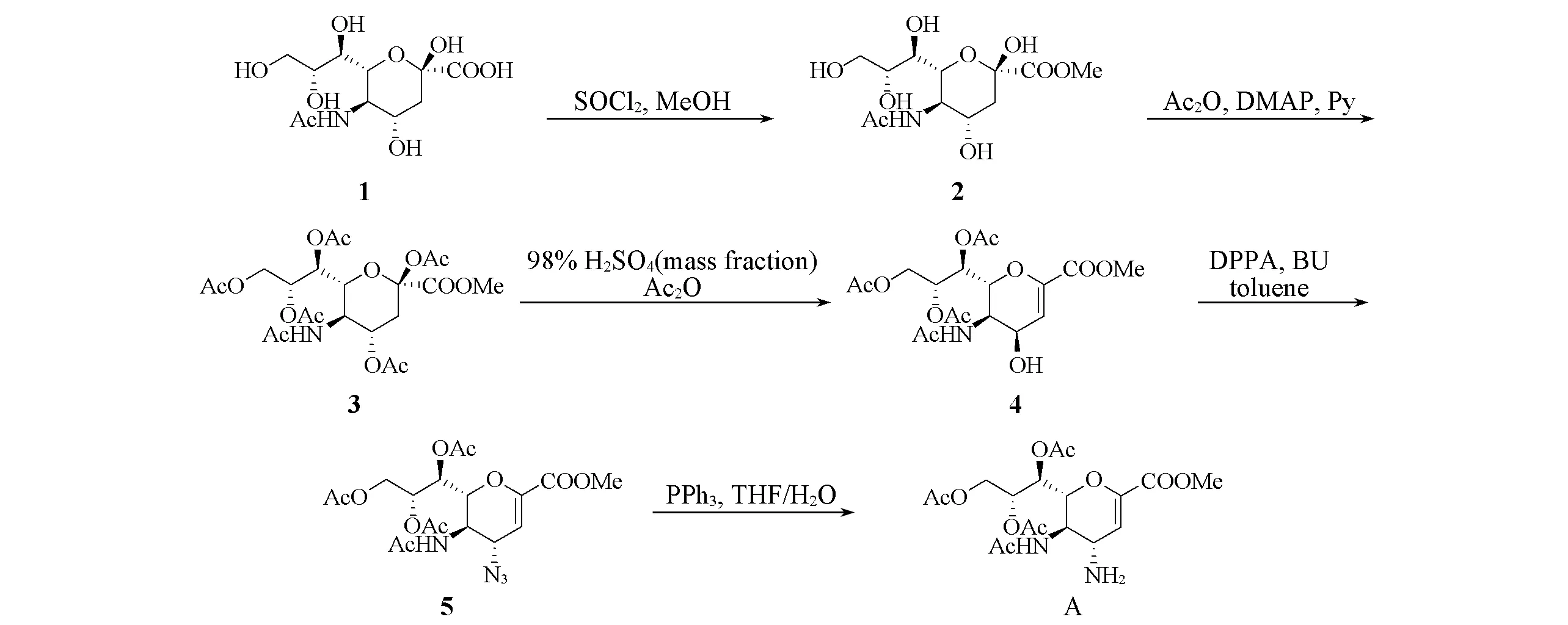
Scheme 3 Synthetic route of Zanamivir precursor A
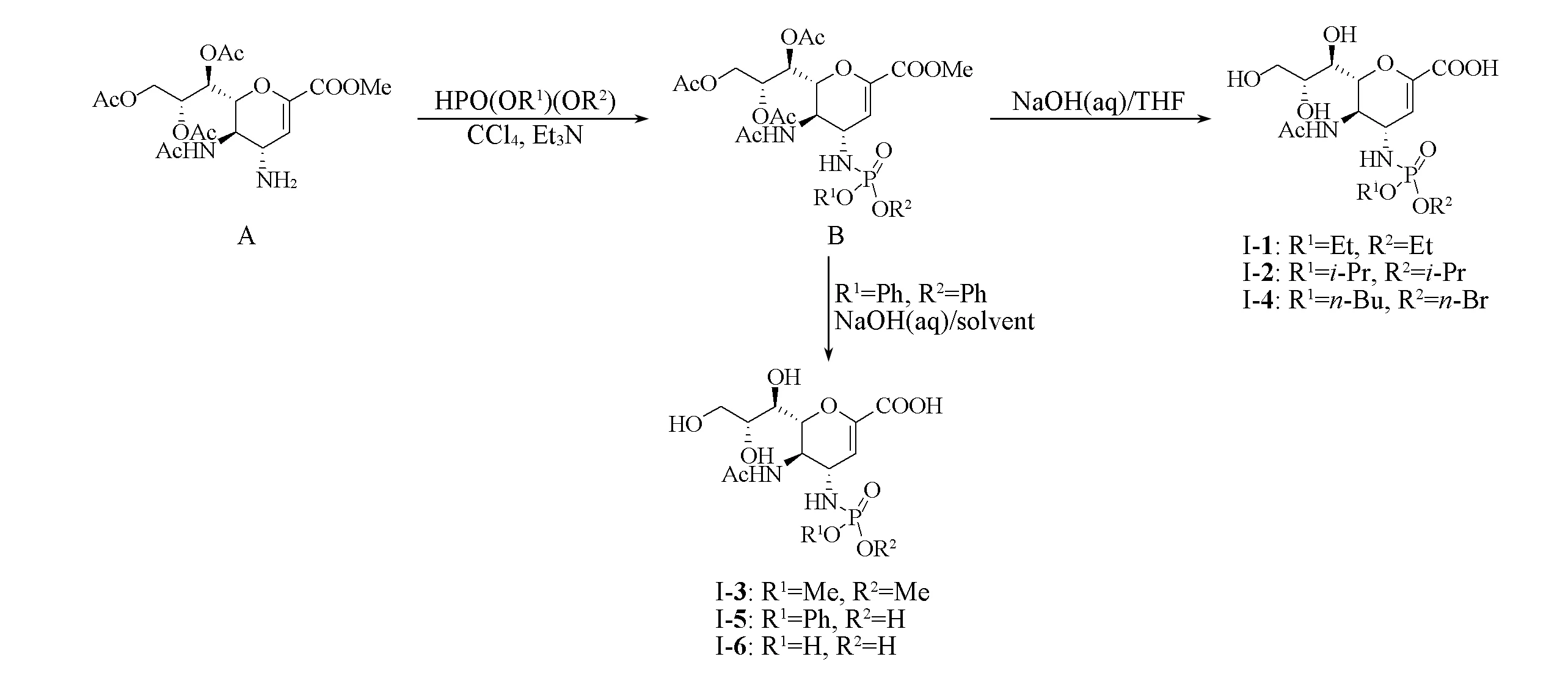
Scheme 4 Synthetic routes of compounds I-1—I-6

Scheme 5 Synthetic routes of compounds I-7—I-9
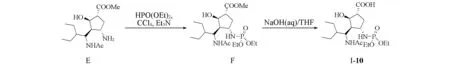
Scheme 6 Synthetic route of compound I-10
1.2.1 扎那米韦前体A的合成 参照文献[12~16]方法合成扎那米韦前体A.将3.85 g(16.2 mmol)唾液酸1加入60 mL MeOH中,0℃下缓慢滴加2.4 mL(32.4 mmol)SOCl2,室温下搅拌反应24 h;在冰浴条件下,向反应体系中加入6.0 g NaHCO3粉末,搅拌至无气泡产生,析出大量白色沉淀;抽滤、洗涤滤饼,旋转蒸干滤液得到白色固体化合物2粗产物8.5 g(产率99%).将化合物2溶解在20 g(20 mL)吡啶中,加入0.14 g(1.1 mmol)DMAP,0℃下缓慢滴加11.6 g(10.6 mL)Ac2O,室温下搅拌反应24 h;依次使用1 mol/L HCl、饱和碳酸氢钠和饱和氯化钠溶液洗涤,合并有机相,脱除溶剂后得7.2 g化合物3粗产物.将450 mmol(45 mL)化合物3溶解在Ac2O中,0℃下逐滴加入5.95 g(60.75 mmol)质量分数为98%的H2SO4,滴加完毕于室温下搅拌反应24 h;然后加入饱和碳酸氢钠溶液调节pH=8,用EA萃取,合并有机相,脱除溶剂柱层析,分离得到4.1 g化合物4,产率60%.将1.5 g(3.48 mmol)化合物4放入烧瓶中,充入氮气保护,加入30 mL无水甲苯和1.0 mL(4.64 mmol)DPPA,加热使其完全溶解,0℃冰浴下逐滴加入0.69 mL(4.64 mmol)DBU,于室温搅拌反应24 h;旋转蒸发反应液,经柱层析分离得到1.45 g化合物5,产率91%. 将1.45 g(3.18 mmol)化合物5加入80 mL THF和3.7 g(206.5 mmol)H2O的混合溶液中,加入2.1 g(7.94 mmol)PPh3,在氮气保护下于室温反应24 h;反应完成后,用CH2Cl2萃取,合并有机相,脱除溶剂后柱层析分离得到1.24 g扎那米韦前体A,产率91%.
1.2.2 扎那米韦衍生物的合成 参照文献[17~19]方法合成扎那米韦衍生物.在0℃下,将138 mg(1 mmol)亚磷酸二乙酯溶于3 mL四氯化碳中,10 min后慢慢加入1 mL三乙胺和100 mg(0.2 mmol)扎那米韦前体A的混合物,于0℃反应1 h;待反应完全后,经柱层析分离得到中间体B,产率88%.将中间体B溶于1 mL 1 mol/L NaOH和1 mL THF的混合溶液中,常温下搅拌12 h;反应完全后,加入阳离子交换树脂调节溶液pH值至弱酸性,过滤除去树脂,旋干滤液得化合物I-1.化合物I-2和I-4的合成分别以亚磷酸二异丙酯和亚磷酸二正丁酯为原料,操作步骤同化合物I-1的合成.以亚磷酸二苯酯为原料得到中间体B,再通过不同的反应体系(NaOH/MeOH或NaOH/THF),水解得到相应的化合物I-3,I-5和I-6.
1.2.3 奥司他韦衍生物的合成 在0℃下,将亚磷酸二乙酯溶于四氯化碳中,缓慢加入三乙胺和奥司他韦的混合物,于0℃反应1 h;待反应完全后,旋转蒸发反应液,经柱层析分离得到相应中间体D,产率56%.将中间体D溶于1 mol/L NaOH和THF的混合溶液中,常温下搅拌12 h;反应完全后,加入阳离子交换树脂调节溶液pH值至弱酸性,过滤除去树脂,柱层析分离得化合物I-7.以亚磷酸二苯酯为原料得到中间体D,再通过不同的反应体系(NaOH/MeOH或NaOH/THF)水解,得到相应的化合物I-8和I-9.
1.2.4 帕拉米韦衍生物的合成 参照[20,21]文献方法制备帕拉米韦前体E.将亚磷酸二乙酯溶于四氯化碳中,缓慢加入三乙胺和帕拉米韦前体E的混合物,于0℃反应1 h;待反应完全后,旋转蒸发反应液,经柱层析分离得到F,产率56%.将化合物F溶于1 mol/L NaOH和THF的混合溶液中,常温下搅拌12 h;反应完全后,加入阳离子交换树脂调节溶液pH值至弱酸性,过滤除去树脂,经柱层析分离得到目标化合物I-10.
化合物I-1~I-10的理化性质数据列于表1,核磁共振波谱数据列于表2.
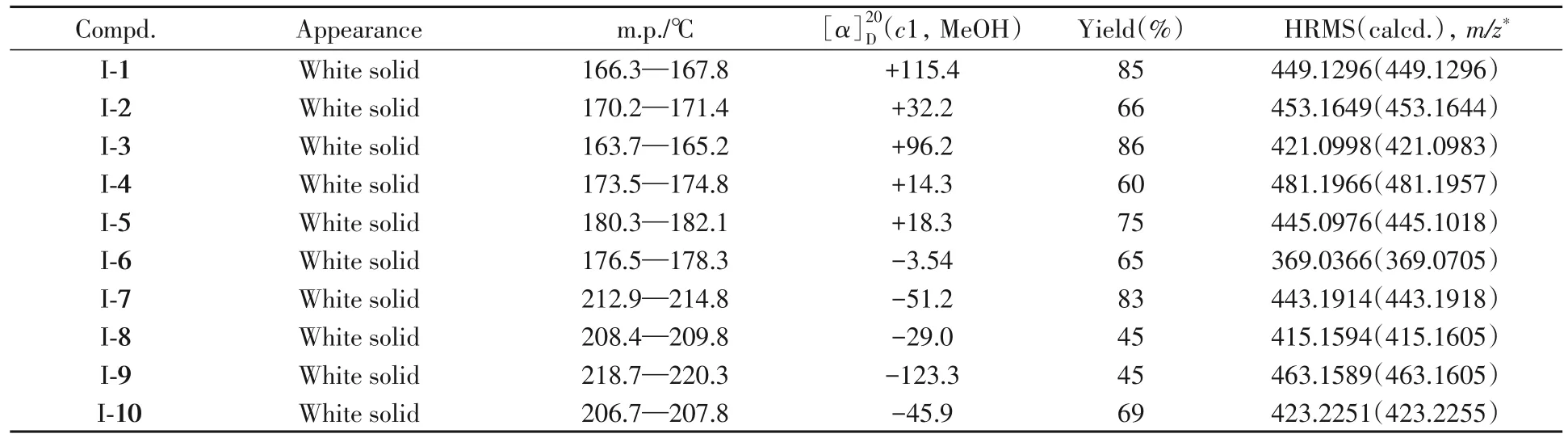
Table 1 Appearance,yields and HRMS data of compounds I-1—I-10

Table 2 11H NMR,13C NMR and31P NMR data of compounds I-1—I-10*
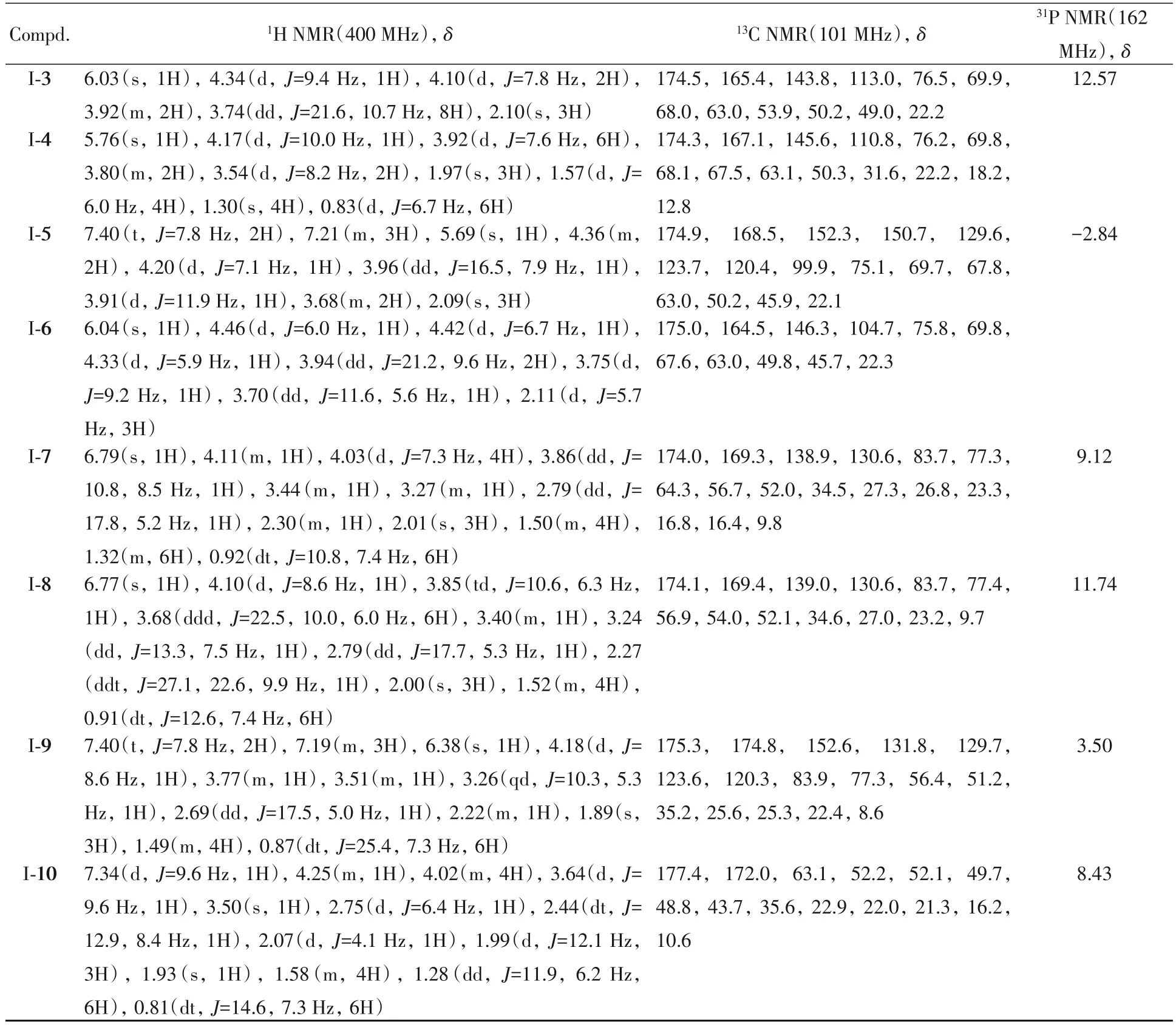
Continued
1.2.5 化合物与神经氨酸酶复合物的结合自由能预测 采用分子动力学模拟软件AMBER9,参照文献[22~24]方法对化合物与神经氨酸酶复合物的结合自由能进行了预测.
1.2.6 化合物对神经氨酸酶的抑制活性实验 参照文献[25,26]方法进行化合物的神经氨酸酶抑制活性实验.
1.2.7 化合物的抗病毒活性测试 以甲型流感病毒A/HK/8/68(H3N2)和A/WSN/33(H1N1)为病毒毒株,参照文献[27,28]方法进行化合物的抗病毒活性测试.
2 结果与讨论
2.1 目标化合物的合成
基于文献[29~33]报道,优化了扎那米韦前体A的合成路线[12~16](Scheme 3). 从唾液酸1出发,在氯化氢的甲醇溶液中进行酯化得到化合物2,该反应操作方便,容易控制;化合物2经DMAP催化与醋酸酐反应得到乙酰化产物3;化合物3被浓硫酸氧化成化合物4,该步反应选用普通经济的浓硫酸,反应条件温和,与文献[32]报道的三氟甲磺酸三甲基硅酯(TMSOTf)关环反应法相比有很大改进;化合物4经DPPA叠氮化得到化合物5,该步反应条件温和,比文献[29~31]报道的叠氮化钠法更适合大规模生产;化合物5经过三苯基膦还原得到关键中间体A,此步反应条件温和,不需要使用铂碳或钯碳等贵金属催化剂,也不会导致环内双键的还原.整条反应路线步骤简单、条件温和、操作方便且经济环保.
在低温下将相应的亚磷酸酯溶于四氯化碳,搅拌后缓慢加入三乙胺和扎那米韦前体A,反应完全得到磷酰化中间体B,随后在碱性条件下水解分别合成了扎那米韦前体C4位磷酰化衍生物I-1~I-6(Scheme 4).
从奥司他韦C出发,将其与相应的亚磷酸酯反应,得到磷酰化中间体D,随后在碱性条件下水解分别合成了奥司他韦C5位磷酰化衍生物I-7~I-9(Scheme 5).
参照[20,21]文献方法制备帕拉米韦前体E,再将前体E与相应的亚磷酸酯反应,得到磷酰化中间体F,最后在碱性条件下水解得到帕拉米韦前体C4位磷酰化衍生物I-10(Scheme 6).
2.2 化合物与神经氨酸酶复合物的结合自由能预测
采用分子动力学模拟软件AMBER9对部分新化合物进行了活性预测[22~24].结果显示,新化合物I-1,I-6和I-7与神经氨酸酶的结合自由能分别为−100.05,−143.87和−105.65 kJ/mol,均小于奥司他韦与神经氨酸酶的结合自由能(−93.01 kJ/mol),表明抗病毒活性可能会优于奥司他韦.
2.3 目标化合物对神经氨酸酶的抑制活性
分别选择野生型H1N1神经氨酸酶(sH1N1 Neuraminidase,R&D Systems)和突变型H1N1神经氨酸酶(rH1N1 Neuraminidase,R&D Systems),以(4-甲基伞形酮)-N-乙酰基-α-D-神经氨酸钠盐(MUNANA)为底物,奥司他韦为阳性对照,采用荧光法测定了化合物对神经氨酸酶(NA)的抑制活性,结果列于表3.可见,所有化合物均具有一定的抑制活性,其中化合物I-8对野生型神经氨酸酶(NAs),化合物I-5对突变型神经氨酸酶(NAr)分别显示出很好的抑制活性,与阳性药奥司他韦相当,也优于扎那米韦C4位氨基未经修饰的前体药4-氨基-DANA(Scheme 1).
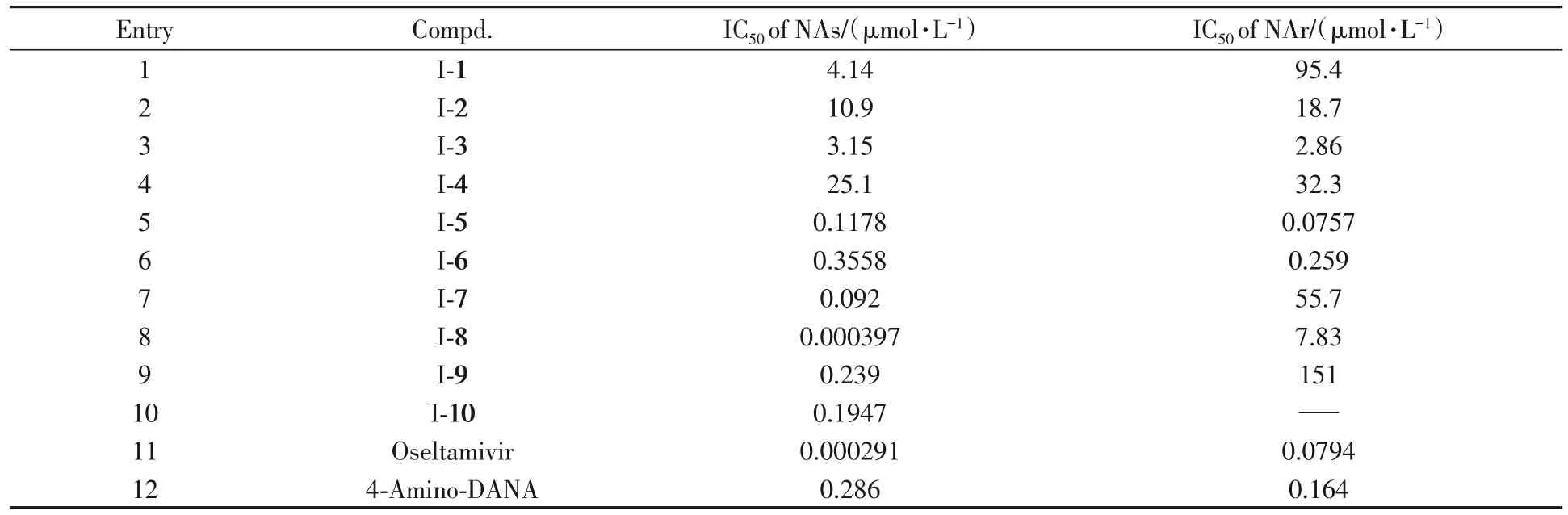
Table 3 Inhibition activities against NAs and NAr enzymes
由表3可见,新化合物对野生型NAs的抑制活性优于对突变型NAr的抑制.从化合物I-1到化合物I-4,随着亚磷酸酯基团的增大,抑制活性逐渐下降,说明亚磷酸酯附近的位阻会影响抑制作用;化合物I-6对NA的抑制活性不如化合物I-5,可能原因是化合物I-5的苯环有一定的疏水性,可以和NA的S2区域的疏水口袋结合,从而增强了活性.另外,NA的S2区域是由酸性氨基酸组成的负电荷区域,化合物I-6的亚磷酸基团显酸性,不利于与NA的结合.综上,3类不同骨架的磷酰化衍生物I-1~I-6,I-7~I-9及I-10对野生型NAs均有较好的抑制作用.
2.4 目标化合物的抗流感病毒活性
选取部分新化合物进行了抗流感病毒实验.以犬肾上皮细胞(MDCK)为病毒宿主,奥司他韦为阳性对照药,测定样品抑制病毒引起细胞病变程度(CPE),结果列于表4.可见,新化合物对流感病毒均具有一定的抑制作用,化合物I-5,I-6,I-9和I-10显示出更强的抑制活性.新化合物对甲型流感病毒A/HK/8/68(NA亚型为H3N2,病毒对NA和M2离子通道均敏感)的体外抑制活性优于对甲型流感病毒A/WSN/33(NA亚型为H1N1,病毒对NA敏感,对M2离子通道耐受),说明化合物对H3N2型流感病毒有更好的选择性,且对M2离子通道敏感型流感病毒的抑制效果更好.化合物I-6对流感病毒A/HK/8/68的IC50值为0.121 μmol/L,与阳性对照药奥司他韦相当,优于扎那米韦前体药4-氨基-DANA.
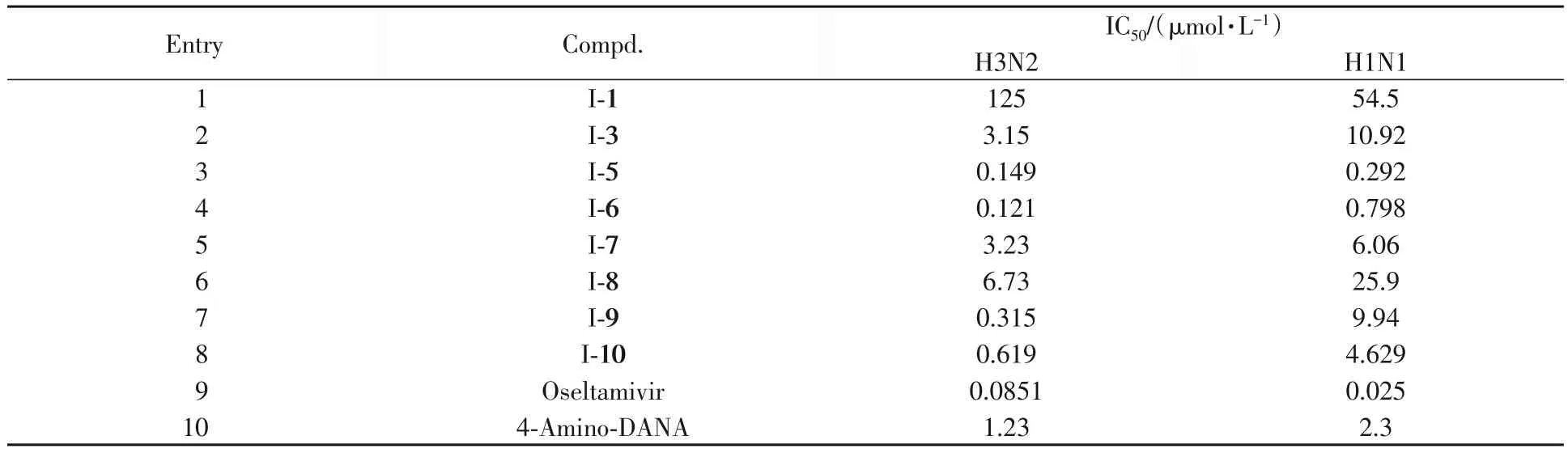
Table 4 In vitro anti-influenza virus activities in MDCK cells using the CPE protection assay
3 结 论
基于现有的流感病毒神经氨酸酶抑制剂,结合亚磷酸基团的抗流感活性,分别对扎那米韦C4位、奥司他韦C5位及帕拉米韦C4位氨基进行磷酰化,设计合成了10个新衍生物.初步生物活性测试结果表明,新化合物I-1~I-10对流感病毒神经氨酸酶均有一定的抑制活性,在细胞水平的测试中也表现出一定的病毒抑制活性,尤其是化合物I-8在酶水平、化合物I-6在细胞水平具有和阳性对照药奥司他韦相当的活性.