肺腺癌组织中抑微管装配蛋白1和葡萄糖调节蛋白78的表达情况及与患者临床特征的关系
2020-09-15胡星明陈跃军王子尧方理周彬吴安邦肖高明
胡星明,陈跃军,王子尧,方理,周彬,吴安邦,肖高明
湖南省肿瘤医院/中南大学湘雅医学院附属肿瘤医院胸外科,长沙 410005
肺腺癌是一种非小细胞肺癌,非小细胞肺癌约占全部肺癌的80%,其中约50%是肺腺癌[1]。肺腺癌是女性亚洲人和45岁以下人群中最常见的肺癌类型,而且更可能发生于非吸烟者,遗传、被动吸烟等也可能是病因。有报道显示,肺腺癌发生的分子改变包括ALK[2-3]、ROS1[4-5]、RET[6-8]基因重排以及EGFR、HER2、KRAS、ALK、BRAF、PIK3CA、MET基因突变。由于肿瘤信号通路较为复杂,因此仍有大量的研究工作需要进行。有研究报道,抑微管装配蛋白 1(stathmin 1,STMN1)是细胞质磷酸化蛋白,可以调节微管动力学,与肿瘤发生发展和微管结合抗癌药物的耐药性有关[9]。不同的细胞外信号能够导致不同的磷酸化类型,如乳腺癌中STMN1 Ser25和Ser38磷酸化是维持细胞运动所必须的,与患者的无瘤生存期较短有关。葡萄糖调节蛋白 78(glucose-regulated protein 78,GRP78)是一种新型Ser25/Ser38磷酸化STMN1结合蛋白,这种依赖磷酸化的相互作用受甲乙酮(methyl ethyl ketone,MEK)激酶调节和STMN1-GRP78复合物稳定性及STMN1介导的迁移所影响。磷酸化STMN1和GRP78也被认为可评估乳腺癌的转移风险。有报道显示,STMN1高表达与食管鳞状细胞癌、肺腺癌、子宫内膜癌的预后差有关,而GRP78也与一些药物作用有关[10]。本研究分析了肺腺癌组织中STMN1和GRP78的表达情况及与患者临床特征的关系,现报道如下。
1 资料与方法
1.1 一般资料
选择2015年1月1日至2015年12月31日于湖南省肿瘤医院胸外科接受手术治疗的肺腺癌患者。纳入标准:术前均未接受过化疗、放疗等治疗;术前经支气管窥镜或肿块穿刺标本病理检查确诊为肺腺癌。排除标准:合并其他类型肺癌;合并其他器官恶性肿瘤;肿瘤已转移。依据纳入和排除标准,本研究共纳入51例肺腺癌患者,其中,男37例,女14例;年龄为44~72岁,中位年龄为59岁。收集肺腺癌患者的肺腺癌组织51例。同时选取27例正常肺组织作为对照,包括肺良性病变组织18例和癌旁正常肺组织9例。其中,男20例,女7例;年龄为43~71岁,中位年龄为58岁。51例肺腺癌组织与27例正常肺组织对应患者的性别、年龄比较,差异均无统计学意义(P>0.05),具有可比性。
1.2 主要试剂
GRP78 BiP抗体和STMN1抗体均购自美国Abcam公司,工作液浓度均为1∶100。磷酸盐缓冲液(phosphate buffered saline,PBS)、二氨基联苯胺(diaminobenzidine,DAB)染色试剂盒及相应二抗均购自武汉博士德生物工程有限公司。
1.3 免疫组织化学染色方法
石蜡切片常规脱蜡脱水,3%过氧化氢孵育20min,PBS冲洗后,置于0.01 mol/L枸橼酸盐缓冲液中微波处理进行抗原修复,PBS冲洗3次,每次3 min;滴加封闭血清,37℃孵育20 min,滴加一抗,4℃孵育过夜,PBS冲洗3次,每次5 min,滴加辣根过氧化物酶标记的二抗,37℃孵育20 min,PBS冲洗3次,每次5 min;DAB溶液显色;自来水冲洗,苏木素复染,梯度乙醇脱水,二甲苯透明,中性树脂封片,光镜下观察。PBS代替一抗作为阴性对照。
1.4 免疫组织化学染色结果判定标准
STMN1和GRP78阳性细胞表现为细胞膜或细胞质中出现棕黄色颗粒。由病理科高级医师对免疫组织化学染色结果进行评价。依据阳性细胞百分比评分:0%~4%的阳性细胞记为0分,5%~25%的阳性细胞记为1分,26%~50%的阳性细胞记为2分,51%~75%的阳性细胞记为3分,>75%的阳性细胞记为4分。依据染色强度评分:无染色或边缘染色记为0分,浅黄色记为1分,黄色记为2分,棕褐色记为3分。阳性细胞百分比评分与染色强度评分相加,0分记为(-),1~4分记为(+),5~8分记为(++),9~12分记为(+++),其中0分为阴性,其余为阳性。
1.5 统计学方法
采用SPSS 18.0软件对数据进行统计分析。计数资料以例数和率(%)表示,组间比较采用χ2检验;采用Pearson相关分析法进行相关性分析。以P<0.05为差异有统计学意义。
2 结果
2.1 肺腺癌组织及正常肺组织中STMN1和GRP78的表达情况
STMN1和GRP78阳性表达呈棕黄色(图1)。肺腺癌组织中STMN1和GRP78的阳性表达率分别为66.7%(34/51)和60.8%(31/51),分别明显高于正常肺组织的18.5%(5/27)和22.2%(6/27),差异均有统计学意义(χ2=16.370、10.528,P<0.01)。肺腺癌组织中STMN1和GRP78的表达呈正相关(r=0.455,P<0.05)。

图1 肺腺癌组织和正常肺组织中STMN1和GRP78的表达情况(免疫组织化学染色,×20)
2.2 不同临床特征肺腺癌患者肺腺癌组织中STMN1和GRP78表达情况的比较
不同性别、年龄、淋巴结转移情况肺腺癌患者肺腺癌组织中STMN1和GRP78的阳性表达率比较,差异均无统计学意义(P>0.05)。不同分化程度、TNM分期肺腺癌患者肺腺癌组织中STMN1的阳性表达率比较,差异均有统计学意义(χ2=9.82、8.56,P<0.05)。不同分化程度、TNM分期肺腺癌患者肺腺癌组织中GRP78的阳性表达率比较,差异均有统计学意义(χ2=14.89、13.65,P<0.05)。(表1)
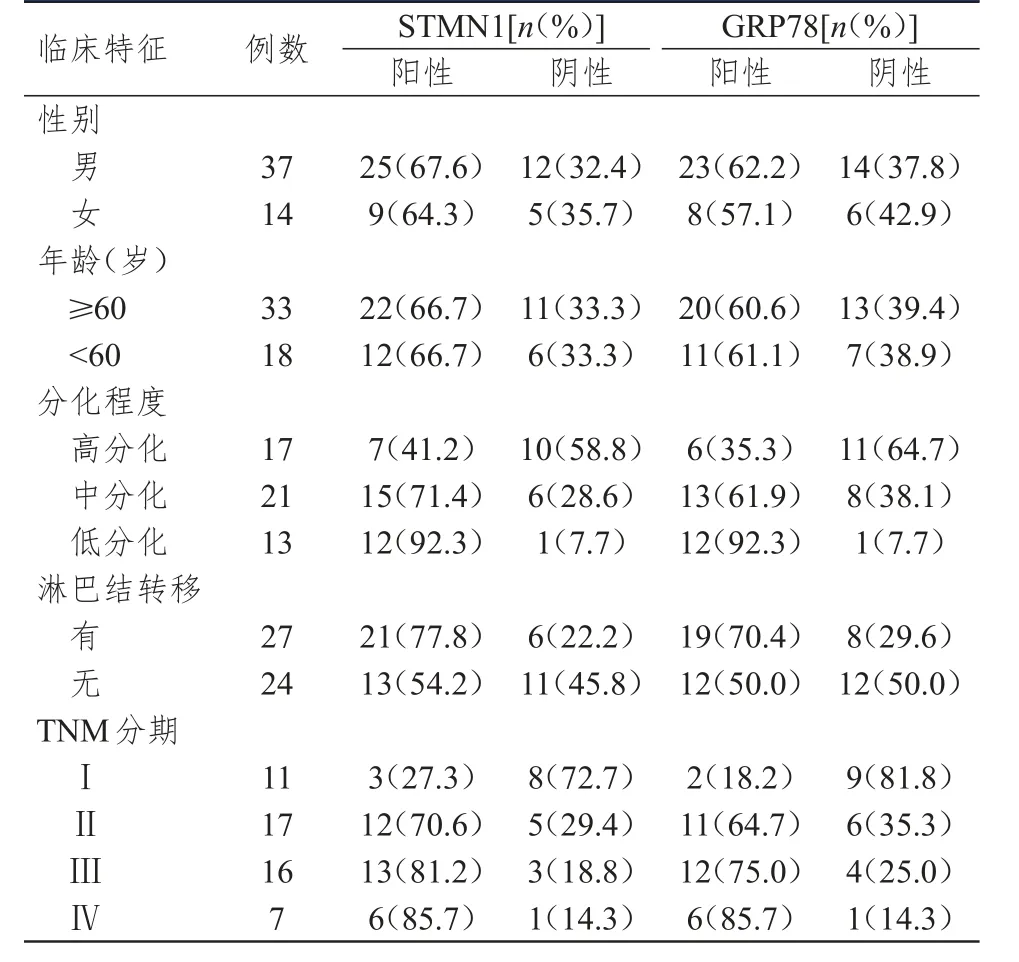
表1 不同临床特征肺腺癌患者肺腺癌组织中STMN1和GRP78的表达情况(n=51)
3 讨论
本研究对肺腺癌组织中STMN1和GRP78的表达情况及临床意义进行了初步研究。结果显示,肺腺癌组织中STMN1和GRP78的阳性表达率分别为66.7%和60.8%,分别明显高于正常肺组织的18.5%和22.2%,差异均有统计学意义(P<0.01),且肺腺癌组织中STMN1和GRP78的表达呈正相关(r=0.455,P<0.05)。提示STMN1和GRP78可能与肺腺癌的发生有关。研究报道显示STMN1在多种恶性肿瘤中高表达,与肿瘤的发生有关[11]。研究表明,STMN1高表达与食管鳞状细胞癌的浸润深度、淋巴结转移、淋巴管浸润和静脉侵犯有关,STMN1高表达患者的生存率低于STMN1低表达患者,STMN1高表达与新辅助放化疗的反应性差有关,抑制STMN1的表达可增强食管鳞状细胞癌对放化疗的敏感性[12]。
本研究结果还显示,不同性别、年龄、淋巴结转移情况肺腺癌患者肺腺癌组织中STMN1和GRP78的阳性表达率比较,差异均无统计学意义(P>0.05)。不同分化程度、TNM分期肺腺癌患者肺腺癌组织中STMN1和GRP78的阳性表达率比较,差异均有统计学意义(P<0.05)。分化程度越低,STMN1和GRP78的阳性表达率越高;临床分期越晚,STMN1和GRP78的阳性表达率越高。有一些研究支持这些结果,如抑微管装配蛋白(stathmin)过表达与淋巴管浸润、分期晚、生存率低有关[13]。有报道认为血清stathmin水平是肺癌尤其是进展期和有淋巴结转移的肺腺癌的潜在生物标志物[14]。stathmin表达情况与子宫内膜癌患者的无瘤生存期和总生存期显著相关[15]。研究发现,下咽鳞状细胞癌组织中STMN1表达水平明显升高,且其表达水平与分化程度、临床分期、肿瘤体积、淋巴结转移及生存率等因素有关;体外实验表明,STMN1能够促进下咽鳞状细胞癌细胞的增殖和迁移,且与上皮-间充质转化有关[16]。另有研究表明,口腔鳞状细胞癌中stathmin过表达,且其表达情况与性别、TNM分期、分化程度、生存期、淋巴结转移情况有关[17]。STMN1也在胆囊癌的发生和发展中发挥重要作用[18]。
关于GRP78与肺腺癌关系的研究较少,有报道认为该分子参与一些化学物质的抗肿瘤作用。如血根碱和淫羊藿苷均具有抗肺腺癌的作用,研究发现二者的作用均涉及内质网应急相关分子如GRP78的表达改变[19-20]。伴侣蛋白L-异天冬氨酸(D-天冬氨酸)O-甲基转移酶的高表达出现在晚期肺腺癌患者中,与GRP78调节的内质网应激有关,提示预后差[21]。有研究显示,STMN1在肝癌、胶质瘤、胰腺癌等恶性肿瘤中癌基因作用的发挥受多种微小RNA(microRNA,miRNA)的调控,表明在肺腺癌中可能存在其他机制调控STMN1的表达[22]。此外,CDC2蛋白抑制剂purvalanol A可通过癌蛋白18(oncoprotein 18,Op18)/stathmin信号通路增强紫杉醇的毒性作用[23]。
综上所述,STMN1和GRP78的高表达与肺腺癌的发生发展密切相关,可能是肺腺癌发生中的重要信号分子。
