薄荷油纳米乳液的制备及其性质分析
2019-06-11綦玉曼寻崇荣车佳玲江连洲马文君张潇元王中江
綦玉曼,寻崇荣,车佳玲,江连洲,马文君,张潇元,李 杨,2,王中江,*
(1.东北农业大学食品学院,黑龙江 哈尔滨 150030;2.哈尔滨食品产业研究院,黑龙江 哈尔滨 150028)
薄荷油是一种具 有浓郁薄荷香味的植物油,因其具有除臭、去腥、抑菌、防腐、增加风味等功效[1],在食品工业中被广泛用于糖果、清凉饮料、糕点等加工中。但是,薄荷油与大多数精油一样具有较强的挥发性,在高温加工以及长时间储存过程中,将会导致加入产品中的薄荷油挥发殆尽。为改善薄荷油的易挥发性质,文献[2-4]采用不同壁材制备微胶囊包埋薄荷油提高其稳定性,方便填料和运输。但是,微胶囊化产品大多是固体香料,不方便作为食品添加剂加入到饮料等液体食品中,且其工业化生产操作繁琐,产品粒径较大,生物利用度相对不高,限制其应用[5]。
近年来,纳米乳液针对特定功能性物质而构建的营养素包埋与传递极大程度上解决了挥发型营养素在水性介质中溶解度差、生物利用率低、易挥发等问题。而且,纳米乳液较普通乳液在贮存过程中可以抵抗重力分离、絮凝和聚结,被看成是一种“近热力学稳定”体系[6]。高压均质乳化技术作为常用的高能法制备纳米乳液技术,具有乳液粒径小、分布窄、乳液稳定、表面活性剂的需量小、生产成本低、易操作、污染小等优势[7-8]。本研究以大豆分离蛋白(soy protein isolate,SPI)为表面活性剂、磷脂酰胆碱为助表面活性剂,通过高压均质乳化技术制备薄荷油纳米乳液,使薄荷油能够稀释并溶解于水相中,以提高其稳定性及吸收利用率。同时优化SPI质量分数、薄荷油质量分数、均质压力等影响纳米乳液理化性质的主要因素,为制备均一、稳定的薄荷油纳米乳液提供一定参考。
1 材料与方法
1.1 材料与试剂
SPI 哈尔滨高科技(集团)股份有限公司;磷脂酰胆碱、薄荷油、胃蛋白酶、胰酶、猪胆盐 美国Sigma公司;磷酸氢二钠、磷酸二氢钠 天津市东丽区天大化学试剂厂。
1.2 仪器与设备
Nano-ZS90粒度分析仪 英国马尔文公司;ULTRA-TURRAX UTL2000乳化机 德国IKA仪器设备公司;SPCH-10高压均质机 英国Stansted Fluid Power公司;PHSJ-4A型实验室pH计 中国上海雷磁公司;电子分析天平(0.000 1 g) 北京赛多利斯仪器系统有限公司;H-7650B型透射电镜 日本日立公司;7890-5795C型气相色谱-质谱联用仪、19091N-136型毛细管色谱柱 美国Agilent公司;Gemini HR Nano流变仪英国Malvern仪器有限公司。
1.3 方法
1.3.1 粗乳液的制备
参考Lee等[9]的方法,将SPI和磷脂酰胆碱溶于缓冲液(0.1 mol/L、pH 7.0磷酸盐缓冲溶液)中,室温下连续搅拌120 min,形成水相;在高速分散器的搅拌下把薄荷油作为油相加到水相中,20 000 r/min均质5 min,形成粗乳液。
1.3.2 薄荷油纳米乳液的制备
将粗乳液通过高压均质机进一步均质乳化即得高压均质薄荷油纳米乳液。高压均质处理方法及条件设定参考Dybowska等[10]并进行一定修改,采用冰水浴保持低温。
1.3.3 薄荷油纳米乳液单因素试验
以SPI质量分数、薄荷油质量分数、均质压力为考察因素进行单因素试验,测定制备的薄荷油纳米乳液平均粒径、多分散性指数(polydispersity index,PDI)、Zeta电位、浊度、乳化产率、乳液稳定性指数(turbiscan stability index,TSI)。
1.3.3.1 SPI质量分数
分别配制质量分数为1.5%、2.0%、2.5%、3.0%、3.5%的SPI和0.2%磷脂酰胆碱混合溶液,室温下连续搅拌120 min,缓慢加入5%薄荷油,制备粗乳液。高压均质机均质压力为80 MPa,均质4 次,测定制备的薄荷油纳米乳液平均粒径、PDI、Zeta电位、浊度、TSI。
1.3.3.2 薄荷油质量分数
配制质量分数为2.5%的SPI和0.2%磷脂酰胆碱混合溶液,室温下连续搅拌120 min,缓慢加入2%、5%、8%、11%、14%薄荷油,制备粗乳液。高压均质机采用均质压力为80 MPa,均质4 次,测定制备的薄荷油纳米乳液平均粒径、PDI、Zeta电位、浊度、TSI。
1.3.3.3 均质压力
配制质量分数2.5%的SPI和0.2%磷脂酰胆碱混合溶液,缓慢加入5%薄荷油,制备粗乳液。设置均质压力分别为60、80、100、120、140 MPa,均质4 次,测定制备的薄荷油纳米乳液平均粒径、PDI、Zeta电位、浊度、TSI。
1.3.4 薄荷油纳米乳液的平均粒径、PDI及Zeta电位的测定
用Zetasize r Nano-ZS 90光散射粒度分析仪分别测定上述薄荷油乳液的平均粒径、粒径分布规律及Zeta电位变化,薄荷油油滴的折射率为1.45,水相溶液折射率为1.33。为降低多重光散射效应,分析前用pH 7.5磷酸盐缓冲液(0.05 mol/L)稀释薄荷油乳液1 000 倍测定粒径及PDI,稀释50 倍测定Zeta电位。
1.3.5 薄荷油纳米乳液的浊度测定
将薄荷油纳米乳液用磷酸盐缓冲液溶液稀释40 倍,以磷酸盐缓冲液为空白对照,用紫外分光光度计 测定600 nm波长处的吸光度,浊度(T)计算见公式(1):

式中:A为稀释乳液在600 nm波长处的吸光度;V为稀释倍数;I为光程差0.01 m。
1.3.6 薄荷油纳米乳液的乳化产率测定
1.3.6.1 标准曲线的绘制
准确称取不同质量的薄荷油,分别置于50 mL的容量瓶中,用无水乙醇稀释定容至刻度,则得到一系列质量浓度梯度的标准溶液,以无水乙醇作为空白组,在最大吸收波长下测定标准溶液的吸光度。以吸光度对质量浓度进行线性回归,得到标准曲线回归方程。
1.3.6.2 纳米乳液中薄荷油提取
首先称取一定质量的薄荷油纳米乳液,用无水乙醇洗去表面的油。接着把薄荷油纳米乳液放入烧瓶中,并加入一定量的无水乙醇进行40 ℃水浴加热,15 min后将此溶液用超声波处理1 h,随后用离心 机除去溶液中的不溶性物质,取上层清液,用50 mL容量瓶定容。
1.3.6.3 乳化产率计算
采用紫外光谱法定量分析薄荷油纳米乳液的乳化产率,测定样品的吸光度,再根据标准曲线回归方程计算乳化产率,计算见式(2):
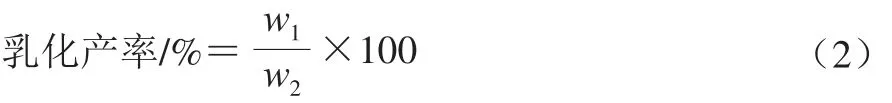
式中:w1为纳米乳液中薄荷油质量;w2薄荷油总质量。
1.3.7 TSI的测定
参考刘蕾等[11]方法,取18 mL薄荷油纳米乳液于Turbiscan专用圆柱形的玻璃杯(外径27.5 mm,高度70 mm)中。在55 ℃每30 min扫描1 次,扫描时间6 h。由此可获得反映薄荷油纳米乳液稳定性的差值反射光量随时间的动态变化,即可作为衡量薄荷油纳米乳液稳定性的图谱。
1.3.8 纳米乳液透射电镜测定
将薄荷油纳米乳液样品用蒸馏水稀释10 倍后,滴加在覆盖有碳膜的铜网上,用2%磷钨酸溶液进行染色处理,放至通风处干燥后,通过透射电镜观察纳米乳液的形态并拍照。
1.3.9 纳米乳液中薄荷油的成分分析
1.3.9.1 样品准备
将对照组薄荷油纯品与从纳米乳液中提取的薄荷油直接进行气相色谱-质谱联用仪检测。
1.3.9.2 气相色谱-质谱联用仪测定条件
气相色谱条件:1 9 0 9 1 N-1 3 6型色谱柱(60 m×0.25 mm,0.25 μm),进样量10 μL,升温程序:40 ℃持续3 min,然后以4 ℃/min上升至100 ℃,接着以7 ℃/min上升至240 ℃,持续7 min,分流比为10∶1。载气为氦气,流速为0.8 mL/min,进样口温度为250 ℃。
质谱条件:离子源温度为200 ℃,检测器电压为350 V,电子能量为70 eV,灯丝发射电流为200 μA,接口温度为250 ℃,质量扫描范围m/z50~500。
1.3.9.3 化合物鉴定
利用Xcalibur软件对实验数据进行分析。通过计算机自动查找化合物,然后与谱库NIST和Wiley化合物进行匹配度检测,再手动检索核对,选择匹配度大于800的结果,采用归一化法得到各成分的相对含量。
1.3.10 纳米乳液的流变学特性测定
采用AR550型流变仪检测薄荷油纳米乳液的流变学特性,选择直径60 mm的锥形板,并控制板间距为50 μm。将1 mL薄荷油纳米乳液置于平板上,剪切速率0.01~1 000 s-1,温度25 ℃。
1.4 数据处理
每组实验重复测量3 次,采用SPSS Statistics 22软件对数据进行ANOVA差异显著性分析,P值小于0.05为显著性差异,数据均为 ±s,使用Origin Pro9.0软件绘制曲线图。
2 结果与分析
2.1 高压均质制备薄荷油纳米乳液工艺优化单因素试验结果
2.1.1 SPI质量分数对薄荷油纳米乳液理化稳定性的影响

表1 SPI质量分数对纳米乳液理化稳定性的影响Table 1 Effects of SPI content on physical and chemical stability of nanoemulsion

图1 SPI质量分数对纳米乳液粒径分布的影响Fig. 1 Effect of SPI content on particle size distribution of nanoemulsion
从表1可以看出,随着SPI质量分数的增加,薄荷油纳米乳液的平均粒径、PDI、浊度呈现先减小后增加的趋势。分析认为SPI质量分数在1%~1.5%范围内,此时乳液中的蛋白质浓度过低,即使全部吸附在油-水界面仍未能达到饱和,溶液中的小液滴因而发生聚合现象,形成粒径较大的液滴。乳液浊度是粒径大小和浓度的函数,乳液浊度越大则表明较大粒径的液滴分布越多,随着SPI质量分数的增加,蛋白乳液体系在稀释过程中多余的表面活性 剂胶束发挥作用,吸附破乳过程中释放出来的油滴,从而使得油滴被包裹,进而使透明度增强。当SPI质量分数为2.5%时,液滴平均粒径、PDI、浊度同时达到最小值,表明在此条件下蛋白在液滴表面形成紧密的界面膜,同时界面蛋白之间的电荷斥力以及空间位阻作用,使得油滴可以保持粒径相对较小(约为200 nm)且其分布较为集中(图1),此时乳液处于相对均一、稳定的状态[12]。当SPI质量分数大于2.5%时,液滴的平均粒径具有缓慢上升的趋势,粒径分布呈双峰分布,并逐渐向大粒径方向移动。说明随着蛋白分子的不断吸附,液滴间相对平衡的状态被破坏,在此条件下,平均粒径主要受均质条件而非乳化剂性能的影响[13],吸附在不同液滴上的蛋白分子的结合可能造成液滴之间的聚合,从而导致总体系中平均粒径和浊度的增大。这一现象也可用排斥絮凝理论解释,即当高分子乳化剂的浓度超过临界值时,连续相中没有吸附的蛋白会因为渗透作用引起液滴絮凝,从而引起蛋白质分子链从两液滴表面排斥而出[14]。此趋势与Mahdi等[15]结果一致,说明过量的乳化剂会影响乳液的均一性,进而影响乳液的稳定性。
从表1可以看出,随着SPI质量分数的增加,薄荷油纳米乳液Zeta电位呈现先逐渐增大后减小的趋势,当SPI质量分数为2.5%时,纳米乳液电位为-30.6 mV,而后,随着SPI质量分数的增加,纳米乳液Zeta电位逐渐降低。这表明,带负电荷的SPI分子能够吸附至纳米乳液液滴表面,随着SPI质量分数的增加,SPI在液滴表面吸附逐渐达到饱和,从而使得纳米乳液的Zeta电位值达到平衡值,趋于稳定,不再随着SPI质量分数增加而增加。
从表1可以得出,随着SPI质量分数的増加,薄荷油纳米乳液的乳化产率逐渐提高。当SPI质量分数大于2.5%时,纳米乳液乳化产率不再随着SPI质量分数的增加而显著提高(P>0.05)。这是因为当SPI质量分数增加时,包裹在水-油界面上的SPI增加,提高了薄荷油纳米乳液的乳化产率。根据Bi Lin等[16]的研究可知,乳化剂浓度越大,界面的吸附层越厚,从而提高了薄荷油的乳化产率,当SPI质量分数大于2.5%时,薄荷油纳米乳液的乳化产率为95%以上,达到比较高的乳化产率。
从表1可以看出,随着SPI质量分数的增加,TSI值逐 渐减小,当SPI添加量大于2.5%时,TSI值趋于稳定。以上结果表明,当SPI质量分数较小时,薄荷油纳米乳液的TSI变大,表明此时乳液稳定性变差,说明此SPI质量分数并不足以覆盖乳液液滴表面,可能使得薄荷油液滴发生絮凝,从而降低薄荷油纳米乳液的稳定性。当SPI质量分数逐渐增大时,界面上吸附的蛋白分子也增加,膜的强度相应增大,液滴难以聚结,纳米乳液能够保持较好的物理稳定性。同时,随着SPI质量分数的增大,乳液的黏度增加,根据斯托克斯定理,高黏度体系中,液滴具有较低的沉降速率,从而有利于得到更稳定的乳状液体系。
本实验制备以不同添加量的SPI为乳化剂的薄荷油纳米乳液,当SPI添加量较少时,界面 蛋白发生构象改变以完全覆盖水油界面;当SPI添加量较多时,有较多的SPI吸附在界面上,从而使吸附在界面上的SPI不能发生构象改变。界面上SPI较多时,形成较厚的界面膜,对油滴的保护提高;同时因为SPI没有发生构象改变,其因空间位阻而使液滴相互排斥的作用比较大,进一步防止液滴粒径增大,提高乳液稳定性[17]。综合考虑乳化剂浓度对平均粒径和粒径分布宽度、乳化产率、浊度、TSI的影响,2.5%的SPI足够吸附到油滴界面而形成比较稳定的薄荷油纳米乳液,此质量分数最适合薄荷油纳米乳液的制备。
2.1.2 薄荷油质量分数对薄荷油纳米乳液理化稳定性的影响

表2 薄荷油质量分数对纳米乳液理化稳定性的影响Table 2 Effect of peppermint oil content on stability of nanoemulsion

图2 薄荷油质量分数对纳米乳液粒径分布的影响Fig. 2 Effect of peppermint oil content on particle size distribution of nanoemulsion
在乳液的制备过程中,高芯壁比往往是配方 中所追求的,不仅可以提高该运载体系的效率,而且有利于乳液在后续加工和应用中的可操作性。但是,芯材载入量过大时,颗粒间易发生聚集,从而对乳液粒径和稳定性产生不利影响。由表2可知,乳液的平均粒径、PDI、浊度、TSI随薄荷油质量分数的增加先降低后增大。由图2可知,当薄荷油质量分数为5%时,乳液具有最小粒径分布宽度。分析原因在于较高的油载荷会使均质化的液滴更多更小,从而使蛋白质有更大的可吸附表面积,这会使围绕油滴的界面膜更稳定且聚结力更强。因此,制备的纳米乳液均比较稳定。薄荷油质量分数为11%、14%的薄荷油纳米乳液粒径分布在1 000 nm处出现了1 个新的峰(图2),说明过量的油相不能很好地被乳化剂所包埋,极易通过介质的流动而扩散到大油滴中,从而引起乳液粒径的增加,发生奥氏熟化现象[18],导致粒径分布变宽,粒径与浊度变大。
随着薄荷油质量分数的进一步增加,乳液的Zeta电位绝对值减小。这表明高油负荷降低了乳液的稳定性。在较低的Zeta电位下,分散油滴之间的空间排斥可能不足以克服液滴和能量位垒之间的分子间吸引力(即范德华力和疏水吸引力)[19]。因此,乳液在自然条件下絮凝,并且液滴倾向于聚集,提高了分层率。薄荷油质量分数的增加对乳化后的产率影响不大。因此确定薄荷油的质量分数为5%。
2.1.3 高压均质压力对薄荷油纳米乳液理化稳定性的影响

表3 均质压力对纳米乳液理化稳定性的影响Table 3 Effect of homogenization pressure on stability of nanoemulsion

图3 均质压力对纳米乳液粒径分布的影响Fig. 3 Effect of h omogenization pressure on particle size distribution of nanoemulsion
研究表明,高压均质采用的压力参数对粒径的大小具有显著影响。由表3和图3可知,随着均质压力的增加,乳液的平均粒径、PDI、浊度和TSI急剧下降,粒径分布范围变窄,集中分布在80~400 nm波长之间,均质压力高于80 MPa,平均粒径、PDI、浊度和TSI缓慢上升,粒径分布峰逐渐向大粒径方向偏移。影响乳液粒径主要因素是高压均质过程中巨大的机械力作用(巨大剪切力、撞击和空穴效应)[20],两者间存在一定的函数关系,即均质压力越高,机械作用越强,粒径越小,液滴细化程度越高,分布越均匀,但均质压力过高时,作用在乳液上的冲击力较大,乳液的液滴过小[21],颗粒之间由于彼此的布朗运动速率加快、相互碰撞的次数增加足以破坏界面膜而发生聚集现象[22],同时高压可以引起蛋白质变性[23],变性蛋白质分子相互作用形成聚集体,溶解度下降,并从界面上脱落,进而阻碍液滴被均质破坏,降低均质的效果[24],与此同时,由于液滴过小,比表面积增大,乳化剂的数量不足以覆盖液滴表面,导致液滴聚集。类似结果在Schulz等[25]的研究中也曾被报道。由表3可知,均质压力对乳液Zeta电位影响不大。当均质压力小于80 MPa时,随着均质压力的增加,乳化产率逐步提高,超过80 MPa时,乳化产率随均质压力的增加而快速下降。这是因为均质时的剪切力和空穴效应,导致薄荷油破碎[26]。综上,均质压力选择为80 MPa。
2.2 薄荷油纳米乳液的形态及粒径分布

图4 薄荷油纳米乳液的透射电镜图Fig. 4 TEM pictures of peppermint oil nanoemulsion
由图4可直观地看出,乳液的平均粒径小,液滴分布均匀,表明高压均质过程中产生的巨大剪切、湍流作用、空穴效应的确能起到较好的乳化效果。有研究表明:乳液平均粒径的减小,不仅有效提高乳液的稳定性,有效抑制沉淀和乳析的发生,也显著提高功能成分和营养素,尤其是非水溶性物质的生物利用率[14]。
2.3 纳米乳液中薄荷油主要成分的检测结果
对薄荷油纳米乳液物理化学稳定性的研究发现,薄荷油纳米乳液具有较好的理化稳定性。将单因素试验优化的最佳工艺条件制备的薄荷油纳米乳液和对照组薄荷油进行气相色谱-质谱检测,结果如表4所示。结果表明薄荷油经过乳化后其中的部分烯类物质,如2-β-蒎烯、α-蒎烯、柠檬烯、δ-杜松烯、D-大根香叶烯、β-波蒡烯的比例部分降低,分析原因在于一方面可能与上述几类物质在空气中极易挥发的性质有关,另一方面可能在高压均质的作用下造成了这些物质的氧化损失,进而导致总含量稍有下降,此结果与陈硕[27]与梁蓉[28]等研究结果类似。而薄荷油主要的功能性成分薄荷酮、薄荷醇等含量未出现明显改变,表明薄荷油经高压均质制备 成纳米乳液后,能够形成一种更稳定的乳液体系,从 而迅速将功能性成分稳 定地乳化在纳米体系中,降低薄荷油在生产加工和运输储存过程中的损失。

表4 纳米乳化包埋前后薄荷油中主要成分相对含量Table 4 Change in relative quantity of main components in peppermint oil before and after incorporation into nanoemulsions
2.4 纳米乳液的流变学特性
纳米乳液的流变特性在食品领域实际生产中具有一定的指导意义,乳化体系的黏度变化曲线在一定程度上可以表征乳液的聚合程度,进一步反映乳液的动力学稳定性。由图5可知,随着纳米乳液剪切速率的增大,乳液的黏度逐渐降低。在较小的剪切速率(0.1~400 s-1)时,薄荷油纳米乳液的黏度急剧下降,呈现出剪切变稀的特征,主要原因在于流速场中,薄荷油纳米乳液的乳滴形成絮体并瓦解[29]。当剪切速率大于400 s-1后,纳米乳液的黏度未发生明显变化,呈现牛顿流体性质,这是因为絮体被裂解成为单个液滴,也可能是乳化体系形成与瓦解絮体的速率相同,絮体具有相对稳定的状态[30]。薄荷油纳米乳液纳米级粒径进一步增大乳液的比表面积,增加乳滴之间的相互作用,导致薄荷油纳米乳液的黏度增加,根据Stoke定律,当乳液具有较大的黏度时,有利于减缓液滴的上浮速度,保持更好的稳定性。流变学特性结果补充说明了高压均质制备的薄荷油乳液具有良好的动力学稳定性。

图5 薄荷油纳米乳液的流变性Fig. 5 Rheological property of peppermint oil nanoemulsion
3 结 论
以SPI-磷脂酰胆碱复合物作为乳化剂,采用高压均质法制备薄荷油纳米乳液,研究SPI质量分数、薄荷油质量分数及均质压力对薄荷油纳米乳液的平均粒径、PDI、Zeta电位、浊度、乳化产率、TSI的影响机制,并通过动态光散射和透射电镜验证,当SPI质量分数2.5%、薄荷油质量分数5%、均质压力80 MPa时,制备出的薄荷油纳米乳液平均粒径小且分布均匀;通过气相色谱-质谱检测发现SPI-磷脂酰胆碱为乳化剂制备的纳米乳液可有效保护薄荷油功能成分;流变学特性结果说明薄荷油纳米乳液具有良好的动力学稳定性。因此,此方法能够快速地制备稳定性好的薄荷油纳米乳液,是一种较为实用、高效的薄荷油纳米乳液制备技术,为今后薄荷油在食品领域中的应用提供依据和参考。
