牛多杀性巴氏杆菌病二价灭活疫苗的研究
2019-05-21姜志刚徐和敏潘春刚
姜志刚,徐和敏,邵 葳,潘春刚,于 力*
(1.中国农业科学院哈尔滨兽医研究所 牛羊传染病研究创新团队,黑龙江 哈尔滨 150069;2.中牧实业股份有限公司,北京 100070)
多杀性巴氏杆菌(Pasteurella multocida,Pm)是具有异质性特征的革兰氏阴性病原菌群,一般寄生于家养和野生动物的上呼吸道,具有条件致病性,在某些应激条件刺激下,可以引起带菌动物发生以败血和/ 或呼吸系统疾患为主的疾病[1]。根据荚膜抗原的特异性,可将 Pm 分为 A、B、D、E 和 F 等 5个荚膜型[2]。荚膜 A 型和荚膜 B 型 Pm 是引起我国牛巴氏杆菌病的病原。其中荚膜B 型Pm 引起的牛出血性败血症是牛的重要疫病[3],牛荚膜A 型 Pm是2008年首次被分离鉴定的引起牛纤维素性化脓性肺炎的新病原[4-8],是近10年来严重危害我国养牛产业的新发疫情[7]。由于Pm 不同血清型之间的交叉保护力差[3],现有的牛出血性败血症灭活疫苗(荚膜B 型Pm 单价苗)不能有效防控荚膜A 型Pm 引起的牛纤维素性化脓性肺炎。因此,研发针对荚膜A 型Pm 的灭活疫苗是必要而紧迫的。
本研究团队前期研究已经确定了牛荚膜A 型Pm 与牛纤维素性化脓性肺炎因果关系[7],并且建立了荚膜 A 型 Pm 的牛体免疫攻毒模型[8];同时,参考现行的《 牛多杀性巴氏杆菌病灭活疫苗制造及检验规程》(荚膜 B 型 Pm 单价苗)[9],重新测定了牛荚膜B 型疫苗菌株对牛的最小致死量(MLD)以及最小免疫剂量(未发表资料)。在上述研究的基础上,本研究将毒力强、免疫原性好的牛荚膜A 型Pm-TJ株,与已商品化的牛荚膜B 型Pm 灭活苗生产用菌株C45-2 株(CVCC 44502)作为制苗菌种,制备牛荚膜Pm 病二价灭活疫苗,并对该制品的安全性、免疫效力、免疫持续期进行研究,为全面控制我国牛巴氏杆菌病提供有效的技术手段。
1 材料与方法
1.1 菌株、实验动物与主要试剂 牛荚膜A 型Pm-TJ 株(简称 Pm-TJ 株)由哈尔滨兽医研究所保存并提供;牛荚膜 B 型 Pm C45-2 株(简称 C45-2 株)由中牧兰州生物药厂保存并提供。体质量为1.5 kg~2.0 kg 的家兔由中牧实业股份有限公司兰州生物药厂自繁自养;体质量为 18 g~22 g SPF 级 BALB/c小鼠购自北京维通利华实验动物技术有限公司;6月龄西门塔尔杂交肉牛(西杂牛)和3 岁龄荷斯坦奶牛分别来自重庆某肉牛场和甘肃某奶牛场。脑心浸液培养基和马丁肉汤培养基均购自北京奥博星生物技术有限责任公司;氢氧化铝胶佐剂由中牧兰州生物药厂配制。
1.2 Pm 二价灭活疫苗的制备 取Pm-TJ 株活化菌液按 2 %量接种于 BHI 培养基,置 37 ℃、75 r/min培养 8 h 后收获;同时,取 C45-2 株活化接种于含0.1 %裂解血球全血的马丁肉汤中,37 ℃培养12 h后收获。对收获的两种菌液分别进行纯粹性检验和活菌计数后离心浓缩,分别加入0.1 %甲醛溶液于37 ℃灭活12 h,灭活检验合格后将菌液与氢氧化铝胶佐剂按5∶1 的比例混匀分别制成灭活疫苗,混合两种灭活疫苗,使Pm-TJ 株和C45-2 株的终浓度分别为 1×1010cfu/mL 和 5.0×109cfu/mL,制备 Pm 二价灭活疫苗。
1.3 Pm 二价灭活疫苗的安全性试验
1.3.1 非靶动物安全性试验 将制备的Pm 二价灭活疫苗分别皮下接种10 只小鼠和10 只家兔,参考现行的 《 牛多杀性巴氏杆菌病灭活疫苗制造及检验规程》(荚膜 B 型 Pm 单价苗),分别接种 0.3 mL/ 只和 4 mL/ 只[9],同时设置相同数量的未接种动物作为对照,10 d 内观察动物的接种部位、精神状态及存活情况。
1.3.2 靶动物安全性试验 将制备的Pm 二价灭活疫苗分别以单剂量(2 mL/ 头)、单剂量重复(间隔 2周)以及超剂量(4 mL/ 头)经肌肉途径分别接种10 头6月龄西杂牛以及3 岁龄10 头荷斯坦奶牛,同时设置相同数量的未接种动物作为对照。于接种后每日测量动物体温、观察动物的接种部位和精神状态,并记录存活情况,观察期为14 d。为评价疫苗对牛生产性能的影响,在观察期内每日记录荷斯坦奶牛的产奶量;于免疫前和免疫后30 d 测量西杂牛的体重,并计算月增重。
1.4 Pm 二价灭活疫苗对牛的免疫保护试验 将24头6月龄西杂牛随机分为 3组,每组 8 头,分别以每头 2.0 mL、1.0 mL 和 0.5 mL 的 Pm 二价灭活疫苗颈部肌肉注射接种每组实验牛,另设6 头未接种疫苗牛作为对照组。接种后第21 d,随机选择各实验组4 头牛和对照组3 头牛经气管接种Pm-TJ 强毒株(5.3×108cfu/ 头),每日观察牛的临床表现,于攻毒后第10 d 剖检、记录肺部病理变化,并进行细菌再分离及PCR 鉴定[7]。根据本团队前期的病原菌回归牛体致病试验结果[7-8],本研究对攻毒牛的临床症状及病理变化打分评价该二价灭活疫苗对免疫牛的保护效果。各实验组另4 头牛与对照组另3 头牛采用肌肉注射 C45-2 强毒株(5.2×106cfu/ 头)[9]攻毒,观察14日。参照 《 牛多杀性巴氏杆菌病灭活疫苗制造及检验规程》(荚膜 B 型 Pm 单价苗)[9],本研究将二价灭活疫苗免疫效力的标准确定为:若攻毒后对照组牛全部(3/3)发病(A 型菌攻毒)或死亡(B 型菌攻毒)时,免疫牛应至少3/4 获得保护;若攻毒后对照牛2/3 发病或死亡,免疫牛应全部(4/4)获得保护。根据攻毒后牛的存活情况评价疫苗接种对攻毒牛的保护效果。
1.5 Pm 二价灭活疫苗接种牛免疫持续期的测定将Pm 二价灭活疫苗肌肉接种32 头西杂牛,2.0 mL/头,同时设24 头未免疫牛作为对照。在免疫后3、6、9 和 10 个月,分别对免疫牛和对照牛攻毒。即在每个攻毒时间点随机挑选4 头免疫牛和3 头对照牛攻击A 型菌Pm-TJ 株,另随机挑选4 头免疫牛和3 头对照牛攻击B 型菌C45-2 株攻毒,攻毒方法同1.4。统计每个时间点的攻毒保护结果,确定该疫苗的免疫持续期。
2 结 果
2.1 二价灭活疫苗安全性试验结果 将制备的Pm二价灭活疫苗皮下接种非靶动物小鼠和兔,观察期内接种动物均健活,未出现精神萎靡以及接种部位红肿、结节等不良反应,与未接种动物无可见差异。将疫苗分别以单剂量、单剂量重复以及超剂量接种西杂肉牛及荷斯坦奶牛。观察期内所有接种牛均健活,未出现体温升高、精神萎靡以及接种部位红肿、结节等不良反应,与对照牛无可见差异。此外,本研究还通过测量6月龄肉犊牛月增重以及3岁泌乳牛日产奶量来评价疫苗对免疫牛生产性能的影响,结果显示,将疫苗以一次单剂量、单剂量重复以及一次超剂量免疫肉犊牛后,犊牛在首免后30 d内平均月增重分别为 17.0 kg、16.3 kg、17.1 kg,对照组犊牛平均月增重为16.7 kg (图1A),免疫组与对照组之间无统计学差异(t 检验,p>0.05);采用该3 种方式接种泌乳牛,14 d 内观察每日产奶量,方差分析显示免疫组与对照组之间无统计学差异(p>0.05) (图1B)。上述结果表明,制备的牛 Pm 病二价灭活疫苗具有良好的安全性。
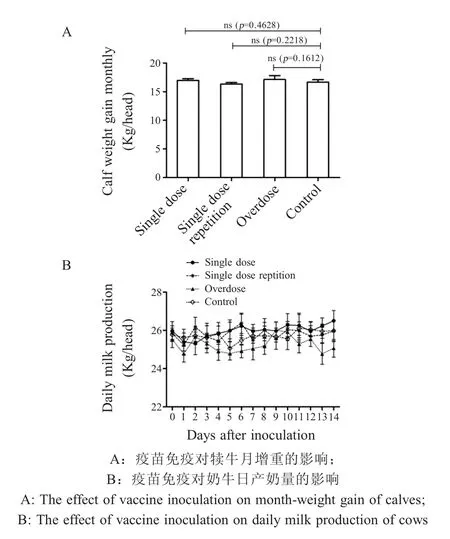
图1 接种二价灭活疫苗对牛生产性能的影响Fig.1 Effect of the bivalent inactivated vaccine inoculation on production performance of cattle
2.2 二价灭活疫苗对牛的免疫保护试验结果 将二价灭活疫苗分别以每头2.0 mL、1.0 mL 和 0.5 mL的剂量经颈部肌肉途径接种实验牛,于免疫后21 d分别以 Pm-TJ 株和 C45-2 株强毒攻击,结果显示,当免疫剂量为2 mL/ 头时,免疫犊牛无论用A 型菌还是B 型菌攻毒,保护率均能达到100 % (4/4);当免疫剂量降低至1 mL/ 头时,免疫犊牛用A 型菌攻毒后的保护率可达75 % (3/4),用B 型菌攻毒后的保护率仍能够达到 100 % (4/4);用 0.5 mL 疫苗免疫犊牛后,其对A 型和B 型菌攻毒后的保护率均为25%(1/4);未免疫的对照犊牛用A 型菌攻毒后100%(3/3)发生纤维素性化脓性肺炎,用 B 型菌攻毒后100 % (3/3)发生牛出血性败血症而死亡,结果详见表1。表明二价灭活疫苗能够同时保护对荚膜A 型和B 型Pm 的攻击产生有效的免疫保护,且最小免疫剂量为1 mL/ 头份。
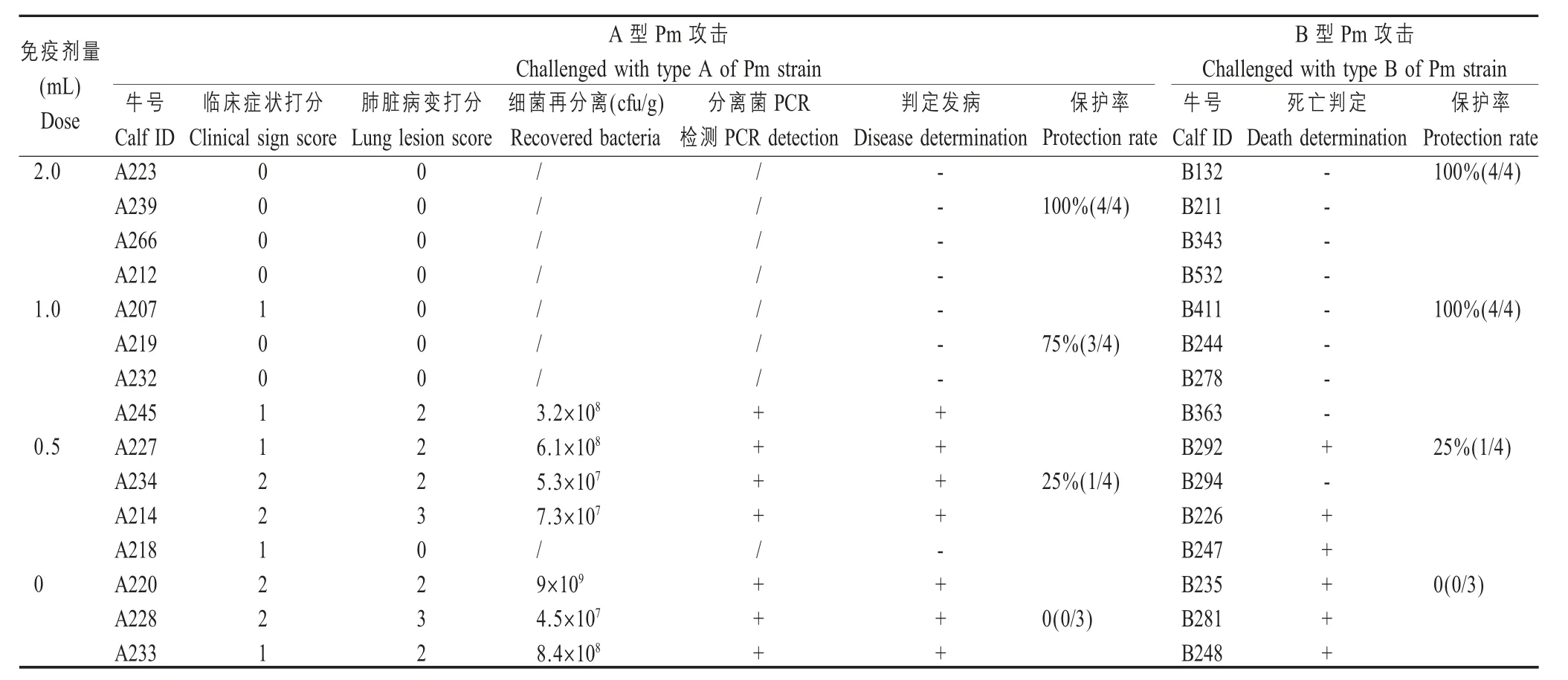
表1 二价灭活疫苗对犊牛免疫效力的评价Table 1 Evaluation of immune potency of the bivalent inactivated vaccine for calves
2.3 二价灭活疫苗对牛的免疫持续期测定结果 将本研究疫苗制品按推荐剂量(2 mL/ 头份)接种西杂牛,在接种疫苗后分别于不同时段采用A 型Pm-TJ株和 B 型C45-2 株对免疫牛进行攻击,结果显示,实验牛在免疫后各时段对A 型菌和B 型菌的攻毒保护率均能够达到75 % (3/4)及以上(表2),符合免疫效力标准。表明该二价灭活疫苗免疫10 个月内能够同时对A 型菌和B 型菌的攻击提供有效保护,疫苗免疫持续期至少10 个月。
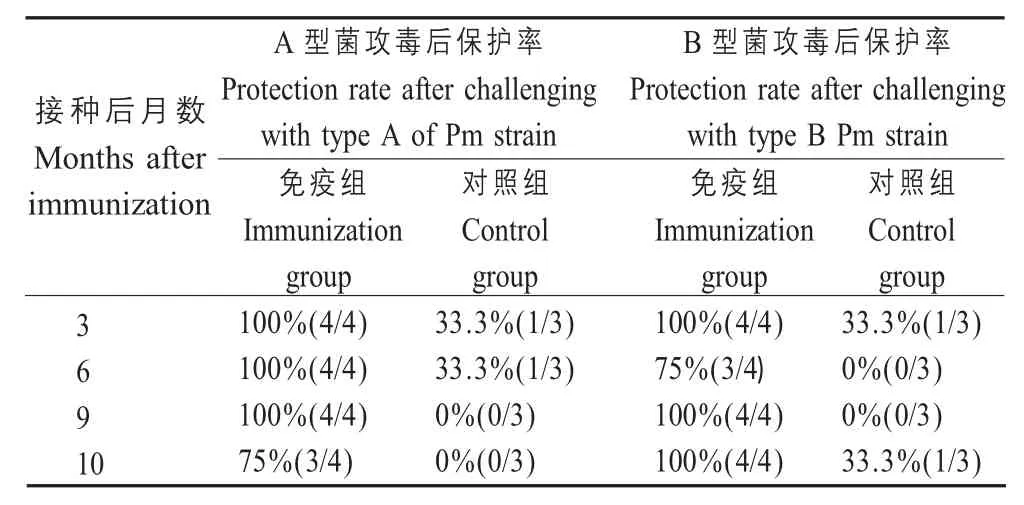
表2 二价灭活疫苗对犊牛免疫持续期的测定Table 2 Immune duration of the bivalent inactivated vaccine-inoculated calves
3 讨 论
本研究按照兽用新生物制品研制的要求,对制备的牛 Pm A 型 Pm-TJ 株和 B 型 Pm C45-2 株二价灭活疫苗开展了安全性和免疫效力的研究,为该疫苗产品的产业化研发奠定了实验基础。
在疫苗研究中,用非靶动物替代本动物进行安全性检验,在保证疫苗安全检验要求的前提下,可以减少本动物安全性检验中牛的使用,这不仅符合动物伦理方面的要求,同时也可以降低批次检验的成本。在现行《 牛多杀性巴氏杆菌病灭活疫苗制造及检验规程》[9](荚膜B 型Pm 单价苗)的安全性检验中,小鼠和兔均采用皮下注射,小鼠接种剂量为0.3 mL,兔接种剂量为本动物的1 倍剂量,即5.0 mL;本制品采用了小鼠安全检验的方法,而用兔检验时接种剂量提高至本动物使用剂量的2 倍,即4.0 mL(本制品为浓缩苗,本动物推荐使用剂量为2 mL),因此本研究中的安全性检验标准更高、结果更加可靠。
在本动物牛的安全性和免疫效力研究中,接种剂量以及攻毒剂量的确定,是依据前期研究中建立的荚膜A 型Pm 免疫攻毒模型结果[8],以及中牧兰州生物药厂对荚膜B 型Pm 的毒力与免疫原性重新测定的结果(未发表资料)。在攻毒试验中,用荚膜A 型和荚膜B 型Pm 攻击时采用不同的标准判定结果,这是由于两种血清型细菌对牛的致病性明显不同。B 型菌侵入牛体形成败血症,引起全身性多系统病理变化导致其急性死亡,因此建立攻毒模型是以牛死亡作为判定指标,效力试验依然参照现行的《 牛多杀性巴氏杆菌病灭活疫苗制造及检验规程》[9](B 型 Pm 单苗)操作。与之明显不同的是,荚膜 A型Pm 人工感染牛所引起的病理变化局限在肺脏,呈现纤维素性化脓性肺炎,无全身性病理变化,在无明显应激因素刺激时,多数牛呈现亚急性或慢性发病,短期内不会引起死亡,因此建立攻毒模型是以临床症状、病理变化结合实验室检测对发病牛进行判定[7-8]。免疫后攻毒结果显示,接种二价灭活疫苗可使犊牛同时抵抗荚膜 A 型 Pm 和荚膜B 型 Pm的攻击,其最小免疫剂量为1 mL。然而,考虑到牛荚膜A 型Pm 属于典型的条件致病性病原,现地牛背景复杂而且易受多种应激因素的影响,为保证疫苗的免疫效果,在实际应用中将接种剂量定为2 mL/ 头。
在免疫持续期的研究中,考虑到现有牛Pm 病灭活疫苗(荚膜B 型Pm 单价苗)产品的免疫持续期为9 个月,本研究将持续期试验的攻毒时间节点定为 3、6、9、10 个月。结果显示,犊牛接种疫苗后10 个月仍能够同时抵抗 A 型和B 型Pm 的攻击,可见该疫苗免疫持续期至少可达到10 个月,这也与预期相符。然而,考虑到牛群中其它病原混合感染等应激因素,为保证牛持续处于最佳免疫状态,在实际应用时,二价灭活疫苗的免疫持续期定为9 个月。
综上所述,本研究在前期建立的荚膜A 型Pm免疫攻毒模型的基础上,联合A 型和B 型Pm 菌株研制牛Pm 病二价灭活疫苗,该二价疫苗对牛安全、有效,可以同时预防牛纤维素性化脓性肺炎和牛出血性败血症,该疫苗将对全面有效地控制我国的牛多Pm 病疫情具有重要价值。
