磁性分子印迹聚合物在食品安全检测领域的研究与应用
2019-02-16高婉茹黄昭李跑覃思曹亚男刘霞
高婉茹,黄昭,李跑,覃思,曹亚男,刘霞
(湖南农业大学食品科学技术学院食品科学与生物技术湖南省重点实验室,湖南长沙410000)
食品安全问题,一直以来都是人民群众和政府高度重视的问题。如果蔬中的农药残留、牛奶等乳制品中的抗生素残留,以及非法添加违禁物或过量使用食品添加剂等,这不仅会给消费者健康带来潜在威胁,也会限制我国食品的出口贸易。检测技术是食品安全预防与控制的重要支撑技术。虽然食品安全的检测方法有很多,如化学法、免疫法、光谱法、色谱法及传感器法等,但也常常受到准确度、灵敏度、检测时间、基质干扰和样品前处理费时等问题的制约。对于食品等具有复杂基质的样品,直接测定痕量污染物还比较困难,若对其采用适当的样品前处理技术,可降低基质干扰,有效富集分离样品中的待测物,可提高后续检测结果的准确度和灵敏度。因此开发灵敏、简便、准确的前处理技术,是当下的任务和需求所在[1]。磁性分子印迹聚合物即为一种方便有效,可通过外部磁场对待测物选择性富集分离的材料,该聚合物的应用极大的推动了食品安全检测领域的发展。本文简要介绍分子印迹技术的原理,及磁性分子印迹聚合物的制备方法;综述磁性分子印迹聚合物在食品安全检测领域的相关研究进展,并对其发展趋势进行展望。
1 磁性分子印迹聚合物简介
1.1 分子印迹聚合物
分子印迹技术(molecular imprinting technology,MIT)是指对某一特定的目标分子,具有特异性识别的聚合物制备技术,其工作原理常被比喻为“锁钥模型”。该技术与以往的样品分离提纯方法相比,具有制备简单、特异性强和应用广泛等优点。分子印迹聚合物(molecularly imprinted polymers,MIPs)的制备,主要是通过以下方式实现的[2-4]:1)使模板分子与功能单体之间通过共价键或非共价键结合,形成稳定的模板分子-功能单体复合物;2)在模板分子-功能单体复合物中加入交联剂,引发剂,以光或热引发,使模板分子-功能单体复合物周围产生聚合反应,形成高度交联刚性的分子印迹聚合物。在此过程中,聚合物链通过自由基聚合将模板分子-功能单体复合物“捕获”到聚合物的立体结构中;3)将聚合物中的模板分子,通过适当的方法洗脱或解离出来,形成具有识别模板分子的特异结合位点。由于该技术具有量身定做、制备简单,稳定且可反复使用的优势[5],目前已被广泛应用在分离提纯[6-7]、免疫分析[8]、化学传感[9-10]、食品安全[11-12]、环境检测[13-14]和药物分析[15]等领域。
1.2 磁性纳米颗粒
磁性纳米颗粒由于其特有的物理化学性质,可通过外部磁场,从体系中快速分离,操作简单且易于分离[16-18],其主要包括:金属氧化物、纯金属、磁性合金及其他磁性化合物。目前,Fe3O4纳米粒子由于具有制备方法简单、价廉易得、低毒,在外加磁场下具有可控运动等优点,已被广泛用作制备分子印迹聚合物的磁性载体[19-21]。
1.3 磁性分子印迹聚合物
磁性分子印迹聚合物(magnetic molecularly imprinted polymers,MMIPs)是将磁性材料与分子印迹技术相结合,得到兼具磁性快速分离和分子识别特性的聚合物。该MMIPs解决了MIPs在实际应用中分离难、吸附量小的问题,有助于缩短检测时间,提高检测的准确度。
自从Ansell R J等[22]首次报道了在全氟化碳中,使用悬浮聚合方法制备出平均直径为13 μm的超顺MMIPs以来,关于MMIPs的研究得到迅速发展,其应用领域也在不断拓展。MMIPs的制备大致可分为以下4个步骤:1)制备出具有良好磁响应性能的磁性纳米颗粒;2)在磁性纳米颗粒表面接上双键和其他功能基团(如-NH2,-COOH 等),进行功能化修饰;3)在功能化磁性纳米颗粒表面进行分子印迹聚合反应;4)采用洗脱剂(如甲醇、乙酸等)对聚合物中的模板分子进行洗脱,制得具有特异性识别位点的MMIPs。
2 磁性分子印迹聚合物制备方法
早期的MIPs均采用本体聚合法制备,生成块状产物,经研磨、过筛后获得所需粒径的粒子,之后除去模板分子,得到聚合物粉体。由于该法制备的MIPs形状不规则且产率较低,所以基于磁性纳米颗粒为载体,制备粒径均一、大小可控、且具有优良磁响应性能的MMIPs受到研究者的广泛青睐。目前,已发展了多种MMIPs的制备方法,主要有悬浮聚合法、乳液聚合法、沉淀聚合法和表面印迹法等,方法各有优缺点(见表 1)。
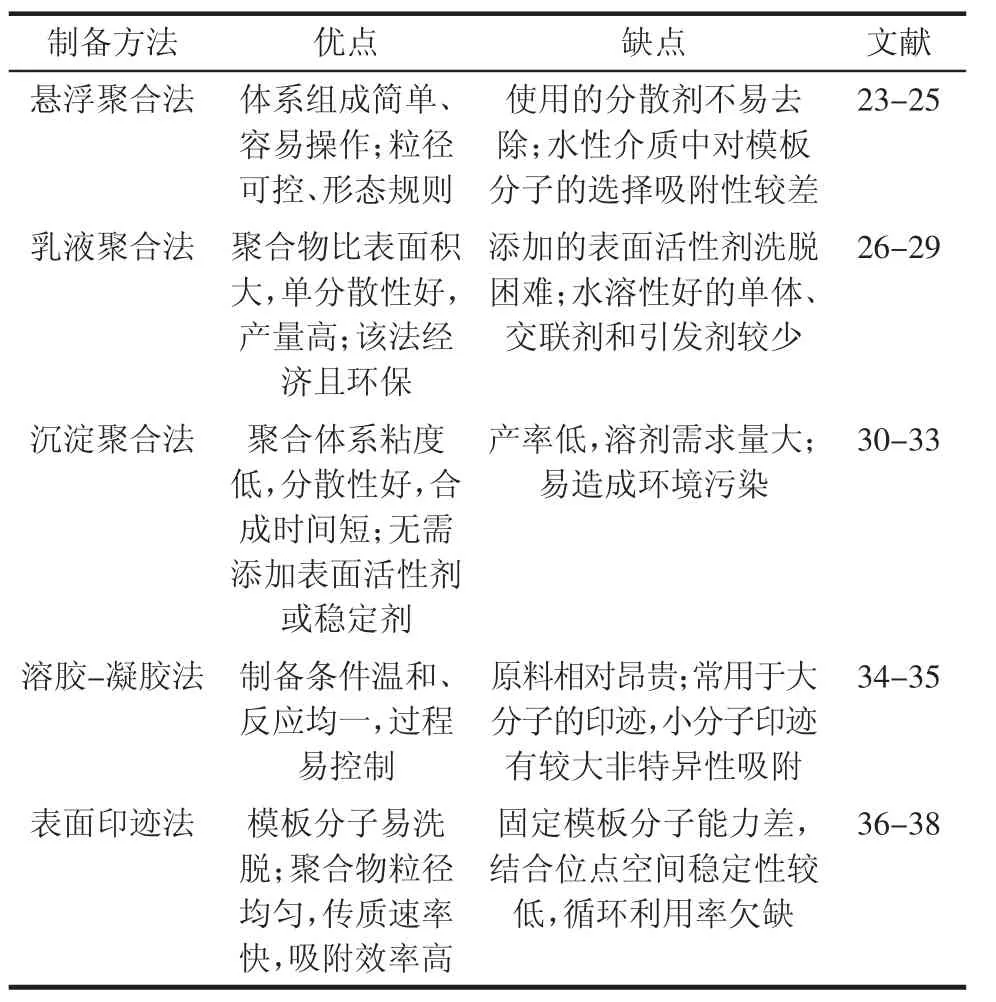
表1 磁性分子印迹聚合物制备方法的优缺点比较Table 1 Advantages and limitations of MMIPs preparation methods
2.1 悬浮聚合法
悬浮聚合法是将功能单体以液滴状悬浮于水或高极性溶剂中,通过加入引发剂引发自由基聚合反应的方法,也是制备MIPs常用且简便的方法之一。该法通常使用疏水性的功能单体,所以对溶剂的极性要求较高,而溶剂极性过高时会干扰模板分子和功能单体的非共价键作用,进而降低聚合物的识别能力。针对上述问题,Sellergren等[39]提出以乙醇作为分散剂的悬浮聚合法。此法不仅避免溶剂的强极性对识别能力的干扰,而且与本体聚合法相比,体系的聚合温度更容易控制,MIPs的吸附量高且吸附速率快。同样,为了避免悬浮聚合法对溶剂极性要求高的问题,Wang等[40]以2,4-二氯苯氧乙酸(2,4-D)为模板分子,甲基丙烯酸羟乙酯作为亲水性单体,在硅油中采用反向悬浮聚合法制备了亲水MMIPs。与疏水MMIPs[印迹因子(imprinting factor,IF)为 1.50]相比,该亲水 MMIPs[印迹因子(IF)为3.03]对模板分子具有更高的特异识别性[一般用印迹因子(IF)表示,IF值越大,对模板分子的特异性识别越好],使得模板分子洗脱后也更容易与其重新结合。该聚合物对于识别和分离天然水溶性分子及抗体、蛋白质等物质具有一定的潜力。
传统的悬浮聚合法反应时间一般在12 h以上。为了缩短反应时间,Hu等[41]采用微波热引发悬浮聚合法制备了MMIPs,并将其用作吸附剂,成功用于猪肉和猪肝中莱克多巴胺的富集分离。然后应用高效液相色谱(high performance liquid chromatography,HPLC)对其进行检测,检测限为0.52 ng/mL,猪肉和猪肝样品的加标回收率分别为82.0%~90.0%和80.4%~86.8%。该试验用微波加热替代传统加热,不仅显著缩短了MMIPs的制备时间(低于传统加热方式的1/10),而且MMIPs的磁性能和热稳定性均得到改善。虽然悬浮聚合法制备方法简单,且产物形态规则,然而试验过程中使用到的分散剂不易洗脱,而且该方法不适合高黏度的功能单体。
2.2 乳液聚合法
乳液聚合法能够在水环境中制得分散性良好的MIPs,可有效解决水溶性MIPs的制备问题。该法是功能单体借助乳化剂,在水中分散形成乳液状态的聚合过程,由此制得粒径较为均一的球状聚合物。Zhu等[28]采用三步微乳液聚合法制备了MMIPs,用于识别水杨酸。该聚合物的饱和磁化强度为33.584 emu/g,其中磁性纳米颗粒的包覆率为43.4%。该聚合物通过外部磁场,可在2 min内实现富集分离。乳液聚合法所制备的MMIPs,虽然具有减少有机溶剂用量,降低试验成本,减少环境污染等优点,但在聚合中加入的乳化剂不易被洗脱,一旦发生破乳现象,易产生漏磁现象。因此,Ou等[29]采用Pickering乳液聚合法制备MMIPs,用于样品中红霉素的富集分离。他们使用的是嵌入式磁性载体,不仅可以轻松地将该MMIPs从水溶液中分离出来,且内部的磁性载体不易发生漏磁现象。在3次以上的重复吸附-解吸重复循环中,该聚合物表现出优异的再生能力,吸附效率相比于首次吸附仅损失约5.04%。该方法为开发新的乳液聚合法合成MMIPs提供了新方向。但目前水溶性好的功能单体、交联剂和引发剂还较少。
2.3 沉淀聚合法
沉淀聚合法是指将模板分子、功能单体、交联剂和引发剂等溶解在溶剂中,采用加热等方法引发聚合,随着聚合反应的进行,聚合链逐渐增长,聚合物在溶剂中的溶解性逐渐降低而沉淀出来[33]。由于沉淀聚合法在反应体系中不需要加入任何活性剂或稳定剂,因此可制得表面干净的聚合物,同时也避免了活性剂或稳定剂对模板分子的非选择性吸附。Phutthawong等[42]以咖啡因为模板分子,通过超声辅助沉淀聚合法制备了MMIPs。该法中制备的MMIPs磁性颗粒无需功能化修饰或使用表面活性剂,且磁性颗粒的包覆率可达41.4%,可实现在外加磁场下的分离过程中,保持对模板分子的高特异选择性。Li等[43]通过可逆加成-断裂链转移(reversible addition-fragmentation chain transfer,RAFT)沉淀聚合法制备 MMIPs,用于选择性识别和去除17β-雌二醇。其制备流程及应用如图1所示,他们首先对制备的磁性纳米颗粒进行硅烷化修饰;然后采用RAFT沉淀聚合法制备MMIPs,除去模板分子后得到相对应的MMIPs;将其应用在磁性固相萃取(magnetic solid phase extraction,MSPE)中,循环吸附至少5次,且吸附效率并未明显下降。从环境和食品样品中富集和去除痕量17β-雌二醇的加标回收率在71.7%~108.3%之间。虽然上述这些沉淀聚合法减少了非特异性吸附,但与其他合成方法相比,具有产率较低、溶剂需求量大且毒性高的缺点,增加成本的同时还容易引起环境问题。
2.4 溶胶-凝胶法
溶胶-凝胶法是将溶胶-凝胶制备技术和分子印迹技术相结合,即在溶胶-凝胶过程中加入模板分子,具有特定官能团的前驱体和模板分子,通过主客体作用形成预组装体;在水解缩合反应中,模板分子被包埋到凝胶的空间三维结构内,得到溶胶-凝胶MIPs[44]。1949年Dickey[45]首次报道了一种制备溶胶-凝胶MIPs的方法。此后,该方法在MIPs的合成中得到了广泛关注。Kia等[35]先是采用共沉淀法制备SiO2功能化的磁性颗粒后,再用溶胶-凝胶法制备了MMIPs。SiO2层通过溶胶-凝胶增强了MIPs的吸附性能。该MMIPs可在60 min内将78%的甾醇从溶液中分离出来,其结合容量为19.5 mg/g。但溶胶-凝胶法的空间网络空隙大、较疏松,导致结合容量可能不够理想。且该法常用于大分子的印迹,小分子印迹会产生较大程度的非特异性吸附。
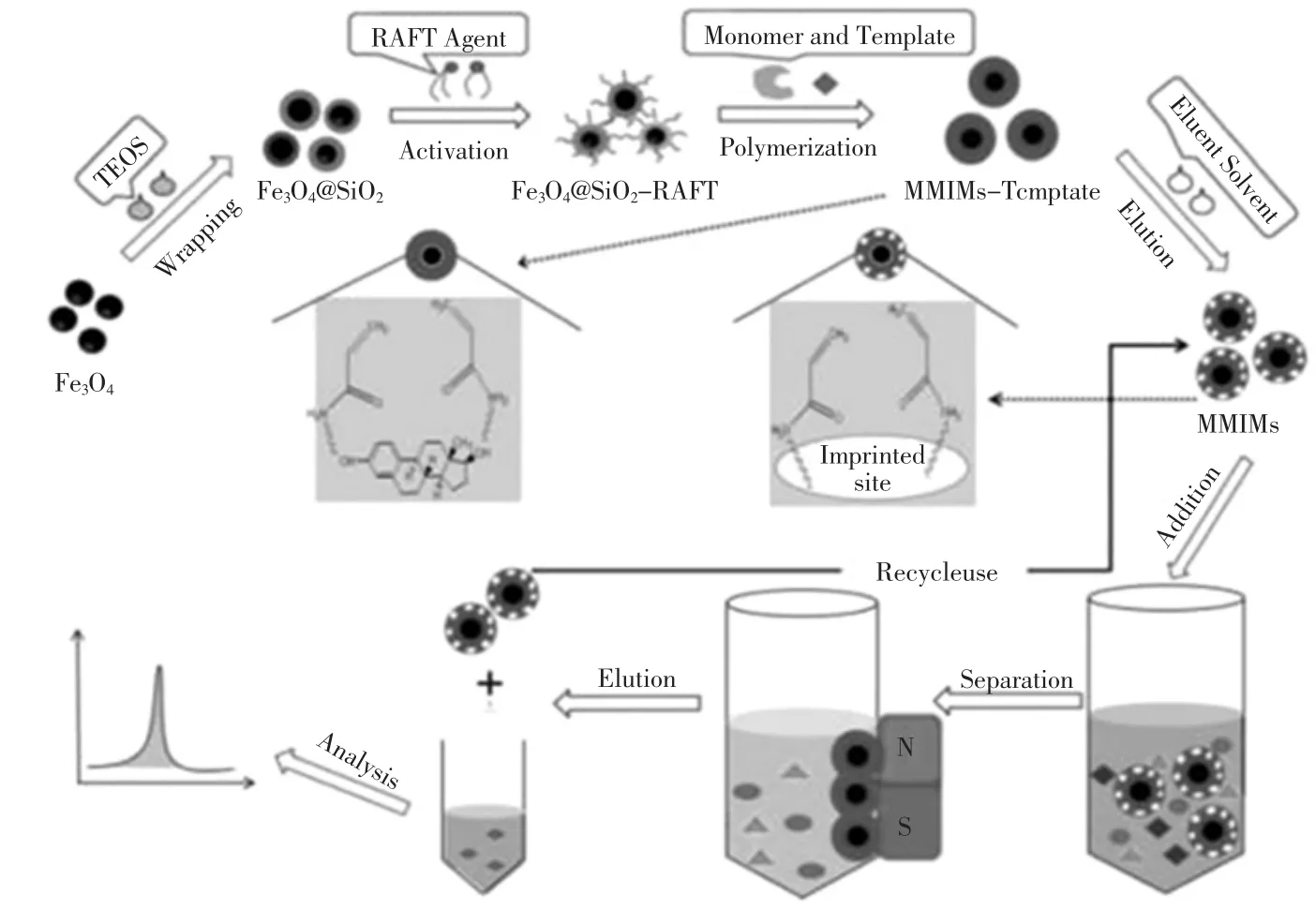
图1 RAFT沉淀聚合法制备MMIPs示意图及其在磁性固相萃取中的应用Fig.1 Preparation of MMIPs by RAFT precipitation polymerization and its application in MSPE
2.5 表面印迹法
表面印迹法是近几年新兴的一种合成分子印迹印迹聚合物的方法。一般是以固相基体为载体,在其表面发生聚合反应,从而形成表面MIPs的制备方法。表面印迹法制备的MMIPs,其大多数特异性结合位点分布在表面,有利于模板分子的去除和再结合,提高了印迹聚合物的吸附量和传质速率[46]。Gao等[47]通过表面印迹法,制备了用于检测痕量λ-三氟氯氰菊酯的荧光MMIPs。该聚合物同时具备分子识别、快速分离和对目标分子的荧光检测能力。将其吸附λ-三氟氯氰菊酯后进行荧光检测,其线性范围是0~50 nmol/L,相关系数为0.996 2。该试验不仅为实现非荧光菊酯类农药的选择性荧光检测提供了新的途径,而且为MMIPs在分析领域的应用提供了可能。先前的一些研究表明,以Fe3O4-石墨烯复合材料为底物的MIPs具有高特异性,更加利于分析物的识别和分离,但对于蛋白质方面的研究还较少,Chen等[38]以牛血清白蛋白(bovine serum albumin,BSA)为模板分子,采用表面印迹法在Fe3O4-氧化石墨烯(graphene oxide,GO)表面上,通过多巴胺(dopamine,DA)自聚合的方式,制备了用于高度识别和分离蛋白质的二维(2D)MMIPs。与具有相同体积的3D球形基底相比,2D Fe3O4-GO基底在表面积和体积比上更有优势,为大分子蛋白质的识别和分离提供便利。2D MMIPs的合成,为表面印迹技术提供了新方向,推动了MMIPs对蛋白质的识别和分离的应用。表面印迹法制备的聚合物,模板分子易洗脱,且有效减少包埋现象。但同时固定模板分子的能力下降,结合位点空间稳定性较低,循环利用率欠佳。
3 磁性分子印迹聚合物在食品安全检测领域的应用
3.1 农药残留
农药在保障、促进农作物的生长,满足人们对农副产品的需求等方面发挥着重要作用。若农药不规范使用,则导致农作物、土壤和水中农药残留量的超标。当人们长期摄入农药残留的食品后,会对健康造成潜在危害。
拟除虫菊酯类农药是农业上应用较为广泛的一类广谱杀虫剂。常规的样品前处理方法对食品中痕量拟除虫菊酯类农药的富集、分离效果并不理想,继而影响后续检测的准确度。Zhu等[48]利用Pickering乳液聚合法建立了稳定的水包油体系,其中油相中包括Fe3O4磁性纳米颗粒和模板分子λ-氯氟氰菊酯,以改性后的酵母在水相中作稳定剂,制备出吸附效率高,热、磁稳定性均良好的MMIPs。将此MMIPs用作选择性识别λ-氯氟氰菊酯的吸附剂,经过3次吸附-解吸循环后,其吸附容量约为第一次的87.99%,具有良好的再生能力,适合于实际应用。Yang等[49]以甲基丙烯酸(methacrylic acid,MAA)为功能单体,N-异丙基丙烯酰胺为热敏单体,采用Pickering乳液聚合法合成了联苯菊酯热敏/磁性分子印迹聚合物,并将其用作联苯菊酯选择性分离的吸附剂。通过透射电镜、红外光谱、热重分析及振动样品磁强计等系列表征,结果表明该热敏/磁分子印迹聚合物同时具备磁敏感性、磁稳定性和热稳定性。同时,在水溶液中,该热敏/磁分子印迹聚合物对联苯菊酯的吸附具有温度响应,为实际样品中联苯菊酯的吸附和分离提供了思路。
将MMIPs用作磁性固相萃取(magnetic solid phase extraction,MSPE)的吸附剂,可有效简化固相萃取的步骤,省时快速,同时具有较高的萃取能力和萃取效率,避免了传统固相萃取中,吸附剂装柱和样品上样等耗时问题[50]。将其与色谱检测技术相结合,可明显提高检测方法的准确度和灵敏度,得到更低的检测限,已用于农药残留检测领域。Cheng等[51]以滴滴涕为虚拟模板,采用水相悬浮聚合法制备了MMIPs。将该聚合物作为选择性吸附剂,建立了一种简单、快速的涡旋辅助磁性分散固相微萃取的方法,对茶产品中的三氯杀螨醇进行了提取分离,并通过气相色谱(gas chromatography,GC)进行检测,其线性范围是 0.2 ng/g~160 ng/g,检测限为0.05 ng/g。Kumar等[52]以Fe3O4纳米粒子作为磁性组分,采用沉淀聚合法合成了吡虫啉MMIPs。他们通过液相色谱-串联质谱法(liquid chromatographytandem mass spectrometry,LC-MS/MS),对加标茄子和蜂蜜样品中的吡虫啉进行检测,其检测限为0.05 μg/g,加标回收率分别为94.98%和94.15%。
采用传感器检测农药残留时,大多采用生物受体(如抗体、酶等)作为识别元件,存在生物分子价格昂贵、易失活及传感器使用寿命短等问题。相关学者致力于合成仿生抗体,将其代替生物受体作为传感器的识别元件。Tang等[53]基于Fe3O4羧基功能化的多壁碳纳米管/壳聚糖纳米复合物,利用溶胶-凝胶法制备了农药的分子印迹膜。将其作为特异性识别元件,开发了一种新型仿生电化学传感器。他们使用循环伏安法和差分脉冲伏安法研究了该印迹膜的性能,验证了方法的适用性和灵敏性,并成功用于加标菜豆和黄瓜样品中乙酰甲胺磷和敌百虫的检测,加标回收率在85.7%~94.9%间。该研究克服了分子印迹传感器响应时间长、信号稳定性差及识别力低等缺点,是食品中检测多种农药残留的新发展方向。
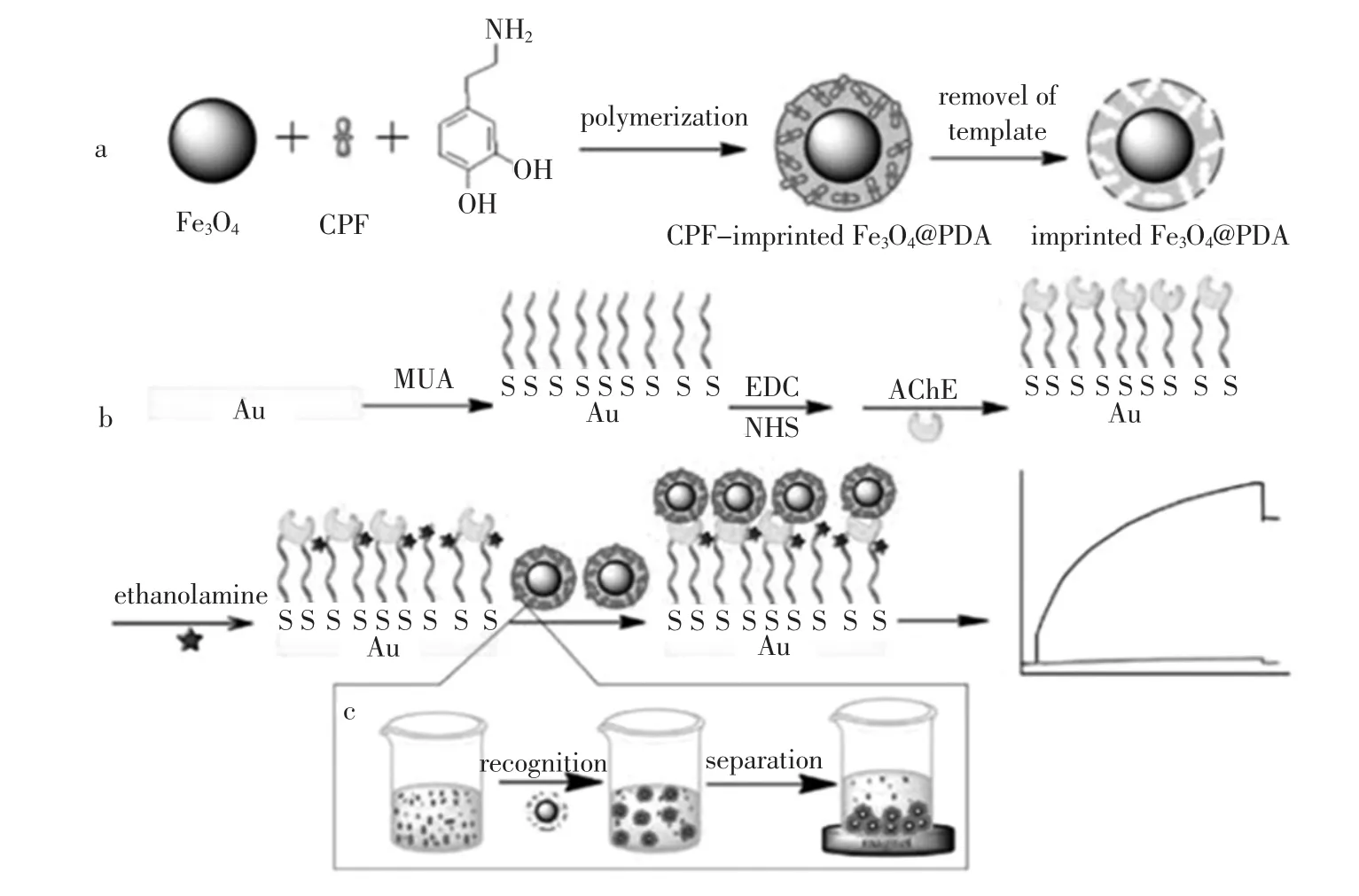
图2 毒死蜱MMIPs的制备及其在SPR传感器中的应用Fig.2 Preparation process of chlorpyrifos MMIPs and its application in SPR sensors
表面等离子体共振(surface plasmon resonance,SPR)传感器无需标记,具有易于微型化、实时监测和自动化等优点[54]。Yao等[55]将毒死蜱MMIPs与SPR传感器相结合,实现了食品中毒死蜱简单、快速且高选择性的检测。该MMIPs的制备(图2)是在模板分子毒死蜱的存在下,通过多巴胺自聚合的方式在Fe3O4纳米粒子表面制得。制备的MMIPs表现出优异的磁性能,借助外部磁场,高效、快速的将毒死蜱从样品中富集并分离。再将上述吸附了不同浓度毒死蜱MMIPs,直接注入特异性识别毒死蜱的乙酰胆碱酯酶修饰的SPR传感器中,对其进行检测。试验结果显示,SPR传感器的角度变化与毒死蜱浓度在 0.001 μmol/L~10 μmol/L内有着良好的线性关系,检测限为0.76 nmol/L。检测相同浓度的毒死蜱,上述SPR传感器的响应信号约为传统SPR传感器的64倍。该MMIPs既作为高特异性的毒死蜱识别受体,又作为放大器提高了SPR传感器的响应信号,该试验为简化样品前处理和传感器实时检测的完美结合提供了思路。
3.2 兽药残留
兽药常被用于预防、控制和治疗动物疾病或者有目的地调节动物生理机能,若不合理使用,易造成动物源食品中兽药的残留,不仅对畜牧业的发展造成了影响,且食用后对人体健康有着间接危害。
针对于改善样品中四环素类抗生素的富集分离效率问题,Chen等[56]以氯霉素为模板分子,合成了MMIPs,对6种蜂蜜样品中的氯霉素进行了吸附。采用40%的甲醇将氯霉素洗脱后,通过LC-MS/MS对其进行检测,最低检测限为0.047 ng/g,日内相对标准偏差(relative standarddeviation,RSD)和日间RSD分别为 4.1%~5.3%和2.9%~7.1%,样品回收率为84.3%~90.9%。Xu等[57]以氨基功能化的磁性纳米颗粒为载体,DA和BSA为双功能单体,制备了新型四环素类MMIPs。将其应用于选择性的富集和分离痕量四环素类抗生素,并采用HPLC对牛奶样品中的4种四环素类抗生素进行测定,其检测限为 1.02 μg/L~1.21 μg/L,回收率为 84.1%~95.8%,RSD小于6.7%。由于BSA的使用可以排除类似电荷的蛋白质,且促进小分子四环素类抗生素的吸附,因此该方法十分适用于直接从富含蛋白质的样品中选择性富集和分离目标物。
喹诺酮类抗菌药对多种革兰阴性菌具有杀菌作用,广泛的应用于呼吸道感染、胃肠疾病及其他相关疾病的治疗。然而它在人体内残留量低,不易被检出。Zheng等[58]利用化学氧化和溶剂热法制备了磁性纳米颗粒,将其与商品化的MIPs在甲醇中共混自发组装成氟喹诺酮类抗菌药的MMIPs,将其用作MSPE的吸附剂,建立了简便、高效检测牛奶中3种氟喹诺酮类的HPLC 方法,检测限为 1.8 μg/g~3.2 μg/g。该试验证明了本体聚合法制备的MIPs,可以通过简单共混的方式合成MMIPs。虽然该方法简单,但其实际应用仍需进一步研究。Wang等[59]采用悬浮聚合法合成了一种氧氟沙星MMIPs,用于分离和富集鱼类样品中氧氟沙星的对映异构体。在外加磁场下,MMIPs不仅可实现快速分离,也表现出对氧氟沙星对映异构体的高度特异性识别和结合能力(121.4mg/g)。将其作为MSPE的吸附剂,在最佳吸附与解吸条件下,HPLC对左氧氟沙星和右氧氟沙星的检测限分别为0.059 μg/mL和0.067 μg/mL。该研究表明MMIPs在MSPE中有良好的应用前景,有望替代传统固相萃取。
3.3 食品违禁添加物残留
食品中违禁添加物和滥用食品添加剂也是当下食品安全问题之一。卫生部现已公布包括47种可能在食品中违法添加的非食用物质,尚有20种无明确检测的方法。
三聚氰胺是一种被用作化工原料的三嗪类含氮杂环有机化合物,不可用于食品中。Anirudhan等[60]采用表面印迹法合成了三聚氰胺MMIPs,其饱和磁化强度为1.72 emu/g。静态、动态吸附实验表明,该聚合物对三聚氰胺的最大吸附容量为62.25 mg/g。采用HPLC对牛奶样品进行了测定,验证了该MMIPs作为牛奶中三聚氰胺吸附剂的可行性。该聚合物即使在大量干扰物(如牛奶中蛋白质、脂肪等)的存在下,依然表现出对三聚氰胺的高识别能力,高吸附容量及优良的质量传递速率。但表面印迹法制备的MMIPs,存在结合位点的稳定性较弱、循环利用率较低等问题。为改善上述问题,Zhao等[61]采用水热法制备了三维(3D)磁性石墨烯-碳纳米管杂化复合物,然后将该复合物作为载体,合成了3D三聚氰胺MMIPs。由于3D MMIPs的比表面积更大,使其具有更大的吸附容量(123.1 mg/g),传质效率更快,10 min内即可完成吸附。将其用作奶粉中三聚氰胺的吸附剂,采用超高效液相色谱-串联质谱法进行检测,最低检测限为0.000 45 mg/kg,三聚氰胺的回收率在90.3%~95.7%范围内,适用于痕量三聚氰胺的测定。随后他们采用该方法对6种奶粉样品中的三聚氰胺进行了检测。该3D MMIPs的吸附量和吸附效率明显优于普通方法制备的MMIPs,且有机溶剂消耗少。通常,采用HPLC进行检测,不仅操作复杂且对样品的纯度要求较高。此外,检测前需将分析物从MMIPs上洗脱下来,这极有可能导致结果的不准确性。针对此问题,You等[62]构建了一种基于磁性组装分子印迹光子晶体比色传感器,对三聚氰胺的含量进行检测。他们以MAA和丙烯酰胺为双功能单体,采用微乳液聚合法制备了三聚氰胺MMIPs。将MMIPs对三聚氰胺进行吸附后,直接通入光子晶体比色传感器,该传感器可将MMIPs引起的磁响应信号转换为光学信号,肉眼可见的对三聚氰胺进行了定性及半定量的分析,其检测限为10-5mg/mL。这种方法与经典的HPLC仪器分析相比,具有操作简便,实时性好等优点,但如何提高其选择性和稳定性,是推动其在实际样品检测中应用的关键所在。
苏丹染料是一种具有基因毒性致癌的化学染料,不允许以任何目的或含量出现在食品中。Piao等[63]以MAA为功能单体,利用表面印迹法制备出苏丹IVMMIPs,用于从辣椒粉样品中分离苏丹染料。通过等温吸附实验,动力学吸附实验,考察了MMIPs的吸附性和选择性。将最佳条件下制备的MMIPs对苏丹染料富集分离后,通过HPLC检测,4种苏丹染料的检测限分别为6.2、1.6、4.3 ng/g 和 4.5 ng/g。该试验证明利用 MMIPs,能够快速、高效的将辣椒粉样品中的苏丹染料分离出来,且减少了有机溶剂的使用,缩短了分析时间。
邻苯二甲酸酯类(phthalate esters,PAEs)是最为常见的塑化剂,长期摄入或在人体中积累,会对人体的肾脏、肝脏等造成损伤,对人体健康构成危害。Qiao等[64]针对塑化剂问题,以邻苯二甲酸二异壬酯为模板分子,通过悬浮聚合法制备出虚拟MMIPs。将其用作固相萃取的吸附剂,采用GC测定了塑料瓶装饮料中的PAEs,并成功的从塑料瓶装饮料中提取和分离出5种PAEs。
3.4 重金属残留
随着现代化工业进程的加快,重金属如汞、铬、镉、铅、砷等残留在环境及食物链中逐渐富集,通过农畜产品进入人体内,长期累积可造成慢性中毒。
原子吸收光谱法是重金属检测的常用方法,需要对样品进行消化,存在基质干扰较大、灵敏度不高等缺陷。近年来,相关研究者通过采用磁性离子印迹聚合物(magnetic ion imprinted polymers,MIIPs)对样品进行预处理,从而达到对食品中痕量重金属的快速分析测定。Aboufazeli等[65]制备了磁性多孔硅胶纳米Pb(Ⅱ)离子印迹聚合物,其对Pb(Ⅱ)离子的最大吸附容量为68.1 mg/g。结合火焰原子吸收光谱(flame atomic absorption spectrometry,FAAS)对痕量 Pb(Ⅱ)离子污染的食品进行了检测,检测限低于1.3 μg/L。由于该吸附剂的特异选择性,使其成为优于FAAS直接测定Pb(Ⅱ)离子含量的方法。Asgharinezhad等[66]合成磁性Ni(Ⅱ)离子印迹聚合物,用于快速提取、富集和测定果蔬及鱼中的微量Ni(Ⅱ)离子。他们采用响应面法,对吸附的pH值(8.0)、吸附时间(10 min)和磁性Ni(Ⅱ)离子印迹聚合物的用量(7.0 mg)进行了选择,同时优化了洗脱步骤。通过FAAS定量测定了其含量,检测限为0.25 μg/L,RSD小于10%。该磁性Ni(Ⅱ)离子印迹聚合物作为吸附剂,具有良好的稳定性,可重复使用15次,将其用于不同实际样品中微量Ni(Ⅱ)离子的提取,获得了良好结果。Jalilian等[67]以Fe3O4@SiO2@TiO2磁性纳米颗粒作为载体,运用溶胶-凝胶法,制备了粒径约45 nm~75 nm的磁性Ag(I)离子印迹聚合物。该聚合物可在6个吸附-解吸循环中重复使用,最大吸附容量为62.5 mg/g,6次使用后吸附能力降低约6%。将其结合FAAS对Ag(I)离子进行检测,检测限为0.5 ng/mL。此试验制备的磁性Ag(I)离子印迹聚合物,相比于具有相同电荷和相似离子半径的干扰离子(如K+、Na+及 Cd2+等),对 Ag(I)离子表现出优越的选择性,适用于萃取食品样品中微量的Ag(I)离子。
电感耦合等离子体发射光谱法(inductively coupled plasma optical emission spectrometer,ICP-OES)同样是重金属检测的方法之一,与FAAS相比,具有分析速度快、灵敏度高等优势,它的发展将检测限提高了5倍~10倍。Najafi等[68]制备了粒径60 nm的磁性Hg(Ⅱ)离子印迹聚合物,其最大吸附容量为(147±2)mg/g。该聚合物因其准确性及特异选择性,成为食品样品中Hg(Ⅱ)离子提取和预浓缩的合适吸附剂。利用ICPOES,对标准参考物质中微量的Hg(Ⅱ)离子进行测定,其检测限为0.03 μg/mL,回收率为98.3%,RSD为1.47%。随后该方法成功用于多种鱼样品中微量Hg(Ⅱ)离子的测定。
4 结论与展望
MMIPs是近年来发展的一种新型功能材料,具有良好的超顺磁性和特异选择性等特点。目前有关磁性分子印迹材料的研究日益完善,但仍存在一些问题,例如:1)大多数MMIPs主要在有机相中制备和应用,而在水环境中识别性能或吸附容量较低;2)聚合物对磁性颗粒有效包覆率不高,依然存在漏磁现象,其稳定性有待提高;3)功能单体和交联剂种类较少,开发新型功能单体有助于提高MMIPs特异识别性及稳定性。今后的研究应主要集中在以下方面:1)开发先进的MMIPs的制备方法,同时改进表面印迹技术,提高表面印迹层的印迹效率。有效提高聚合物对磁性颗粒的包覆率,提高聚合物的稳定性、磁响应性和特异性。2)深化分子印迹的识别机理,探索温和的制备条件,简化制备步骤,以扩大MMIPs对不同类型分子的识别,这对其在不同研究领域的应用具有重要意义。3)加强MMIPs与其他分析方法和检测仪器的联用,节省分析时间,提高检测效率,拓宽检测范围,使其在快速富集检测痕量分析物方面具有更广阔的发展。
