次氯酸钠氧化—磷酸铵镁沉淀法处理草甘膦废水并回收磷
2018-01-08李永峰朱利军贺子良刘锐平
李永峰,王 欢,,朱利军 ,贺子良,刘锐平
(1. 东北林业大学 林学院,黑龙江 哈尔滨 150040;2. 中国科学院 生态环境研究中心饮用水科学与技术重点实验室,北京 100085)
草甘膦作为一种广谱、低毒、高效的内吸传导性除草剂被广泛应用。我国是草甘膦生产和出口大国,产能已接近1 Mt/a[1]。草甘膦生产普遍采用甘氨酸法、亚氨基二乙酸法工艺[2],会产生大量磷浓度高、难降解的废水。另一方面,磷矿作为不可再生资源日益枯竭,而磷需求量逐年稳步提高。因此,含磷废水处理由传统的“除磷”模式转向“磷回收”模式势在必行。
“磷回收”具有较好的技术经济可行性[3]。如果农药厂废水中的草甘膦直接进入生化系统则可能与微生物体内的DNA、RNA和蛋白质反应,显著抑制污泥活性[4]。筛选驯化草甘膦降解菌株有望提高其对毒性的耐受性,但要实现规模化应用仍有许多限制因素[5]。吸附[6]、沉淀[7]、Fenton氧化[8]等物理化学方法存在吸附剂再生困难、污泥量过高等不利因素。草甘膦分子较不稳定,容易被氧化生成磷酸盐[9],而次氯酸钠具有较强的氧化性[10],无污泥产生,且成本较低,具有应用前景。将草甘膦转化为无机磷后再进行回收,可避免对生化系统的影响,且具有很好的经济价值。研究发现磷酸铵镁沉淀法可有效回收废水中的磷酸盐[11-13]。磷酸铵镁中磷含量高达51.8%(以P2O5质量分数计),是优质的缓释肥。
本研究采用次氯酸钠氧化草甘膦得到磷酸盐,再采用磷酸铵镁沉淀法回收磷,考察了次氯酸钠加入量、溶液pH、氧化时间等工艺条件对草甘膦氧化效果的影响,探讨了草甘膦废水处理与磷回收的可行性。
1 实验部分
1.1 材料、试剂和仪器
草甘膦溶液(纯度95%,美国阿达玛斯公司提供),pH = 4.93,质量浓度16.38 g/L。实验用水为超纯水。二氯甲烷为色谱纯,实验所用其他试剂均为分析纯。硅烷化试剂∶双(三甲基硅烷基)三氟乙酰胺(BSTFA)与三甲基氯硅烷(TMCS)体积比99∶1。
D8 venture型X射线衍射仪:布鲁克公司;U-4100型紫外-可见分光光度计:日立公司;TOC-V CPN型总有机碳分析仪:岛津公司;7890A/5975C型气相色谱-质谱(GC-MS)联用仪:安捷伦公司。
1.2 实验方法
1.2.1 次氯酸钠氧化草甘膦
在草甘膦溶液初始质量浓度为16.38 g/L、一定的溶液pH条件下,加入一定量的次氯酸钠溶液,在转速200 r/min的磁力搅拌下反应一段时间,每间隔一定时间取样测定草甘膦的质量浓度,计算草甘膦转化率。
1.2.2 氧化产物分析
在草甘膦溶液初始质量浓度为50.00 mg/L、溶液pH为9、次氯酸钠加入量为109 g/L的条件下,反应20 min后用亚硫酸钠猝灭。取样冷冻干燥,将所得固体粉末溶于5.00 mL二氯甲烷中,加入0.10 mL硅烷化试剂(BSTFA-TMCS),在60 ℃水浴中硅烷化反应60 min。采用无水硫酸钠(使用前450 ℃煅烧4 h)脱水,经0.45 μm膜过滤器过滤,氮气吹扫浓缩为1.00 mL转移至样品瓶中,采用GC-MS联用仪进行分析。
升温程序:50 ℃保持3 min;以5 ℃/min升温至150 ℃,保持5 min;以5 ℃/min升温至250 ℃,保持20 min。进样口温度为250 ℃,载气为高纯氦气,气流量为1 mL/min。
1.2.3 磷酸铵镁沉淀法回收磷
次氯酸钠氧化草甘膦后,磷主要以PO43-的形式存在。磷酸铵镁沉淀法回收磷的反应见式(1)。

磷酸铵镁的形成受溶液pH,Mg2+,,的质量浓度及反应时间等因素影响[14]。本实验采用正交实验的方法优化磷酸铵镁生成条件。选取溶液pH、镁磷摩尔比、氮磷摩尔比、反应时间4个主要影响因素,每个因素设置4个水平,考察指标为磷酸盐去除率。
采用XRD分析沉淀组成及磷酸铵镁含量,其中固体样品生成条件为溶液pH 9.0,镁磷摩尔比1.2,氮磷摩尔比1.4,氧化时间15 min。
1.3 分析方法
采用X射线衍射仪测定沉淀组成及磷酸铵镁含量;采用紫外-可见分光光度计测定PO43-质量浓度;采用总有机碳分析仪测定TOC;采用GC-MS联用仪分析有机物含量。
2 结果与讨论
2.1 次氯酸钠氧化草甘膦的工艺条件优化
2.1.1 次氯酸钠加入量
在溶液pH为4.9、氧化时间为60 min的条件下,次氯酸钠加入量对草甘膦转化率和TOC的影响见图1。由图1可见:随着次氯酸钠加入量的增加,草甘膦转化率先逐渐升高;当次氯酸钠加入量为109 g/L时,草甘膦转化率达98.2%;继续增加次氯酸钠加入量,草甘膦转化率基本没有提高。由图1还可见:在草甘膦转化率快速升高阶段,溶液中的TOC较高;当次氯酸钠加入量为109 g/L时,TOC为3817.6 mg/L;当次氯酸钠加入量为259 g/L时,TOC降至2431.2 mg/L;继续增加次氯酸钠加入量,TOC变化不大。本实验次氯酸钠加入量选择109 g/L较适宜。

图1 次氯酸钠加入量对草甘膦转化率和TOC的影响
草甘膦转化率与TOC变化规律的不一致与次氯酸钠氧化机理有关。次氯酸钠氧化过程中,首先水解产生ClO-及HClO,由于ClO-价层电子对的空间构型高度不对称并且中心氯原子具有较大的电子势,导致其具有较强的获得电子的能力。另一方面,次氯酸钠可分解产生具有强氧化性的新生态氧原子[O][15]。次氯酸钠首先攻击草甘膦分子中的C—P键,含磷基团被氧化为磷酸根;之后,次氯酸钠才进攻其他有机基团,部分有机碳被转化为CO2。
2.1.2 溶液pH
在次氯酸钠加入量为109 g/L、氧化时间为60 min的条件下,溶液pH对草甘膦转化率的影响见图2。由图2可见:当溶液pH为7.0时,草甘膦转化率为99.5%;增大溶液pH至9.0时,草甘膦转化率为99.6%;再继续增大溶液pH,草甘膦转化率基本保持不变。本实验选择溶液pH为9.0较适宜。

图2 溶液pH对草甘膦转化率的影响
ClO-在酸性体系中的标准电极电势1.482 V)高于在碱性体系中但实验表明,碱性体系中草甘膦转化率高于酸性体系中的转化率,这主要是因为酸性条件下次氯酸钠存在以下反应:

ClO-与次氯酸钠较Cl2氧化能力更强。溶液pH为2.0时,Cl2为主要存在形态,随溶液pH增大,次氯酸钠与ClO-所占比例逐渐增大[16]。式(2)反应的摩尔吉布斯函数表明该反应在标准状态下可自发进行,且草甘膦氧化为放热反应,可进一步促进该反应进行。另一方面,溶液中H+可催化分解次氯酸钠[17],且pH越低反应越剧烈,pH每降低一个单位,有效氯分解速率提高20%左右。碱性体系下,次氯酸钠自分解速率显著降低,从而可以提高其有效利用率。
2.1.3 氧化时间
在次氯酸钠加入量为109 g/L、溶液pH为9.0的条件下,氧化时间对草甘膦转化率的影响见图3。由图3可见:随着氧化时间的延长,草甘膦转化率显著提高;氧化时间为2 min时,草甘膦转化率为76.8%;氧化时间为10 min时,草甘膦转化率为96.9%;氧化时间延长至15 min时,草甘膦转化率进一步提高至97.6%;氧化时间超过20 min后,进一步延长氧化时间,草甘膦转化率无明显变化。故本实验氧化时间控制在20 min即可。
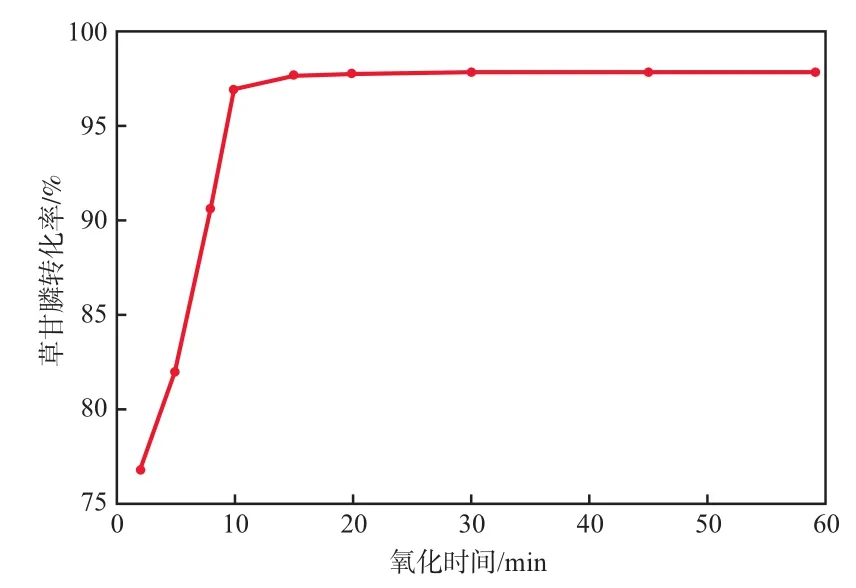
图3 氧化时间对草甘膦转化率的影响
2.2 次氯酸钠氧化草甘膦产物分析
次氯酸钠氧化草甘膦产物的总离子流图见图4。由图4可见,次氯酸钠氧化草甘膦的过程中生成了羟基乙酸、磷酸、乙酸等产物。进一步提出了次氯酸钠氧化草甘膦的主要降解途径为:C—N键断裂,生成羟基乙酸和乙酸;C—P键断裂生成磷酸。总离子流图中磷酸浓度最高,乙酸次之,羟基乙酸浓度最低。上述结果表明,C—P键断裂生成磷酸是主要反应,这对于后续磷的回收是有利的。
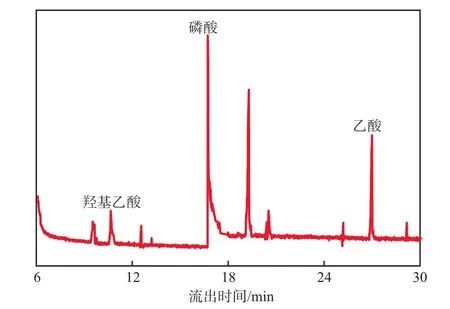
图4 次氯酸钠氧化草甘膦产物的总离子流图
2.3 磷酸铵镁沉淀法回收磷的正交实验结果
磷酸铵镁沉淀法回收磷的正交实验因素水平见表1。正交实验结果见表2。其方差分析结果见表3。

表1 磷酸铵镁沉淀法回收磷的正交实验因素水平
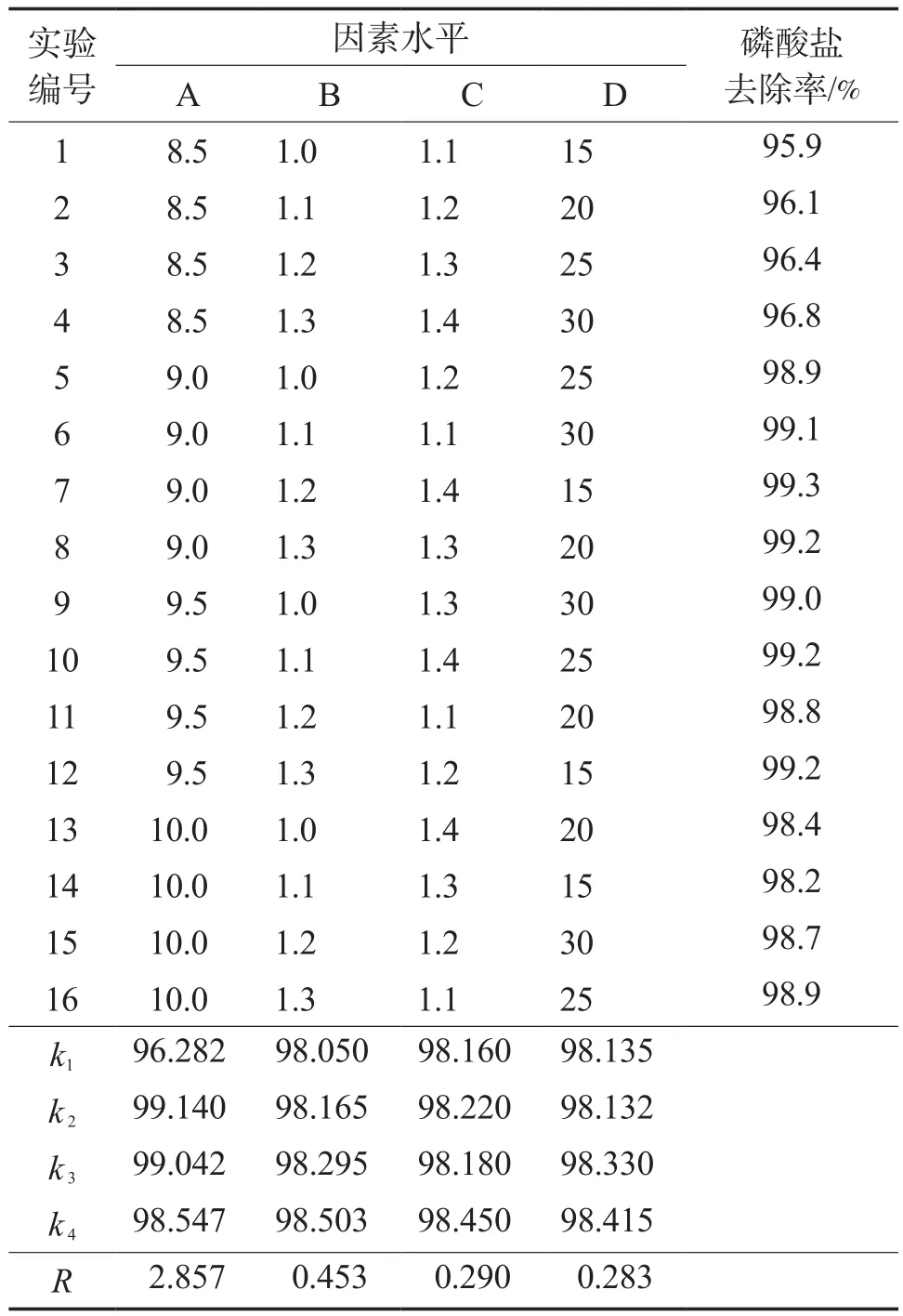
表2 正交实验结果

表3 正交实验方差分析表
正交实验结果表明,对磷回收影响大小的顺序为:溶液pH >镁磷摩尔比>氮磷摩尔比>反应时间。溶液pH对磷回收有显著影响,其F值与F临界值分别达到21.8237和7.226,这与前人的研究结果一致[18]。在本研究的实验条件下,镁磷摩尔比、氮磷摩尔比对应的F值小于1,表明其对磷回收无显著影响。正交实验得到的最佳工艺条件:溶液pH为9.0,镁磷摩尔比为1.2,氮磷摩尔比为1.4,反应时间为15 min,在此条件下磷酸盐回收率达99.3%。
采用XRD分析最佳工艺条件下所得固体沉淀的组成及磷酸铵镁含量,XRD谱图见图5。由图5可见,所得固体沉淀的X射线衍射特征峰与磷酸铵镁标准谱图(JCPDS:71-2089)的特征峰吻合,拟合度为87,证实所得固体主要成分为磷酸铵镁。

图5 最佳工艺条件下所得固体沉淀的XRD谱图
3 结论
a)采用次氯酸钠氧化草甘膦得到磷酸盐,再采用磷酸铵镁沉淀法回收磷。次氯酸钠氧化草甘膦的最佳工艺条件为:次氯酸钠加入量109 g/L,溶液pH为9.0,氧化时间20 min。
b)次氯酸钠氧化草甘膦的主要降解途径为:C—N键断裂生成羟基乙酸和乙酸;C—P键断裂生成磷酸。其中,C—P键断裂生成磷酸是主要反应。
c)正交实验得到的磷酸铵镁沉淀法回收磷的最佳工艺条件:溶液pH为9.0,镁磷摩尔比为1.2,氮磷摩尔比为1.4,反应时间为15 min,在此条件下磷酸盐回收率达99.3%。
d)所得固体沉淀的X射线衍射特征峰与磷酸铵镁标准谱图(JCPDS:71-2089)的特征峰吻合,证实所得固体主要成分为磷酸铵镁。
[1] 秦龙,姜胜宝,郑新,等. 草甘膦制剂废水的资源化利用工艺[J]. 农药,2015,54(6):411 - 413.
[2] 姜延雄,张悦,陈亚平,等. 草甘膦生产废水治理技术探讨[J]. 环境科技,2015,28(4):76 - 80.
[3] 付雄,刘敏,陈滢. 污泥灰中磷的湿化学法回收技术研究进展[J]. 化工环保,2017,37(3):276 - 281.
[4] Lu Zijin,Hegemann W. Anaerobic toxicity and biodegradation of formaldehyde in batch cultures[J].Water Res,1998,32(1):209 - 215.
[5] 王晓星,黄应平,邹雪,等. 草甘膦废水有机污染物的微生物降解[J]. 环境科学与技术,2010(8):28 -32.
[6] 谢明,徐炎华. 载铁活性炭对水中草甘膦吸附性能研究[J]. 中国环境科学,2011,31(2): 239 - 244.
[7] McConnell J S,Hossner L R. pH-dependent adsorption isotherms of glyphosate[J]. J Agricul Food Chem,1985,33(6):1075 - 1078.
[8] Huang Yingping,Li Jing,Ma Wandong,et al. Efficient H2O2oxidation of organic pollutants catalyzed by supported iron sulfophenylporphyrin under visible light irradiation[J]. J Phys Chem B,2004,108(22):7263 - 7270.
[9] 申元丽,马金锋,赵旭,等. 臭氧氧化降解除草剂草甘膦的实验研究[J]. 环境科学学报,2011,31(8):1647 - 1652.
[10] Veisi H. Sodium hypochlorite(NaOCl)[J]. Synlett,2007(16):2607 - 2608.
[11] Huang Haiming,Zhang Peng,Zhang Zhao,et al. Simultaneous removal of ammonia nitrogen and recovery of phosphate from swine wastewater by struvite electrochemical precipitation and recycling technology[J].J Cleaner Product,2016,127:302 - 310.
[12] Ishii S K L,Boyer T H. Life cycle comparison of centralized wastewater treatment and urine source separation with struvite precipitation:Focus on urine nutrient management[J]. Water Res,2015,79:88 - 103.
[13] Kataki S,West H,Clarke M,et al. Phosphorus recovery as struvite from farm,municipal and industrial waste:Feedstock suitability,methods and pre-treatments[J]. Waste Manage,2016,49:437 - 454.
[14] 郝晓地,衣兰凯,王崇臣. 磷回收技术的研发现状及发展趋势[J]. 环境科学学报,2010,30(5):897 - 907.
[15] 王万林. 次氯酸钠溶液稳定性研究进展[J]. 无机盐工业,2007,39(9):12 - 14.
[16] Nadupalli S,Koorbanally N,Jonnalagadda S B.Kinetics and mechanism of the oxidation of amaranth with hypochlorite[J]. J Phys Chem A,2011,115(27):7948 - 7954.
[17] 平静. 次氯酸钠溶液稳定性的研究[J]. 中国医院药学杂志,1995,15(10):455 - 456.
[18] Le Corre K S,Valsami-Jones E,Hobbs P,et al.Agglomeration of struvite crystals[J]. Water Res,2007,41(2):419 - 425.
