广藿香酮在大鼠体内的药动学研究
2014-03-15张若琪李芸霞彭成
张若琪,李芸霞,彭成
·药理毒理·
广藿香酮在大鼠体内的药动学研究
张若琪,李芸霞,彭成
目的:建立广藿香酮GC-MS测定方法,并进行药动学研究。方法:采用Agilent HP-5ms色谱柱(30 m × 0.25 mm i.d. × 0.25 μm,5 %苯基甲基硅氧烷);电子碰撞离子源(EI),电子倍增电压(EMV)模式,检测离子m/z 168.0。将大鼠分为高、中、低剂量组,分别灌胃给予大鼠广藿香酮4 mg.kg-1、8 mg.kg-1、16 mg.kg-1,测定不同时间点的血药浓度,绘制药时曲线,计算药动学参数。结果:广藿香酮高、中、低剂量Cmax分别为48.33±13.07 ng.mL-1、98.83 ±36.14 ng.mL-1、190.52 ±42.78 ng.mL-1、Tmax分别为1.33±0.52 h、1.33 ±0.52 h、1.16 ±0.41 h;t1/2z分别为4.91 ±1.03 h、4.64 ±1.23 h、4.29 ±1.49 h。结论:所用方法处理简单、灵敏、特异性高、定量准确,可为广藿香酮的药动学研究提供方法。大鼠口服广藿香酮4 mg.kg-1~16 mg.kg-1剂量范围内,药动学符合线性动力学过程。
]广藿香酮; 气相色谱串联质谱法; 血药浓度;药动学
广藿香油有多种药理活性,包括止吐作用、杀锥虫活性、抗细菌、抗真菌和Ca2+拮抗活性[1~3]。广藿香酮是广藿香的一个重要成分,药理研究表明,广藿香酮具有抗细菌和抗真菌[4]的活性。本实验采用GC-MS法,测定大鼠血浆中广藿香酮的浓度,并对广藿香酮灌胃给予大鼠的药动学进行研究。
1 实验部分
1.1 仪器与试药
Agilent 7890A气相色谱仪,Agilent 5975C串联质谱检测器,Agilent ChemStation软件(美国Agilent)。广藿香酮(Pogostone)标准品(自制,纯度分别为98 %);内标( internal standard, IS)为异土木香内酯标准品(上海一基生物试剂有限公司);甲醇为色谱纯;水为超纯水;其余试剂为分析纯。
1.2 方法与结果
1.2.1 色谱条件 采用Agilent HP-5ms色谱柱(30 m × 0.25 mm i.d. × 0.25 μm,5 %苯基甲基硅氧烷);升温程序为:起始柱温为110 ℃,保持1 min;以25 ℃.min-1升温至240 ℃ 并保持1 min;之后以35 ℃.min-1升温至280 ℃并保持1 min。质谱采用电子碰撞离子源(EI),电子倍增电压(EMV)模式,增益系数为1.01,实际EMV为1576.47 V。检测离子为:广藿香酮m/z 168.0,内标异土木香内酯m/z 190.1。
1.2.2 溶液的制备 分别称取适量广藿香酮和内标,用甲醇溶解配制成81.2和503.2 μg.mL-1的对照品贮备液,于4 °C冰箱中冷藏。用甲醇稀释贮备液,依次配制广藿香酮工作溶液:2.04、10.06、20.4、100.6、204.0、406.0、812.0 ng.mL-1;内标溶液:5.03 μg.mL-1。
于空白血浆中分别精密加入广藿香酮工作液和内标溶液,配成广藿香酮浓度为1.02, 5.03, 10.2, 50.3, 102.0, 203.0, 406.0 ng.mL-1的对照品血浆,内标的血浆浓度为0.503μg.mL-1。
四个浓度的质控样品(QC)于样品分析当天配制,广藿香酮的浓度依次为: 1.02 (LLQC)、5.03(LQC)、50.3 (MQC)、203 (HQC) ng.mL-1。
1.2.3 血浆样品的处理 于100 μL空白血浆中加入10μL内标溶液,再加入50μL对照品工作液,涡旋30 s后,加2 mL乙酸乙酯,涡旋3 min后于5.0×10 3 rpm离心10 min,取上清液,于30 ℃下氮气吹干,用100 μL甲醇复溶,于5.0×10 3 rpm离心10 min,取上清液进行GC-MS分析,进样量为1 μL。
1.2.4 专属性试验 取LLQC、LQC、MQC、HQC质控样本,按“1.2.3”项方法处理后,以“1.2.1”项色谱条件测定广藿香酮。图1所示为试验条件下的广藿香酮和内标的质谱图。在试验条件下,广藿香酮和内标的保留时间分别为6.1 min和7.4 min(图2),峰形良好。6份来自不同大鼠空白血浆样品经“1.2.3”项方法处理后,无明显干扰。
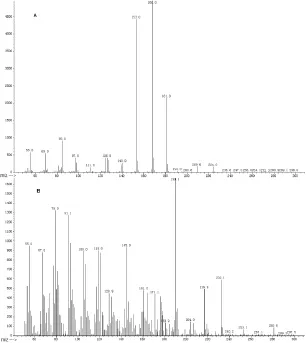
图1. 广藿香酮(A)和内标异土木香内酯(B)的EI-MS质谱图
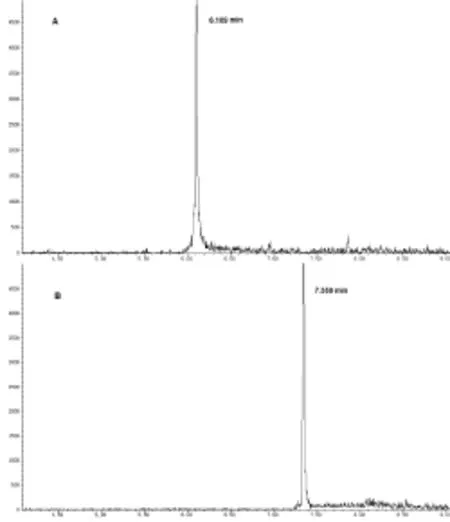
图2 广藿香酮m/z 168.0 (A) 和内标异土木香内酯m/z 190.1 (B)的GC-MS色谱图
1.2.5 标准曲线及定量下限 以待测物的峰面积与内标物的峰面积的比值对相应的待测物质量浓度(ng.mL-1) 做标准曲线。结果表明:广藿香酮血浆浓度的回归方程为: y=0.0968x-0.1273, r=0.9958,线性范围为1.02~406 ng.mL-1,最低定量限为1.02 ng.mL-1。
1.2.6 准确度及精密度 按“1.2.3”项方法操作,处理LLQC、LQC、MQC、HQC 4个浓度的:广藿香酮的QC样本,每浓度做 6个样本,连续测定 3 个分析批,以相应分析批的标准曲线计算混合 QC 样本中各待测物的浓度。结果表明:广藿香酮批内、批间的方法回收率分别在98.68-103.92 %和97.17-102.83 %以内,批内、批间精密度RSD均<8 %(表1) 。
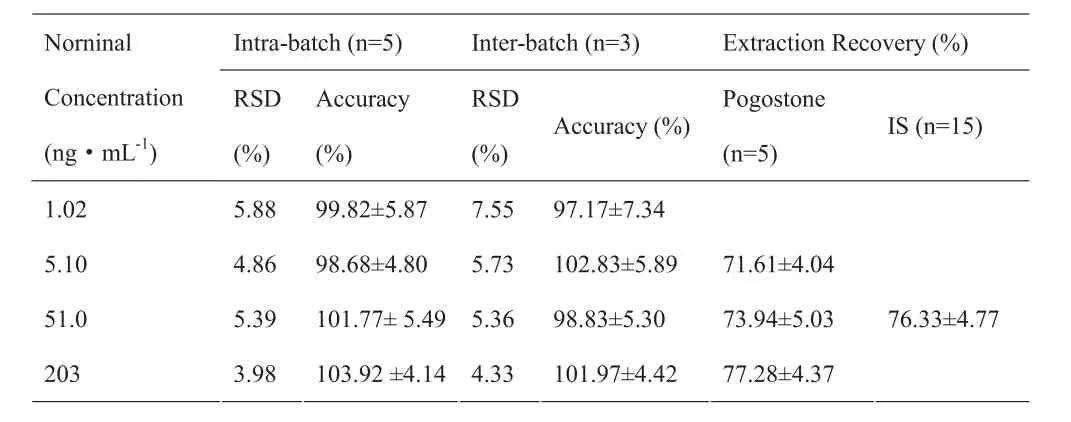
表1 广藿香酮大鼠血浆样品的准确度、精密度和萃取回收率
1.2.7 萃取回收率 按“1.2.3”项方法操作,处理血浆样品中广藿香酮LQC、MQC、HQC 3个浓度的质控样品进样分析后所得待测物的峰面积,与未萃取的样品进样分析后所得待测物的峰面积相比,计算萃取回收率。广藿香酮萃取回收率的平均值为74.3 % ;内标萃取回收率的平均值为 76.3 % ( 表 1) 。
1.2.8 稳定性试验 取LQC、MQC、HQC 3个浓度的广藿香酮的QC 样本,分别考察血浆样本于室温下放置 14 h、血浆样本经处理后在自动进样器中室温下放置 12 h、经 3 次冻融及- 20 ℃ 长期冰冻放置 21 d后的稳定性。表2显示,血浆样本在以上各种贮存条件下均稳定。
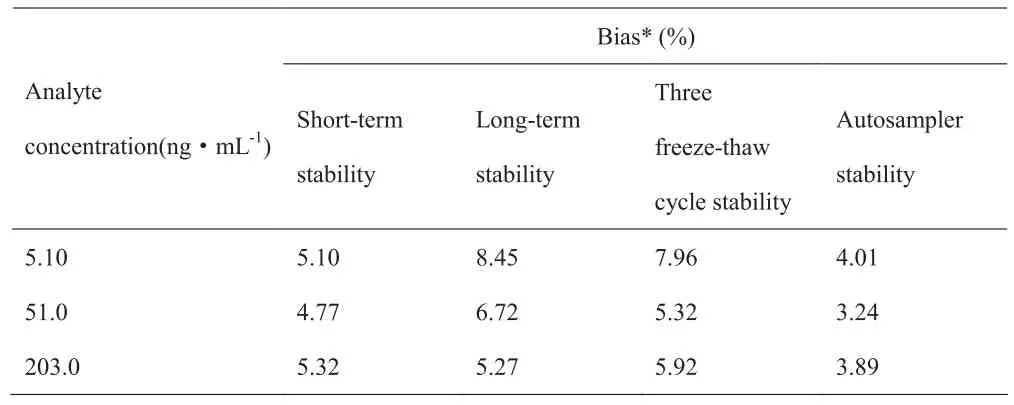
表2 广藿香酮大鼠血浆样品的稳定性 (n =3)
1.2.9 药动学实验 SD大鼠 (SPF, 雌性),体重200~220 g,购自成都中医药大学实验动物中心。试验前将大鼠适应性喂养3 d,全程不禁饮水。将18只大鼠分为高、中、低剂量组,分别灌胃给予大鼠广藿香酮4、8、16 mg/kg。于给药前及给药后5、15、30、45 min,1、2、4、6、9、12、16和24 h时,经眼眶取血0.3 mL,至于肝素离心管中。于5.0×103 rpm 离心10 min分离血浆,储存于-20 ℃冰柜中冷藏待测。按“1.2.3”项方法处理后,以“1.2.1”项色谱条件检测广藿香酮的浓度。所有数据均用Phoenix WinNonlin 6.3 (Pharsight Corporation, USA)软件处理,计算药动学参数,结果见表3。采用Newman-Keuls test对三个剂量之间AUC0-t/dose、Cmax/dose和t1/2z进行统计学分析;采用Wilcoxon t rank sum test对三个剂量的Tmax进行统计学分析。结果表明:灌胃给予大鼠广藿香酮4、8、16 mg.kg-1,Cmax分别为48.33±13.07、98.83 ±36.14、190.52 ±42.78 ng.mL-1;Tmax分别为1.33±0.52、1.33 ±0.52、1.16 ±0.41 h;t1/2z分别为4.91 ±1.03、4.64 ±1.23、4.29 ±1.49 h。经统计学分析,三个剂量下AUC0-t/dose、Cmax/dose、t1/2z和Tmax均无统计学差异,大鼠口服广藿香酮4-16 mg.kg-1剂量范围内,药动学符合线性动力学过程。平均药-时曲线见图3。
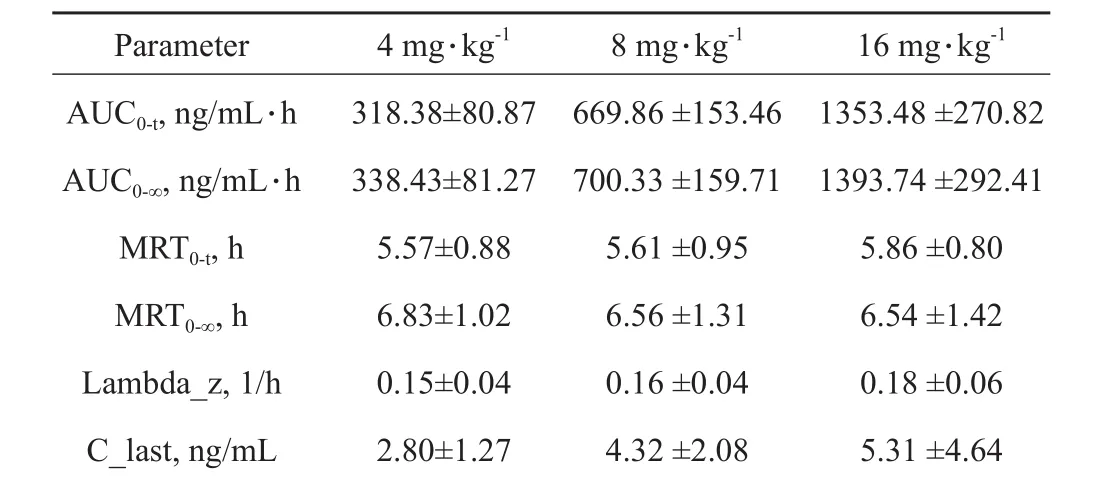
表3 大鼠灌胃给予广藿香酮的主要药动学参数(Mean ±SD , n = 6)

t1/2z, h 4.91 ±1.03 4.64 ±1.23 4.29 ±1.49 Tmax, h 1.33±0.52 1.33 ±0.52 1.16 ±0.41 Vz/F, L 17.19±4.13 15.47 ±3.57 14.56 ±5.45 CLz/F, L/h 2.47±0.53 2.38 ±0.52 2.37 ±0.47 Cmax, ng/mL 48.33±13.07 98.83 ±36.14 190.52 ±42.78
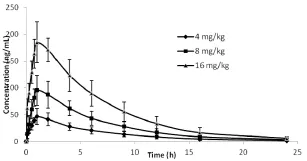
图3 大鼠灌胃给予广藿香酮的平均药-时曲线 (n= 6)
2 讨论
本实验采用GC-MS法测定大鼠血浆中广藿香酮的浓度,用异土木香内酯作为内标物,方法专属性高,保留时间合适,峰形良好,血浆样品处理采用液液萃取法,操作简单,适用于药动学的研究。广藿香酮见光不稳定,需避光保存。经统计学分析,高、中、低剂量下AUC0-t/dose、Cmax/dose、t1/2z和Tmax均无统计学差异,大鼠口服广藿香酮4~16 mg/kg剂量范围内,药动学符合线性动力学过程。随着剂量的增加,Cmax和AUC符合剂量依赖性,其增加的比例与剂量增加的比例一致。广藿香酮在大鼠体内吸收较快,血药浓度约1 h达到峰值,说明其具有良好的透膜性。
[1] Y. Yang, K. Kinoshita, K. Koyama, K. Takahashi, T. Tai, Y. Nunoura, K. Watanabe. Anti-emetic principles of Pogostemon cablin (Blanco) Benth [J]. Phytomedicine, 1999, 6:89.
[2] Fumiyuki Kiuchi, Kenji Matsuo, Michiho Ito, Tran Kim Qui, Gisho Honda. New Norditerpenoids with Trypanocidal Activity from Vitex trifolia [J]. Chemical and Pharmaceutical Bulletin, 2004, 52: 1495.
[3] 杨得坡, Chaumont Jean-Pierre, Millet Joeue, 等.藿香和广藿香挥发油对皮肤癣菌和条件致病真菌的抑制作用[J]. 中国药学杂志, 2000, 35(1): 9.
[4] Yi YY, He JJ, Su JQ, Kong SZ, Su JY, Li YC, Huang SH, Li CW, Lai XP and Su ZR. Synthesis and antimicrobial evaluation of pogostone and its analogues [J]. Fitoterapia, 2013, 84:135.
(责任编辑:何瑶)
Pharmacokinetic study of pogostone in rats after oral administration by GC/MS /
ZHANG Ruo-qi, LI Yun-xia, PENGCheng//( Pharmacy College, Chengdu University of Traditional Chinese Medicine; The Ministry of Education Key Laboratory of Standardization of Chinese Herbal Medicine; State Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources Co-founded by Sichuan Province and MOST, Chengdu 611137, China)
Objective: To establish a method for determination of pogostone in rat plasma by GC-MS and to apply it to the study on pharmacokinetics in rats.Method: The chromatographic separation was performed on a capillary column of Agilent HP-5ms, and the spectrometer was operated in electron-impact ionization with an electron multiplier voltage mode. Three dose groups of 4 mg.kg-1, 8 mg.kg-1, 16 mg.kg-1were adopted in the pharmacokinetic experiment. Concentration-time curves were obtained and the pharmacokinetic parameters were calculated. Result: After oral administration of pogostone in three doses, the Cmaxwere 48.33±13.07 ng.mL-1, 98.83 ±36.14 ng.mL-1, 190.52 ±42.78 ng.mL-1. And the Tmaxwere 1.33±0.52 h, 1.33 ±0.52 h, 1.16 ±0.41 h, respectively. Conclusion: The method is successfully applied to a pharmacokinetic study after the oral administration of pogostone to rats. The mean Cmax and AUC0-t values are both linear in the range of doses administered 4 mg.kg-1~16 mg.kg-1to rats.
Pogostone; GC-MS; plasma concentration; pharmacokinetics
R 285.5
A
1674-926X(2014)02-022-03
成都中医药大学药学院 中药材标准化教育部重点实验室 中药资源系统研究与开发利用省部共建国家重点实验室培育基地,四川 成都 611137
张若琪(1982-),女,河南偃师人,讲师,从事中药药动学研究
Tel:13882271228 Email: zrq1007@qq.com
彭成,教授,博士生导师,主要从事疾病动物模型与中药复方药理毒理研究和中药新药开发
2013-09-03
