2种喜树碱类拓扑异构酶1抑制剂ADE信号的挖掘与分析Δ
2024-05-14吴镇江刘建军白翔宇杨茂凡樊文海王攀杨钧淞川北医学院临床医学院四川南充67000川北医学院附属医院胃肠外科四川南充67000川北医学院附属医院重症医学科四川南充67000
吴镇江 ,刘建军 ,白翔宇 ,杨茂凡 ,樊文海 ,王攀 ,杨钧淞 (.川北医学院临床医学院,四川 南充 67000;.川北医学院附属医院胃肠外科,四川 南充 67000;.川北医学院附属医院重症医学科,四川 南充 67000)
拓扑异构酶(topoisomerase,TOP)是一种广泛存在于生物体中的多核酶,能够消除DNA在复制和转录过程中产生的扭转应力,松弛DNA超螺旋结构,在细胞DNA复制和转录过程中发挥重要作用[1―2]。现有研究表明,人类编码的TOP共有6种,包括TOP1、TOP1MT、TOP2α、TOP2β、TOP3α和TOP3β[2]。以TOP1为靶点的抗肿瘤药物具有良好的活性,包括喜树碱类、茚并异喹啉酮类、吲哚咔唑类等[3],其中喜树碱类TOP1抑制剂(目前在我国上市的有伊立替康和托泊替康)被广泛用于治疗转移性结直肠癌、肺癌、胃癌、卵巢癌和宫颈癌等疾病[1,4]。随着伊立替康和托泊替康的广泛应用,其引起的药物不良事件(adverse drug event,ADE)越来越受到业界关注。由于患者存在个体差异,给药方式及剂量等都不同,伊立替康和托泊替康引起的ADE也存在差异。研究表明,伊立替康常见的ADE有中性粒细胞减少症、腹泻、黏膜炎以及非酒精性脂肪性肝炎[5],还会引起构音障碍和视网膜病变[6―7]。托泊替康常见的ADE为骨髓抑制,其中30%发生骨髓抑制的患者会出现血小板减少症,80%的骨髓抑制患者会出现严重中性粒细胞减少症进而危及生命[2]。
为进一步了解伊立替康和托泊替康的ADE发生特点,为临床安全使用喜树碱类TOP1抑制剂提供数据参考,本研究基于美国FDA不良事件报告系统(adverse events reporting system,FAERS)数据库中的公开信息,收集了伊立替康和托泊替康相关的ADE报告,挖掘了潜在的ADE信号并对其进行了分析。
1 资料与方法
1.1 数据来源
本研究基于美国FAERS数据库下载了2004年1月1日建库开始至2023年3月31日的原始数据,包括患者人口统计学和管理信息(DEMO)、药物信息(DRUG)、给药适应证(INDI)、患者结局(OUTC)、不良事件(REAC)、报告来源(RPSR)、报告药物的治疗开始日期和结束日期(THER)数据包。
1.2 数据处理
根据美国FDA推荐的去除重复报告的方法,选取DEMO表的PRIMARYID、CASEID和FDA_DT字段,按照CASEID、FDA_DT以及PRIMARYID排序,若CASEID相同,则保留FDA_DT值最大的报告;若CASEID和FDA_DT均相同,则保留PRIMARYID值最大的报告。自2019年第1季度后,每个季度的数据包中均存在官方说明的删除报告列表,故本研究在数据去重后,根据删除报告列表中的CASEID剔除相应报告。然后,本研究使用《监管活动医学词典》(MedicalDictionary forRegulatoryActivities,MedDRA)映射报告中涉及的首选术语(preferred terms,PT)对所选ADE进行分类整理,并将其匹配到相应的系统器官分类(system organ class,SOC)。分别限制伊立替康和托泊替康的通用名为“Irinotecan”和“Camptosar”,商品名为“Topotecan”和“Hycamtin”,并对drugname和prod_aid字段进行模糊匹配,从而筛选出以伊立替康和托泊替康为首要怀疑药物的ADE报告。
1.3 数据挖掘
国际上常采用比例失衡测量法中的报告比值比(reporting odds ratio,ROR)法对ADE信号进行挖掘,当报告数≥3且95%置信区间(confidence interval,CI)下限>1,则提示生成1个阳性信号[8]。其优点是计算相对便捷,但假阳性较高且稳定性低。贝叶斯置信传播神经网络(Bayesian confidence progressive neural network,BCPNN)法的计算相对复杂,但其特异度较高。其检测指标为信息成分(information component,IC)值,当IC下限(即IC-2SD)>0,则提示生成1个阳性信号[9]。本研究采用ROR法联合BCPNN法进行信号挖掘(同时满足2种方法的检出标准算作1个阳性信号),以此降低假阳性率。
2 结果
2.1 ADE报告的一般情况
本研究从美国FAERS数据库中共收集到19 514 140份ADE报告。经去重、剔除官方说明的报告后,对2014年第3季度及之前的数据按照drugname字段进行筛选,对2014年第3季度之后的数据根据drugname和prod_aid字段进行筛选(prod_aid是美国FAERS数据库在2014年第3季度后才新增的字段),共筛选出相关ADE报告14 738份,其中伊立替康11 483份、托泊替康3 255份。伊立替康ADE报告中的性别以男性为主(构成比45.17%),托泊替康以女性为主(构成比51.77%);两药使用患者年龄均主要集中于45~<75岁。伊立替康的ADE报告主要来自美国、日本和法国;托泊替康的ADE报告主要来自美国、日本和德国。伊立替康和托泊替康ADE报告的一般情况详见图1、表1。

图1 伊立替康和托泊替康ADE报告趋势图

表1 伊立替康和托泊替康ADE报告的基本信息
2.2 ADE信号累及SOC分布
本研究通过ROR法联合BCPNN法进行ADE信号挖掘,检测出ADE信号所累及SOC共24个,其中伊立替康累及24个SOC,托泊替康累及22个SOC。伊立替康ADE累及SOC排前5位的分别是胃肠系统疾病、全身性疾病及给药部位各种反应、血液及淋巴系统疾病、各类神经系统疾病、各类检查;托泊替康ADE累及SOC排前5位的分别是全身性疾病及给药部位各种反应,各类检查,血液及淋巴系统疾病,胃肠系统疾病,呼吸系统、胸及纵隔疾病。结果详见图2、表2。
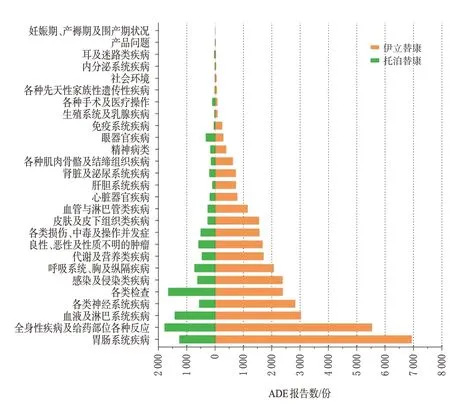
图2 伊立替康和托泊替康ADE报告累及SOC分布
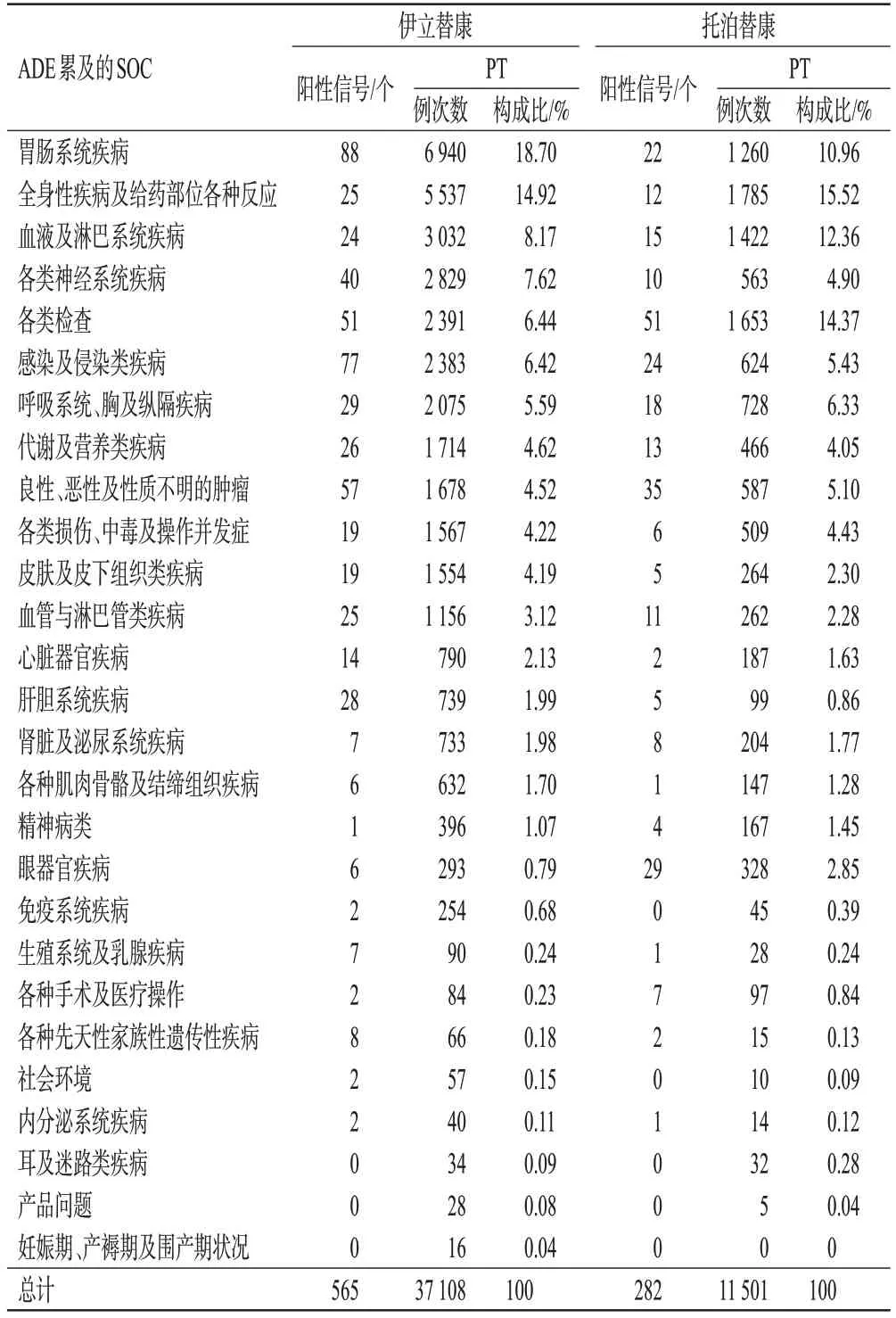
表2 伊立替康和托泊替康ADE累及SOC的检出信号情况
2.3 ADE信号特征
本研究采用ROR法联合BCPNN法共检测出阳性信号847个,其中伊立替康565个、托泊替康282个(表2)。根据ADE报告频数和信号强度(IC-2SD)降序排序(表3、表4),选择排前20位的PT进行分析。
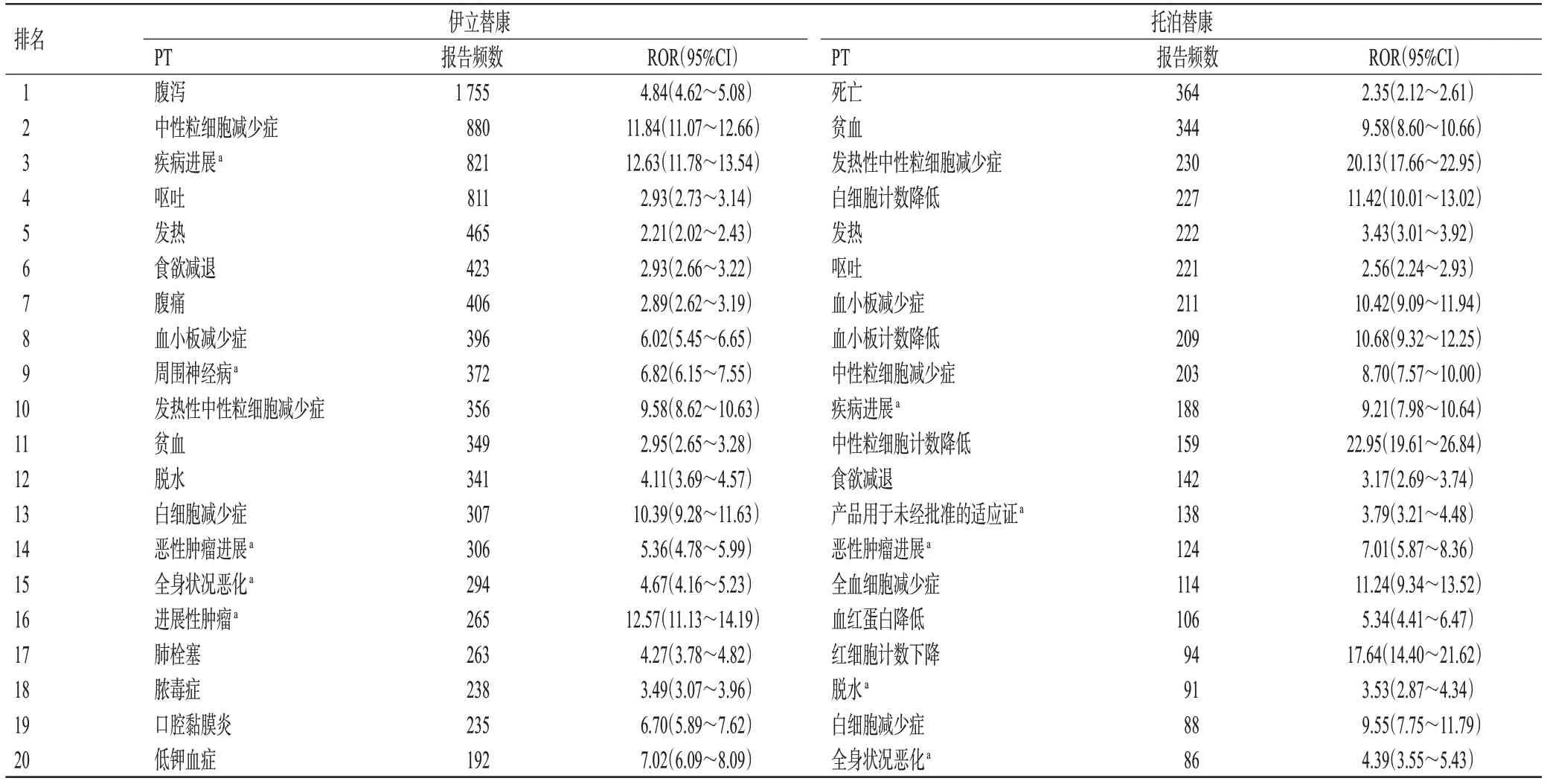
表3 伊立替康和托泊替康报告频数排前20位的PT
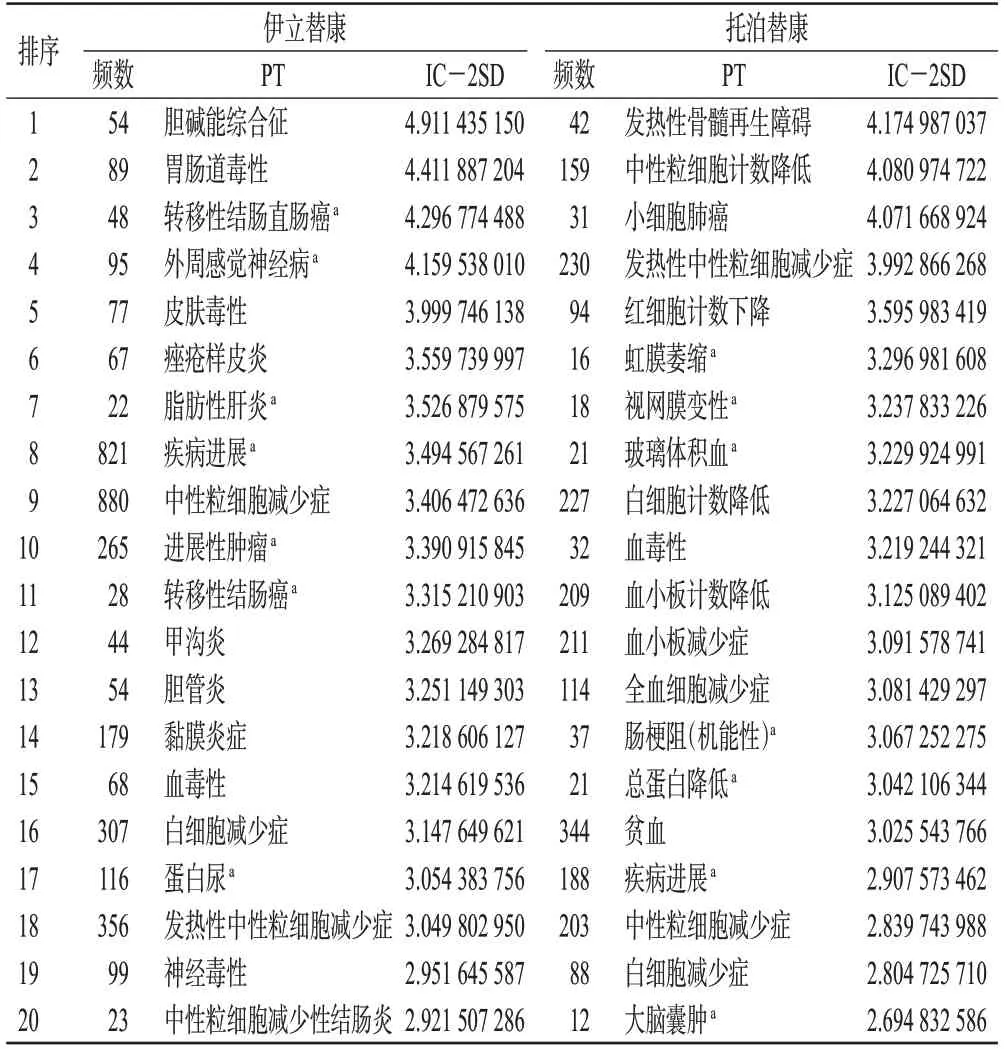
表4 伊立替康和托泊替康信号强度排前20位的PT
由表3可知,伊立替康报告最多的PT是腹泻,共1 755例;随后为中性粒细胞减少症、疾病进展、呕吐等。托泊替康报告最多的PT是死亡,共364例;随后为贫血、发热性中性粒细胞减少症、白细胞计数降低等。由表4可知,伊立替康信号强度最高的PT是胆碱能综合征,其IC-2SD约为4.91;随后为胃肠道毒性、转移性结肠直肠癌、外周感觉神经病、皮肤毒性等。托泊替康信号强度最高的PT是发热性骨髓再生障碍,其IC-2SD约为4.17;随后为中性粒细胞计数降低、小细胞肺癌、发热性中性粒细胞减少症、红细胞计数下降等。伊立替康排前18位和托泊替康排前16位PT的IC-2SD均大于3.0,表示其信号强(+++)。
3 讨论
3.1 伊立替康和托泊替康ADE报告的人口学特征
从伊立替康和托泊替康ADE报告的性别来看,伊立替康ADE报告以男性为主,托泊替康ADE报告以女性为主。Kuipers等[10]研究表明,造成伊立替康和托泊替康用药人群性别差异的原因可能与药物使用情况有关——伊立替康常用于晚期结直肠癌的治疗,而男性结直肠癌的年龄标准化发病率高于女性;托泊替康多用于卵巢癌及小细胞肺癌的治疗,而女性小细胞肺癌的发病率较男性高[11]。本研究还表明,伊立替康和托泊替康ADE报告中的患者年龄主要集中于45~<75岁,这可能与中老年人是肿瘤疾病的高发人群有关。伊立替康和托泊替康的ADE报告均主要来自美国,这可能与上述两药在美国的上市时间较其他国家早,以及美国对FAERS数据库的使用较其他国家多等因素有关。本研究还显示,来源于医师的ADE报告伊立替康有40.02%、托泊替康有35.12%;来源于药师的ADE报告伊立替康有15.51%、托泊替康有14.32%,这提示药学相关工作者应加强药物监测。
3.2 伊立替康和托泊替康ADE报告的特征
本研究结果显示,伊立替康和托泊替康上报频数排前20位的PT有12个相同(中性粒细胞减少症、疾病进展、呕吐、发热、食欲减退、血小板减少症、发热性中性粒细胞减少症、贫血、脱水、白细胞减少症、恶性肿瘤进展、全身状况恶化),而且在两者累及的SOC中,托泊替康所累及的22个SOC均包含于伊立替康累及的24个SOC中,主要原因可能与两药的药理作用类似有关。在胃肠系统疾病、全身性疾病及给药部位各种反应、血液及淋巴系统疾病、各类检查中,两药的ADE构成比均较大,这提示临床使用这2种药物时应该对上述SOC的ADE引起重视,例如腹泻、腹痛、呕吐、食欲减退以及骨髓抑制引起的贫血、血小板减少症、白细胞降低等,在药物使用之前和使用期间予以干预,以降低发生严重ADE的可能性,同时减少疾病治疗期间给患者带来的不适,提高患者的用药依从性。在两药信号强度排前20位的PT中,伊立替康与皮肤毒性、痤疮样皮炎相关性较强,但ADE较少,其相互关系还需进一步研究验证;托泊替康大多是血液系统类ADE,同时还涉及眼器官病变。本研究所挖掘的ADE信号大部分与药品说明书[12―13]一致,证明了本研究的可靠性。但是,本研究发现了伊立替康说明书中未提及的转移性结肠直肠癌、外周感觉神经病、脂肪性肝炎、疾病进展、进展性肿瘤、转移性结肠癌、蛋白尿等ADE,以及托泊替康说明书中未提及的虹膜萎缩、视网膜变性、玻璃体积血、肠梗阻(机能性)、总蛋白降低、疾病进展等ADE,且其IC-2SD均大于3,表明其相关性强,提示临床对使用伊立替康的患者应监测外周感觉神经、肝功能及尿液蛋白水平等相关指标,对使用托泊替康的患者应加强眼器官病变的监测。
3.3 伊立替康与胆碱能综合征
在临床工作中,对于化疗患者,医护人员往往关注的是化疗后骨髓抑制和消化道两方面的ADE,而可能忽略了其他方面的ADE。本研究结果显示,伊立替康ADE报告中相关性最强的PT是胆碱能综合征。刘慧龙等[14]研究表明,应用伊立替康治疗转移性结直肠癌患者,其胆碱能综合征的发生率可达59.6%。乙酰胆碱酯酶是灭活乙酰胆碱的重要物质,而伊立替康是乙酰胆碱酯酶抑制剂,会导致胆碱能神经与相应神经、肌肉突触间的乙酰胆碱浓度升高,从而引起胆碱能中毒[15]。研究表明,伊立替康所致胆碱能综合征主要表现为唾液分泌过多、腹部绞痛和血压下降,伴有大汗、面部皮肤潮红、眼结膜充血、流泪、视物模糊等症状[15―16],其主要原因与药物代谢产物的累积、体内乙酰胆碱酯酶含量不足、给药速度过快及静脉滴注给药有关[17]。此外,也有文献表明女性及伊立替康的使用剂量是胆碱能综合征发生的重要预测因素[18]。因此,对于需要使用伊立替康的患者(尤其是女性患者),用药前完善肝、肾功能检测及乙酰胆碱酯酶含量测定显得尤为重要;用药时还应适当调整药物剂量和给药速度,以减少胆碱能综合征发生的可能性。另有研究表明,对于既往无青光眼病史的患者,在发生严重急性胆碱能综合征时可立即给予阿托品皮下注射,并在严密观察下减慢伊立替康的滴注速度,可缓解患者不适症状[16];在后续的治疗过程中,使用伊立替康前给予患者阿托品类药物预处理,可预防或减轻胆碱能症状[19]。
3.4 本研究的局限性
本研究存在以下局限性:(1)美国FDA并不要求上报事件与产品之间的因果关系,因此来源于FAERS数据库的数据不能用于计算ADE的发生率。(2)美国FAERS数据库是自发呈报系统,其上报数据可能存在误报、重复或缺失等情况,在统计分析时易产生偏倚。(3)美国FAERS数据库的数据主要来源于欧美发达国家,与我国人群存在种族差异,可能影响分析结果的准确性。(4)本研究使用ROR法与BCPNN法检出的阳性信号并非与目标药物存在必然的因果关系,ROR值和IC-2SD值的大小仅表明目标药物发生目标ADE相关性的强弱,其因果关系仍需进一步临床研究加以验证。
综上所述,本研究采用ROR法联合BCPNN法对美国FAERS数据库中伊立替康、托泊替康2种喜树碱类TOP1抑制剂的ADE信号进行挖掘,检测出的ADE信号所累及的SOC基本一致,与药品说明书重合性高,证明了本研究的可靠性。伊立替康和托泊替康的ADE主要累及消化系统和血液系统,临床上应对此重点监测;伊立替康所引起的胆碱能综合征应引起关注。此外,本研究还发现了两药说明书未提及的ADE,因此建议除了上述重点监测ADE以外,对使用伊立替康的患者还应关注转移性结肠直肠癌、外周感觉神经病、脂肪性肝炎、蛋白尿等ADE,对使用托泊替康的患者还应加强眼器官病变的监测。
