荧光纳米探针的合成及其应用研究进展
2024-01-24侯可心王在玺
侯可心,丁 晟,杨 焜,王在玺,李 钒
(军事科学院系统工程研究院,天津 300171)
荧光探针作为一种荧光传感器,以荧光物质为指示剂,可通过荧光信号变化用于对特定分子的检测。荧光探针通常由三部分组成,分别为识别基团、连接基团以及信号报告基团[1]。识别基团用于对待测物质的识别,其决定了荧光探针的特异性和选择性。信号报告基团用于将识别基团与待测物质反应所引起的化学环境变化转化为荧光信号。连接基团则用于连接识别基团和信号报告基团。随着荧光技术的不断进步,荧光探针技术已广泛应用于分析测试、生命科学、光学、化学等领域[2]。理想的荧光探针通常需满足两个条件:首先,荧光探针对于待测物质有较强的亲和性;其次,荧光信号要尽量避免受外界环境因素的干扰,例如光漂白作用、待测物质的浓度以及周围环境等因素[3]。目前常见的荧光探针包括有机类荧光探针及荧光纳米探针两大类。其中,有机小分子组装形成的有机类荧光探针一般选择有机小分子作为信号报告基团,例如蒽、香豆素、氟硼荧染料、萘酰亚胺以及罗丹明等,通过对其进行修饰可使发射波长范围覆盖达650~900 nm。有机小分子荧光探针种类多、资源丰富,近年来科研工作者也日益关注此类荧光探针的研究及应用。此外,量子点、上转换纳米材料、荧光蛋白等也可用作信号报告基团。荧光纳米探针既具备荧光性质,也可用于标记纳米材料。近年来涌现的荧光纳米探针具备较高的荧光量子产率、较好的光稳定性以及生物相容性而引起了研究者极大的兴趣。纳米材料以其特殊的纳米尺寸与结构,呈现与宏观物质截然不同的性质,其具备量子限域效应、较高的荧光量子产率、较高的比表面积、易于吸附其他物质并产生相互作用的性质。随着纳米技术的不断发展,纳米材料的合成方法日益完善,人们更容易控制其尺寸、形貌及功能性等特征,为荧光纳米探针满足化学传感器、生物探针等领域的技术要求奠定了基础。荧光纳米探针的荧光性质可随着外界环境的微小变化而产生变化,具有灵敏度高以及响应时间短等优势[4]。目前,常见的荧光纳米探针包括量子点[5]、金属-有机框架[6]、金属纳米簇[7]等。本文着重介绍其合成及应用,并对该领域的发展前景和存在的问题进行讨论。
1 量子点
量子点(Quantum dots,QDs)又称半导体纳米晶,是由Ⅱ-Ⅵ或者Ⅲ-Ⅴ族元素组成的尺寸在1~100 nm 之间的“零维”新兴半导体纳米粒子。QDs 具有多种优异的荧光性质,如荧光寿命长、激发光谱宽、Stocks位移大、发射峰窄且对称、光稳定性好等,可作为一种优异的荧光纳米探针。QDs具备独特的性质,主要考虑其自身的量子效应及尺寸效应影响。当其为纳米尺度时,特殊的结构可引起量子限域效应、介电限域效应、表面效应、宏观量子隧道效应,QDs表现出不同于宏观物体的特殊光学性质,使得其在生物医学、光电领域具有广阔的应用前景[8]。 《Science》杂志将QDs列为2003年度十大科技突破之一。2006 年,《Nature》杂志将其列为最有可能实现大规模应用的4 种纳米材料之一(图1 所示QDs应用场景)。QDs 是一种核壳结构的纳米材料,其内部为无机核,外部为配体分子。早在1983 年,科学家Brus 及其团队首次报道合成了一种纳米荧光半导体晶体—硫化镉(CdS),并将其命名为量子点,由此拉开了荧光量子点研究的序幕[9]。1994 年,Alivisatos 教授及其团队在《Nature》杂志报道了通过CdSe 构建发光二极管,QDs 得到了实际应用并成功用于光电转换领域[10]。直到1998 年,Alivisatos 教授[11]以及Nie 教授[12]解决了QDs 的生物相容性问题,各自报道了可作为活细胞体系荧光探针的水溶性QDs,并证实其在生物医学领域大有可为,为之后QDs研究的飞速发展奠定了基础。QDs的荧光性质受多种因素影响,其存在空穴效应可被较大范围的激发光激发[13]。另外其尺寸与发光性质密切相关,可通过调节QDs 的粒径优化其发光性质[14]。QDs 的发光性质由电子、空穴以及周围环境的相互作用决定(如图2),其发光原理是在光照条件下,QDs吸收光子后其价带上的电子则会跃迁至导带,原来价带的位置则产生空穴。而导带上的电子有两种可能,其可与价带顶部的空穴复合从而发射光子,也可落入电子陷阱。当电子落入较深的电子陷阱,则大部分电子会以非辐射的形式产生猝灭,仅存在少数电子可以光子的形式重新跃迁至价带或导带。由于QDs 的紫外可见光谱存在多个能级态,其中由最低能级态激发产生的峰是量子限制峰,还有很多电子状态存在于更高能级水平,因而单一波长的光可用于激发多种颜色的QDs[15]。根据QDs 的发光原理,通过在其连续的激发光谱中选择适合的激发波长,使得生物样本的自发荧光最低,从而提高QDs的灵敏度和分辨率[16]。

图1 量子点的应用场景[8]Fig.1 The application scenarios for quantum dots[8]
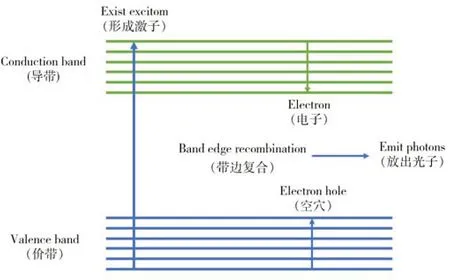
图2 量子点荧光产生原理图Fig.2 Schematic diagram of fluorescence generation of quantum dots
与众多有机染料相比,QDs 具有更大的Stocks 位移以及较窄且对称的荧光光谱峰,可应用具备不同光谱特征的QDs 进行不同组分的荧光标记,从而避免发射光谱与激发光谱的重叠或只产生很小程度的重叠,使得其可在低信号强度环境中进行荧光检测,荧光光谱的区分、识别更容易[17]。此外,与常规有机染料罗丹明6G相比,QDs的荧光强度是其20倍,QDs具备更为优异的抗光漂白作用,光稳定性达到普通荧光染料的100 倍以上。有机荧光染料在光激发作用下易产生光致化学反应而具有很快的光漂白速率,QDs 的抗光漂白能力很强,几乎不存在光褪色现象[18]。常规有机荧光染料的荧光寿命为几纳秒,而QDs 的荧光寿命可达到数十纳秒且摩尔消光系数是常规有机荧光染料的10~50 倍。当光激发数纳秒之后,自发荧光背景减弱,QDs 的荧光仍然存在,其可克服自发荧光背景的影响而清晰辨别到荧光检测信号[19]。另外,经表面修饰后可使得QDs 具有优异的生物相容性,可作为理想的细胞体系荧光探针。
1.1 量子点的合成
经不断探索,研究者发现QDs 较为常用的合成方法可分为有机相合成法及水相合成法。在早期研究中,QDs 的合成以有机相合成法为主。借助高沸点的有机溶剂,以有机金属作为反应的前驱体热解合成QDs。即于250~300 ℃的配体溶液中添加前驱体有机金属,前驱体快速热解并成核,晶核缓慢生长成为纳米晶体QDs。在配体的吸附作用下,晶核不再继续生长从而稳定存在于溶剂中[20]。早在1993年,Murray 等[21]以Cd(CH3)2及Se/Te 为金属前驱体,以三正辛基氧化膦(TOPO)为有机溶剂,首次通过有机相合成法制备得到油溶性QDs。2001 年Talapin 等[22]将十二胺(DDA)替代TOPO 用作反应溶剂合成CdTe,荧光量子产率高达65%。然而,有机镉等有机金属前驱体具有毒性大、不稳定、易燃易爆、成本高、操作复杂且须控制整个过程无水无氧等缺点,极大限制了QDs的推广和应用。Peng 等[23]继续优化此合成体系,将金属前驱体Cd(CH3)2更换为更环保的CdO或Cd(CH3COO)2,合成了粒径均一的CdTe及CdSe。
通过有机相合成法制备得到的QDs 具有种类多、粒子分散性好、粒径可控、荧光强度高以及量子产率高等优势,然而,该方法操作较为复杂且需要较高的反应温度,合成得到的QDs 不溶于水,生物相容性有待提高。通过有机合成法制备的QDs 表面可能包覆三辛基膦(TOP)/TOPO 层,可通过表面修饰小分子有机配体或者大分子聚合物的方式提高其亲水性,降低毒性[24]。QDs 的表面修饰方法主要包括链交换法、聚合物包覆法以及表面硅烷化法(如图3)[25]。链交换法通过亲水性分子置换QDs 表面的TOP/TOPO 层从而得到具有良好水溶性的粒子[26],其成功与否取决于QDs 与配体结合的稳定程度。亲水性分子一端带有与金属原子具有较强作用力的巯基等基团从而固定在QDs 表面,另一自由端的亲水基团(羧基、胺基、羟基)赋予QDs 水溶性并可作为官能团进行后续生物偶联。链交换法常见的含巯基配体主要有巯基十一酸、巯基乙酸、巯基丙酸等[12]。在此基础上,二巯基的配体(如二巯基硫辛酸)可用于QDs 的修饰以提高配体与QDs 结合的稳定性[27]。然而,链交换法在合成过程中需超过量的前驱体进行反应,且所合成的水溶性QDs 表面结构易被破坏,可能影响稳定性及荧光强度[28]。通过聚合物包覆法利用两亲性聚合物(如聚乙烯亚胺、多肽、壳聚糖)的疏水端与QDs 的疏水配体相互作用将QDs 封装在内部,而两亲性聚合物的亲水端赋予QDs水溶性[29]。例如Park 等[13]通过合成聚乙烯亚胺衍生物并将其用于封装数十个QDs,所合成的粒子水合粒径为100 nm 且表面带正电荷,适用于细胞内化。由于部分QDs含有重金属元素,从而一定程度上限制其生物应用。聚合物包覆法可保护QDs 的内部结构,保留其特殊光学性质[30]。然而,与链交换法相比,聚合物包覆法显著增加了粒子的水合粒径[31]。表面硅烷化法通过将水解的硅烷化试剂置换QDs 表面的原有机配体,硅烷化试剂通过水解作用在QDs 表面形成SiO2壳层[32]。表面硅烷化修饰的QDs 具有良好的稳定性、水溶性和生物相容性,且引入的水溶性基团可用于负载其他功能性小分子[33]。此外,在QDs 表面构建SiO2壳层,可在一定程度上防止QDs 内部重金属元素泄漏。然而,表面硅烷化修饰法操作步骤复杂、所合成的粒子粒径不均,不利于大规模生产[34]。
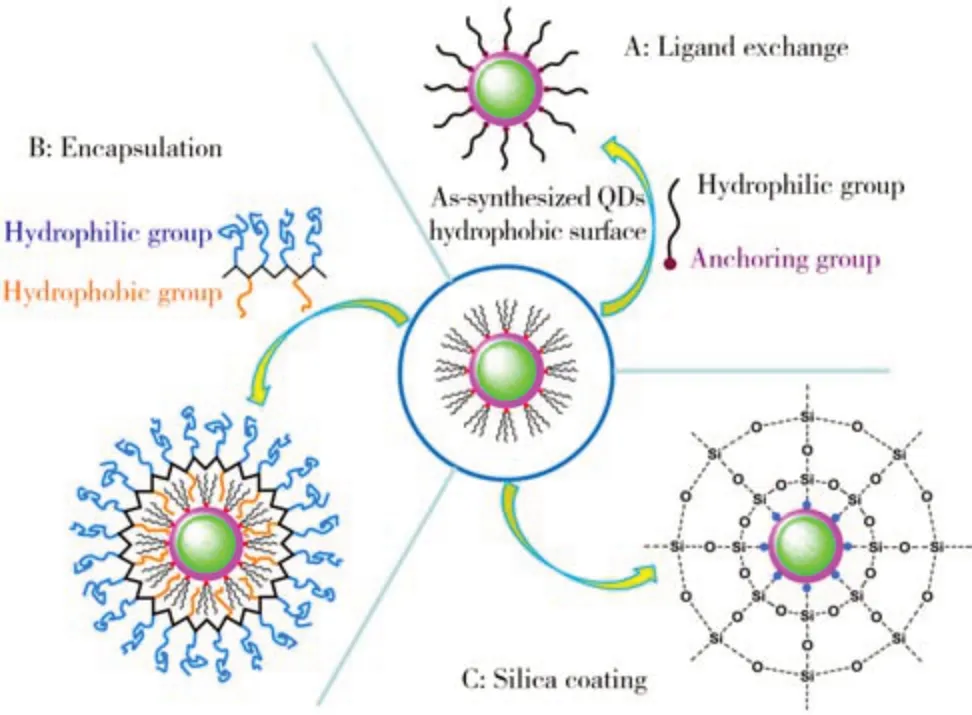
图3 量子点的表面修饰方法:链交换法(A)、 聚合物包覆法(B)以及表面硅烷化法(C)[25]Fig.3 Methods for modifying the surface of quantum dots:ligand exchange(A),encapsulation(B) and silica coating chemistries(C)[25]
有机相合成法可制备得到高质量的QDs,然而所得到的QDs为油溶性,无法直接应用于生物体系。而经表面修饰后合成的QDs 表面难以钝化且操作较为繁琐,易发生荧光量子产率下降现象。水相合成法即在有机配体存在下,阴离子与阳离子前驱体在水相介质中直接反应合成得到QDs。与有机相合成法相比,水相合成法具有操作简单、反应试剂无毒、成本低、表面电荷及表面性质易于控制等优势。除此之外,通过水相合成法合成的QDs 解决了粒子的水溶性问题,具有更优异的生物相容性。早在1987年,Spanhel等[35]在水相体系中以多聚磷酸盐为稳定剂,通过Cd离子与H2S反应合成了CdS。1993年Rajh 等[36]报道在水溶液中以硫代丙三醇为稳定剂,合成得到水溶性巯基甘油包覆的CdTe。1999 年Rogach等[37]以巯基丙三醇以及巯基乙酸为稳定剂,合成了CdTe并实现粒子表面的功能化。自此水溶性QDs 逐渐成为研究热点。水相合成法通过离子型前驱体,以多官能团巯基小分子为配体,在水相介质中加热回流前驱体溶液使得纳米晶逐渐成核并生长。例如Liu 等[38]以CuCl2、InCl3以及CS(NH2)2为原料,3-巯基丙酸为配体合成得到了水溶性的CuInS2。Zhou等[39]以CuCl2、InCl3以及Na2S为原料,以巯基乙酸为配体合成得到了纤维锌矿晶型的CuInS2。以巯基小分子为配体合成QDs具有操作简单、成本低、易于大规模生产、可进一步复合与组装等优势,然而含有巯基的小分子具有一定毒性,且通过该方法制备的QDs 存在种类少、部分QDs 荧光量子产率低、荧光半峰较宽等不足。针对这些问题,科研人员致力于开发低毒或无毒的高效配体[40]。Gao 等[41]以L-谷氨酸为配体,以CuCl2、InCl3、CS(NH2)2为原料,通过水相合成法制备水溶性的CuInS2。CuInS2与具有荧光的抗癌药物阿霉素结合得到可用于实时监控阿霉素释放情况的功能化量子点。随着研究的不断深入,除了有机相合成法及水相合成法之外,电化学合成法也引起人们的广泛关注。由于天然产物具有温和的生物还原作用,可以多酚、水稻提取物等天然物质为还原剂,将金属离子还原为金属原子,进而以金属原子为前驱体形成具有稳定荧光性质的QDs。此外,电化学合成法还可用于制备碳量子点(CQDs),主要是通过使用具有导电功能的含碳材料为工作电极,通过施加直流电压,阳极氧化水分子,电解液中的离子进入工作电极从而在碳材料中剥离出碳纳米粒子。电化学合成法制备成本低、能耗低、对于含碳前体的利用率高、所合成CQDs粒径较为均匀,且有利于监测CQDs合成过程并实现较大规模生产。
1.2 量子点的应用
通过几代科研人员不断改进QDs 的合成方法并优化结构组成,QDs 的光学性质得到不断提升,使得其成为一类性能优异的荧光探针在生物分析领域具有极大的发展潜力,尤其是在分析传感与生物成像方面[15]。在基于光诱导电子转移、荧光共振能量转移等原理的基础上,QDs 的生物传感技术可用于体外对于生物样品中特定物质的检测。QDs 可与DNA、糖、酶、蛋白质、病毒、抗原及抗体等物质结合实现对其定性或定量检测[42]。传统对于体外生物标志物的识别具有一定局限性,例如常见的酶联免疫吸附法中生物酶易受外界环境因素(如温度、光照等)影响,且该法的显色过程需要一定的时间从而限制了其在特定场景中的应用。基于QDs 的免疫吸附法可较好地规避上述问题,QDs 的稳定性较好且能与多种生物分子结合实现快速、精确的定量或者定性检测。例如,Wu 等[43]合成苯硼酸修饰CdTe/ZnTe/ZnS 量子点用于对活细胞内葡萄糖的检测,该荧光探针通过巯基苯硼酸与葡萄糖分子发生反应引发荧光猝灭从而对葡萄糖具有高灵敏度和选择性。Wang 等[44]合成了基于QDs 的比色-荧光双模式横向流动免疫分析生物传感器用于检测新冠病毒,其可定量检测生物样本中SARS-CoV-2 特异性的IgM/IgG。该检测方式具有两种模式:首先,对于普通人群,通过比色法快速筛查出疑似感染者。其次,通过荧光法定量检测生物样本中的IgM/IgG 进一步确定早期感染者。之后,Wang 等[45]将QDs 吸附到SiO2纳米粒子表面制得QDs 纳米珠,基于双通道荧光免疫色谱法可用于对SARS-CoV-2 以及甲型流感病毒的定量联检,检测时间仅为15 min,对SARS-CoV-2抗原的检测限为5 pg/mL,对甲型流感病毒的检测限仅为50 pfu/mL。与传统的金纳米粒子相比,通过该方法可将检测灵敏度提高约2 个数量级。由于QDs 表面可经过修饰与多种生物分子结合从而应用于多种肿瘤标志物的定量检测。例如通过将甲胎蛋白抗体与QDs 偶联,基于QDs 以及金纳米粒子之间的荧光共振能量转移现象从而实现对于生物样本中甲胎蛋白的定量检测。除对于肝癌相关的甲胎蛋白之外,以QDs 作为荧光信号,还可用于肺癌、卵巢癌肿瘤标志物的检测。另外,以QDs 为荧光标记物也可用于对食品杂质的精确检测。例如,单独使用QDs或将QDs与其他荧光材料联合用于对酪蛋白、鼠伤寒沙门氏菌等物质的定量检测[34]。
与有机染料相比,QDs 不会对细胞膜产生明显损伤,因此其可与生物大分子偶联进入细胞体内实现对细胞、蛋白质、DNA 等物质的生物标记。1998 年,Bruchez 等[11]以及Chan 等[12]报道称QDs 可应用于小鼠成纤维细胞荧光成像,证实QDs是实现生物成像的有力工具。He等[46]通过一步微波辅助法合成水溶性CdTe,实现对小鼠肿瘤的靶向成像。根据QDs具有优异荧光性能的优势,还可将QDs作为载药平台应用于动态监测药物在活体细胞内的分布和代谢行为,从而为设计和开发新型的药物提供理论依据和技术支持。人们认为近红外窗口为生物组织的光学“透明”窗口,与可见光相比,其具有更强的组织穿透能力,适合用作光激发源。在生物成像领域,可用于近红外发射的非Cd 的QDs 材料还有CuInSe[47]、CuInS[48]、Ag2S[49]等。该类QDs 材料由于不含有重金属元素,生物相容性更好。Kuo 等[50]合成氮掺杂石墨烯QDs 材料,其具备较高的光致发光量子产率以及双光子性能,通过使用特异性抗体标记癌细胞细胞器及鉴定核抗原,从而能够在双光子波长下同时检测细胞中的4 个靶标,可用作细胞成像的有效探针。由于QDs 粒径可调且与有机荧光染料相比更不易生物降解,除了可用于细胞或生物体的成像之外,还可用于细胞中某个细胞器的靶向成像。近年来在线粒体荧光探针的研究中报道了较多的CQDs,其具有毒性低、来源广、环境友好的优势。Hua等[51]通过一步水热法以壳聚糖、乙二胺以及巯基琥珀酸为原料首次合成了具备线粒体靶向功能的CQDs,其无需修饰其他线粒体配体即可实现线粒体成像以及线粒体靶向光动力治疗。Geng 等[52]以罗丹明的亲脂性阳离子作为CQDs 的发光中心合成了具备线粒体靶向功能的CQDs,其具有线粒体成像功能以及从绿色荧光到红色荧光的可调长波长荧光。另外,根据CQDs 颜色的可调性,可实现对同一细胞的多色标记。例如,可使用5 种不同颜色的CQDs实现对人上皮细胞的多色成像[53]。Liu 等[54]以地塞米松以及1,2,4,5-四氨基苯为原料,通过微波水热法合成活细胞中溶酶体靶向CQDs,其可作为比率荧光探针用于检测甲醛。
然而在QDs应用过程中发现其对于水、氧气、热的耐受性较低,这可能是因为其为核壳结构材料,外部起保护作用的配体分子在受到外界因素影响时易发生脱落或在化学反应作用下失效。另外,在应用过程中QDs团聚导致其体积变大,影响发光稳定性甚至猝灭失效。
2 金属纳米簇
金属纳米簇(Metal nanoclusters,MNCs)是由几个到上百个不等的Au、Ag、Pt 等原子组成的金属核与配体壳的典型核壳结构,其尺寸在2 nm 左右且具有明确的组成及结构(如图4)。此类超小的纳米粒子表现特殊的行为,这种改变由电子共享以及量子限制引起,导致MNCs具有高比表面积、强光致荧光、量子尺寸效应、表面效应以及宏观量子隧道效应等[55]。MNCs 介于金属原子以及等离子体金属纳米粒子之间,由于其尺寸接近电子的费米波长,呈现出离散态能级,进而导致MNCs具有特殊的物理化学性质以及类分子性质,例如最高占据轨道和最低未占据轨道(HOMO-LUMO)跃迁、高催化活性、分子手性及固有的磁性、确定的分子公式以及分子结构等[56]。

图4 MNCs示意图(A)及尺寸与性质关系图(B)[66]Fig.4 Schematic illustration of MNCs(A) and important properties of MNCs related to their ultrasmall size(B)[66]
MNCs 的物理化学性质取决于其金属核以及壳体保护配体[57]。金属核的原子结构对于MNCs的稳定性至关重要,高度对称结构导致高结合能,MNCs从而具有较高的稳定性。MNCs表面的配体壳结构对于金属核具有重要保护作用,当选择的金属核相同而保护配体不同时,MNCs 的荧光发射不同[58]。目前MNCs 常用的保护配体包括巯基化合物[59]、聚合物[60]、蛋白质[61]以及DNA[62]等,其中报道较多的是巯基化合物,特别是谷胱甘肽,由于其含有的巯基官能团可与金属原子产生强烈的相互作用而达到修饰及稳定MNCs的作用[63]。谷胱甘肽保护的金银纳米簇已被广泛应用于生物成像及生物传感等领域。Zhou 等[64]合成谷胱甘肽保护的金纳米簇,其可用于生物成像并具有较高的肾脏清除率。此外,一系列与硫醇有关的化合物(如巯基琥珀酸、苯乙基硫代、硫代α-环糊精等)被用于合成稳定的金纳米簇[65]。尽管MNCs的研究已取得较快发展,然而仍存在多数水相MNCs的抗聚集稳定性以及对环境氧的抵抗力不足,有机相的MNCs 在生物医学领域的应用受限制等问题[66]。在实际应用过程中,可通过MNCs 与MOFs、石墨烯、生物分子或者无机材料等物质结合从而达到增强MNCs性能的目的[67]。例如Ao等[68]通过在铜纳米簇表面使用含有硫醇的三烷氧基硅烷原位生成硅壳的方法增强其荧光性质及光稳定性,且通过在硅壳表面水解及聚合具有不同官能团的三烷氧基烷烃衍生物为其提供多功能的表面官能团。近年来,金、银纳米簇在生物医学领域得到广泛应用,常被用作癌细胞的荧光探针[69]。此外,科研人员合成了众多以Cu、Pt、Pd、Ir 为核的MNCs,双金属或者三金属纳米簇(如AuxAgy、AuxCuy、PtxAuyAgz)也得到了广泛关注[70]。
不同类型的MNCs 可广泛应用于多种领域,例如催化、生物分析及成像、电子器件制备、环境检测等,是一种具有应用潜力的理想纳米材料。其中,MNCs 以其优异的荧光性能而成为新一代的荧光材料。传统荧光探针例如有机荧光小分子探针的抗光漂白性能一般[71],而QDs具有一定的细胞毒性[72],MNCs具备超小粒径、更优异的光稳定性及生物相容性,因此MNCs可作为传统荧光探针有前途的替补材料。科研人员对于具有优异荧光性能MNCs 的合成方法具有浓厚兴趣,目前已有多种策略可以高度受控的方式合成MNCs,包括自下而上、自上而下的方式,其中应用最多的为自下而上合成法。
2.1 金属纳米簇的合成
一般来说,MNCs 的合成策略可分为:自下而上以及自上而下。自下而上的方法是在有保护配体或模板存在的情况下,将离子还原为原子进而形成原子团簇。自上而下的方法是利用配体(例如硫醇化合物)将较大的纳米材料刻蚀成较小的MNCs。
在自下而上的合成过程中,常见的几种方法包括化学还原法、光还原法、模板法、电化学法、超声化学法等。化学还原法是封盖剂以及还原剂起作用的方式,金属前体(例如CuSO4、HAuCl4、AgNO3等)起基质作用,还原剂(例如NaBH4、抗坏血酸、H2等)将金属离子还原为原子并最终聚集形成纳米簇。在合成过程中由于纳米簇表面积很高以及位于外层的原子价键不饱和导致其表面自由能较高,纳米簇不稳定并可产生不可逆的聚集[73],因此,通常需要保护剂以降低表面自由能从而制得稳定的MNCs。与化学还原法相比,光还原法是MNCs的绿色合成方法,以光照作用代替使用有毒还原剂从而避免了沉淀反应的发生[74]。电化学法通过牺牲阳极得到金属离子,之后其在阴极被还原为MNCs。例如González 等[75]通过电化学法在阳极溶解金电极,还原Au-PVP 配合物合成得到了只有2 个和3 个原子的金纳米团簇。模板法作为一种简单高效且无污染的MNCs 合成方法被广泛关注,以金属离子为前驱体,通过特定结构的模板可与金属离子发生相互作用并使得MNCs 稳定分散而不易产生聚集。模板的性质可影响MNCs的尺寸及荧光发射[76]。近年来,用于合成MNCs的模板主要有硫醇分子[77]、高分子聚合物[78]、蛋白质[79]、核酸[80]等物质。超声化学法利用超声场中气泡经历形成、生长及破裂过程,可导致化学反应增强。超声化学法具有绿色无污染、反应速度快、反应过程可控及所合成的纳米粒子形状规则、粒径均一等优势[81]。Wang等[82]通过超声化学法以谷胱甘肽为还原剂和稳定剂采用一锅法合成了具有荧光性质及磁性的铜纳米团簇。自下而上合成法无需颗粒较大的前驱体,是合成MNCs 的一种简单高效的方法。
自上而下合成法是在过量配体以及粒径较大的非发光金属纳米粒子或者纳米簇之间通过化学刻蚀作用形成MNCs的方法[83]。在化学刻蚀过程中,常见的刻蚀剂为氨及谷胱甘肽[84]。粒径不同的MNCs稳定性不同,最终只有稳定性最好的MNCs可进一步形成粒径最小的粒子。配体诱导刻蚀是合成MNCs的主要刻蚀方法,特别是以硫醇小分子、胺及高分子聚合物为配体时,配体与金属核的相互作用引起科研工作者的关注。例如,Deng等[85]以铜纳米粒子为前驱体,以氨为刻蚀剂通过化学刻蚀法合成了具有绿色荧光的铜纳米簇并用于对尿素的检测。Guével 等[86]以谷胱甘肽为刻蚀剂,以铂纳米粒子为前驱体合成了在570 nm 具有荧光的铂纳米簇,且随着反应时间的延长,荧光发射峰逐渐蓝移。自上而下的方法易于控制MNCs 形状从而实现图案化,可通过调节不同配体作为刻蚀剂合成具有不同荧光发射的MNCs。然而,该方法合成过程复杂、不利于实现多功能性且需要特定的设备以及技术支持。此外,所合成的MNCs粒径不均一,较大的粒子在纯化过程中易丢失从而造成浪费。
2.2 金属纳米簇的应用
MNCs 由金属核以及配体组成,二者均可与靶标识别从而实现检测的目的。其作用机理可能为基于MNCs与靶标物质之间的电荷或者能量转移导致的动态荧光猝灭,基于靶标物质与MNCs构成不发光的络合物而导致静态荧光猝灭。MNCs 作为新型的荧光纳米探针在生物分析检测、环境监测、生物成像、分子传感、抗菌、催化等领域得到广泛关注及应用。对于离子的检测始终是分析测试领域的重要研究内容,MNCs可与多种离子发生特异性响应导致其荧光强度发生改变。重金属离子(如Pb、Cd、Hg及Fe)是危害环境及人体健康的剧毒污染源,因此对于重金属检测的重要性不言而喻。Bhamore等[87]通过一锅法合成谷胱甘肽及组氨酸稳定的金纳米簇荧光探针,其可应用于水溶液及血液中Pb2+的检测(如图5)。MNCs还可用于检测部分有毒的阴离子,例如Cang等[88]研制一种用于NO-3及CN-检测的双传感荧光探针硫代水杨酸为保护配体的铜纳米团簇。在酸性条件下,NO-3离子通过HNO2和硫代水杨酸的氧化还原反应产生荧光猝灭,而CN-离子在碱性溶液中通过蚀刻过程产生荧光猝灭。除了对多种金属离子及阴离子的检测之外,MNCs 可用于多种具有重要生物功能的小分子检测,通过小分子与金属原子相互作用使得MNCs 的荧光猝灭或增强。Li等[89]提出一种可用于检测Fe3+、NO-3及半胱氨酸的多功能荧光探针金纳米团簇,其在H+的触发下通过自组装形成具有红色荧光的生物探针。Wang等[90]利用硫醇诱导化学刻蚀法聚集发射活性金纳米团簇用于快速、灵敏及选择性地检测半胱氨酸。Zhai 等[91]合成可用于高效检测谷胱甘肽的金银双金属纳米团簇材料作为“Turn-off”荧光纳米探针。在过硫酸盐的作用下,荧光纳米探针产生荧光猝灭,而谷胱甘肽可与其反应并诱导荧光恢复。

图5 具有绿色荧光的谷胱甘肽及组氨酸稳定的金纳米簇荧光探针应用于Pb2+的检测[87]Fig.5 Glutathione and histidine stabled AuNCs fluorescence probe applying to Pb2+ detection[87]
蛋白质作为重要的生物大分子具有多种生理功能,是生命活动的基础,因此,对蛋白质的准确检测对于疾病诊断具有重要意义。蛋白质与MNCs 存在一定程度上的相互作用,基于该性质可合成用于蛋白质检测的荧光纳米探针。早在2006 年,Triulzi 等[92]首次报道基于MNCs 检测蛋白质的方法,将PAMAM-金纳米团簇与抗人免疫球蛋白抗体组装,通过化学发光酶免疫测定法实现对蛋白质的检测。生物酶的生物活性可直接或间接地影响MNCs 的荧光性质,基于这一特性设计了用于检测生物酶的纳米荧光探针。近年来,已有科学家设计了多种MNCs用于检测生物酶(如乙酰胆碱酯酶、蛋白激酶、金属蛋白酶、凝血酶等)。Liu 等[93]将金纳米簇与荧光素结合合成了比率型荧光探针,用于检测乙酰胆碱酯酶及其抑制剂对氧磷,并利用光子晶体的选择性增强其荧光强度。核酸作为生物最重要的物质之一,Bonis-O'Donnell等[94]合成了银纳米簇用于对DNA浓度的比率荧光检测,当添加目标序列时,该序列在银离子及还原剂的作用下形成具有荧光的银纳米簇,反之则抑制其形成,且银纳米簇的合成数量取决于目标结合域的接近程度。
与其他成像方式相比,荧光成像在多种物质检测、设备灵敏度及成本等方面具有显著优势。以生物分子为模板合成MNCs可赋予其优异的生物相容性。MNCs以较小的粒径、优异的荧光性质、易于表面修饰、结构组成明确等优势易应用于生物成像领域。Wu 等[95]以牛血清白蛋白为模板合成金纳米簇,首次将其用于小鼠体内肿瘤活体成像分析。此后,多项研究报道MNCs 用于生物成像研究,例如Pan等[96]通过一锅法合成甲硫氨酸保护的金纳米簇,其可特异性识别癌细胞并显示强荧光,而在正常细胞不显示荧光。
此外,MNCs还可用作抗菌剂治疗细菌感染引起的多种疾病,这是由于MNCs具有尺寸小、比表面积高的优势,当其进入细胞内部时可诱导细胞代谢失衡,增加活性氧自由基,并最终发挥抗菌作用。科学家以杆菌肽为生物模板制备金、银、铜纳米簇,其可诱导产生大量活性氧自由基,呈现较强的抑菌作用。另外,也有多种具备广谱抗菌作用的MNCs被成功合成[70]。由于MNCs具备较小的尺寸、独特的电子结构、高比例的表面原子以及低配位数,因此MNCs 的化学性质可能更活泼,且结构可设计,从而在催化等领域具有应用潜力。研究发现,MNCs 除了在化学催化反应中具有应用价值外,还具备类酶活性,例如可能具有类过氧化物酶、类葡萄糖氧化酶活性,而关于具有类酶活性的MNCs 设计研究对相关生物医学领域的应用具有重要指导意义。然而,在MNCs 应用过程中,由于MNCs 粒径较小、比表面积较大,当其粒径持续降低时,表面能增加,且MNCs 高度配位不饱和,使得其热力学性能不稳定,在应用及储存方面带来困难。
3 金属-有机框架
金属-有机框架(Metal-organic frameworks,MOFs)通过金属节点(金属离子或金属簇)与桥连的多齿有机配体以配位作用形成配位化合物,其具有高比表面积、高孔隙度、多功能、结构可调等优势并成为新一代的多孔杂化材料[97]。上世纪90 年代,Yaghi 团队在《Nature》杂志报道了具有热稳定性的MOFs材料可用于选择性地吸附芳香族分子[98]。MOFs是一类具备丰富发光中心的优秀的发光平台,其荧光通常基于金属离子发光、有机配体发光、电子转移发光以及负载在MOFs 中的客体分子发光。因此,荧光传感材料是MOFs 重要的应用方向之一。刺激响应型MOFs 材料在光照[99]、温度[100]、电磁[101]、pH[102]、力[103]等作用下可改变自身理化性质,从而将光、热等信号转化为化学信号。在众多外界刺激作用下,光刺激具有非接触、成本低、环境友好、易于操作等优势而成为刺激响应型材料的研究焦点。在外界光刺激作用下,MOFs的分子结构、孔隙结构等发生改变,同时伴随着物理化学性质的变化从而呈现不同的形态。MOFs 通常以光响应基团为配体,与金属节点构成配位键进而通过自组装的方式形成[104]。MOFs 结构中的光响应基团作为配体可分为可逆型及不可逆型。其中,不可逆型光响应配体对于外界环境中的光刺激仅做出一次反应,额外的光刺激并不能促使其恢复至初始状态。可逆光响应配体则可进行可逆调控操作,从而使得MOFs实现在不同状态之间的可逆切换。
根据几种常见的光致异构化合物,可逆光响应MOFs可分为螺吡喃类[105]、偶氮苯类[106]、二芳基乙烯类[107]等。螺吡喃是光致变色分子的重要代表性化合物之一,受到研究人员的广泛关注。总体来说,螺吡喃在光刺激作用下,由无色的闭环型转化为有色的开环部华菁构型,当再次经过光刺激时其可逆地回归初始无色闭环状态[108]。螺吡喃在金属离子传感器、分子光开关材料、分离材料等方面展现潜在的应用价值[109]。例如Fleming 等[110]合成了基于螺吡喃的分子光开关,其特点在于可显示3 种不同的光响应性质,可控制同一光致变色骨架上的顺-反或者螺-部花青异构化的激活。Liu 等[111]通过原位生长的方法合成由螺吡喃包埋的MOFs 材料用作可光开关离子门控亚纳米通道。偶氮苯类化合物是以氮氮双键连接两个苯环作为基本结构的光响应性分子,具有顺式和反式两种构型。当偶氮苯类化合物经过紫外光照处理后,氮氮双键产生结构的变化,偶氮苯分子将从热力学稳定的反式异构体转化为不稳定的顺式异构体[112]。偶氮苯类化合物在分子结构变化过程中,其物理化学性质随之发生改变,表现为孔径、颜色、形状、溶解度、折射率等变化[113]。根据其产生相应的变化,具有偶氮苯侧基的MOFs 常可用于药物运输、气体分离等领域。例如,多孔的MOFs 用于气体分子的吸附、可控释放以及混合物的连续可调膜分离[114],光响应性的超分子囊泡用于靶向细胞内药物递送并可实现光照条件下的可控药物释放[115]。二芳基乙烯类化合物同样是基于顺反异构的光响应性分子,具备良好的热稳定性以及抗疲劳性而在近年来逐渐成为研究热点之一。由于二芳基乙烯类化合物异构变化前后,分子的吸收光谱变化较小具有部分重叠,使得其部分性能并不突出[116]。为了提升其光响应性能,研究者们主要对其分子中的核心部位烯桥进行改性或对分子的侧基做修饰,例如引入弱芳香性基团噻吩、呋喃等[117]。该类MOFs材料通常在数据存储等领域展现出可观的应用价值[118]。Xiong团队以基于二芳乙烯的铁晶体为材料,实现了非接触式的数据写-读-擦除数据存储操作[119]。
微米级孔径的MOFs 材料广泛应用于气体分离等领域,而纳米级的材料已被证明可应用于包括荧光探针、药物递送在内的生物医学领域[120]。其中,MOFs 以其多种优势而在荧光纳米探针领域备受关注[121]。MOFs 具备可调节结构和多功能性,通过调节金属离子、有机配体、客体分子可使其适用于大多数被分析物质(如图6)。通过添加剂的使用可调节MOFs 的孔径及晶体结构从而调节其发光性能[122]。MOFs具有多孔结构可富集被分析物,增加荧光探针周围被分析物的浓度[123]。当MOFs与其他荧光物质结合,可增强电子转移作用从而提高荧光强度。当MOFs 同时封装两种荧光物质时,其成为比率型荧光探针,荧光探针的检测准确度得到提高[124]。另外,相比普通荧光探针,MOFs 具备更好的耐热、耐酸及耐碱性能[125]。

图6 装载不同模块的MOFs材料用于对特定分子的测定示意图[122]Fig.6 MOFs loaded with different molecular building blocks realize the sensing of specific molecules[122]
3.1 光响应金属-有机框架的合成
由于MOFs 具有丰富的发光中心,其荧光通常基于金属离子发光、有机配体发光、电子转移发光以及负载在MOFs 中的客体分子发光。因此,MOFs 荧光纳米探针的合成策略可分为两大类:单独的MOFs 作为荧光探针,可根据有机配体及金属离子对被检测物质产生特定的反应。另外,MOFs 可用于负载其他荧光物质,例如荧光染料、MNCs、QDs 等实现与被检测物质的特定反应。对于单独的MOFs材料作为荧光探针,其荧光特性可基于金属离子、配体,例如配体-金属电荷转移跃迁(LMCT)、配体-配体电荷转移跃迁(LLCT)、金属-配体电荷转移跃迁(MLCT)。基于LMCT 荧光机理,Wang等[126]通过调节Eu3+、Tb3+、Dy3+金属离子比例,以3,5-二羧基苯基硼酸(5-bop)作为有机配体得到lab-on-MOFs材料,其与金属离子、阴离子、小分子、生物大分子等不同目标物质相互作用后产生独特的颜色变化,可用于多目标物质检测。根据LLCT 荧光机理,Cornelio等[127]通过改变有机配体得到了具有不同发射光的MOFs材料MUF-77。
MOFs 可用于封装分子荧光染料合成荧光探针。分子荧光染料(如罗丹明、异硫氰酸盐等)以成本低、灵敏度高及易操作而广泛应用于荧光探针、荧光成像等领域,是最常用的荧光物质之一。然而,分子荧光染料具有聚集诱导猝灭现象、光稳定性差、生物相容性低等缺点从而限制了其应用。通过将分子荧光染料封装于多孔的MOFs材料可增加其稳定性,提高荧光传感能力[121]。Ye等[128]将5-氨基荧光素负载于MOFs 材料MOF-801,可阻断大分子的干扰从而增强探针的选择性及生物相容性,探针可用于体外检测ClO-。对于本身具有荧光传感能力的MOFs 材料,将其封装分子染料可得到比率型纳米荧光探针。Zhang等[129]将罗丹明B负载于锆-萘基MOFs合成比率型荧光探针,其对于水中Fe3+及Cr2O72-的检测分别具有更高的选择性及灵敏度。聚集诱导发光(AIE)荧光分子具有良好的生物相容性及抗光漂白性,近年来已有越来越多的AIE 材料被研究及应用。据推测,AIE 的基本原理可能是分子处于聚集态,分子内部运动限制从而使得激发态的电子以辐射跃迁的方式回到基态而产生荧光。将AIE 荧光染料封装进MOFs 材料内部空腔进一步限制AIE 分子运动可得到一种新的荧光探针。基于MOFs 材料及AIE荧光分子,Lu等[130]合成的新型荧光探针具有更强的荧光传感能力,可用于检测Cu2+。
碳量子点(CQDs)作为一种具有优异光学性质的零维碳纳米材料,具有较好的水溶性、成本低、原料来源广、生物相容性好等优势而广泛应用于分析检测、生物成像、药物递送等领域[131]。然而,在具体应用过程中,CQDs 可能存在聚集沉淀等现象而影响作用效果。CQDs 与MOFs 材料的复合可在一定程度上抑制其聚集作用,赋予其pH及温度耐受性从而提高稳定性。根据荧光内滤效应以及荧光共振能量转移原理,Wang 等[132]合成了CQDs@Eu-MOF 材料用于溶液中Cr(Ⅵ)的检测。CQDs也可与其他荧光分子共同负载于MOFs 材料合成比率型荧光探针,可用于检测两种或多种物质,从而降低了实验失误率。Qin等[133]以MIL-53为基本框架,引入CQDs以及Eu3+合成可用于检测尿液中二氨基甲苯的MOFs材料。除了CQDs外,Chen等[134]将巯基乙酸修饰的碲化镉量子点与CQDs共同负载于ZIF-8从而避免二者聚集沉淀造成的荧光猝灭,所合成的复合MOFs材料可用于检测抗坏血酸以及脱氢抗坏血酸。与CQDs类似,钙钛矿量子点的稳定性问题也可通过负载于MOFs 材料解决。Zhang 等[135]成功将钙钛矿量子点CH3NH3BbBr3封装于MOF-5 中,所合成的材料可在30~230 ℃范围内用于检测水溶液中的多种金属离子。
MNCs 虽然具有优异的物理化学性质,然而其具有较高的表面自由能从而存在一定程度的不稳定性,易产生不可逆聚集从而限制其应用。当AuNCs负载于MOFs材料中时,由于MOFs材料中有限的空间可限制AuNCs 的分子运动,具有更强的荧光强度及光稳定性。Xia 等[136]将AuNCs 引入ZIF-8 中得到的复合材料的量子产率及荧光寿命大幅提高,当荧光探针检测胆红素时,MOFs材料降解导致荧光强度显著降低。Hu 等[137]将PEI 稳定的CuNCs 负载于ZIF-8 合成得到可用于检测血清样品中H2O2的荧光探针,并证实其在检测葡萄糖氧化酶活性方面具有潜力。
镧系金属作为一类重要的发光材料,其荧光发射峰位覆盖从紫外光到红外光的极宽光谱范围,不仅具备长发光寿命、大Stokes 位移、窄带发射等优势,还表现出可调的配位行为,在光学材料、荧光探针、生物成像等领域得到了广泛应用。当镧系金属封装在MOFs 材料中,有机配体可作为天线吸收激发光能量,之后将能量传递给镧系金属离子从而实现高效荧光发射[138]。基于稀土元素构建的MOFs荧光纳米探针具有独特的发光机理,称为“天线效应”:通过有机配体吸收能量至激发态,之后能量转移至稀土元素发光。与其他配合物相比,基于镧系金属配位聚合物的MOFs 荧光纳米探针的发光性能具有更好的可调控性。这可能是因为镧系金属MOFs 材料的荧光性能可通过多种途径进行调节,例如中心离子的配位环境、主客体相互作用、主体框架孔结构等。自2004 年首次报道稀土MOFs 材料用于金属离子(如Ag+、Zn2+等)的检测后,基于稀土的MOFs荧光纳米材料研究逐步成为热点。Liu等[139]报道了首例澜系金属MOFs 材料用于检测Ag+。Zhang 等[140]合成具有良好生物相容性的Eu3+/Ag+@UiO-66-(COOH)2用于检测肺中H2S,通过负载稀土复合光敏剂Ag+后可有效增强Eu3+的发光性质。Li等[141]合成可测定ClO-以及DPA 的高效多功能荧光探针。首先合成的NH2-HPU-17 中功能氨基对于ClO-具有响应性,可使MOFs 材料由蓝色转化为黄绿色。另外,NH2-HPU-17可用于负载Tb3+并增强其在水溶液中的荧光特性,从而实现检测DPA 的目的。Wang 等[142]合成了两种镧系Lu及Y 纳米多孔MOFs材料,将Eu+以及Tb3+引入Lu-MOF 合成双发射比率型荧光探针用于检测抗生素奥硝唑以及罗硝唑,所合成的YMOF荧光探针用于检测血清中阿米巴肝脓肿的生物标志物C反应蛋白自身抗体。
3.2 光响应金属-有机框架的应用
MOFs材料在荧光纳米探针领域已得到广泛应用,常用于金属离子、阴离子以及小分子的检测。作为荧光纳米探针使用的MOFs 材料主要通过两种方式构建:以具有光响应性的金属离子/簇构建单独的荧光MOFs 或以MOFs 为原料封装光学活性客体。由于MOFs 材料具有高孔隙率、大比表面积、孔径可调节以及可剪裁等优势,可用于精确识别、吸附目标分析物。对于部分有机物质,由于其分子较小且其含有的氨基、羟基等基团可与MOFs材料中的有机配体产生分子间作用力,因而MOFs材料对于目标物质具有较好的灵敏度和选择性。MOFs材料的荧光性能受多种因素影响,如配位环境、温度、主客体相互作用等,当主客体发生超分子相互作用时导致MOFs 材料的电荷分布发生改变,进而导致该荧光纳米探针的发射光谱波长、荧光强度及寿命等发生改变,从而实现对目标物质的检测。MOFs材料对于目标物质的检测主要通过荧光猝灭及荧光增强的方式进行。对于荧光猝灭型MOFs,当其与客体分子相互作用后特征性荧光降低或消失,因此待测物质的浓度较高时则几乎难以检测到荧光变化,故检测限相对较高,对检测某些具有荧光猝灭性质的物质(Cu2+、Hg2+)具有良好的应用价值。增强型荧光探针则相反,其本身无荧光或只有很弱的荧光,当其与客体分子相互作用时荧光增强,荧光信号的变化更易有效检测。
MOFs材料在金属离子检测领域已有广泛应用,例如过渡金属离子、碱金属离子等。对于Hg2+以及CH3Hg+的选择性检测,Chen等[143]合成了配位聚合物[Zn(ppvppa)(1,4-NDC)]n,通过吡啶上的氮原子可实现对上述两种离子的选择性检测。此外,Wang 等[144]合成了BA-Eu-MOF 增强型荧光探针实现对Hg2+以及CH3Hg+的高效检测。对于碱金属离子,Huang 等[145]合成了猝灭型荧光探针用于K+的检测,由于金属阳离子与N、O 原子配位能力降低从而产生分子内电荷转移效应,导致MOFs材料的荧光性质降低。基于2-Eu的荧光增强作用,Wang等[146]合成了增强型荧光探针Ln-MOFs用于Mg2+的检测。
阴离子在环境科学、生物医药等领域扮演重要角色,近年来,对于阴离子的检测越来越受到研究人员的重视[147]。基于此,Yao等[148]合成了荧光猝灭型MOFs材料Zn-Ⅱ-MOF材料(即NUM-5),其对于水溶液中Cr2O72-以及CrO42-具有高选择性、快速响应特征,检测限分别为0.7、0.3 ppm。Li 等[149]在MOFs 腔内组装荧光团以及识别基团(即蒽基基团和含半花菁的CN-连接体),CN-与半花菁的选择性结合抑制了两者之间的能量转移,从而导致荧光增强,所合成的荧光探针对CN-的检测限可达0.05 µmol/L(如图7)。Yang等[150]报道通过硼酸调节镧系金属MOFs材料的光学性质制备比率型荧光探针并用于水溶液中F-检测,检测限为2 µmo/L。当F-离子浓度增加时,在275 nm光激发下Eu-MOF1在366 nm波长的荧光增强,而在625 nm 波长的荧光减弱,且荧光颜色由红色转变为蓝色。Yang 等[151]将具有固有荧光的氨基衍生物用于选择性地检测水溶液中的PO43-,MOFs材料中的Zr-O 节点对于PO43-具备很强的捕获能力。在UiO-66-NH2MOFs 材料中,Zr-O 以及BDC-NH2分别为PO43-识别位点及信号报告基团,且几乎不受其他离子干扰,具有良好的选择性。MOFs荧光纳米材料除了可检测水溶液中的阴离子外,还可用于含水量的检测。传统检测固体或液体样本中含水量的方法为Karl Fischer 滴定法,具有操作相对繁杂、成本高的不足。使用MOFs 材料可构建基于稀土元素的双色比率荧光传感器,通过荧光变化实现对含水量的快速检测。

图7 多组分MOFs材料“turn on”型荧光探针设计示意图(A)以及含有蒽和半花菁基团的MOFs材料合成路线图(B) [149]Fig.7 Schematic representation for the design of a turn-on fluorescence sensor in multicomponent MOFs(A) and synthetic routes of MOFs with anthracene and hemicyanine moieties(B) [149]
通过选择合适的有机配体、金属节点或修饰方式,MOFs 材料可广泛用于有机小分子检测。2007年Chen 等[152]采用发光MOFs 材料检测有机小分子,稀土MOFs 材料EuBTC 可高效检测水中的有机小分子DMF 及丙酮分子。Du 等[153]选择PCN-224 为识别单元,AgNPs 同时作为猝灭剂及H2O2的识别单元合成了一种可用于检测葡萄糖的荧光纳米探针。AgNPs 与在GOx 催化氧化葡萄糖过程中产生的H2O2反应生成Ag+并从PCN-224中释放出来,从而恢复PCN-224的荧光性质。Hao等[154]首次使用镧系MOFs材料用于人类尿液样本中1-羟基芘的检测,其荧光性质可通过荧光共振能量转移过程被1-羟基芘猝灭。Hu等[155]合成了多孔且可高效发射强蓝光的猝灭型荧光探针LMOF-241 用于检测黄曲霉毒素B-1,由于荧光探针的孔径大于黄曲霉毒素B-1 且电子可转移至被检测物质,黄曲霉毒素B-1 可进入LMOF-241 发生反应并产生荧光猝灭效应。Dong 等[156]通过在银硫簇基MOFs 材料的连接体中引入氨基基团实现了来自同一连接体发色团的双荧光-磷光发射,并实现了超快双功能荧光开关,由O2触发荧光关闭,由挥发性有机化合物触发荧光开启。
由于MOFs 材料的荧光性质受到温度、溶剂、客体分子等多方面因素影响,通过调节配体分子结构和中心离子的类型可设计具有不同荧光发射波长的探针,因此,MOFs材料可应用于多种物质、多领域的荧光检测。然而,多数MOFs 材料是由非极性的芳环构成的配体,在水溶液中分散性不佳是导致其在水相中应用受限的重要原因。通过设计合成能稳定分散于水相的MOFs 材料将对拓展其在分析检测领域的应用具有重要意义。
4 其他荧光纳米探针
除上述荧光纳米探针外,随着纳米材料科学的发展,也发展了其他荧光纳米探针如稀土荧光纳米探针、碳量子点(CQDs)等。其中,稀土掺杂荧光纳米探针被称为最具应用潜力的近红外二区纳米探针。稀土离子特殊的4ƒ-4ƒ电子层赋予其优异的光学性能,稀土荧光纳米探针具有发射宽度窄、Stocks位移大、荧光寿命长、生物相容性较好等优势,有利于实现高质量荧光成像。然而其仍面临吸收截面小、发光效率低、表面缺陷会导致荧光猝灭等问题[157]。稀土荧光纳米探针的荧光来源于稀土离子的4ƒ电子发生能级跃迁,由于4ƒ电子的组态分裂且能级结构丰富,使得其发射范围可覆盖紫外区到短波近红外区(200 ~1 700 nm),且由于稀土离子的4ƒ电子发生跃迁受到外层电子屏蔽作用,表现出较窄的发射谱线以及良好的正交性[158]。稀土荧光纳米探针仅涉及离子能级的跃迁,因而其稳定性较好、抗光漂白能力优异[159]。此外,稀土离子(例如Yb3+及Nd3+)可吸收近红外激发光能量并由于自身的辐射弛豫传递给其他离子发光。稀土荧光纳米探针主要由基质材料(通常为光学惰性且晶格声子能量低的物质)、敏化剂(需具备较大的吸收截面)及发光中心(正三价稀土离子)组成。该荧光纳米探针的敏化主要通过掺杂合适浓度的稀土离子、与有机染料或量子点复合来实现。掺杂合适的稀土离子是提升荧光纳米探针发光性能的核心要素。适当增加稀土离子浓度有助于增加吸收截面,然而由于稀土离子之间存在交叉弛豫现象,稀土离子浓度过大可能造成荧光猝灭。由于有机染料等材料具有吸收截面较大的优势,因此可用于敏化稀土掺杂的荧光纳米探针。另外,功能化的有机染料也便于赋予荧光纳米探针额外的生物功能。有机染料作为敏化剂要解决光漂白、与稀土离子光重叠度不高等问题,且多数有机染料的激发波长低于1 000 nm 不利于实现深层组织的生物成像[160]。稀土掺杂的荧光纳米探针常采用核壳结构,内部核结构常含有敏化剂及发光中心,外壳层为多层惰性或活性壳层,其中惰性壳层主要用于阻隔壳层之间的能量传递及钝化表面缺陷,通过核壳结构设计可调节壳层之间的能量传递过程从而提升其发光性能、延长荧光寿命等。常用的稀土荧光纳米探针合成方法主要包括共沉淀法、热分解法以及水/溶剂热法等。共沉淀法应用较早,具有制备成本低、工艺简单、效率高、反应条件温和等优势,然而其制备的纳米粒子存在较多表面缺陷。热分解法制备条件相对复杂苛刻,需在氮气保护下的300 ℃油酸/十八烯体系中进行反应,所制备的荧光纳米探针不能直接应用于生物体系。而水/溶剂热法操作简单,可在相对温和的反应条件下通过“一锅法”制备得到结晶度较高的荧光纳米探针。虽然稀土掺杂荧光纳米探针具有上述诸多优势,然而其仍面临应用局限,未得到实际临床应用。其存在的主要共性问题有水溶液中的分散稳定性差、量子产率和组织穿透深度不够。由于稀土掺杂荧光纳米探针尺寸较小且制备过程中反应体系多为有机溶剂,导致其易发生团聚。由于稀土掺杂荧光纳米探针存在浓度猝灭效应,使得量子产率无法持续提升。而低量子产率导致荧光纳米探针的组织穿透深度不足以达到临床应用要求。
CQDs作为近些年新型的荧光纳米材料引起科研工作者的广泛关注。与上述传统QDs相比,其粒径较小有利于应用于细胞体系,而生物相容性则明显优于QDs,可作为一种理想的荧光纳米探针应用于分析检测、生物成像以及生物传感等领域。CQDs表面丰富的氨基以及羧基等亲水性基团可赋予其优异的水溶性。此外,与其他荧光纳米探针相比,CQDs 的荧光性质表现出以下特征:首先,CQDs 的荧光发射峰位置以及强度随激发波长改变。其次,CQDs具备上转换发光优势,更适合应用于生物体内的成像及检测。另外,CQDs可通过单波长激发后产生两次以上的荧光发射,从而实现利用两个以上荧光峰的信号变化进行物质的比率检测。CQDs制备方法简单、原料廉价易得,成本较低,易应用于生物医学领域。通常CQDs的制备方式可分为“自上而下法”和“自下而上法”两类。一般情况下CQDs的合成需经历脱水、聚合、碳化及钝化等过程。“自上而下法”是通过化学或物理法将大尺寸的碳材料制备为小尺寸的CQDs,例如通过应用电弧放电法、电化学法以及激光烧蚀法等。“自下而上法”则是以更小尺寸的碳材料为前驱体制备CQDs,采用的方法有微波法、模板法以及水热溶剂法等。制备方法的差异使得CQDs的荧光性质不尽相同,由于CQDs具有原料来源广泛、生物相容性较好、易于制备等优势使得其可作为荧光纳米探针而在生物医学领域具有广泛应用。CQDs的单发射荧光探针可通过与目标物质发生相互作用引起荧光猝灭或重新恢复荧光从而实现对目标物质的定量检测。比率型荧光探针则可通过两个或两个以上的不同发射波长下的荧光强度从而降低测定误差。比率型CQDs 荧光纳米探针主要分为纳米复合探针以及双发射荧光探针。纳米复合探针可通过引入其他荧光材料(如有机荧光染料、MOFs 等材料)与CQDs 通过物理或化学方式结合构建比率型荧光纳米探针。双发射荧光探针则通过合成具有双波长荧光峰的双发射CQDs 进行比率荧光检测,其在单一激发波长的作用下产生两个不同发射波长峰,相比纳米复合探针,其操作过程更简便[161]。然而,CQDs 仍存在缺陷,例如其荧光量子产率低于QDs,发射光谱宽,发射波长接近于蓝光区从而易受到生物体自发荧光干扰。
5 总结与展望
本文主要介绍了目前研究较多的QDs、MNCs、MOFs 及其他荧光纳米探针,阐述其基本组成、主要合成方法以及应用(不同种类荧光纳米探针的性质比较见表1)。QDs较为常用的合成方法可分为有机相合成法及水相合成法,MNCs 的合成策略可分为自下而上法以及自上而下法,MOFs荧光纳米探针的合成策略为单独的MOFs或负载其他物质。QDs的荧光强度及光稳定性等优于传统有机染料,随着其与不同分子连接技术的成熟,QDs 可作为有机荧光染料的有效补充替代,将在当前热门的生物医学领域(如基因组学、蛋白质组学以及体内目标物质的检测等方面)具有广阔的应用前景。而与传统有机染料及QDs相比,MNCs 具有粒径小、尺寸依赖及可调控荧光、生物相容性较好等优势。MNCs已发展成为一类新兴的超小型、具有优异生物相容性的荧光纳米材料,其在生物标记以及光电发射器等领域均有发展前景。MOFs材料具有高度可定制、丰富的化学功能性等特点,近年来逐渐成为研究热点,其在化学传感、物质吸附及分离、化学催化等领域均有应用,在小分子及生物大分子检测、细胞成像、活体诊断等领域具有广阔的应用前景。

表1 不同种类荧光纳米探针的基本性能及其优缺点Table 1 The properties,advantages and disadvantages of different types of fluorescent nanoprobes
近年来纳米科学的研究及应用为纳米生物光子学的发展带来新机遇,尤其是荧光纳米探针对于重大疾病的诊断及特定物质的识别和分析。通过借助纳米材料独特的物理化学性质,利用荧光纳米探针可实现对细胞以及特定分子的定位、标记及检测,逐渐成为化学传感、生物医学研究中的有力工具。为了进一步发展荧光纳米探针以将其从实验室推广至大规模应用,需要开发简单、低成本的合成方法以及设计具备高量子产率、优异稳定性和生物相容性的荧光纳米探针。此外,荧光纳米探针的生物安全性问题仍需重点关注,开发不依赖于重金属离子的高质量荧光纳米探针仍是研究热点之一。荧光纳米探针的物理化学性质与众多因素有关,例如粒径、组成成分、合成条件等,因此需要更好地理解荧光纳米探针的化学组成、表面性质、纳米结构,从而更好地推动荧光纳米探针的发展。在合成性能优良的荧光纳米探针的基础上,利用荧光纳米探针建立灵敏度高、选择性好的分析测试方法是研究人员的关注点之一。展望未来,虽然荧光纳米探针与大规模生产及应用仍有一定距离,但随着新颖纳米材料的研发及相关光子学技术的进步,更多具备优异性能的荧光纳米探针将被合成,同时,借助设计荧光纳米探针的独特性质从而促进检测手段不断丰富和多元化。
