高选择保护性迷走神经切断术在腹腔镜胃底折叠手术中的应用
2023-12-29张小虎任书林安大立李志霞伍冀湘
张小虎 任书林 刘 靖 安大立 李志霞 于 磊 伍冀湘
(首都医科大学附属北京同仁医院普外科,北京 100730)
胃食管反流病(gastroesophageal reflux disease,GERD)是由胃十二指肠内容物反流至食管和食管以外部位,引起的一系列临床综合征。临床主要表现为烧心和反酸,引起并发症包括食管炎、咽炎、哮喘等,严重影响患者的生活质量。GERD的治疗包括:生活饮食调理、心理治疗、药物治疗、胃镜下治疗及抗反流手术治疗。抗反流手术通过修复和加强胃食管连接部(gastroesophageal junction,GEJ)的功能和解剖结构,通常可持久控制大多数形式的反流和反流症状,已证明具有良好的疗效。腹腔镜胃底折叠术(短松Nissen术式)是治疗GERD应用最多的手术方式[1~3],将游离后的胃底部在食管末端形成360°包绕,通过增加食管远端压力发挥抗反流作用,同时降低胃底储存食物空间促进胃排空减少反流,从而达到治疗目的。腹腔镜胃底折叠术需要对GEJ及胃底进行游离,在传统手术方式中,通常是经小网膜无血管区直接向胃小弯侧近端及食管末端分离裸化GEJ,该路径操作简捷出血风险小,但是需要切断迷走神经前干,迷走神经肝胆支也极易受到损伤。迷走神经损伤尤其是主干及主要分支损伤会影响其支配器官的功能,在胃癌、脾切除等手术中保护迷走神经被尝试并推荐[4~6]。在切断迷走神经治疗十二指肠溃疡历程中,高选择性迷走神经切断术仅切断迷走神经前后干发出的胃支,保留前后干终末端的鸭爪支,保护迷走神经支配远端胃运动功能同时达到降低胃酸及胃蛋白酶分泌的目的,获得良好治疗效果并减少手术并发症被认可接受[7]。目前,针对腹腔镜胃底折叠术(短松Nissen术式)是否需要完整保留腹腔迷走神经及如何保留迷走神经还没有形成共识。2015年9月我院将高选择保护性迷走神经切断术引入腹腔镜胃底折叠术(短松Nissen术式),术中仅切断迷走神经前后干向近端胃发出的胃支,保留迷走神经主干及其余分支,尽可能保护迷走神经,本文探讨其安全性、可行性及有效性,并与传统手术进行比较,报道如下。
1 临床资料与方法
1.1 一般资料
回顾性分析我院2014年1月~2019年12月78例GERD合并食管裂孔疝而接受腹腔镜胃底折叠术(短松Nissen术式)和食管裂孔疝修补术的临床资料。男44例,女34例。年龄25~76岁。BMI 21.0~31.0。均有典型反酸、烧心等反流症状,应用质子泵抑制剂治疗史6个月以上,胃食管反流病调查问卷(GERD Q)量表[8,9]均≥8分,24 h食管pH监测均存在病理性反流(DeMeester评分>14.72分[10,11]),食管测压提示食管下括约肌静息压力(lower esophageal sphincter pressure,LESP)下降(固态管检测<15 mm Hg),胃镜、上消化道造影检查证实合并食管裂孔疝。18例合并原发性高血压、冠状动脉粥样硬化性心脏病、糖尿病。根据是否对迷走神经进行保护把患者分为2组,传统手术组38例(2014年1月~2015年8月病例)和迷走神经保护组40例(2015年9月~2019年12月病例)。2组一般资料差异无显著性(P>0.05),有可比性,见表1。
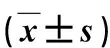
表1 2组术前一般资料比较
食管裂孔疝分型[12]:Ⅰ型,滑动型食管裂孔疝,胃食管连接部迁移至膈肌上方,胃保持其正常的形态,胃底低于GEJ;Ⅱ型,食管旁疝,胃食管连接部保持在其正常的解剖位置,一部分胃底通过膈肌食管裂孔旁疝入胸腔;Ⅲ型,Ⅰ、Ⅱ型的混合型疝,GEJ和部分胃底一起通过食管裂孔疝入胸腔,GEJ和胃底均高于膈肌;Ⅳ型,巨大食管裂孔疝,疝内容物除胃以外,还有腹腔内其他脏器如大网膜、结肠或小肠等。
病例选择标准:内科药物治疗反流症状控制失败;内科药物治疗有效,应用药物治疗6个月以上,患者有意愿接受手术治疗或摆脱长期药物治疗;有GERD并发症,如Barrett食管、反流相关哮喘、咳嗽等;明确合并食管裂孔疝;无严重器质性疾病;术后6个月完成24 h食管pH监测、食管测压及相关问卷调查等术后随访。
1.2 方法
1.2.1 传统手术组 全身麻醉。仰卧分腿头高脚低位。脐部置入10 mm trocar,为腹腔镜进镜孔,左锁骨中线肋缘下(10 mm trocar)、右锁骨中线肋缘下(5 mm trocar)为术者左右操作孔,左腋前线肋缘下(5 mm trocar)为助手辅助操作孔,剑突下置入肝左叶拉钩。腹腔镜下腹腔探查后,经左侧入路,沿胃大弯离断部分胃底韧带及胃短韧带,游离胃底至左膈肌脚根部,局部填塞纱布。转至右侧,经肝胃韧带无血管区直接向GEJ分离,使GEJ完全裸露,分离过程切断迷走神经前干,迷走神经肝胆支同时切断可能性大,解剖左右膈肌脚,暴露食管裂孔。经GEJ后方将胃底自右侧拖至左前方,包绕食管,4号丝线行胃底折叠360°缝合第1针,7号丝线缝合关闭食道裂孔2~4针,使其与食管之间在食管没有张力时不存在间隙。放入防粘连合成补片[型号:PCO2H1,美国柯惠,批文号:国食药监械(进)字2008第3462344号],并固定。距离胃底折叠360°第1针缝合1.5 cm左右,4号丝线行胃底折叠360°缝合第2针(胃底右侧、食管、胃底左侧三点缝合),最后,将抗反流瓣与膈肌固定3针。局部放置腹腔引流管,手术结束。
1.2.2 迷走神经保护组 全身麻醉。仰卧分腿头高脚低位。脐部置入10 mm trocar,为腹腔镜进镜孔,左锁骨中线肋缘下(10 mm trocar)、右锁骨中线肋缘下(5 mm trocar)为术者左右操作孔,左腋前线肋缘下(5 mm trocar)为助手辅助操作孔,剑突下置入肝左叶拉钩。手术在裸化右侧GEJ时采取高选择保护性迷走神经切断术操作,自胃小弯近GEJ 1/3处紧贴胃壁向GEJ游离,术中仅切断迷走神经向近端胃发出的胃支,保留迷走神经前后干及其他分支,完成GEJ的裸化。其余操作同传统手术组。腹腔段迷走神经分支走行见图1,高选择性迷走神经切断手术示意图见图2,高选择保护性迷走神经切断术应用于腹腔镜胃底折叠术中迷走神经离断示意图见图3。

图1 迷走神经腹腔段分支(自绘) 图2 高选择性迷走神经切断术(自绘) 图3 高选择保护性迷走神经切断术应用于腹腔镜胃底折叠术(自绘)
1.3 观察指标
手术时间(术区消毒至穿刺口缝合完毕)、手术出血量(术中纱布血液浸透程度和吸引器吸出血液综合评估)、肛门排气时间、术后住院时间(出院标准:自主活动,可以经口进食流食,切口愈合,无需要住院处理的术后并发症)、术后30 d内发生腹胀、腹泻、吞咽困难等手术并发症,术后6个月GERD Q评分、DeMeester评分、LESP和消化道反流症状控制情况。
1.4 疗效评价
根据消化道反流症状程度和发作频次进行术前以及术后6个月问卷调查,参考RDQ评分标准[13]进行评分,症状评分=程度分+频次分,见表2。疗效评价[14]:①治愈:术后反流症状完全消失,停止应用抑酸、抗反流等药物;②治疗有效:术后评分较术前评分下降,术后仍有反流症状,程度及频次较术前降低,抑酸、抗反流药物应用减少;③治疗无效:术后反流症状较术前无改善,仍需要长期应用抑酸、抗反流药物。

表2 反流症状评分
1.5 统计学处理
2 结果
2组均顺利完成手术,无术中脏器副损伤发生。传统手术组术后住院时间明显长于迷走神经保护组(P<0.05),2组手术时间、术中出血量、术后排气时间差异无显著性(P>0.05),见表3。2组术后发生吞咽困难11例,术后3个月内全部缓解;迷走神经保护组并发症发生率显著低于传统手术组(P=0.012),见表4。78例术后随访6~60个月,平均35.6月,其中54例随访时间>36个月,随访者详细叙述问卷表的各项内容,让患者对每种症状的发作频率及严重程度进行回答。术后6个月治疗效果差异无显著性(P=0.816),见表3。术后2组6个月GERD Q量表评分、DeMeester评分、LESP差异无显著性(P>0.05),见表5。
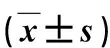
表3 2组术中、术后情况比较

表4 2组术后30 d并发症比较
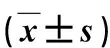
表5 2组术后6个月GERD Q量表评分、DeMeester评分和LESP比较
3 讨论
腹腔镜抗反流手术应用至今已有30年,早期的安全性、有效性和10年左右的抗反流持久性已被充分证明[15~18]。我院开展腹腔镜手术治疗GERD的初始阶段,采用传统的手术方式分离GEJ,这种方法通常会对迷走神经前干及肝胆支造成损伤。迷走神经损伤可导致术后上腹饱胀、腹泻以及胆囊结石发生等相关并发症[4,19~21],也可能引起胃排空延迟甚至胃瘫进而需要二次手术[22],胃排空延迟进一步可引起GERD患者术后反流症状复发[23]。为降低迷走神经损伤导致的术后并发症,术中采取保护迷走神经措施是十分必要的。保护腹腔迷走神经是胃肠外科医生长期以来关注的焦点,在GERD手术中,迷走神经应如何保护尚未达成广泛共识。高选择性迷走神经切断术可以降低胃酸分泌并且保护胃排空功能,减少术后并发症[7,24],完全契合腹腔镜胃底折叠术迷走神经保护理念。高选择性迷走神经切断术切断胃体近端迷走神经胃支的过程即是胃底折叠术GEJ游离过程,在操作上二者具有一致性。将高选择性迷走神经切断术近端胃迷走神经胃支切断方式应用于腹腔镜胃底折叠术中GEJ游离,无论从功能保护理念还是手术操作都是保护迷走神经理想的手术方法。
在腹腔镜胃底折叠手术中,进行高选择保护性迷走神经切断术操作,需要贴近胃壁游离小弯侧上1/3胃体近端及食管末端,切断迷走神经部分胃支、贲门支,保留肝胆支及迷走神经前干主干,增加了手术难度及出血风险,对手术精细程度要求更高。我院GERD手术均在3D腹腔镜设备及超声刀等能量平台应用下完成,术中能够良好地辨识迷走神经以及术区的细微解剖结构。本研究2组手术时间、术中出血量无显著差异(P>0.05),2组术后6个月GERD Q量表评分、DeMeester评分、LESP、手术治愈率差异无显著性(P>0.05),提示将高选择保护性迷走神经切断术应用于腹腔镜胃底折叠术中操作可行,与传统手术方式相比治疗效果相同。
以往研究中显示腹腔镜胃底折叠术存在术后腹胀及腹泻风险[25,26]。术后腹胀与迷走神经损伤胃排空延迟有关。迷走神经保护组术后腹胀发生率低于传统手术组(7.5% vs. 10.5%),但无显著性差异(χ2=0.005,P=0.943),可能与传统手术组迷走神经后干得以保留有关,还需要进一步研究证实。胃癌根治术中保留迷走神经腹腔支及肝胆支可明显降低腹泻发生率[27],本研究中传统手术组发生1例术后腹泻,考虑术后腹泻发生与迷走神经腹腔支损伤可能性更大。腹腔镜胃底折叠术后短期内吞咽困难发生相对常见,发生原因一方面与术区组织水肿导致食管末端张力增高有关,另一方面与迷走神经损伤导致食管下段失去神经支配导致食管、贲门舒张力减弱、张力增加有关。2组术后吞咽困难发生率分别为23.7%、5.0%,迷走神经保护组术后吞咽困难发生明显低于传统手术组(χ2=5.616,P=0.018),证实保护迷走神经有助于维持食管末端及贲门的正常运动功能。与传统手术组比较,迷走神经保护组手术时间和术中出血量无增加(P>0.05),术后并发症发生率显著性低(χ2=6.267,P=0.012),术后住院时间明显缩短(t=-2.172,P=0.033),证实采取高选择保护性迷走神经切断术保护迷走神经更加安全可行。
综上所述,胃底折叠术是治疗GERD的有效治疗方法,手术中正常的迷走神经功能应尽可能予以保护,将高选择保护性迷走神经切断术应用于腹腔镜胃底折叠术(短松Nissen术式)是保护正常迷走神经功能的方法之一,安全、可行、有效。
