乳腺钼靶定位体表标记在触诊阴性乳腺钙化灶开放活检中的应用
2023-12-29王芹芹
栗 辰 王芹芹 张 春
(北京大学国际医院乳腺外科,北京 102206)
乳腺癌是女性常见恶性肿瘤,乳腺钼靶是乳腺疾病筛查的重要方法,广泛应用于乳腺钙化灶良恶性鉴别。中国抗癌协会乳腺癌诊治指南与规范(2021年版)[1]指出,对于乳腺钼靶发现的可疑钙化(如不定形钙化、粗糙不均质钙化、细小多形性钙化、细线样或细线分枝状钙化),需要进一步活检明确诊断。将临床触诊阴性、超声无异常回声的可疑钙化灶准确定位后完整切除进行活检,对乳腺癌及癌前病变的早期诊断和治疗有重要意义。对于此类可疑钙化灶,临床多采用乳腺X线立体定位真空辅助活检、导丝定位手术活检。但乳腺X线立体定位床或配备定位活检装置的乳腺X线机价格昂贵,对设备要求高,操作过程复杂,手术过程辐射暴露量高,且患者需能够耐受长时间俯卧式定位活检。我们自创利用乳腺钼靶X线片定位触诊阴性可疑乳腺钙化灶范围并体表标记的方法,2018年9月~2023年8月对63例的65处可疑钙化灶进行开放活检,报道如下。
1 临床资料与方法
1.1 一般资料
本组63例,均为女性,年龄33~70岁,中位年龄51岁。乳房疼痛47例,无症状16例,均因要求乳腺检查就诊乳腺外科。临床查体未触及乳腺结节。乳腺超声结果阴性。57例40岁及以上女性按中国抗癌协会乳腺癌筛查指南[2]常规行乳腺钼靶检查,6例小于40岁女性均为患者要求行乳腺钼靶检查,提示钙化灶,单侧61例(左侧37例,右侧24例),双侧2例(每侧均为单发),共65个病灶,位于外上象限48个,外下象限5个,内上象限7个,内下象限5个;深度为8个位于乳腺前1/3,30个中1/3,27个后1/3;钙化灶长径3~70 mm,中位数7 mm。钙化的形态特征及分布情况按照BI-RADS标准[1],形态为不定形钙化45个,粗糙不均质钙化6个,细小多形性钙化14个;散在分布6个,区域状分布1个,集群簇状分布55个,线样分布2个,段样分布1个。
入组标准:①临床查体触诊阴性,乳腺超声未提示可疑钙化,乳腺钼靶头足位(craniocaudal,CC)和内外侧斜位(mediolateral oblique,MLO)摄片均提示可疑钙化[1];②术前检查无手术禁忌证。
排除标准:①超声下可定位的钙化;②重度全身性疾病或凝血功能障碍。
1.2 方法
1.2.1 乳腺钼靶定位 术前于立位行乳腺钼靶X线摄片(如为近期外院乳腺钼靶胶片,按胶片比例尺计算钙化位置),在CC位片上,自乳头根部做乳腺基底部垂线,测量钙化灶两端与垂线间距离(图1),在MLO位(斜60°)片上,自乳头根部做胸大肌垂线,测量钙化灶两端与垂线间距离(图2)。根据测量结果画出立位体表投影定位示意图(图3)。
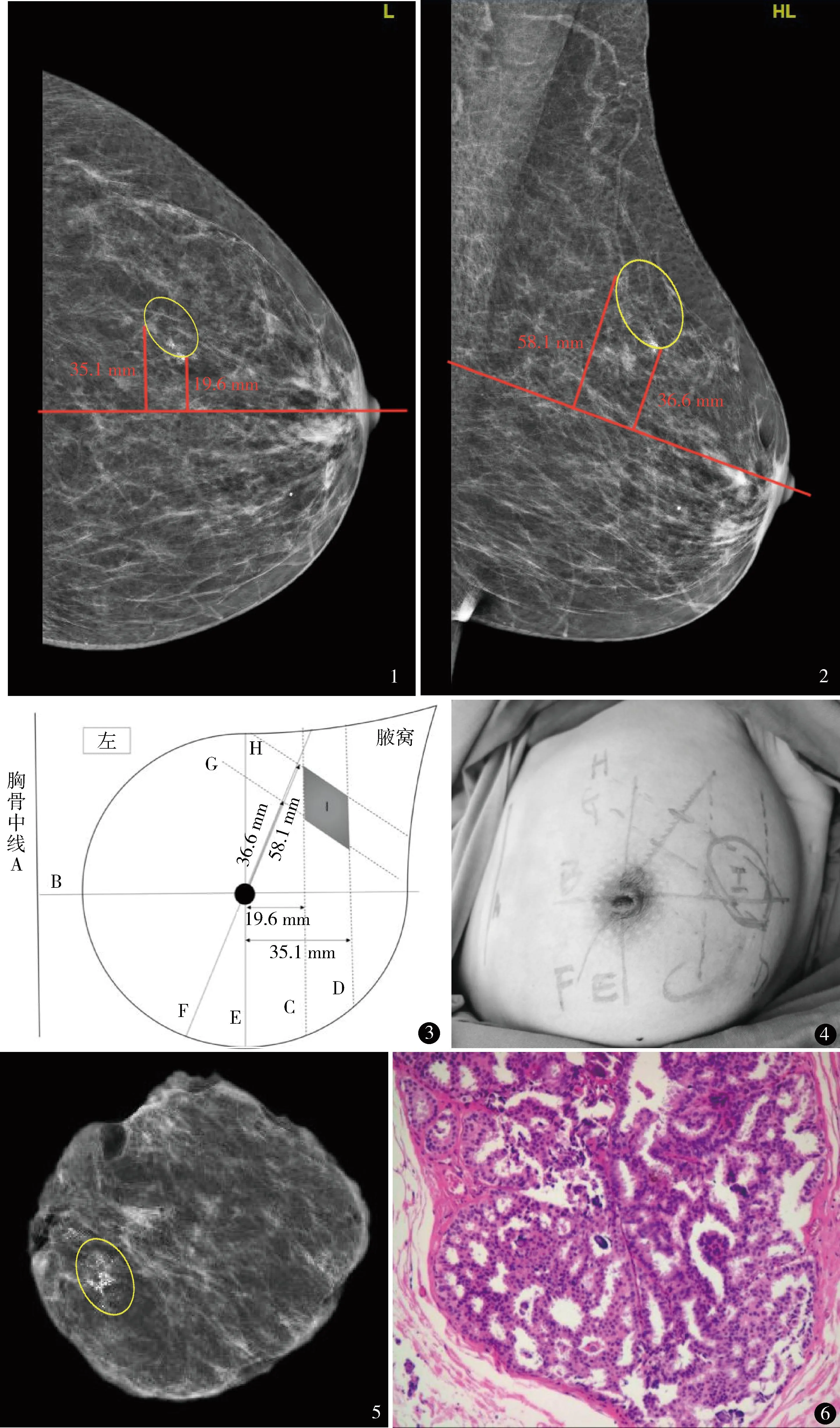
图1 左侧外上象限簇状不定形钙化,CC位确定钙化位于外象限,测量钙化灶两端在CC轴距乳头根部距离分别为19.6和35.1 mm 图2 MLO位确定钙化位于上象限,测量钙化灶两端在MLO轴距乳头根部距离分别为36.6和58.1 mm 图3 体表投影示意图:A-胸骨中线;B-经乳头垂直于胸骨中线(CC轴);C-乳头外19.6 mm,垂直于B;D-乳头外35.1 mm,垂直于B;E-自乳头中点垂直于B;F-自乳头中点与B夹角60°(MLO轴);G-乳头外上36.6 mm,垂直于F;H-乳头外上58.1 mm,垂直于F;I-C、D、G、H相交范围为钙化灶 图4 术前体表标记(上方为头侧) 图5 切除标本钼靶摄片,标本与术前钙化灶一致且切缘>2 mm且<1 cm 图6 病理诊断导管原位癌(HE染色 ×100)
1.2.2 开放活检 站立位按体表投影定位示意图于皮肤标记出切除钙化灶范围(图4)。改平卧位,常规消毒铺巾,局部浸润麻醉,切除定位的钙化灶及周围邻近1 cm左右腺体,标记上、下、内、外切缘,将标本送钼靶室摄片,明确钙化灶是否位于标本内及切缘距钙化距离(图5)。术中钼靶摄片确认标本与术前钙化灶一致且切缘>2 mm[3]。确认完整切除后标本送病理(图6),如未完整切除,则根据钙化灶距标本切缘情况再次扩大切除,并再次钼靶X线摄片确认,直至判定为完整切除。
2 结果
65个乳腺钙化灶均经体表定位后手术完整切除,其中64个病灶(98.5%)一次完整切除,1个病灶2次完整切除,无并发症发生。术中钼靶摄片可见钙化灶切缘距钙化灶距离>2 mm且<1 cm。
病理诊断良性病变47个(72.3%),包括乳腺增生16个,纤维腺瘤14个,硬化性腺病6个,导管内乳头状瘤3个,乳腺黏液性囊肿1个,非典型增生5个,小叶原位癌2个[4];恶性病变18个(27.7%),包括导管原位癌15个,导管原位癌伴微浸润2个,浸润性非特殊型癌1个。
3 讨论
临床工作中主要通过乳腺钼靶来筛查乳腺钙化灶,乳腺钙化灶是诊断乳腺癌的重要征象,特别是乳腺导管原位癌[5~7],需要对可疑钙化灶行组织学评估明确其病理性质[8]。超声阴性且临床触诊阴性但乳腺钼靶提示的可疑钙化灶,定位活检取材困难,有漏诊可能,如何对这类可疑钙化灶精准定位并活检是需要解决的问题。
乳腺钙化灶定位活检方法主要有空芯针穿刺活检、乳腺X线立体定位真空辅助活检、导丝定位手术活检[9~14]。钙化灶多散在分布,体积较小,质地硬,且肿瘤组织具有异质性,空芯针穿刺和真空辅助微创旋切虽然损伤小,但获得的组织量较少,在一定程度上存在病理低估延误病情的可能,还可能引起旋切刀堵塞损坏等[15~17]。乳腺X线导丝定位手术活检是应用乳腺钼靶二维定位或三维立体定位系统,向乳腺钙化灶内穿刺留置有倒钩的导丝,沿定位导丝将钙化灶完整切除。该技术虽然定位准确,但在定位及置入导丝过程中需要反复钼靶摄片,辐射暴露高,患者体位改变及手术操作过程中导丝有移位、脱出、折断等可能,反复操作延长手术时间,容易加重患者紧张情绪,甚至引发迷走神经反射。新技术学习曲线长,临床医生需要一定的学习时间及操作数量积累,且可能需要放射科医生参与合作,人力成本高。此外,三维立体定位系统价格昂贵,机器成本高。这些因素导致该技术推广存在一定难度。
我们采用自创的乳腺钼靶定位钙化灶并体表标记指导切除活检的方法,65个钙化灶均完整切除,其中98.5%(64/65)一次完整切除,术后病理乳腺癌占27.7%(18/65)。冯宇等[18]报道67例临床不能触及的乳腺病灶行乳腺钼靶X线三维立体定位系统引导下导丝定位活检,完整切除率100%(67/67),术后病理乳腺癌占25.4%(17/67),我们的结果与之相近。
综上所述,应用乳腺钼靶对乳腺超声阴性、临床触诊阴性的可疑钙化灶定位并体表标记后开放活检,简单易学,无需特殊设备,价格低,患者接受辐射量少,一次完整切除率高,安全可行。
