Smith-Magenis 综合征眼部多发异常表现1例
2023-11-06何晓健金玉奇郭曼赵江浩胡勇平
何晓健 金玉奇 郭曼 赵江浩 胡勇平
Smith-Magenis 综合征(Smith-Magenis syndrome,SMS)又称为染色体17p11.2 缺失综合征[1],是一种罕见的遗传病,发生率约为1/25 000,多为散发。SMS 常见症状包括独特的面部特征、骨骼畸形、不同程度的智力运动发育迟缓、睡眠障碍以及自伤行为,影响身体多个器官、系统[2]。不同患者具体症状可能因人而易。该疾病也会出现眼部异常,如小角膜、上睑下垂、斜视、虹膜异常、白内障、视神经黄斑发育不全、近视、视网膜脱离和格子样变性等[1-7],但未见葡萄膜炎、带状角膜变性等报道。现回顾分析1 例经分子遗传学确诊SMS 患儿的眼部临床资料,探索SMS 可能引起的眼部表现。
患儿女,12 岁,2021 年6 月30 日因“发现双眼视力下降半年”来浙江大学医学院附属杭州市第一人民医院就诊。患儿自出生起生长发育水平明显低于同龄儿童,伴语言发育迟缓;平时睡眠时间短,早醒;脾气急躁,动作多,注意力不集中;生气时会打脸、抠手指等自伤行为,对疼痛不敏感,但患儿家长否认有明确的眼部外伤史;无法和同龄人正常相处;生理自控力差,有遗尿现象,声音嘶哑。患儿系孕1 产1 自然分娩,无窒息抢救史,其父母及弟弟身体健康。2011 年11 月18日因语言发育迟缓在上海交通大学附属儿童医学中心经SNP 6.0 芯片进行全基因组分析,结果显示17 号染色体短臂p11.2存在约3.2 Mb 缺失(17038384-202434)。2014 年1 月22 日在浙江大学医学院附属妇产科医院经外周血荧光原位杂交技术(fluorescence in situ hybrization,FISH)分析再次证实17p11.2 微缺失。入院体格检查:体质量56 kg,身高153 cm,身材偏胖,两肺呼吸音清,腹、脊柱、四肢正常,听力无殊。特殊面容:头发浓密质地硬,方脸、鼻梁塌陷、嘴唇轻度外翻、嘴角向下,短指并有多处抓伤、中度智力低下,声音嘶哑。眼科检查:视力检查不合作,双眼角膜睑裂区带状角膜变性,角膜后可见色素性角膜后沉着物(keratic precipitate,KP),前房浅,无明显前房反应,虹膜膨隆,瞳孔尚圆,对光反应差,虹膜局部后粘连明显,晶状体表面有色素黏附,右眼晶状体呈乳白色混浊,左眼晶状体中度混浊,眼底欠清。压平眼压:18.9/16.7 mmHg(1 mmHg=0.133 kPa)。眼部B 超提示晶状体在位,玻璃体轻度混浊,视网膜平伏,见图1。A 超检查:右眼22.44 mm,左眼22.26 mm,角膜水平直径(white-towhite,WTW):右眼11.2 mm,左眼11.2 mm。血TORCH 检查提示巨细胞病毒(cytomegalovirus,CMV)IgM(+)。眼内液检查:病毒核酸检测(-),单纯疱疹病毒(herpes simplex virus,HSV)IgG(+),EB病毒(epstein-barr virus,EBV)IgG(+),其中HSV-IgG 为795.36 U/mL,远高于<9 U/mL 的参考范围。炎症因子IL-8、IL-6 均中度增高,自身抗体及免疫球蛋白正常范围,类风湿因子及人类白细胞抗原(human leucocyte antigen,HLA)B27(-),T 细胞斑点试验(-),甲状腺功能(-)。诊断:双眼慢性前葡萄膜炎;双眼带状角膜变性;双眼并发性白内障;SMS。2021 年11 月26 日患者儿入院后予以右眼全麻下白内障摘除+人工晶体植入+前段玻璃体切割+后囊膜截开术,术中晶状体悬韧带未见明显异常,术后患儿视物较术前明显好转,人工晶状体位正,眼底可见视网膜平伏,见图2。
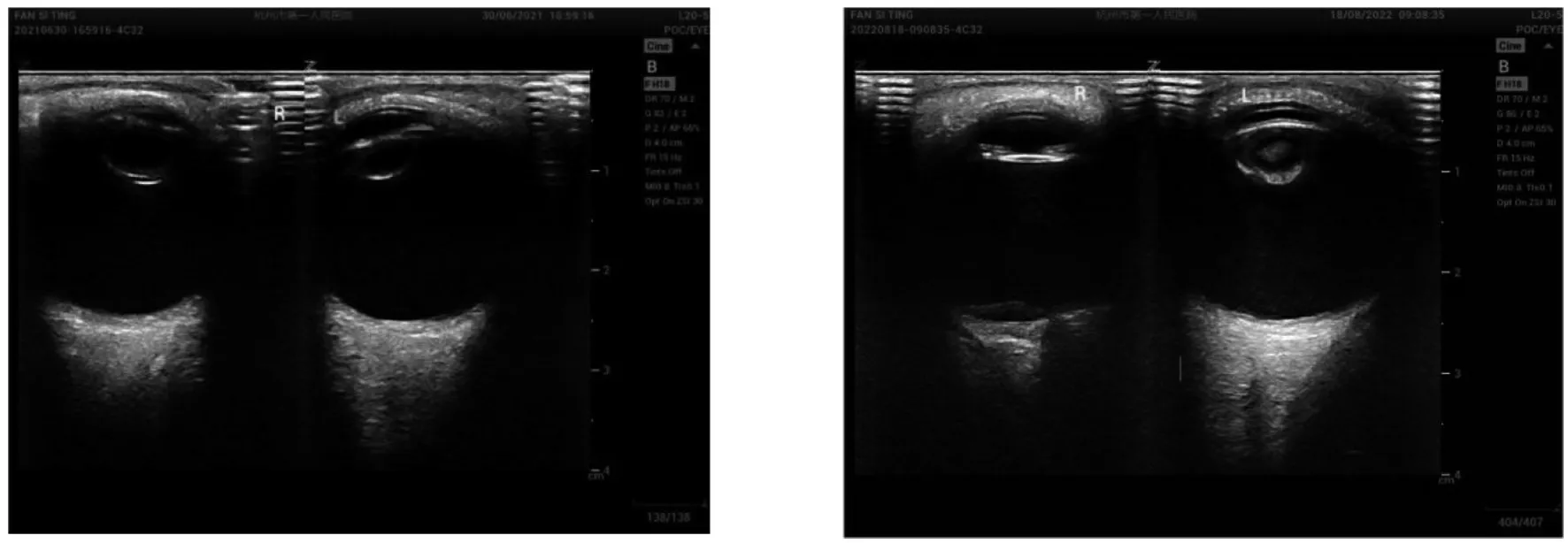
图1 患儿术前眼部B 超照片

图2 患儿术后眼部B 超照片
讨论SMS 最早在上世纪80 年代年被报道。90%SMS 患者是由于染色体17p11.2缺失,10%的患者是该部位基因突变导致[1-2,8]。而视黄酸诱导蛋白1(retinoic acid- induced-1,RAI1)基因作为一种计量敏感基因,是其中的主要基因,在核受体信号通路中发挥重要作用,参与神经系统、心脏、骨骼等多个器官和系统的发育[2]。RAI1 与患者多发异常表现密切相关,患者通常有典型的颅面部特征,如短头畸形,毛发浓密,唇外翻,凸额,面中部发育不全[2-3]。特殊性的面部特征可以作为诊断的重要依据[9]。大部分患者伴随全身骨骼畸形,如脊柱侧弯,身材矮小,指短畸形等[10]。生长发育迟滞,尤其语言发育落后更明显。大多数患者有轻度至中度智力障碍[2],头部影像学可见脑室或枕大池扩大[3]。RAI1 还会影响褪黑素周期[11],因此大部分患者有严重的睡眠障碍[2]。约88%患者有行为异常举动[2],表现为多动,注意力不集中,脾气暴躁及自我伤害行为,如撞头、打自己等,皮肤常见抓伤,可能原因与SMS 患者周围神经对疼痛刺激不敏感有关[12]。SMS 患者还可能合并声音嘶哑[2]。37%的SMS 患者有心脏病变[3],包括房间隔缺损、室间隔缺损、法洛四联症等。本例患儿面容特殊,智力运动及语言发育落后,睡眠障碍,有典型的自我伤害行为,声音嘶哑,但未伴听力障碍、骨骼改变及心脏问题。染色体17p11.2 存在3.2 Mb 缺损。与SMS 在表型及细胞遗传学上是相符的。
SMS 患者伴眼部病变,发生率可达85%~90%[1,3,6]。约50%的SMS 患者有小角膜,66.7%的患者可存在虹膜异常[1],虹膜结节多见,也有患者有虹膜缺损,甚至后期出现青光眼[5]。斜视的发生率为32%~81%,包括内斜视和外斜视。常见屈光不正,尤其是进行性近视。白内障表现一般是核性混浊,多见于伴发高度近视的SMS 患者。此外,患者出现晶状体半脱位发生可能与其长期撞头、拍脸等暴力自残行为有关[2]。随着年龄增长视网膜脱离发生率增加,可能的原因是近视引起眼底周边格子样变性和患者暴力自残[4]。视网膜、色素膜缺损[1]、黄斑瘢痕[7]及视神经发育异常也可见于SMS 患者。本例患儿自幼不能配合视力检查,本次检查发现眼位正,眼轴及角膜直径均属于正常范围。患儿眼部病变主要涉及眼前部,表现为双眼虹膜膨隆后粘,周边前房浅,角膜后色素性KP,晶状体表面有明显色素黏附,但前房反应(-),眼内液检查常见病毒核酸(-),HSV-IgG(+),EBV-IgG(+),特别是HSV-IgG 滴度非常高,提示该患儿既往存在HSV 感染,目前属于慢性期。回顾病史,可能是SMS 患儿周围神经病变痛觉不敏感,因而错过了葡萄膜炎急性期。该患儿晶状体无明显脱位,家长否认有明确眼部外伤史,故认为该患儿的晶状体混浊并非外伤引起。且患儿晶状体乳白色混浊,和高度近视引起的核性混浊也明显不同。推测该患儿白内障的发生与反复葡萄膜炎症有关;此外反复的前房炎症还可能诱发角膜浅层钙化变性引起带状角膜变性。
RAI1 基因不影响免疫功能[13],但很多SMS 患者发生反复中耳炎、鼻窦炎、肺炎、肠胃炎。研究认为是17p11.2 区域的其他基因缺失所致。如肿瘤坏死因子受体超家族成员13B 缺失可导致其编码的跨膜激活剂及钙调亲环素配体相互作用分子(transmembrane activator and calaium modulator and cyclophilin ligand interactor,TACI)单倍体不足[14-16],后者参与浆细胞分化和调节抗体类别转换,在调节B 细胞增殖中起重要作用,因而与常见的免疫缺陷病相关并且呈现多样性[14,17]。SMS 一般不引起自身免疫性疾病,Perkins 等[15]研究发现SMS 患者对自身抗体的反应性并不比对照组高。本例患儿自身抗体、风湿因子(-),也无明显关节炎病史,但全身TORCH 化验结果显示CMV-IgM(+),提示该患儿初次就诊时存在CMV 感染,眼内液检查结果显示EBV-IgG(+)、HSV-IgG(+),其全身病毒和眼内液病毒种类不同,可能原因是患儿不配合导致采样有较长时间间隔,但也说明该患儿极易受病毒攻击。考虑该患儿染色体17p11.2 的缺失范围较大,影响了TACI,从而导致免疫缺陷而易于受到病毒感染,但该推测尚需进一步的分子细胞学证据和更长期临床随访观察。
综上所述,对于生长发育迟缓合并睡眠障碍、冲动性格、自伤行为等表现的患者,需警惕SMS 的可能,尽早行染色体基因芯片检查以明确诊断。SMS 患者合并的眼部异常除白内障、斜视、屈光不正外,还有葡萄膜炎、带状角膜变性可能。
