煤矸石制备活性炭-介孔硅复合材料及其过程物相转变
2023-10-21李宏伟燕可洲文朝璐柳丹丹郭彦霞张圆圆
李宏伟 ,燕可洲 ,文朝璐 ,柳丹丹 ,郭彦霞 ,张圆圆
(1.山西大学 资源与环境工程研究所, 山西 太原 030006;2.太原科技大学 环境科学与工程学院, 山西 太原 030024)
0 引 言
煤矸石是煤炭开采和分选过程中产生的工业固体废弃物,其化学组成主要为碳C (25%~30%)、硅SiO2(40%~60%)、铝Al2O3(15%~40%)等[1-2]。目前,针对煤矸石的资源化利用方式包括燃烧发电[3]、充填筑路[4]、建材生产[5]、农业利用[6]、元素回收[7]、功能材料制备[8]等。在这些利用过程中,对于煤矸石中无机灰分和有机质的资源化主要采用单独利用的方式,特别是在无机灰分的利用工艺中,通常也是先脱碳后利用,由此造成了碳排放量高、资源利用率低等的问题。而以煤矸石为原料,通过特定工艺制备碳-硅或碳-铝硅复合材料(如活性炭-介孔硅、活性炭-沸石等)是一种将煤矸石中无机质和有机碳耦合利用的高附加值利用方式。目前,关于煤矸石制备复合材料已有相关研究报道,如:崔明日等[9]以NaOH为活化剂,在Ar 气氛下对煤矸石碱熔活化,后经Na-OH 水热反应,制得晶型完好的活性炭-沸石复合材料,对SO2吸附量为50.3 mg/g;ZHANG 等[10]以KOH为活化剂,在N2气氛下对煤矸石进行酸浸-碱熔活化,得到多孔网状交联结构C/SiOx复合材料,在0.1 A/g 下具有1 175.8 mAh/g 的高可逆容量,库仑效率达99.8%。LI 等[11]以NaOH 为活化剂,在CO2气氛下对煤矸石(辅以少量煤粉)碱熔活化,后经Na-OH 和NaAlO2水热反应制得比表面积为669.4 m2/g的活性炭-沸石复合材料,对Cu2+和罗丹明B 的吸附量分别可达116.7 mg/g 和32.8 mg/g;石凯等[12]以ZnCl2为活化剂,在He 气氛下对煤矸石碱熔活化,后经HCl 酸浸制得比表面积为412.23 m2/g,平均孔径为4.9 nm 的活性炭-介孔硅复合材料,对罗丹明B的平衡吸附量达到49.81 mg/g。这些研究均证实了利用煤矸石制备复合材料的可行性;而且通过对比发现,以煤矸石为原料制备活性炭-介孔硅复合材料的工艺流程更为简单、产品性能更易调控。纵观现有研究,目前关于煤矸石制备活性炭-介孔硅复合材料的研究多侧重于制备工艺的建立和反应条件的探索,对于制备过程物相转变规律的认识尚不清晰,致使制备工艺的改进和优化方向难以确定,产品性能难以有效提升。
以煤矸石为主要原料,通过碱熔、酸浸等过程制备活性炭-介孔硅复合材料,考察了不同反应条件对煤矸石基活性炭-介孔硅复合材料孔容和比表面积的影响规律,并通过XRD、FTIR 等分析方法研究了煤矸石基活性炭-介孔硅复合材料制备过程的物相转变机理,为煤矸石制备活性炭-介孔硅复合材料提供理论指导和技术支撑。
1 试验部分
1.1 原料与试剂
试验所用煤矸石取自山西省朔州市中煤平朔安太堡露天煤矿选煤厂,经颚式破碎、行星式球磨后,粒径控制在<80 μm;粉磨样品于105 °C 下烘干24 h后,贮于自封袋内保存备用。此外,试验所用其他化学试剂,如氢氧化钾(KOH)、盐酸(37% HCl)等,均为分析纯试剂。
采用GB/T 212-2008《煤的工业分析方法》对煤矸石进行了工业分析,并通过X 射线荧光光谱仪测定了煤矸石的灰分组成,结果见表1。选用煤矸石原料的无机灰组成为:SiO2(35.16%)、Al2O3(25.90%)、Fe2O3(3.81%)等,固定碳含量为13.04%。
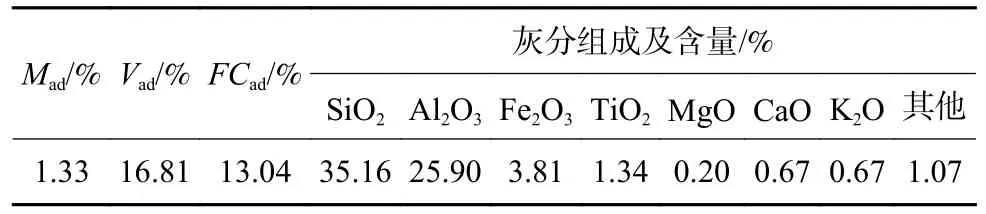
表1 煤矸石的工业分析及灰组成Table 1 Industrial analysis and ash composition of coal gangue
1.2 试验过程
以煤矸石为主要原料,通过碱熔、酸浸等过程制备活性炭-介孔硅复合材料的工艺流程如图1 所示:

图1 煤矸石制备活性炭-介孔硅复合材料的工艺流程Fig.1 Preparation process of activated carbon-mesoporous silica composite from coal gangue
将煤矸石按照固液质量比为1∶5 置于不同浓度(3.6~19.4 mol/L)KOH 溶液中,于室温下搅拌24 h,经固液分离、干燥、研磨制得煤矸石浸渍样;在管式气氛滑轨炉(BTF-1200C-SC,安徽贝意克设备技术有限公司)中还原焙烧煤矸石浸渍样,焙烧气氛为N2气氛,焙烧温度为500~900 °C,焙烧时间为30~120 min;将煤矸石碱熔焙烧样按照固液质量比为1∶5 置于不同浓度(1.4~7.8 mol/L)盐酸溶液中,在三口烧瓶中进行酸浸处理,酸浸温度为20~105 °C,酸浸时间为30~150 min;待到达反应设定时间后,将酸浸浆液进行固液分离,并用去离子水反复冲洗酸浸渣至中性,烘干所得样品即为活性炭-介孔硅复合材料(AC-SiO2)。
1.3 分析表征
比表面积与孔结构:采用Micromeritics 公司制造的ASAP2460 物理吸附仪(Brunner Emmet Teller Measurement,BET),对制得样品的比表面积、孔容和孔径进行测定分析,测定条件:样品经120 °C 真空预处理8 h 后,于-196 °C 下进行N2吸脱附等温线测定,以相对压力范围为0.6~0.15 的吸附等温线为基础,由相对压力为0.95 时的液氮吸附值换算成液氮体积得到孔容V;通过Brunner Emmet Teller 方法计算比表面积(SBET);基于非限定域密度泛函理论(NLDFT)计算样品微孔-介孔全范围分布[13]。
物相组成和特征基团分析:采用D2 PHASER型X 射线衍射仪(X-ray Diffraction,XRD),对制得样品物相组成进行测定分析,测试条件:光源Cu Kα 靶,电压30 kV,电流10 mA,扫描范围10°~80°,扫描间隔0.02°,步长0.1 s[14];采用Spectrum II 傅里叶变换红外吸收光谱仪(Fourier Transform Infrared Spectroscopy,FTIR),对制得样品特征基团进行测定分析,测试条件:KBr 压片法,激光功率1 mW,波长532 nm,扫描范围为4 000~500 cm-1,分辨率 ≤ 2 cm-1[15]。
其他产品性能分析:采用JSM-7001F 型热场发射扫描电子显微镜(Scanning Electron Microscope Energy Dispersive Spectrometer,SEM-EDS),对制得样品的微观形貌和元素分布进行测定分析,测试条件:待测样品通过导电胶固定于载样台上,经喷金预处理后,以背散射电子或二次电子成像模式观察样品形貌及其元素分布,电压10.0 kV,电流84.6 μA[16];采用754PC 型紫外分光光度计(UV spectrophotometer),通过测定样品吸附反应前后溶液中甲基橙和罗丹明B 的吸光度变化,评价AC-SiO2产品对不同分子量有机物的吸附性能,吸附条件:甲基橙或罗丹明B 的初始质量浓度100 mg/L,pH=4,温度45 °C,吸附材料的投加量0.05 g/L[17-18]。
2 结果与讨论
2.1 碱熔-酸浸条件对AC-SiO2 孔容和比表面积的影响
对不同制备条件下所得AC-SiO2孔容和比表面积进行分析,结果如图2 所示。

图2 不同碱熔-酸浸条件下AC-SiO2 的孔容和比表面积变化Fig.2 Changes of pore volume and specific surface area of AC-SiO2 obtained from different conditions
如图2 所示,在碱熔过程中,随着KOH 浸渍液浓度、焙烧温度、焙烧时间的增加,AC-SiO2的孔容和比表面积整体呈现上升趋势。其中,KOH 浸渍液浓度对孔容和比表面积的影响较大,当浓度从3.6 mol/L 增加至17.9 mol/L,AC-SiO2的比表面积由198.51 m2/g 增加至782.1 m2/g,孔容由0.17 cm3/g 增加至0.53 cm3/g;进一步提高浓度至19.6 mol/L,ACSiO2的孔容和比表面积均不发生明显变化。而焙烧温度超过850 °C 或者焙烧时间超过90 min 后,ACSiO2的孔容和比表面积均出现小幅下降,这可能与反应温度过高、反应时间过长导致样品发生熔融,导致孔道被堵塞有关。同样,在酸浸过程中,随着HCl酸浸浓度、酸浸温度、酸浸时间的增加,AC-SiO2的孔容和比表面积整体也呈现上升趋势。其中,HCl 酸浸浓度对孔容和比表面积的影响较大,当浓度从1.4 mol/L 增加至4.4 mol/L,AC-SiO2的比表面积由141.13 m2/g 增加至627.40 m2/g,孔由0.2 cm3/g 增加至0.51 cm3/g;进一步提高浓度超过6.0 mol/L 时,ACSiO2的孔容不发生明显变化,但比表面积出现一定程度下降,这可能与酸浸浓度过高导致溶出反应剧烈,介孔尺寸偏大有关。
2.2 煤矸石碱熔-酸浸过程物相转变
采用XRD 分析方法,对煤矸石原料、焙烧样和酸浸渣进行物相组成测定,结果如图3 所示。
煤矸石原样的物相组成主要包括石英(SiO2)、高岭石(Al2O3·2SiO2·2H2O)等。经KOH 浸渍后,焙烧样的物相组成发生明显变化,高岭石衍射峰消失,而出现了钾霞石(KAlSiO4)和硅酸钾(K2SiO3)衍射峰,表明在此过程中发生了高岭石向钾霞石和硅酸钾物相的转变,具体反应见式(1)-式(2)[19]。焙烧样再经HCl 酸浸处理后,钾霞石和硅酸钾物相溶解,其中KCl 和AlCl3以离子形式存在于溶液,而SiO2则富集于酸浸渣,形成多孔的AC-SiO2产品,具体反应见式(3)-式(4)[19]。另外,酸浸渣的XRD 图谱中,仅呈现漫反射“鼓包”,表明AC-SiO2产品主要以无定型形式存在[20]。
SiO2(石英) +2KOH →K2SiO3(硅酸钾) +H2O(2)
对不同碱熔-酸浸条件下制得AC-SiO2产品的物相组成进行分析,结果如图4 所示。从图2 和图4 中可以看出,KOH 浸渍液浓度和HCl 酸浸浓度对AC-SiO2产品的孔容、比表面积和物相组成影响较大。在KOH 浸渍液浓度较低(≤ 7.1 mol/L)或HCl 酸浸浓度较低(≤1.4 mol/L)时,XRD 图谱中仍有明显的石英或钾霞石衍射峰(图4a,图4b),前者是由于较少的KOH 未能将石英完全转化所致,而后者则是由于较少的HCl 未能将钾霞石完全溶解所致。相应地,该条件下制得AC-SiO2产品的孔容和比表面积均较小。当KOH 浸渍液浓度超过10.7 mol/L,HCl 酸浸浓度超过2.9 mol/L 后, XRD 图谱仅呈现无定形漫反射“鼓包”,说明原煤矸石经碱熔、酸浸处理后已转变为无定型结构;该条件下制得ACSiO2的孔容和比表面积有所提升,但提升幅度仍有限。进一步提高KOH 浸渍液浓度或HCl 酸浸浓度,XRD 图谱中漫反射“鼓包”逐渐宽化。特别是,当HCl 酸浸浓度超过6 mol/L 时,漫反射“鼓包”由原本集中分布在29°左右变为广泛分布在15°~35°,这主要与AC-SiO2产品中介孔硅占比逐渐提升有关。
此外,焙烧温度也将对AC-SiO2产品的孔容、比表面积和物相组成造成影响。当焙烧温度较低(≤ 600 °C)时,XRD 图谱中仍呈现较弱的高岭石和石英衍射峰(图4c);相应地,AC-SiO2产品的孔容和比表面积均较小(图2c)。而当焙烧温度升高至800 °C 后,高岭石和石英的衍射峰消失,AC-SiO2产品的孔容和比表面积也得到显著提升,表明煤矸石中的铝硅酸盐矿物的转化程度影响着AC-SiO2产品的孔容和比表面积。与KOH 浸渍液浓度、HCl 酸浸浓度和焙烧温度相比,焙烧时间、酸浸温度和酸浸时间等因素对AC-SiO2产品的孔容、比表面积和物相组成影响则较小。该结果与图2 中碱熔-酸浸条件对AC-SiO2产品的孔容和比表面积影响规律一致。
2.3 煤矸石碱熔-酸浸过程特征基团变化
采用FT-IR 对煤矸石原料、焙烧样和酸浸渣进行了分析,结果如图5 所示。煤矸石原样在3 692、3 620和914 cm-1处存在吸收峰,是由煤矸石中高岭石矿相的羟基伸缩振动(外羟基、内羟基)和弯曲振动引起;1 034、693 和541 cm-1处呈现吸收峰,可归属于Si-O-Si、Al-O-Si 或Al-O-Al 的振动,表明煤矸石中含有大量铝硅酸盐物相;2 921、2 851 和1 383 cm-1处呈现吸收峰,源自于煤矸石中固定碳表面的C-H 键伸缩振动和弯曲振动;而3 432 和1 623 cm-1处吸收峰则是由于煤矸石样品中含有一定量的吸附水所导致的。KOH 浸渍样经过焙烧处理后,羟基的特征吸收峰消失,C-H 键的特征吸收峰变弱,且原本归属于高岭石中铝硅特征基团的吸收峰发生变化,这主要与焙烧样中生成大量钾霞石和硅酸钾(如1 417 、987、891 和693 cm-1)有关。焙烧样再经HCl 酸浸处理后,钾霞石和硅酸钾的铝硅特征基团吸收峰消失,主要呈现1 094 和964 cm-1处Si-O-Si 反对称(对称)伸缩振动吸收峰和800 cm-1处Si-OH 弯曲振动吸收峰,表明AC-SiO2产品中出现大量介孔硅[21];另外,在2 921、2 851 和1 383 cm-1处还保留有C-H 键伸缩振动和弯曲振动的吸收峰,表明AC-SiO2产品中也含有一定量的活性炭。
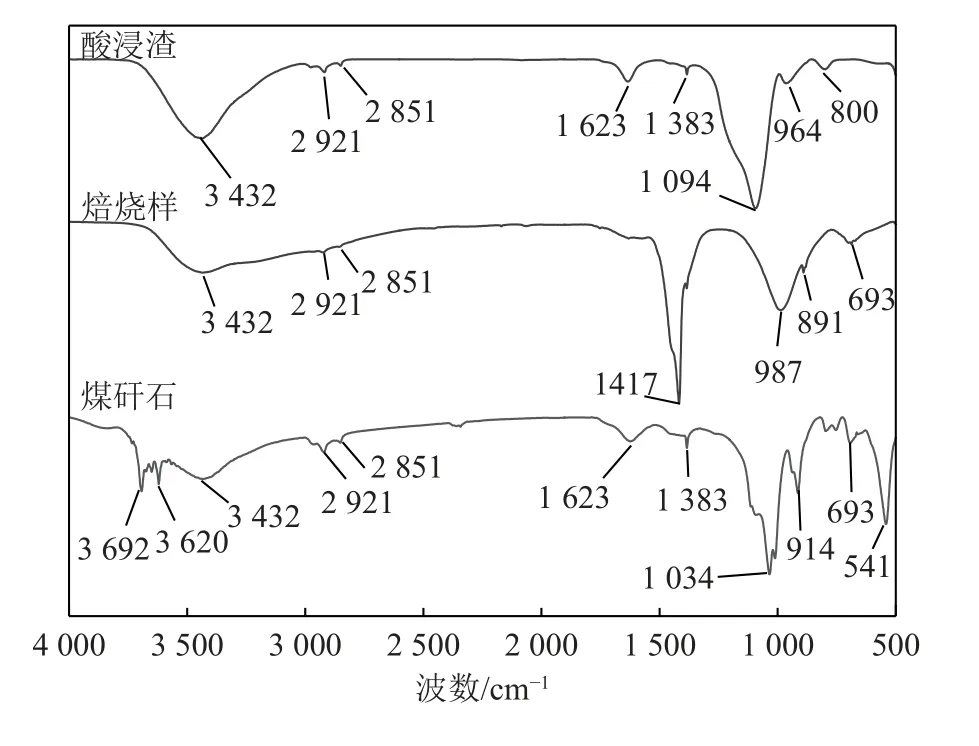
图5 煤矸石原样、焙烧样和酸浸渣的FT-IR 图Fig.5 FT-IR spectra of raw coal gangue, roasted sample and acid-leached slag
对不同碱熔-酸浸条件下制得AC-SiO2产品的特征基团进行分析,结果如图6 所示。从图6 中可以看出, KOH 浸渍液浓度、焙烧温度、焙烧时间、酸浸温度、酸浸时间对AC-SiO2产品的FT-IR 图谱影响不显著,而不同HCl 酸浸浓度下所得AC-SiO2产品的FT-IR 图谱则呈现一定差异性。当HCl 酸浸浓度为1.4 mol/L时,688 cm-1处呈现明显的吸收峰,可归属于Al-O 振动,表明产品中尚存未被溶解的钾霞石;继续升高浓度超过2.9 mol/L 后,则该吸收峰则消失。同时,随着HCl 酸浸浓度从1.4 mol/L 增加至4.4 mol/L,1 012 cm-1处的Si-O-Si 反对称伸缩振动吸收逐步偏移至1 094 cm-1处,表明在此过程介孔硅的存在形态不断发生变化。该变化将导致ACSiO2产品的孔容和比表面积不断增大(图2b)。

图6 不同条件下AC-SiO2 的FT-IR 对比Fig.6 FT-IR spectra of AC-SiO2 obtained from different conditions
2.4 产品性能
综合考虑不同碱熔-酸浸条件下AC-SiO2的孔容和比表面积变化,得出制备煤矸石基AC-SiO2的优化反应条件,即:KOH 浸渍液浓度为19.6 mol/L、焙烧温度为850 °C、焙烧时间为90 min、HCl 酸浸浓度为6.0 mol/L、酸浸温度为105 °C、酸浸时间为120 min。在此条件下,计算AC-SiO2产品得率,即:100 g 煤矸石浸渍后质量变为156.5 g(主要源自负载的氢氧化钠),浸渍样经焙烧处理后质量变为113.07 g(主要源自煤矸石挥发分脱除、高岭石脱羟基以及氢氧化钠分解),焙烧样再经酸浸处理后质量变为40.2 g(主要源自酸浸过程中含铝物相的溶出)。在此过程中,煤矸石中碳、硅组分基本无损失,转化率高达90.28%(少量损失主要源自碳受热分解);相应地,活性炭-介孔硅复合材料的产品得率与原煤矸石中碳、硅含量有关,产率可达40.2%。
对实验制得 AC-SiO2复合材料进行组分分析列于表2。从表2 可以看出,AC-SiO2中主要包括固定碳16.89%和灰分 71.35%,其中灰分又以SiO2为主,即 AC-SiO2主要是由碳-硅组分构成。

表2 AC-SiO2 复合材料的工业分析及灰组成Table 2 Industrial analysis and ash composition of AC-SiO2
采用SEM-EDS 考察了AC-SiO2的微观形貌以及碳、硅元素分布情况,结果如图7 所示。从图7 可以看出,AC-SiO2为不规则状颗粒,碳、硅元素在颗粒表面均匀分布,且颗粒表面分布着大小不一的孔道。通过测定AC-SiO2的N2气吸脱附曲线,发现所得吸脱附曲线为Ⅳ型标准曲线[22],并伴有因毛细凝聚现象出现的H4 回滞环,证实了AC-SiO2表面孔道主要是由层状结构堆积形成(图8a)。

图8 AC-SiO2 材料的N2 吸附-脱附曲线和孔径分布Fig.8 N2 adsorption-desorption curve and pore size distribution of AC-SiO2
进一步考察了AC-SiO2的孔径分布,结果如图8所示。由图8 分析可知,材料的比表面积可达835.1 m2/g,平均孔径为2.97 nm,总孔容为0.62 cm3/g,其中微孔和介孔各占近1/2。相较于孔径单一的活性炭或者介孔硅材料而言,AC-SiO2在吸附脱除多组分污染物方面的应用潜能更高。
选用分子量不同的甲基橙和罗丹明B 作为目标污染物,在优化吸附条件下考察了AC-SiO2的吸附性能,结果如图9 所示。由图9 可知,当初始浓度100 mg/L、吸附剂投加量50 mg、温度45 °C、pH=4时,AC-SiO2对甲基橙和罗丹明B 的吸附反应迅速进行,并在30 min 左右达到吸附平衡,吸附容量分别为99.01 mg/g 和99.87 mg/g。这进一步证实了所制得的AC-SiO2为多级孔材料,可用于吸附分子量不同的有机污染物。

图9 AC-SiO2 材料的吸附性能Fig.9 Adsorption properties of AC-SiO2 for methyl
3 结 论
1)煤矸石基AC-SiO2制备过程中,原料所含的高岭石、石英经碱熔焙烧后生成钾霞石和硅酸钾物相,后在酸性溶液发生溶解,形成无定型硅渣;与此同时,煤矸石中的碳经碱熔焙烧后生成活性炭,同样保留于酸浸渣中。在此过程中,KOH 浸渍液浓度、焙烧温度和HCl 酸浸浓度显著影响AC-SiO2产品品质,当KOH 浸渍液浓度低于10.7 mol/L 或者焙烧温度低于700 °C 时,煤矸石中铝硅物相活化不完全,将残留在AC-SiO2产品,导致AC-SiO2产品的孔容和比表面积较低;当HCl 酸浸浓度低于2.9 mol/L 时,焙烧样中钾铝硅酸盐溶解不完全,同样会对ACSiO2产品的孔容和比表面积也将造成影响。
2)煤矸石经适宜条件的碱熔、酸浸等过程处理后,可制得AC-SiO2产品,优化反应条件为:KOH 浸渍液浓度19.6 mol/L、焙烧温度850 °C、焙烧时间90 min、HCl 酸浸浓度6.0 mol/L、酸浸温度105 °C、酸浸时间120 min;所制得的产品是由碳、硅为主要组分的复合材料,颗粒表面分布有层状结构堆积形成的微孔和介孔,比表面积可达835.1 m2/g,平均孔径为2.97 nm,总孔容为0.62 cm3/g,其中微孔和介孔各占近1/2;该材料可用于吸附分子量不同的有机污染物,对甲基橙和罗丹明B 的吸附容量分别超过99.01 mg/g 和99.87 mg/g。
