0.05%环孢素与0.1%他克莫司滴眼液治疗慢性oGVHD后患者眼表干眼相关指标及泪液炎症因子比较
2023-10-11马骄申展胡博浩赵英涵刘姝婉吴蓉彭荣梅洪晶
马骄 申展 胡博浩 赵英涵 刘姝婉 吴蓉 彭荣梅 洪晶
北京大学第三医院眼科 眼部神经损伤的重建保护与康复北京市重点实验室,北京 100191
吴蓉现在北京大学深圳医院眼科,深圳 518000
同种异体造血干细胞移植术(hematopoietic stem cell transplantation,HSCT)是目前治疗多种血液系统恶性肿瘤的有效手段,慢性移植物抗宿主病(graft-versus-host disease,GVHD)是异基因HSCT术后的常见并发症,发生率为30%~70%,主要由供体淋巴细胞受激活攻击宿主靶器官引起[1-3]。慢性GVHD主要表现为长期的慢性炎症过程,其表现类似于干燥综合征、类风湿性关节炎等自身免疫性疾病[4-5]。60%~90%慢性GVHD患者可发生眼部GVHD(ocular GVHD,oGVHD),造成角结膜组织炎症、泪腺纤维化、睑板腺萎缩等多种眼表组织损害[6-7],主要临床症状为眼干、眼红、眼痛、畏光、有异物感等,若不及时治疗可能会发展为角膜炎、角膜溃疡或穿孔,严重者导致视力下降,甚至盲[8-10]。目前,oGVHD尚缺乏规范的临床治疗方案,主要治疗原则为润滑眼表和控制炎症,如采用人工泪液、生长因子类药物滴眼液点眼以缓解干眼症状并保护眼表组织的结构完整性和功能,同时局部应用糖皮质激素或联合免疫抑制剂控制慢性炎症过程[11-13]。临床实践中发现,大部分患者经过1个月的治疗后干眼及眼表炎症可明显缓解,但部分患者治疗后症状改善不明显,甚至加重。钙调磷酸酶抑制剂他克莫司和环孢素滴眼液是oGVHD常用的免疫治疗药物,然而,由于oGVHD患者发病情况比较复杂,这2种药物所适应的oGVHD患者是否存在差异,以及造成这种差异的潜在机制尚不明确,而针对不同oGVHD患者的具体情况用药对提高疗效具有重要临床意义。慢性oGVHD病理过程受多种免疫细胞及相关炎症因子调节,检测患者泪液中特定的炎症因子是监测慢性oGVHD病情变化、研究相关病理机制的可行方法[14]。近年来,随着微量蛋白检测技术的进步,泪液炎症因子检测已成为研究oGVHD的重要手段。多项研究表明,泪液中白细胞介素(interleukin,IL)-2、IL-6、IL-8、IL-10、IL-17、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)、表皮生长因子(epidermal growth factor,EGF)等含量的改变有助于预测慢性oGVHD的发生,此外IL-6、IL-8、IL-10、TNF-α等炎症因子含量变化程度有助于判断慢性oGVHD的严重程度[15-20]。本研究团队在前期研究中也发现,泪液中IL-6和IL-8含量的改变与慢性oGVHD的治疗效果有关[21]。因此我们推测,泪液中炎症因子含量的动态改变或有助于揭示影响他克莫司和环孢素滴眼液治疗慢性oGVHD效果的分子机制。本研究拟比较采用1%他克莫司滴眼液和0.05%环孢素滴眼液治疗慢性oGVHD患者干眼相关指标及泪液炎症因子的不同变化,探讨影响oGVHD对不同治疗药物反应的因素,为临床上oGVHD治疗的药物选择及预后评估提供参考依据。
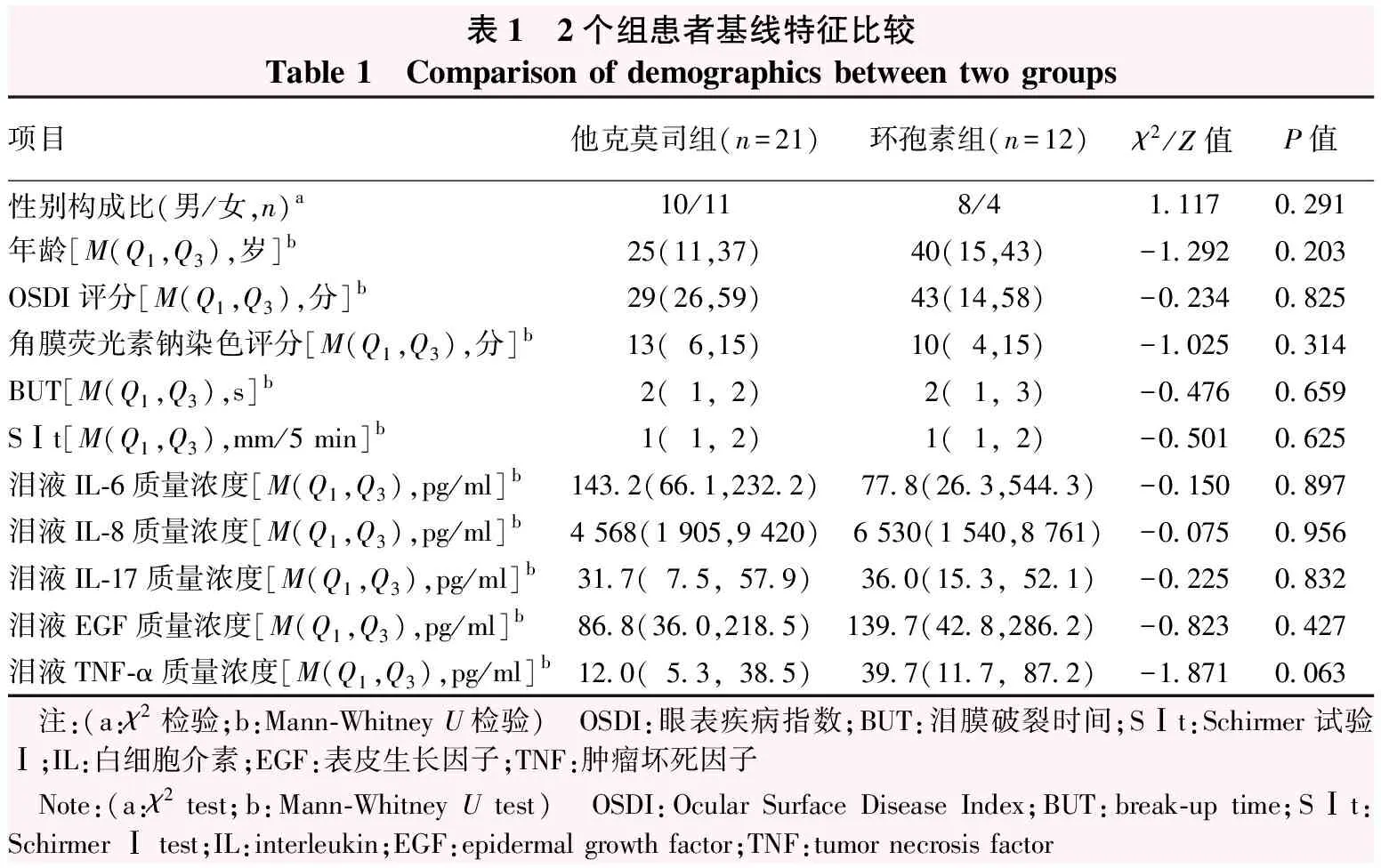
表1 2个组患者基线特征比较Table 1 Comparison of demographics between two groups项目他克莫司组(n=21)环孢素组(n=12)χ2/Z值P值性别构成比(男/女,n)a10/118/41.1170.291年龄[M(Q1,Q3),岁]b25(11,37)40(15,43)-1.2920.203OSDI评分[M(Q1,Q3),分]b29(26,59)43(14,58)-0.2340.825角膜荧光素钠染色评分[M(Q1,Q3),分]b13(6,15)10(4,15)-1.0250.314BUT[M(Q1,Q3),s]b2(1,2)2(1,3)-0.4760.659SⅠt[M(Q1,Q3),mm/5 min]b1(1,2)1(1,2)-0.5010.625泪液IL-6质量浓度[M(Q1,Q3),pg/ml]b143.2(66.1,232.2)77.8(26.3,544.3)-0.1500.897泪液IL-8质量浓度[M(Q1,Q3),pg/ml]b4 568(1 905,9 420)6 530(1 540,8 761)-0.0750.956泪液IL-17质量浓度[M(Q1,Q3),pg/ml]b31.7(7.5,57.9)36.0(15.3,52.1)-0.2250.832泪液EGF质量浓度[M(Q1,Q3),pg/ml]b86.8(36.0,218.5)139.7(42.8,286.2)-0.8230.427泪液TNF-α质量浓度[M(Q1,Q3),pg/ml]b12.0(5.3,38.5)39.7(11.7,87.2)-1.8710.063 注:(a:χ2检验;b:Mann-Whitney U检验) OSDI:眼表疾病指数;BUT:泪膜破裂时间;SⅠt:Schirmer试验Ⅰ;IL:白细胞介素;EGF:表皮生长因子;TNF:肿瘤坏死因子 Note:(a:χ2 test;b:Mann-Whitney U test) OSDI:Ocular Surface Disease Index;BUT:break-up time;SⅠt:Schirmer Ⅰ test;IL:interleukin;EGF:epidermal growth factor;TNF:tumor necrosis factor
1 资料与方法
1.1 一般资料
采用随机对照研究方法,纳入2020年4月至2021年4月于北京大学第三医院眼科确诊为慢性oGVHD的患者60例60眼,采用随机数字表法随机分为他克莫司组30例30眼和环孢素组30例30眼。用药后1个月随访患者信息,排除不符合标准的患者,将他克莫司组21例21眼和环孢素组12例12眼纳入后续研究。病例纳入标准:依据2014年美国国家卫生研究院共识,纳入慢性GVHD且合并新发干眼患者。干眼诊断标准参考2013年版《干眼临床诊疗专家共识》:(1)有干燥感、异物感、灼烧感、疲劳感、不适感、视力波动等眼部主观症状之一,泪膜破裂时间(break-up time,BUT)≤5 s或Schirmer试验Ⅰ(Schirmer Ⅰ test,SⅠt)≤5 mm/5 min,可诊断干眼;(2)有上述主观症状之一,5 s≤BUT≤10 s或SⅠt≤10 mm/5 min时,若角膜荧光素钠染色阳性,可诊断干眼[22]。排除标准:(1)在过去6个月内有眼科手术史;(2)患有其他眼部疾病,如自身免疫性疾病、青光眼、严重感染、视网膜病变、眼部变态反应、白内障、眼外伤等;(3)入组前眼部曾使用免疫抑制剂或糖皮质激素;(4)依从性差,不能定期随访者。2个组间患者性别分布、年龄、干眼相关指标、泪液因子水平等基线特征比较差异均无统计学意义(均P>0.05)(表1)。本研究遵循《赫尔辛基宣言》,研究方案经北京大学第三医院医学科学研究伦理委员会批准(批文号:M2020489)。所有患者均了解本研究目的和方法并自愿签署知情同意书。
1.2 方法
1.2.1治疗方法 2个组分别采用不同的免疫抑制剂局部点眼,他克莫司组主要采用0.1%他克莫司滴眼液(日本千寿制药株式会社)点眼,2次/日;环孢素组采用0.05%环孢素滴眼液(沈阳兴齐眼药股份有限公司)点眼,4次/日。此外,2个组患眼均采用0.1%氟米龙滴眼液[参天制药(中国)有限公司]2次/日、小牛血去蛋白提取物眼用凝胶(沈阳兴齐眼药股份有限公司)3次/日、0.1%玻璃酸钠滴眼液(德国URSAPHARM Arzneimittel GmbH公司)8次/日点眼,进行抗炎和润滑治疗。
1.2.2有效性指标评估 记录治疗前及治疗后1个月检查结果。疗效指标包括治疗前后干眼症状评分、角膜荧光素钠染色评分和BUT。(1)干眼症状评分 采用眼表疾病指数(Ocular Surface Disease Index,OSDI)问卷进行评估,OSDI评分=(100×得分总和)/(4×回答问题总数)[23-24]。(2)角膜荧光素钠染色评分 用1滴无菌生理盐水润湿荧光素钠眼科检测试纸,将试纸条轻轻接触患者下眼睑结膜囊,嘱患者瞬目,使荧光素钠染液与泪液混合后,裂隙灯显微镜(德国蔡司公司)钴蓝光下观察患者角膜染色点数。将角膜分为5个象限,每个象限根据染色点数进行角膜荧光素钠染色评分。无染色为0分;染色点1~30个为1分;染色点>30个但无融合为2分;可见角膜丝状物附着、点状角膜病变融合、角膜溃疡为3分;每眼最终评分为5个象限的评分之和[24]。(3)BUT 嘱患者瞬目3次,双眼平视前方,用裂隙灯显微镜在钴蓝光下观察患者末次瞬目至角膜出现首个黑斑的时间,重复测量3次,取平均值。
1.2.3泪液收集与检测 用30 μl无菌生理盐水点眼,利用毛细管吸取冲洗液并收集于无菌EP管中,-80 ℃冰箱中保存。采用Luminex液相芯片法测定泪液中IL-6、IL-8、IL-17、EGF和TNF-α含量。将泪液标本置于冰上溶解,3 000×g离心10 min,取25 μl上清进行检测。参照ProcartaPlex多重免疫分析试剂盒(美国赛默飞世尔科技公司)说明书的方法梯度稀释标准品,采用超声破碎仪(VCX130,美国Sonics公司)处理预混合微球30 s,涡旋振荡器上振荡1 min,按每孔25 μl加入板中。取25 μl处理好的标准品、样品、空白对照分别加入对应孔中并贴上封口膜,放置在平板摇床上,于4 ℃避光振荡过夜。采用洗涤缓冲液洗板3次,每孔加入25 μl二抗,平板摇床上室温避光孵育2 h。每孔加入25 μl链酶亲和素-藻红蛋白,在平板摇床上室温避光孵育30 min,采用洗涤缓冲液洗板3次。每孔加入150 μl鞘液,摇床上室温避光振荡5 min。将平板置入Luminex 200检测仪器(美国赛默飞世尔科技公司),分析每孔平均荧光强度,采用标准曲线公式计算样品中各细胞因子质量浓度。
1.3 统计学方法
采用GraphPad Prism 8.0统计学软件进行统计分析。计量资料数据经Shapiro-Wilk检验证实不符合正态分布,以M(Q1,Q3)表示。他克莫司组与环孢素组治疗前后各指标的差值比较采用Mann-WhitneyU检验。计数资料用频数表示,组间差异比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 2个组患眼治疗前后干眼相关指标差值比较
他克莫司组和环孢素组治疗后OSDI评分分别为33(16,41)分和10(9,17)分,角膜荧光素钠染色评分分别为3(2,6)分和3(1,5)分,BUT分别为2(2,4)s和4(2,4)s。治疗前后环孢素组OSDI评分改善程度明显优于他克莫司组,差异有统计学意义(Z=-2.547,P=0.009)。2个组间治疗前后角膜荧光素钠染色评分差值和BUT差值比较差异均无统计学意义(Z=-0.526、-0.804,均P>0.05)(表2)。
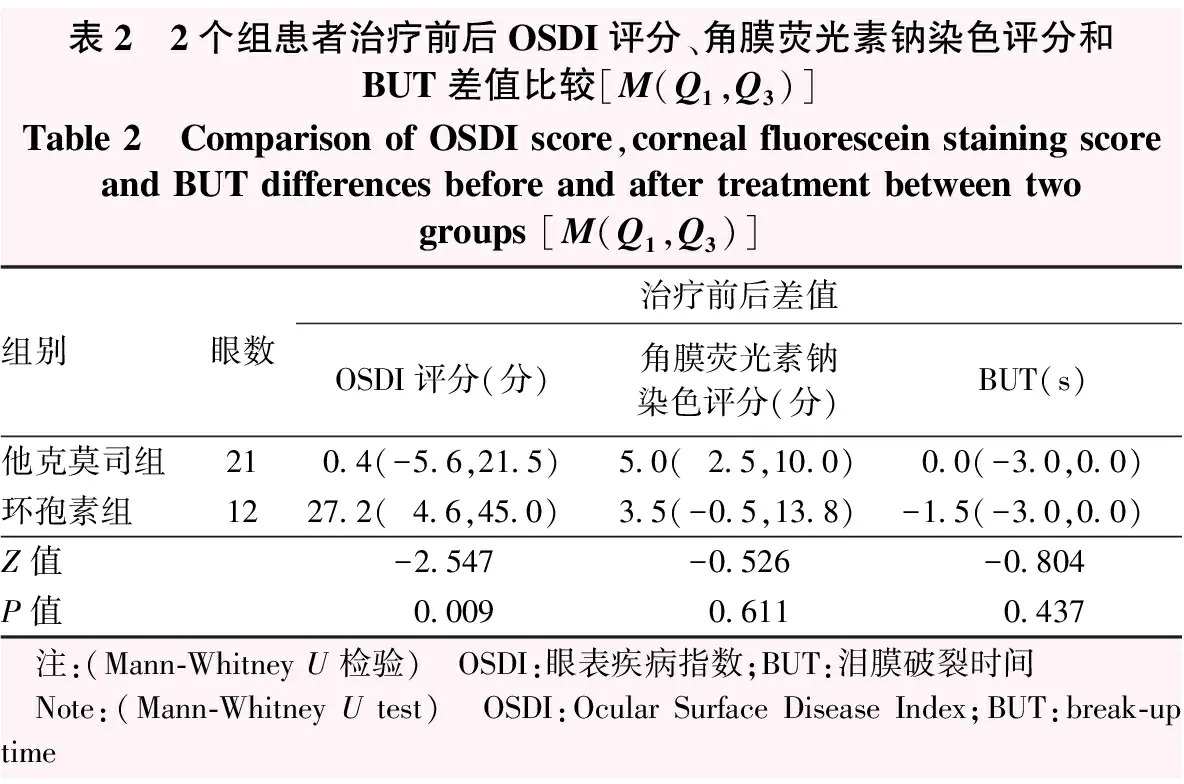
表2 2个组患者治疗前后OSDI评分、角膜荧光素钠染色评分和BUT差值比较[M(Q1,Q3)]Table 2 Comparison of OSDI score,corneal fluorescein staining scoreand BUT differences before and after treatment between twogroups [M(Q1,Q3)]组别眼数治疗前后差值OSDI评分(分)角膜荧光素钠染色评分(分)BUT(s)他克莫司组210.4(-5.6,21.5)5.0(2.5,10.0)0.0(-3.0,0.0)环孢素组1227.2(4.6,45.0)3.5(-0.5,13.8)-1.5(-3.0,0.0)Z值-2.547-0.526-0.804P值0.0090.6110.437 注:(Mann-Whitney U 检验) OSDI:眼表疾病指数;BUT:泪膜破裂时间 Note:(Mann-Whitney U test) OSDI:Ocular Surface Disease Index;BUT:break-up time
2.2 2个组患眼治疗前后泪液炎症因子质量浓度差值比较
他克莫司组治疗后泪液中IL-6、IL-8、IL-17、EGF和TNF-α质量浓度分别为49.8(26.3,91.5)、2 432(957,3 882)、9.6(4.8,47.2)、66.5(26.0,219.1)和14.7(2.5,27.4)pg/ml,环孢素组分别为45.5(10.7,243.9)、3 779(195,7 774)、27.5(12.7,40.6)、39.0(21.9,391.0)和20.0(8.7,47.6)pg/ml。2个组治疗前后IL-6、IL-8、IL-17、EGF和TNF-α质量浓度差值比较差异均无统计学意义(Z=-0.487、-0.112、-0.412、-1.085、-1.198,均P>0.05)(表3)。
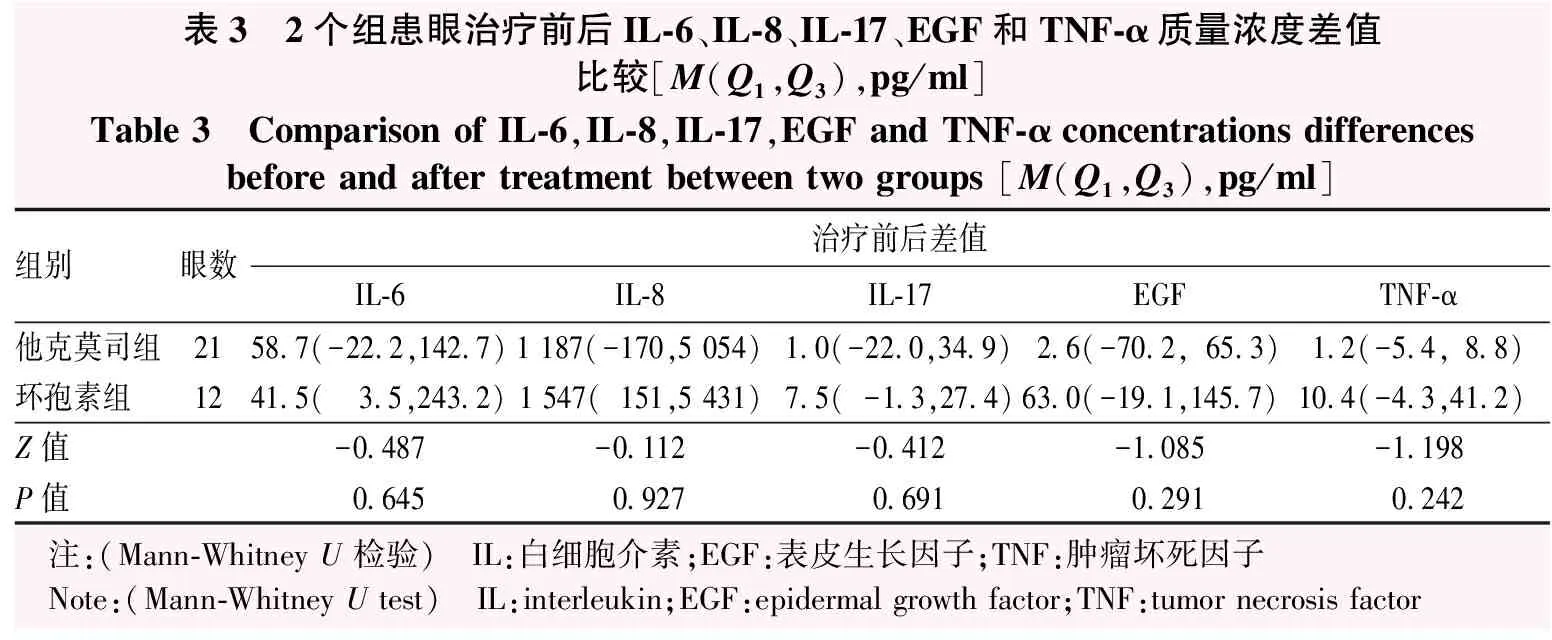
表3 2个组患眼治疗前后IL-6、IL-8、IL-17、EGF和TNF-α质量浓度差值比较[M(Q1,Q3),pg/ml]Table 3 Comparison of IL-6,IL-8,IL-17,EGF and TNF-α concentrations differences before and after treatment between two groups [M(Q1,Q3),pg/ml]组别眼数治疗前后差值IL-6IL-8IL-17EGFTNF-α他克莫司组2158.7(-22.2,142.7)1 187(-170,5 054)1.0(-22.0,34.9)2.6(-70.2,65.3)1.2(-5.4,8.8)环孢素组1241.5(3.5,243.2)1 547(151,5 431)7.5(-1.3,27.4)63.0(-19.1,145.7)10.4(-4.3,41.2)Z值-0.487-0.112-0.412-1.085-1.198P值0.6450.9270.6910.2910.242 注:(Mann-Whitney U 检验) IL:白细胞介素;EGF:表皮生长因子;TNF:肿瘤坏死因子 Note:(Mann-Whitney U test) IL:interleukin;EGF:epidermal growth factor;TNF:tumor necrosis factor
3 讨论
IL-6是一种典型的多效性细胞因子,在正常机体免疫中发挥重要功能,异常表达时可能会引发多种免疫性疾病[25]。目前,已有多项研究报道了IL-6在慢性oGVHD患者泪液中的异常高表达,且IL-6的含量与该病的严重程度显著相关[15-17],这些研究表明IL-6异常高表达与慢性oGVHD的发生和发展密切相关,提示IL-6或许是治疗慢性oGVHD的重要靶点。本研究结果显示,点眼治疗后1个月,2个组患者泪液中IL-6含量均降低,但2个组间差异无统计学意义,提示1%他克莫司滴眼液与0.05%环孢素滴眼液在调节IL-6表达方面无显著差异。IL-8是一种低相对分子质量多肽,其特征性生物效应主要包括趋化及激活中性粒细胞[26],提示0.1%他克莫司滴眼液对慢性oGVHD的治疗效果或与其调节中性粒细胞的功能相关。有研究在慢性oGVHD患者泪液冲洗物的涂片中观察到中性粒细胞相关成分[20],我们在临床检查中也发现部分患者经结膜印迹细胞检查可检出中性粒细胞浸润。本研究结果显示,2种滴眼液在调节oGVHD患者眼表中性粒细胞功能方面无显著差异。
本研究结果显示,治疗后环孢素组患者的OSDI评分改善程度明显优于他克莫司组,提示经0.05%环孢素滴眼液治疗后患者眼表舒适度更佳,这可能与0.1%他克莫司滴眼液具有一定刺激性而引发患者眼表的不适感有关。这提示我们,对于未检出中性粒细胞浸润的慢性oGVHD患者,应用0.05%环孢素滴眼液进行治疗可能有更好的舒适度。
本研究的不足之处主要在于随访时间较短,未能对泪液炎症因子的含量进行多个时间点的检测,且样本量较小,也可能会导致检测结果的偏倚。因此,本研究结果仍有待后续研究进一步验证。
综上所述,本研究结果表明2种药物在调节慢性oGVHD患者泪液中各因子表达方面无显著差异。此外,慢性oGVHD患者应用0.05%环孢素滴眼液治疗可能比0.1%他克莫司滴眼液有更好的舒适度。
利益冲突所有作者均声明不存在利益冲突
作者贡献声明马骄:设计试验、实施研究、采集数据、分析/解释数据、文章撰写;申展、胡博浩、赵英涵、刘姝婉、吴蓉:实施研究、采集数据;彭荣梅:实施研究、采集数据、指导试验;洪晶:酝酿和设计试验、实施研究、对文章的知识性内容作批判性审阅及定稿
