超高效液相色谱-串联质谱法测定水产养殖用非规范药品及水中扑草净、阿维菌素和伊维菌素的残留量
2023-09-19陈永平许文龙成振华韩现芹时文博王愿宁
陈永平 ,包 艳 ,许文龙 ,成振华 ,王 辉 ,韩现芹 ,时文博,王愿宁
(1.天津市农业生态环境监测与农产品质量检测中心,天津 300193;2.中国科学院 青岛生物能源与过程研究所,青岛 266101)
在养殖用地不断收缩、因地下水开采限制需养殖用水循环使用的形势下,为了满足人们日益增长的水产品的需求,水产品高密度养殖成为增加产品供应量的主要途径之一。其中,闭环养殖是高密度养殖的常见模式,但闭环养殖易导致水质恶化和水生物疾病频发,从而加剧药物控制的依赖。促生长剂、杀虫剂、除杂剂和环境改良剂等非规范药品因具有抗病、杀虫、除草、促生长等功能,备受养殖者的青睐。有些养殖者专门用扑草净清除养殖水体中的丝状藻类、大型草类及有毒藻类[1-2],用阿维菌素、伊维菌素杀灭单养和混养池塘水体中、增殖水体中,以及与鱼体体表寄生的锚头鳋、中华鳋、鱼鲺、线虫、指环虫、三代虫等寄生虫及松藻虫、水蜈蚣等水生昆虫等[3-5],致使渔业养殖水环境受到扑草净、阿维菌素、伊维菌素等残留污染。非规范药品残留会对水生生物及浮游生物产生严重影响,也会通过食物链富集。当人类食用含有扑草净的水产品后,会引起人体免疫系统、生殖系统、内分泌系统和神经系统异常[6-7];食用少量阿维菌素、伊维菌素会产生运动失调、呼吸缓慢、DNA 损伤等,过量会导致重度昏迷甚至死亡[8-11]。农业农村部制定《2020年水产养殖用兽药及其他投入品安全隐患排查计划》,加大了对水产养殖用非规范药品中药物的监督及排查力度。由于非规范药品为新型投入品,相关学者对其中药物检测技术研究较少,尚无检测标准或方法依据可参考,这给非规范药品中药物的监督、监测造成较大困难,因此开发非规范药品中药物检测技术十分必要。
目前阿维菌素的主要检测方法有酶联免疫吸附测定法[12-14]、液相色谱法[15-22]和液相色谱-串联质谱法[23-30],液相色谱法灵敏度低,干扰影响因素多,而采用荧光检测器时涉及衍生化处理,操作复杂,而高效液相色谱-串联质谱法具有高选择性和高灵敏度,应用较为广泛。扑草净的测定方法主要有高效液相色谱法[31-32]、液相色谱-串联质谱法[33]、气相色谱法[34]、气相色谱-质谱法[35-36]和酶联免疫吸附测定法[1]等,但水产养殖用非规范药品及水中上述药物的同时测定方法还未见报道。鉴于此,本工作采用超高效液相色谱-串联质谱法同时测定水产养殖用非规范药品及水中扑草净、阿维菌素和伊维菌素的残留量。
1 试验部分
1.1 仪器与试剂
AB 5500 Qtrap 型三重四极杆质谱仪;SHIMAD LC-30AD 型超高效液相色谱仪;SIMGA 3-18KS型高速冷冻离心机;IKA-T25型高速组织匀浆机;MS1 Mini-shaker型涡轮振荡器;Milli-Q 型纯水器;NPO HLB固相萃取柱(6 mL/500 mg)。
单标准储备溶液:100 mg·L-1,准确称取扑草净、阿维菌素、伊维菌素标准品各10 mg,分别用甲醇溶解并定容至100 mL,配制成质量浓度为100 mg·L-1的单标准储备溶液,于-18 ℃避光保存。同法配制内标(扑草净-d6)储备溶液。
混合标准溶液:取扑草净标准储备溶液0.1 mL,阿维菌素、伊维菌素标准储备溶液各1.0 mL,用含0.1%(体积分数,下同)甲酸的2 mmol·L-1乙酸铵溶液溶解并定容至100 mL,配制成扑草净质量浓度为0.1 mg·L-1,阿维菌素、伊维菌素的质量浓度均为1.0 mg·L-1的混合标准溶液。
内标溶液:1.0 mg·L-1,移取内标储备溶液1.0 mL,用含0.1%甲酸的2 mmol·L-1乙酸铵溶液稀释并定容至100 mL,配制成质量浓度为1.0 mg·L-1的内标溶液。
混合标准溶液系列:移取适量的混合标准溶液以及内标溶液,用含0.1%甲酸的2 mmol·L-1乙酸铵溶液稀释,配制成扑草净的质量浓度为0.2,0.5,1.0,2.0,5.0,10.0,15.0μg·L-1,阿维菌素、伊维菌素的质量浓度为2.0,5.0,10.0,20.0,50.0,100.0,150.0μg·L-1,内标质量浓度均为10μg·L-1的混合标准溶液系列。
扑草净、阿维菌素、伊维菌素、扑草净-d6标准品的纯度不小于98%;甲醇、乙腈、甲酸、乙酸铵均为色谱纯;试验用水为超纯水。
1.2 仪器工作条件
1.2.1 色谱条件
Waters ACQUITY UPLC C18色谱柱(100.0 mm×2.1 mm,1.7μm);流量0.2 mL·min-1;柱温40℃;进样体积5.0μL;流动相A 为含0.1%甲酸的2 mmol·L-1乙酸铵溶液,B 为甲醇。梯度洗脱程序:0~6.0 min时,B 由30%降至0,保持4.0 min;10.0~10.1 min时,B由0跳转至30%,保持2.9 min。
1.2.2 质谱条件
电喷雾离子(ESI)源,正离子(ESI+)扫描模式;离子源温度550 ℃;气帘气压力138 k Pa;碰撞诱导解离(CAD)设置Medium;喷雾电压4 500 V;辅助气1压力344 k Pa;辅助气2压力344 k Pa;多反应监测(MRM)模式。其他质谱参数见表1,其中“*”代表定量离子。
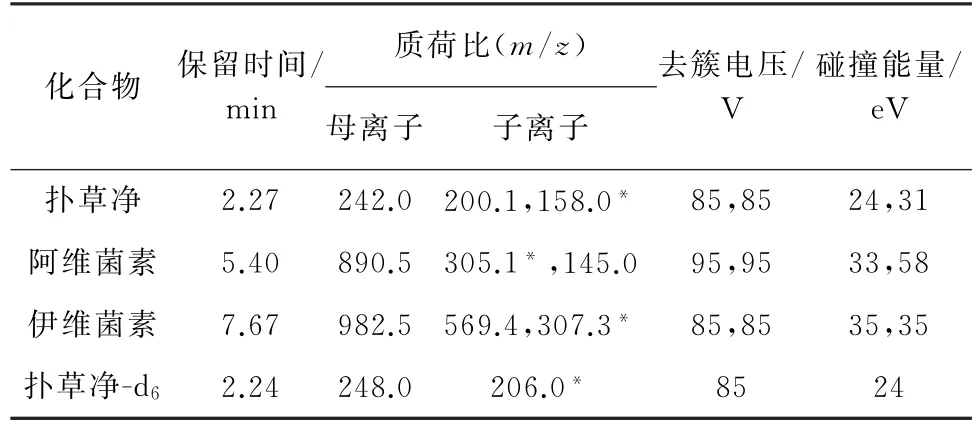
表1 质谱参数Tab.1 MS parameters
1.3 试验方法
1.3.1 样品的前处理
水产养殖用非规范药品固态样品处理:准确称取水产养殖用非规范药品固态样品1.00 g,加入1.0 mg·L-1扑草净-d6溶液10μL 和水20 mL,经均质、超声处理后离心5 min,取上清液用水定容至100 mL。
水产养殖用非规范药品液态样品处理:准确称取水产养殖用非规范药品液态样品1.00 g,加入1.0 mg·L-1扑草净-d6溶液10μL 和水20 mL,经涡旋振荡混匀后离心5 min,取上清液用水定容至100 mL。
养殖水样品处理:养殖水样品经0.45μm 滤膜过滤,取滤液200 mL,然后加入1.0 mg·L-1扑草净-d6溶液10μL,振荡混匀。
1.3.2 样品的净化
用5 mL甲醇、5 mL水活化NPO HLB固相萃取柱,充分浸润填料,以清洗固相萃取柱上的干扰杂质以及溶剂残留。将100 mL待净化的样品溶液以1滴/s的流量过已活化的NPO HLB 固相萃取柱,用5 mL水淋洗。用洗耳球将固相萃取柱内的淋洗液吹干,然后用6 mL甲醇洗脱于15 mL离心管中,再用洗耳球吹干。将洗脱液于40℃氮吹至近干,加入体积比3∶7 的甲醇-含0.1%甲酸的2 mmol·L-1乙酸铵溶液(定容溶剂)1.0 mL,涡旋1 min,超声振荡1 min,转入1.5 mL 离心管中,以转速20 000 r·min-1离心5 min,所得溶液过0.2μm 滤膜,按照仪器工作条件测定。
2 结果与讨论
2.1 色谱条件的选择
2.1.1 流动相
为同时使扑草净、阿维菌素、伊维菌素获得理想的灵敏度与分离效果,试验选取了乙腈-含0.1%甲酸的2 mmol·L-1乙酸铵溶液、甲醇-含0.1%甲酸的2 mmol·L-1乙酸铵溶液、甲醇-水、乙腈-水等4种不同的流动相体系进行对比。结果表明,与甲醇-水、乙腈-水流动相体系相比,乙腈-含0.1%甲酸的2 mmol·L-1乙酸铵溶液、甲醇-含0.1%甲酸的2 mmol·L-1乙酸铵溶液流动相体系可明显提高离子化程度,在同等条件下,甲醇-含0.1%甲酸的2 mmol·L-1乙酸铵溶液作为流动相体系时目标物的信号更强,因此试验选择甲醇-含0.1%甲酸的2 mmol·L-1乙酸铵溶液作为流动相体系。
2.1.2 色谱柱
保持其他条件不变,试验考察了Shim-pack XR-ODS C8柱(75.0 mm×2.1 mm,2.2μm)、Thermo C18柱(100.0 mm×2.1 mm,5.0μm)和Waters ACQUITY UPLC C18柱(100.0 mm×2.1 mm,1.7μm)等不同色谱柱对目标物分离效果的影响,结果见图1。

图1 不同色谱柱下目标物的分离效果Fig.1 Separation effect of targets on different chromatographic columns
由图1可知:以Shim-pack XR-ODS C8柱作为分离柱,阿维菌素、伊维菌素峰形较差,响应强度较低;以Thermo C18柱作为分离柱,阿维菌素、伊维菌素半峰宽较宽,响应强度较低;以Waters ACQUITY UPLC C18柱作为分离柱,目标物峰形好,响应强度高。因此,试验选择Waters ACQUITY UPLC C18柱(100.0 mm×2.1 mm,1.7μm)作为色谱分离柱。
2.2 扫描模式的选择
为获得扑草净、阿维菌素、伊维菌素较理想的信号强度,比较了ESI+与电喷雾离子源负离子(ESI-)扫描模式下目标物的响应强度。结果表明:在ESI-扫描模式下,阿维菌素、伊维菌素响应强度较低,按不小于3倍信噪比(S/N)计算,扑草净的检出限为5μg·kg-1,阿维菌素、伊维菌素的检出限为100μg·kg-1;在ESI+扫描模式下,以体积比3∶7的甲醇-含0.1%甲酸的2 mmol·L-1乙酸铵溶液作为定容溶剂,各目标物母离子[M+NH4]+响应强度增大,按不小于3倍信噪比计算,扑草净的检出限可达到0.2μg·kg-1,阿维菌素、伊维菌素的检出限可达到2.0μg·kg-1。因此,试验选择ESI+模式扫描。
2.3 固相萃取柱的选择
试验分别以NPO HLB 柱、Waters OASIS HLB柱和CNW HLB 柱等3个品牌HLB 固相萃取柱(500 mg/6 mL)作为目标物净化提取柱,考察了不同HLB固相萃取柱对非规范药品中3种目标物的提取效果,结果见图2。

图2 不同固相萃取柱下非规范药品中3种目标物的回收率Fig.2 Recovery of 3 targets in non-standard drugs by different solid phase extraction columns
结果表明:在相同条件下,Waters OASIS HLB柱净化效果较好,但过柱时间长;NPO HLB柱过柱速率最快,回收效果好,但柱净化效果稍差;CNW HLB柱过柱速率较快,净化效果较好,但回收效果不理想。综合考虑,大批量样品处理采用NPO HLB柱作为固相萃取柱,同时满足高效、准确度高的要求。
2.4 标准曲线、检出限和测定下限
按仪器工作条件测定混合标准溶液系列,扑草净、阿维菌素、伊维菌素均以扑草净-d6为内标,用仪器自带工作站按内标法进行自动计算,以目标物质量浓度与内标质量浓度的比值为横坐标,以目标物峰面积与内标峰面积的比值为纵坐标绘制标准曲线。所得目标物的线性范围、线性回归方程和相关系数见表2。按不小于3倍信噪比分别计算非规范药品和水样中各目标物的检出限,按不小于10倍信噪比分别计算非规范药品和水样中各目标物的测定下限,结果见表2。

表2 线性参数、检出限和测定下限Tab.2 Linearity parameters,detection limits and lower limits of determination
2.5 精密度和回收试验
选取空白非规范药品固态样品和液态样品、水样为基质,分别进行3个浓度水平的加标回收试验,每个浓度水平制备6个平行样品,计算回收率及测定值的相对标准偏差(RSD),结果见表3和表4。

表3 在非规范药品样品基质中的精密度和回收试验结果(n=6)Tab.3 Results of tests for precision and recovery in non-standard drug sample matrices(n=6)

表4 在水样基质中的精密度和回收试验结果(n=6)Tab.4 Results of tests for precision and recovery in water sample matrix(n=6)
结果表明:目标物的回收率为84.8%~105%,测定值的RSD 为2.9%~8.4%。说明方法适合水产养殖非规范药品及水中扑草净、阿维菌素、伊维菌素的残留测定。
2.6 样品分析
按照试验方法分析天津市场的80个非规范药品与水样(包括杀虫剂、促生长剂、水质改良剂、底质改良剂、微生态制剂、水产养殖用饲料等)。结果显示,1个非规范药品样品中检出阿维菌素,其残留量为718 mg·kg-1,1个水样中检出扑草净,其残留量为3.2 ng·L-1,其他样品均未检出。
本工作提出了超高效液相色谱-串联质谱法同时测定水产养殖用非规范药品及水中扑草净、阿维菌素、伊维菌素残留量的方法。本方法具有快速、灵敏、准确且简单的优点,可满足实验室质量控制规范的技术要求。
