左归降糖益肾方HPLC指纹图谱及4种成分的含量测定研究
2023-09-07惠博平,易子漾,陈林,陈海刚,喻嵘,黄建华
惠博平,易子漾,陈林,陈海刚,喻嵘,黄建华
〔摘要〕 目的 采用HPLC建立左歸降糖益肾方指纹图谱,并对4个主要成分进行含量测定。方法 对色谱柱型号、流动相系统、梯度洗脱条件、检测波长以及供试品处理方法等条件进行优化,最终确定了最佳液相条件:选用色谱柱为Welch ultimate AQ-C18(4.6 mm×250 mm,5 μm);流动相系统为甲醇-0.1%甲酸溶液;紫外检测波长为254 nm;供试品溶液提取溶剂为甲醇溶液。并对8批次左归降糖益肾方HPLC指纹图谱进行相似性分析判断批次间稳定性。结果 利用HPLC指纹图谱确定了左归降糖益肾方21个共有峰,并指认了9个色谱峰;8批次左归降糖益肾方指纹图谱的相似度均大于0.920;4个有效成分马钱苷、盐酸药根碱、盐酸小檗碱和盐酸巴马汀的平均含量分别为(183.93±9.55)、(42.64±4.77)、(198.01±9.49)、(96.36±9.00) μg·mL-1。结论 建立的左归降糖益肾HPLC方指纹图谱方法简便,准确、重现性好,可为左归降糖益肾方的质量控制体系提供参考。
〔关键词〕 左归降糖益肾方;糖尿病肾病;高效液相色谱法;指纹图谱;含量测定
〔中图分类号〕R284.1 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2023.08.012
HPLC fingerprint of Zuogui Jiangtang Yishen Formula and content determination of its four ingredients
HUI Boping1, YI Ziyang1, CHEN Lin2, CHEN Haigang3, YU Rong1*, HUANG Jianhua1,2*
1. Hunan University of Chinese Medicine, Changsha, Hunan 410208, China; 2. Hunan Academy of Chinese Medicine, Changsha, Hunan 410006, China; 3. China Resources Sanjiu (Chenzhou) Pharmaceutical Co.,Ltd., Chenzhou, Hunan 423000, China
〔Abstract〕 Objective To establish the HPLC fingerprint of Zuogui Jiangtang Yishen Formula and to determine the content of its four main ingredients. Methods The chromatographic column type, mobile phase system, gradient elution condition, detection wavelength, and test product treatment were optimized. The optimal liquid phase conditions were: Welch ultimate AQ-C18 (4.6 mm×250 mm, 5 μm) was selected as the chromatographic column, the methanol-0.1% formic acid solution was taken as the mobile phase system, the UV detection wavelength was 254 nm, and methanol solution was set as the extraction solvent of the test solution. And similarity analysis on the HPLC fingerprints of 8 batches of Zuogui Jiangtang Yishen Formula was performed to determine the stability among batches. Results A total of 21 common peaks were determined, and 9 chromatographic peaks were identified from HPLC fingerprint of Zuogui Jiangtang Yishen Formula. The similarity of fingerprints among 8 batches of Zuogui Jiangtang Yishen Formula was greater than 0.920. The average content of the four active ingredients (loganin, jatrorrhizine hydrochloride, berberine hydrochloride, and palmatine chloride) were 183.93±9.55, 42.64±4.77, 198.01±9.49, and 96.36±9.00 μg·mL-1, respectively. Conclusion The established HPLC fingerprint method is simple, accurate, and reproducible, which can provide references for the quality control system of Zuogui Jiangtang Yishen Formula.
〔Keywords〕 Zuogui Jiangtang Yishen Formula; diabetic kidney disease; high performance liquid chromatography; fingerprint; content determination
糖尿病肾病(diabetic kidney disease, DKD)被认为是2型糖尿病最主要的并发症之一,并且与蛋白尿、高血压、水肿、肾功能不全和肾衰竭有关。然而,由于DKD发病机制的复杂性,其病理生理机制尚未完全阐明[1]。西医治疗DKD虽已取得一些新的进展,可以使患者的病情部分延缓或控制,但长期预后仍不尽如人意[2],血管紧张素转化酶抑制剂和血管紧张素Ⅱ受体阻滞剂具有肾脏保护作用,但很大一部分DKD患者最终会进展为终末期肾衰竭[3]。近些年来,中医药防治是干预临床DKD非常重要的手段。中医学认为,气阴两虚兼血瘀是糖尿病肾病的基本证候,且随着病期的进展,脾肾阳虚、阴阳两虛以及浊毒、水湿等证候增加,提示DKD出现阳虚、湿毒等证候时常意味着病情的加重[4]。在中医药理论指导下引入现代科学、实现中药现代化已成为中药发展的必由之路[5],其在诊治该疾病上具有一定的优势和特色。
课题组长期致力于糖尿病及其并发症的中医药防治研究[6],左归降糖益肾方是以明代医家张景岳阴阳互济法的代表方左归丸、左归饮化裁而成,由黄芪、丹参、山药、黄连、牛膝、益母草、熟地黄、酒山茱萸、玉米须9味中药组成。方中重用熟地黄,滋阴养肾为主药,以填真阴[7];黄芪益气健脾;酒山茱萸、牛膝补益肝肾,强健腰膝;黄连清热燥湿,泻火解毒[8];丹参、益母草活血化瘀;玉米须清热利湿,利尿消肿;诸药合用,共奏滋阴益气,活血解毒,利尿消肿之功效[9]。经过长期的临床实践表明,左归降糖益肾方可降低空腹血糖,改善糖耐量、抑制炎症因子的产生和氧化应激作用,通过解除高血糖对肾小球的刺激,阻断炎症诱导的损伤从而达到减少蛋白尿、改善糖尿病早期肾脏损伤的目的[10]。
开展中药质量控制研究是保证中药安全和疗效的关键,也是中药生产现代化和质量标准科学化发展的关键[11]。对于成分复杂的中药复方来说,中药指纹图谱可整体、全面地反映中药及其复方制剂的化学成分信息,具有专属性、特征性强,且重现性、稳定性好等诸多优点[12-13]。长期的临床实践和实验研究表明,左归降糖益肾方在DKD的防治中疗效显著[14-15],然而该组方的化学成分还未进行系统全面的分析研究。因此,本文拟建立左归降糖益肾方HPLC指纹图谱,并定量分析其主要成分,为更全面开展其质量控制研究,为保证其临床疗效提供依据。
1 材料
1.1 仪器与设备
AgiLent 1200高效液相色谱仪(美国AgiLent公司);KQ2200DB型数控超声波清洗器(昆山市超声仪器有限公司);真空冷冻干燥机(杭州旌斐仪器科技有限公司);EXPE105型电子天平、XS205型十万分之一天平(瑞士梅特勒-托利多仪器有限公司)。
1.2 药材与试剂
1.2.1 药材 左归降糖益肾方组方药材均购于湖南中医药大学第一附属医院中药房,黄芪(批号:CK21063002;产地:四川);熟地黄(批号:2103033;产地:河南);牛膝(批号:SL21060301;产地:河南);黄连(批号:HH21060704;产地:甘肃);益母草(批号:200901;产地:湖南);玉米须(批号:2021042602;产地:河南);丹参(批号:HY21061501;产地:山东);酒山茱萸(批号:TH21060703;产地:河南);山药(批号:CK21061807;产地:河南)。
1.2.2 对照品 盐酸小檗碱(批号:CHB-Y-039)购自成都普菲德生物科技有限公司;异槲皮苷(批号:CHB201210)、京尼平苷酸(批号:CHB201204)均购自成都克洛玛生物科技有限公司;莫诺苷(批号:111998-202104)、腺苷(批号:CHB210104)、盐酸巴马汀(批号:110732-20110)、盐酸药根碱(批号:110733-201619)、马钱苷(批号:CHB180108)均购自中国食品药品检定研究院,纯度均为98%。
1.2.3 试剂 甲醇为分析纯(批号:20211023,湖南汇虹试剂有限公司);甲醇为色谱纯(批号:21115042,美国天地有限公司);甲酸为色谱纯(批号:20210303,天津市科密欧化学试剂有限公司);怡宝水(批号:20211202,华润怡宝饮料有限公司)。
2 方法与结果
2.1 溶液制备
供试品溶液制备:取8批左归降糖益肾方(S1~S8)各味中药分别放于砂锅中以10倍水浸泡30 min,武火加热煮沸后,转用文火煎煮1.5 h,纱布过滤药液,药渣再加8倍量水煎煮1 h并过滤,将两次煎煮的滤液浓缩至约300 mL的流浸膏,于冷冻干燥机中减压干燥得到冻干粉末,取复方冻干粉末约1 g,置具塞锥形瓶中,加入甲醇40 mL,密塞,超声处理30 min,取出,摇匀,放冷,过0.22 μm微孔滤膜,即得,置于4 ℃冰箱保存备用。
对照品溶液的制备:分别精密称取对照品马钱苷2.03 mg、盐酸小檗碱3.02 mg、盐酸药根碱2.60 mg、盐酸巴马汀3.10 mg分别于5 mL容量瓶中,加甲醇制成每1 mL各约含0.406、0.604、0.520、0.620 mg的对照品溶液,摇匀,过0.22 μm微孔滤膜,即得。
空白溶液:色谱甲醇溶液。
2.2 HPLC色谱条件
采用Agilent 1200高效液相色谱仪,Welch ultimate AQ-C18(4.6 mm×250 mm,5 μm)色谱柱;柱温为25 ℃;紫外检测器检测波长254 nm;进样量为5 μL;流动相A为甲醇,流动B为0.1%甲酸水溶液;梯度洗脱(0~15 min,5%~13%A;15~28 min,13%~23%A;28~35 min,23%~26%A;35~50 min,26%~38%A;50~60 min,38%~53%A;60~65 min,53%~60%A;65~75 min,60%~95%A);流速为0.8 mL/min。
2.3 色谱条件的优化
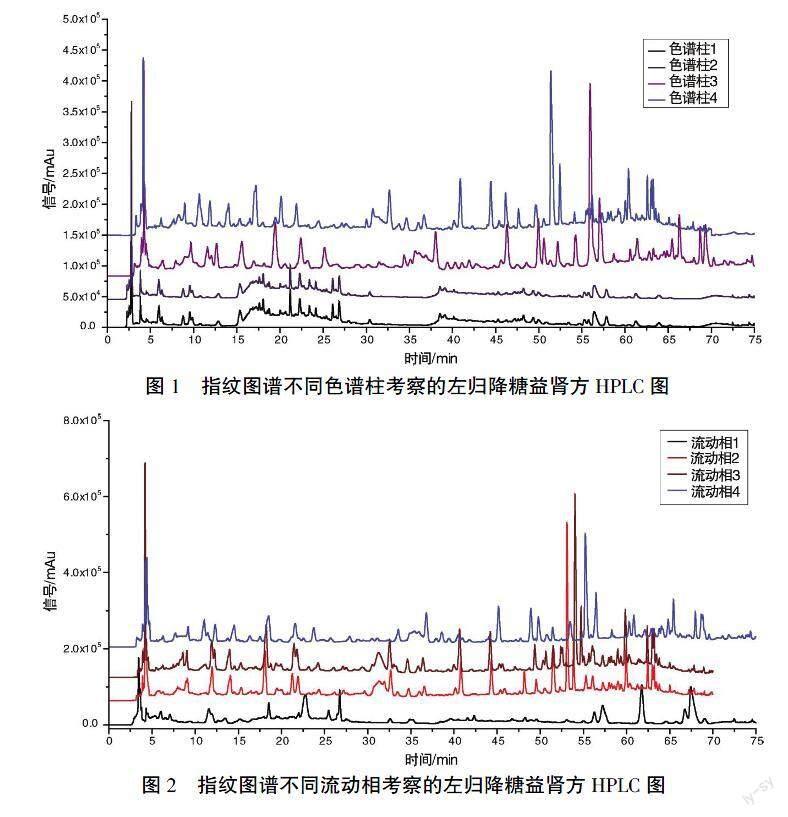
2.3.1 色谱柱考察 采用不同色谱柱:色谱柱1为Agilent ZORBAX SB-C18(4.6 mm×250 mm,5 μm);色谱柱2为InertSustain AQ-C18(4.6 mm×250 mm,5 μm);色谱柱3为Generall C18亲水AQ柱(4.6 mm×250 mm,5 μm);色谱柱4为Welch ultimate AQ-C18(4.6 mm×250 mm,5 μm)。按“2.2”指纹图谱色谱条件进行测定,基于色谱柱4的色谱图基线较为平稳、色谱峰分离效果和峰型较好、色谱峰响应高,故后续实验选用色谱柱4。结果详见图1。
2.3.2 流动相系统考察 考察甲醇、乙腈和水不同组合洗脱条件下的分析结果,选择流动相系统:流动相1(乙腈-0.1%甲酸溶液)、流动相2(甲醇-0.05%磷酸溶液)、流動相3(甲醇-0.1%磷酸溶液)、流动相4(甲醇-0.1%甲酸溶液),按“2.2”指纹图谱色谱条件进行测定,记录254 nm处色谱图。结果如图2所示,甲醇与水组成的流动相洗脱效果更好,得到的色谱图色谱峰数目最多,当在水相中加入少量甲酸后,色谱峰分离效果变得更好,基线波动较缓,各成分色谱峰保留时间适中且数量最多,故选择流动相4(甲醇-0.1%甲酸溶液)为流动相系统。
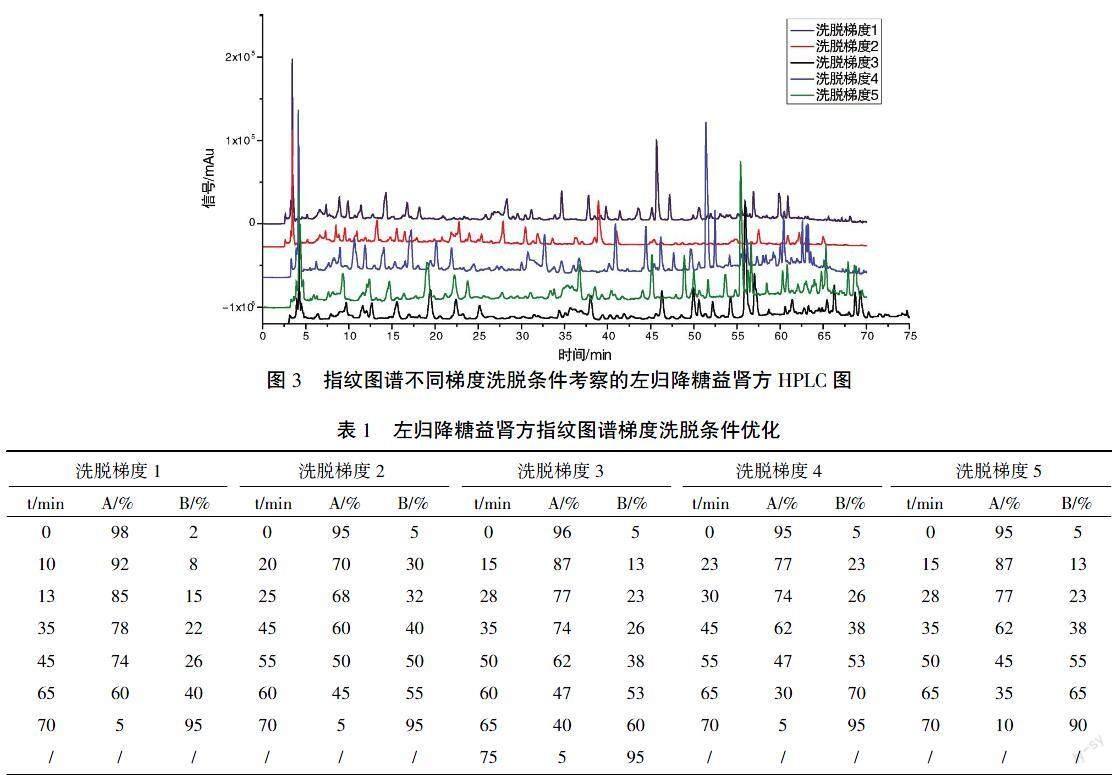
2.3.3 梯度洗脱条件优化 以十八烷基硅烷键合硅胶为填充剂,甲醇-0.1%甲酸为流动相,按表1条件进行梯度洗脱优化;柱温25 ℃;液相使用Agilent 1200高效液相色谱仪;色谱柱使用Welch ultimate AQ-C18(4.6 mm× 250 mm,5 μm)色谱柱。记录检测波长254 nm信号色谱图。各梯度洗脱条件的结果如图3所示,流动相A为甲醇,流动B为0.1%甲酸水溶液,选择“洗脱梯度3”条件进行梯度洗脱,该条件色谱峰紫外吸收响应值较高且峰型、分离度均较好、杂峰较少,故选择“洗脱梯度3”条件。
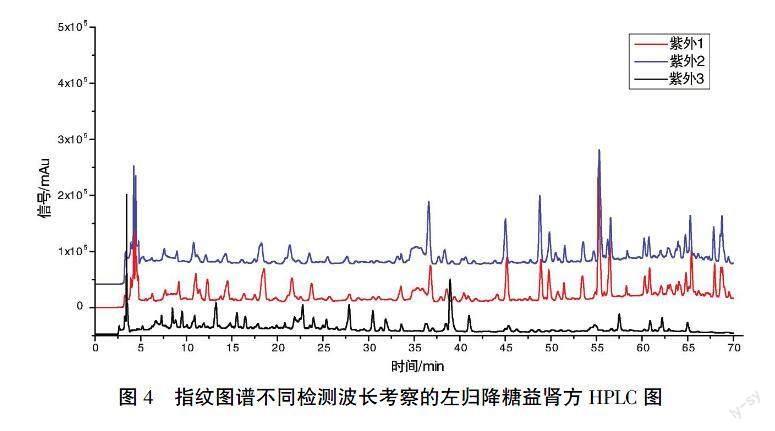
2.3.4 最佳检测波长考察 对比紫外1(254 nm)、紫外2(245 nm)、紫外3(335 nm)不同紫外检测器检测波长,按“2.2”指纹图谱色谱条件进行测定,结果如图4所示,当检测波长选择254 nm时色谱图中各色谱峰响应值较高,图谱信息最为丰富,各峰吸收较均匀,故检测波长选择紫外1(254 nm)。
2.3.5 供试品溶液提取溶剂考察 本试验分别选用提取溶剂1(70%甲醇)、提取溶剂2(50%甲醇)和提取溶剂3(甲醇)作为提取溶剂,按“2.1”项冻干粉末处理方法,分别精密加入70%甲醇、50%甲醇、100%甲醇40 mL。按“2.2”指纹图谱色谱条件进行测定,比较不同溶剂的HPLC图谱,结果如图5所示,提取溶剂为70%甲醇、50%甲醇、色谱图中信号峰数量基本一致,当提取溶剂为甲醇时,色谱图基线较平稳,色谱峰数量多且响应较好,配制较为简便,故提取溶剂选择提取溶剂3(甲醇)。
2.4 指纹图谱研究
2.4.1 指纹图谱的建立 指纹图谱的建立:取8批左归降糖益肾方样品溶液,按“2.2”项下色谱条件进样测定,将8批样品的色谱数据以AIA文件格式导入国家药典委员会《中药色谱指纹图谱相似度评价系统》(2004版)软件,以S1号色谱图为参考,采用多点校正及自动匹配,建立共有模式,时间窗宽度设为0.1,中位数法生成对照图谱,采用“中药色谱指纹图谱相似度评价系统”进行共有峰标识,获得了21个共有峰,与对照图谱相比,不同批次左归降糖益肾方样品化学成分轮廓基本一致。结果详见图6。
2.4.2 共有峰的指认 制备中药化学对照品混合溶液,按照左归降糖益肾方样品指纹图谱测定方法测定,对左归降糖益肾方样品HPLC 21个共有峰中的9个色谱峰进行了指认,分别为1号色谱峰(腺苷)、2号色谱峰(京尼平苷酸)、3号色谱峰(莫诺苷)、4号色谱峰(马钱苷)、5号色谱峰(盐酸药根碱)、6号色谱峰(腺盐酸小檗碱)、7号色谱峰(盐酸巴马汀)、8号色谱峰(β-蜕皮甾酮)、9号色谱峰(异槲皮苷)。结果详见图7。
2.4.3 相似度评价 将8批左归降糖益肾方样品指纹图谱导入国家药典委员会《中药色谱指纹图谱相似度评价系统》软件,经多点校正后,进行色谱峰匹配,计算相似度,结果见表2。8批次左归降糖益肾方样品色谱图的相似度均>0.920,表明不同批次样品之间的差异较小,共有成分基本一致,8批次左归降糖益肾方质量较稳定。
2.5 含量方法学考察
2.5.1 线性关系考察 精密量取等体积“2.1”项下对照品贮备液摇匀,得到4种成分的系列浓度混合对照品溶液,按“2.2”项下色谱条件测定,以对照品浓度为横坐标,峰面积为纵坐标,绘制标准曲线,计算回归方程和线性范围,取对照品溶液进行稀释,分别按信噪比为10∶1和3∶1时的进样量计算定量限和检测限。详见表3。
2.5.2 精密度试验 取左归降糖益肾方供试品溶液,按“2.2”项下色谱条件连续进样6次,以马钱苷、盐酸药根碱、盐酸小檗碱、盐酸巴马汀等色谱峰为参照峰,计算峰面积和保留时间的RSD值,各特征峰保留时间RSD分别为0.45%、0.56%、0.52%、0.42%,峰面积RSD分别为1.86%、1.62%、0.98%、1.29%。表明仪器精密度良好。
2.5.3 稳定性试验 取同一左归降糖益肾方供试品溶液,按“2.2”项下色谱条件,分别于制备后的0、2、4、6、8、10、12 h进样检测,以马钱苷、盐酸药根碱、盐酸小檗碱、盐酸巴马汀等色谱峰为参照峰,计算峰面积和保留时间的RSD值,各特征峰保留时间RSD分别为0.54%、0.65%、0.60%、0.49%,峰面积RSD分别为2.41%、1.80%、1.73%、1.56%。表明供试品溶液12 h内稳定性良好。
2.5.4 重复性试验 取同一批左归降糖益肾方冻干粉末约1 g(6份),按“2.1”项下供试品溶液制备方法进行供试品溶液制备,按“2.2”项下色谱条件进行检测,以马钱苷、盐酸药根碱、盐酸小檗碱、盐酸巴马汀等色谱峰为参照峰,计算相对峰面积和相对保留时间的RSD值,各特征峰相对保留时间RSD分别为0.65%、0.61%、0.53%、0.41%,相对峰面积RSD分别为2.78%、1.74%、2.40%、2.16%,说明方法重复性良好。
2.5.5 加标回收试验 取同一批已知含量的左归降糖益肾方冻干粉末1 g,平行9份,精密称定,按已知成分含量的50%、100%、150%加入相应量对照品,按“2.1”方法制备供试品溶液后,按“2.2”项下条件进样测定,记录峰面积并计算马钱苷、盐酸药根碱、盐酸小檗碱、盐酸巴马汀的加标回收率。结果显示,4种成分的平均加样回收率在101.04%~105.00%之间,RSD在1.92%~3.81%之间(n=9),表明该方法的准确度较好,结果见表4。
2.5.6 样品含量测定 分别取8批次(S1~S8)左归降糖益肾方冻干粉末适量,按“2.1”项下方法制备样品溶液,按“2.2”项下色谱条件进样测定,计算样品中马钱苷、盐酸药根碱、盐酸小檗碱、盐酸巴马汀的含量,结果见表5。
3 讨论
DKD是糖尿病最常见、最严重的微血管并发症之一,是终末期肾衰竭的主要原因。据报道,到2035年,全球糖尿病患者人口估计将达到5.29亿。有30%~40%的患者可能发生DKD[16]。目前,DKD的主要治疗方法主要集中在血压、血脂和血糖控制,改变生活方式,尚无有效的DKD治疗策略[17]。中医学将DKD归为“消渴”“水肿”等范畴,病机在于肾元亏虚、毒损肾络,故治以活血、化瘀、益气滋阴为主[18]。左归降糖益肾方作为控制DKD症状的有效中药复方[19],组方中黄芪具益气、免疫调节之功效,其广泛用于糖尿病及其代谢综合征的治疗,特别是DKD的治疗。多项临床实验表明,黄芪可显著降低DKD患者的血糖、蛋白尿和血清肌酐等水平[20],其活性成分黄芪甲苷在体内外具有多种药理活性,包括抗氧化应激、抗炎、抗糖尿病和肾脏保护等作用[21-22]。熟地黄味甘,微温,归肝、肾经,具有补血养阴、益精填髓等功效。临床证明熟地黄具有抗氧化、降血糖及减少骨丢失等作用[23],因此,其被广泛应用于治疗DKD,其药效成分地黄苷D、梓醇可降低糖尿病模型动物的高血糖水平[24-25]。黄连性味苦、寒,归心、脾、胃、肝、胆、大肠经,能清热燥湿、泻火解毒。研究表明,黄连中的多种生物碱能够减少肝脏糖异生,其药效成分小檗碱、药根碱能抑制磷酸化酶、6-磷酸果糖激酶和果糖双磷酶催化,可降低糖化血清蛋白及糖化血红蛋白,显著降低空腹及餐后血糖[26]。此外,小檗碱还具有改善胰岛素抵抗、降血脂、降血压、降低蛋白尿、减少尿白蛋白排泄,保护肾功能的功效[27]。酒山茱萸中马钱苷、莫诺苷对足细胞凋亡具有保护作用,马钱苷还可改善肾脏病变及纤维化[28]。
本研究尝试使用水煎煮液直接进行分析,但是结果发现液相色谱峰极性太大且谱峰高从而干扰到其他色谱峰检测等问题,故采用提取溶剂(不同浓度的甲醇溶液)进行分析,发现使用甲醇溶液进行提取谱图基线较平稳、色谱峰保留时间适中。进一步对供试品溶液的制备条件,对流动相(乙腈-甲酸水、甲醇-甲酸水)、梯度洗脱程序、紫外吸收波长、色谱柱型号等条件进行考察,最终确定了最佳实验条件。在最优分析条件下,建立了左归降糖益肾方HPLC指纹图谱,在8个批次样品中共标定了21个共有峰,指认了其中的9个色谱峰,8批次指纹图谱的相似度大于0.920,表明各批次样品所含成分相似、质量稳定均一。
中药的物质基础是揭示中药作用本质的关键,更是解决中药质量控制难题的根本保证。但考虑到左归降糖益肾方的制备工艺为水煎煮,且经过甲醇提取后进行分析,因此,择各药味中具有特征性的水溶性成分作为质量指标进行测定。研究发现,组方中马钱苷、盐酸药根碱、盐酸小檗碱和盐酸巴马汀色谱峰分离度较好,且可以准确定量。故研究它们作为含量测定指标。本研究采用HPLC技术建立了同时测定左归降糖益肾方中马钱苷、盐酸药根碱、盐酸小檗碱、盐酸巴马汀中4种药效成分含量的分析方法,并进行了方法学验证:马钱苷、盐酸药根碱、盐酸小檗碱和盐酸巴马汀的线性范围分别为50.49~370.25、32.25~48.06、127.01~330.43、66.90~134.20 μg·mL-1,表明线性关系良好;加样回收率分别为105.00%、92.01%、100.64%、101.04%;含量测定结果显示8批次左归降糖益肾方中4种成分平均含量分别为(183.93±9.55)、(42.64±4.77)、(198.01±9.49)、(96.36±9.00) μg·mL-1。本研究建立的指纹图谱及含量测定方法重复性好、灵敏度高,能较全面、准确地分析左归降糖益肾方的化学成分,该方法的建立有利于进一步研究该复方药效物质基礎,指导临床合理用药以及为后期实验研究提供参考依据,在一定程度上能有效提高左归降糖益肾方的质量控制水平。黄芪与熟地黄作为该组方的君药,由于黄芪皂苷类成分紫外光谱为末端吸收,不适于在紫外检测器下检测,地黄苷D含量较少且该组方药味较多、成分复杂,其受其他药味干扰较大,故本研究并未对以上成分进行含量测定,后期将会考虑采用蒸发光检测器对相关成分进行含量测定。
参考文献
[1] MENG X, MA J, KANG A N, et al. A novel approach based on metabolomics coupled with intestinal flora analysis and network pharmacology to explain the mechanisms of action of bekhogainsam decoction in the improvement of symptoms of streptozotocin-induced diabetic nephropathy in mice[J]. Frontiers in pharmacology, 2020, 11: 633.
[2] 阿曼古丽·阿不都克热木, 马 丽. 中药治疗糖尿病肾病的研究进展[J]. 新疆中医药, 2020, 38(6): 77-80.
[3] XIAO Y, LIU Y, YU K, et al. The effect of Chinese herbal medicine on albuminuria levels in patients with diabetic nephropathy: A systematic review and meta-analysis[J]. Evid Based Complement Alternat Med, 2013, 2013: 937549.
[4] 王 倩, 严美花, 李 平. 糖尿病肾病中医证候的现代研究[J]. 世界中医药, 2018, 13(6): 1320-1324, 1331.
[5] 杨立诚, 夏昀卿, 张萌朱, 等. 牡丹皮道地性物质基础组分结构特征及多维结构质量控制实践与发展[J]. 中国中药杂志, 2020, 45(14): 3340-3350.
[6] 艾碧琛, 肖漫江, 喻 嵘, 等. 糖益肾方对MKR鼠2型糖尿病肾病早期的保护作用[J]. 中国中医药信息杂志, 2010, 17(3): 29-30, 33.
[7] 黄诗雄, 邓德强, 高 旋. 糖尿病肾病中医治疗研究进展[J]. 新中医, 2022, 54(9): 16-22.
[8] 张育娟. 中药治疗糖尿病肾病的研究进展[J]. 内蒙古中医药, 2022, 41(5): 151-153.
[9] 陈 聪, 喻 嵘, 吴勇军, 等. 左归降糖益肾方对糖尿病肾病MKR鼠血糖、血脂、肾功能及血清TNF-α和IL-6含量的影响[J].中华中医药杂志, 2014, 29(5): 1618-1621.
[10] 成细华, 喻 嵘, 明季伍, 等. 左归降糖益肾方对高脂饮食2型糖尿病MKR小鼠糖脂代谢及炎症反应的影响[J]. 中国实验方剂学杂志, 2010, 16(12): 98-101.
[11] 刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker): 中药产品质量控制的新概念[J]. 中草药, 2016, 47(9): 1443-1457.
[12] 郭海姣, 覃洁萍, 刘 雯, 等. 穿黄制剂定性指纹图谱及多组分含量测定方法研究[J]. 中国医院药学杂志, 2020, 40(3): 289-295.
[13] 陈 蒙, 林龙飞, 刘宇灵, 等. 经典名方苓桂术甘汤HPLC指纹图谱的建立及3种成分含量测定[J]. 中草药, 2019, 50(17): 4152-4157.
[14] YI Z Y, PENG Y J, HUI B P, et al. Zuogui-Jiangtang-Yishen decoction prevents diabetic kidney disease: Intervene pyroptosis induced by trimethylamine n-oxide through the mROS-NLRP3 axis[J]. Phytomedicine, 2023, 114: 154775.
[15] 喻 嵘, 陈大舜, 易法银, 等. 左归降糖方治非胰岛素依赖型糖尿病临床研究[J]. 辽宁中医杂志, 1999(8): 13-14.
[16] SUGAHARA M, PAK W L W, TANAKA T, et al. Update on diagnosis, pathophysiology, and management of diabetic kidney disease[J]. Nephrology (Carlton), 2021, 26(6): 491-500.
[17] WANG E, WANG L, DING R, et al. Astragaloside IV acts through multi-scale mechanisms to effectively reduce diabetic nephropathy[J]. Pharmacological research, 2020, 157: 104831.
[18] 國馨月, 刘晓丽. 益气滋阴、活血化瘀中药治疗糖尿病肾病患者的效果[J]. 中国药物经济学, 2022, 17(3): 108-110,114.
[19] 吴 聪, 喻 嵘, 成细华, 等. 降糖益肾方干预胰岛素信号通路改善转基因2型糖尿病MKR鼠肾损伤的研究[J]. 湖南中医药大学学报, 2011, 31(11): 9-11, 29.
[20] DAI Y, GUO M, JIANG L, et al. Network pharmacology-based identification of miRNA expression of Astragalus membranaceus in the treatment of diabetic nephropathy[J]. Medicine, 2022, 101(5): e28747.
[21] ZHAO X, SUN X, GONG X, et al. Astragaloside IV from Astragalus membranaceus ameliorates renal interstitial fibrosis by inhibiting inflammation via TLR4/NF-small ka, CyrillicB in vivo and in vitro[J]. International Immunopharmacology, 2017, 42: 18-24.
[22] CHEN Q, SU Y, JU Y, et al. Astragalosides IV protected the renal tubular epithelial cells from free fatty acids-induced injury by reducing oxidative stress and apoptosis[J]. Biomed Pharmacother, 2018, 108: 679-686.
[23] 许平翠, 朱赋健, 郑纯威, 等. 基于HPLC多波长融合指纹图谱及谱效关系的熟地黄活性成分研究[J]. 中国现代应用药学, 2022, 39(22): 2901-2907.
[24] ZHU H, WANG Y, LIU Z, et al. Antidiabetic and antioxidant effects of catalpol extracted from Rehmannia glutinosa (Di Huang) on rat diabetes induced by streptozotocin and high-fat, high-sugar feed[J]. Chinese medicine, 2016, 11(1): 1-10.
[25] 杜克群, 成颜芬, 李敏敏, 等. 基于特征图谱与5种成分含量的经典名方桃红四物汤量值传递分析[J]. 中草药, 2022, 53(22):7058-7069.
[26] 王元雪, 米 杰. 黄连治疗2型糖尿病肾病的机制研究进展[J].中西医结合研究, 2014, 6(4): 214-215.
[27] 娄文娇, 郭 敬, 张 帆, 等. 黄连素(小檗碱)治疗早期糖尿病肾病有效性和安全性系统回顾及Meta分析[J].中国中西医结合肾病杂志, 2022, 23(6): 510-513.
[28] 柳 洋, 王 丽. 山茱萸治疗糖展病肾病研究概况[J]. 中医药临床杂志, 2022, 34(9): 1778-1782.
(本文编辑 苏 维)
