克罗恩病肛瘘的外科诊治现状
2023-07-20王倩邹贤军
王倩 邹贤军
克罗恩病(Crohn’s disease,CD)是一种慢性非特异性自身免疫性肠道炎症性疾病,病变可累及全消化道,从口腔至肛门,呈节段性或跳跃性分布。CD肛瘘(perianal fistulizing Crohn’s disease,pfCD)是一种由慢性肠道炎症性疾病引发的肛周病变,其病因及发病机制尚不清楚。研究发现[1],15%~45%的CD患者会发生肛瘘或肛周脓肿等直肠肛周病变,有 5%~10%的CD患者首发表现即为肛瘘,而无其他胃肠道症状[2]。pfCD瘘管走行通常都较为复杂,治疗难度大、容易复发。 2016版欧洲克罗恩病和结肠炎组织(European Crohn’s and Colitis Organisation,ECCO)关于CD的诊疗共识中指出CD患者在确诊后1年、5年、10年和20年内肛瘘的发病率分别达到12%、15%、21%和26%[3]。迄今,对于CD 肛瘘的诊疗,国内外专家已达成部分共识,同时尚存在部分争议。
一、pfCD的诊断
1.pfCD的特点
相较于普通肛瘘,pfCD具有以下特征[4-5]:(1)pfCD多为复杂性肛瘘,具有多个内口及外口,内口常见于齿状线以上,外口距肛缘≥3 cm;(2)pfCD瘘管长且走形复杂,瘘管比普通肛瘘更宽大;(3)pfCD常累及肛管直肠环,致使指检时触及肛管直肠环呈僵硬状态;(4)pfCD常合并皮赘、非中线肛裂、肛管直肠狭窄、直肠阴道瘘等其他直肠肛周病变;(5)pfCD易复发,复发部位与原病灶位置常常不同;(6)pfCD患者常伴有慢性腹泻、腹痛、消瘦、贫血等症状。
2.pfCD的检查方法
对有症状和体征的pfCD,应常规进行盆腔磁共振成像(magnetic resonance imaging,MRI)检查,可结合麻醉下探查(examination under anaesthesia,EUA)和腔内超声检查(endoanal ultrasound,EUS)[5]。
盆腔MRI具有无创、快速、准确的优点,是pfCD诊断及分型的首选方法[6]。EUS检查方法可以在部分患者选择使用,其优点是能较好的识别内口和显示括约肌间瘘管,但存在超声波穿透力低、观测视野窄、脓肿形成导致疼痛及局部狭窄等因素导致应用受限[7]。此外,对于临床诊疗经验丰富的外科医生,EUA也是一种可靠的pfCD诊断检查方法。 目前认为EUA联合EUS、MRI两种检查中的任何一种,可以使得pfCD诊断的准确率达到100%[8]。
二、pfCD严重程度的评估
1.分型
美国胃肠病学会(AGA)将pfCD分为简单性和复杂性[9]。简单性肛瘘指低位肛瘘(包括浅表型、低位括约肌间型和低位经括约肌型),且仅有单个瘘管,不合并肛周脓肿、直肠阴道瘘或肛管直肠狭窄。复杂性肛瘘指高位肛瘘(包括高位括约肌间型、高位经括约肌型、括约肌上型和括约肌外型),可存在多个瘘管,可合并肛周脓肿、直肠阴道瘘或肛管直肠狭窄。简单性和复杂性肛瘘的定义比较见表1。AGA分型结果与 pfCD的治疗方法和预后有关[10]。

表1 简单性肛瘘和复杂性肛瘘的定义比较
Park分型方法将肛瘘分为5型,包括括约肌肌间型、经括约肌型、括约肌上型、括约肌外型和浅表型[11],可作为pfCD的解剖学参考。
2.肛周疾病活动指数评分
根据肛周症状及体格检查判断pfCD的严重程度,可参考肛周疾病活动指数(PDAI)评分表,见表2[12]。该评分方法包含肛周的分泌物、疼痛和活动、性生活、肛周表现和硬结5个方面,单项评分按严重程度分为0~4分,总分最高为20分。 PDAI总分大于4分提示活动性瘘管或存在局限性炎症反应,准确率达87%[13-14]。
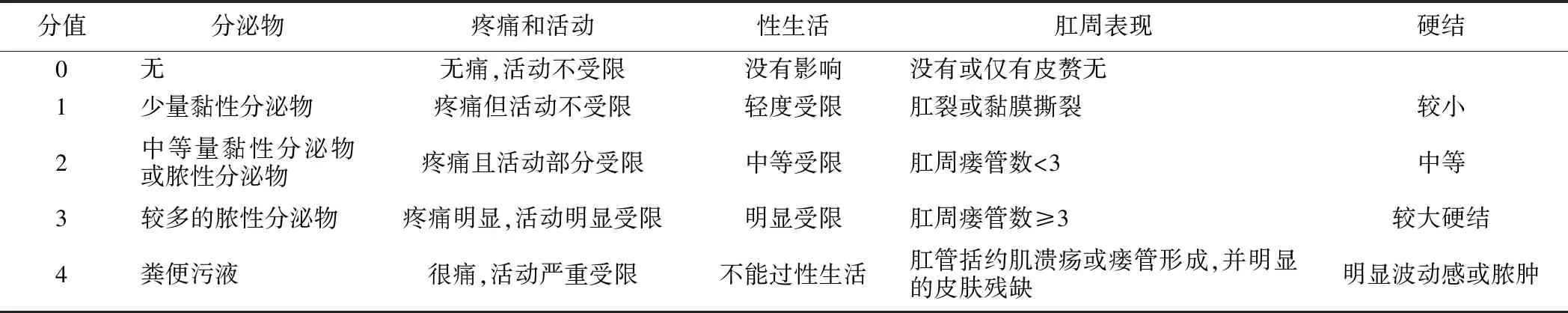
表2 肛周疾病活动指数(PDAI)评分表
国外有临床研究采用瘘管引流评估标准(nstula drainage assessment)进行pfCD疗效的判定,即如果至少连续2次随访,指压后一半或以上数目的瘘管无液体外流则为治疗有效;如果至少连续2次随访时,指压后瘘管无液体外流则为瘘管愈合[15]。
三、pfCD的治疗
1.治疗目标
pfCD需要多学科综合治疗,其治疗目标是缓解症状、促进瘘管愈合、保护肛门直肠功能、改善患者生活质量以及降低直肠切除率。
2.手术时机
无症状的pfCD无需治疗。症状较轻(PDAI≤4)、不影响肛管直肠功能的pfCD,只需内科药物治疗同时辅以对症处理(如中药坐浴等)。症状明显(PDAI≥4)时,首选内科药物治疗,包括抗生素(环丙沙星、甲硝唑),免疫抑制剂(硫唑嘌呤、6-巯基嘌呤),抗肿瘤坏死 因子(tumor necrosis factor,TNF)ɑ单克隆抗体(英夫利昔单抗、阿达木单抗、赛妥珠单抗),内科治疗不能达到治理目标时则需要外科手术干预。
pfCD手术时机的选择异常关键。在CD活动期伴营养不良或激素依赖时,实施确定性手术会导致手术失败,甚至造成肛门失禁、永久性造口等严重后果[16]。此时,除非明确存在直肠肛周脓肿需要进行引流从而缓解急性症状者,否则手术应限制[7]。在CD缓解期炎症得到控制时,方可依据患者瘘管的分布情况选择相应的确定性外科手术。无论是活动期还是缓解期手术均应遵循“损伤最小化”的原则,最大限度地保护肛门功能[5]。
3、手术方法
挂线引流术是pfCD最常用的手术治疗方式。pfCD在脓肿形成时应尽早引流,切口应在脓肿波动最明显处或破溃外口周围切开,切口方向宜选择放射状,切口大小应利于引流且减少损伤。对于范围较大的脓肿,可选择多个放射方向切口,予以多处对口挂线引流。坐骨直肠间隙脓肿等深部脓肿的引流应选择置管,双管或多管引流效果优于单管引流。探查时若发现内口,可予挂浮线引流。复杂性肛瘘也可以采用挂线引流,术前应充分评估瘘管的开口及分布情况,选择合适的切口,鼓励“对口引流挂线”,尽可能彻底的搔刮或切除括约肌外侧间隙瘘管或脓腔的感性肉芽组织,引流挂线应沿自然通道经内口穿出,避免暴力探查。
引流性挂线可以维持瘘管开放状态,有利于预防肛周脓肿的复发,是合并直肠炎的pfCD治疗的首选。但是,长期挂线引流会导致瘘管局部瘢痕化,使得瘘管迁延不愈。撤除挂线的理想时间目前尚无定论,故一般推荐挂线应至少维持到IFX诱导缓解疗程(第6周)结束后,当满足以下条件时[5],可考虑拆线:(1)挂线引流和生物制剂诱导治疗后克罗恩病疾病活动指数 (Crohn’s disease activitv index,CDAI)显著下降;(2)局部瘘管周围红肿明显消退;(3)瘘管管径明显缩小,冲洗有阻力;(4)按压瘘管外口无明显脓性分泌物;(5)手术前后影像学检查显示炎性病灶明显缩小。
在CD缓解期,肠道炎症得到明显控制的情况下,可根据瘘管情况进行pfCD的确定性手术。pfCD的确定性手术实施前,应满足以下条件[5]:(1)CDAI 指数正常;(2)内镜检查溃疡愈合;(3)肛瘘外口无明显分泌物,无新发脓肿或瘘管;(4)挂线和药物治疗前后MRI显示炎性病灶明显缩小,无新发或复发脓肿形成。
对于低位的简单型肛瘘可选择瘘管切开术,不仅愈合率较高而且能有效预防复发[17],但因其对肛门括约肌损伤相对较大,在女性前侧瘘管应禁止。
括约肌间瘘管结扎术(LIFT)适用于低位肛瘘,对于低位的复杂型肛瘘和女性前侧的简单型肛瘘同样适用,其并发症少且轻微,能较好的保护肛门功能[18]。
直肠瓣推移(RAF)作为一种安全性较高的保留肛门术式,可用于治疗复杂性肛瘘,可以避免广泛或难以愈合的伤口,成功率约为50%[19]。与 LIFT 相比,RAF 损伤括约肌功能,故失禁率更高,缺少医学临床实验研究和长期随访数据,远期疗效尚存争议。
直肠切除术加永久性造口是对严重而难治的pfCD的最后治疗手段。当直肠内病变严重损毁肛门功能,最终导致肛门失禁或肛门狭窄时,在药物治疗和局部处理失败后,应及时行直肠切除术或结直肠切除术、永久性结肠造口或小肠造口。
间充质干细胞是治疗CD肛瘘的新兴疗法,将提取的间充质干细胞注射入瘘管内填充,促进瘘管愈合。2003年首次报道用于肛瘘治疗,2016年相关研究及报道达到高峰。有研究报道,间充质干细胞疗法可通过显著减少肿瘤坏死因子、白细胞介素-1β等促炎细胞因子的分泌而抑制炎症反应[20]。但间充质干细胞用于CD肛瘘的长期疗效、安全性、 价格、临床应用规范等均需更多的研究。
总而言之,外科治疗是pfCD多学科综合治疗的重要部分。在治疗的整个过程中,有效控制肠道炎症是pfCD治愈的关键。在活动期予以早期挂线引流,减轻局部炎症,预防脓肿复发;到缓解期再行确定性手术,促进瘘管闭合,从而尽可能保护肛门直肠功能、避免肛门失禁或永久性造口等严重后果的发生,改善患者生活质量。
