金贝口服液抗SARS-CoV-2 的作用机制研究
2023-07-13孝云杨勇山东中医药大学山东济南250355山东宏济堂制药集团股份有限公司山东济南25003山东肺康中医药科技有限责任公司山东济南25000中医药经典理论教育部重点实验室山东济南250355中医药基础研究山东省重点实验室山东济南250355山东省中医药抗病毒工程研究中心山东济南250355
刘 衍 梁,张 爱 均,王 含 雪,叶 冬 雪,4,5,6,孟 兆 青,田 景 振,,陶 凯,张 良 棕,容 蓉,4,刘 孝云,4,5,6,杨勇,4,5,6(.山东中医药大学,山东 济南 250355;2.山东宏济堂制药集团股份有限公司,山东 济南 25003;3. 山东肺康中医药科技有限责任公司,山东 济南 25000;4. 中医药经典理论教育部重点实验室,山东 济南 250355;5. 中医药基础研究山东省重点实验室,山东 济南 250355;6. 山东省中医药抗病毒工程研究中心,山东 济南 250355)
自2019 年12 月以来,由新型冠状病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)引起的新型冠状病毒感染(coronavirus disease 2019,COVID-19)疫情在全球范围内蔓延,抗击新冠仍是一场持久战,且目前大部分抗SARS-CoV-2的药物仍处于研发阶段。3C 样蛋白酶(3C-like protease, 3CLpro)和 木 瓜 样 蛋 白 酶(papain-like protease,PLP)在SARS-CoV-2 的复制过程中发挥着重要作用[1-2],是抗SARS-CoV-2 药物研发的重要靶点。
中医药全程参与我国此次COVID-19 的防治工作,并取得显著效果,在此次疫情中彰显了中医药的特色与优势,中药的疗效和作用机制值得深入研究。金贝口服液是在国家名老中医陶凯先生的临床经验方的基础上研制而成,在2003 年的SARS 流行期间已应用于临床患者的救治。该制剂由黄芪、党参、北沙参等十二味中药组成,具有益气养阴、祛瘀化痰等作用。目前已有临床数据[3]证明,在COVID-19 常规治疗的基础上,加服金贝口服液,较仅使用常规治疗可缩短患者核酸转阴时间,缩短乏力、咳嗽症状消失时间,缩短COVID-19 患者治疗天数。这表明了金贝口服液治疗COVID-19 的有效性,但其具体作用机制仍不明。
本研究拟将开展金贝口服液体外抗SARS-CoV-2的活性评价,以及对3CLpro 和PLP 酶活的抑制作用研究,结合分子对接预测发挥抑制3CLpro 和PLP 的潜在有效成分,以助于阐明金贝口服液治疗COVID-19的作用机制,为其在临床科学合理地干预COVID-19提供实验依据和参考。
1 材料
1.1 细胞株及病毒株 Vero 细胞和SARS-CoV-2,均由中国人民解放军军事医学科学院微生物流行病研究所保存。本研究中体外抗SARS-CoV-2 实验部分由中国人民解放军军事医学科学院微生物流行病研究所完成。
1.2 药物及主要试剂 金贝口服液,山东宏济堂制药集团股份有限公司,批号:2002001;3CLpro 荧光底物Dabcyl-KTSAVLQSGFRKME-Edans、PLP 荧 光 底物Z-Arg-Leu-Arg-Gly-Gly-AMC,南京肽业生物科技有限公司,批号分别为:njp22208、njp22182;胎牛血清,上海逍鹏生物科技有限公司,批号:2244289;DMEM 高糖培养液、胰蛋白酶,美国Gibco 公司,批号分别为:C11995500CP、2445464;磷酸盐缓冲液(PBS),北京索莱宝科技有限公司,批号:G4202;CCK-8 试剂盒,美国MedChemExpress公司,批号:HY-K0301;绿原酸、连翘酯苷A、黄芩苷、丹酚酸B、汉黄芩苷、汉黄芩素,中国食品药品检定研究院,批号分别为:110753-201716、111810-201707、 110715-201821、 111562-201716、112002-201702、111514-201605;新绿原酸、隐绿原酸、异绿原酸B、异绿原酸C、原儿茶醛,成都普菲德生物技术有限公司,批号分别为:17062003、17061401、17121201、18070401、17060708;甘 草酸,江苏永健医药科技有限公司,批号:102574;乙腈、甲醇,美国Fisher 公司,批号分别为:A9984、205308;其他试剂均为国产分析纯试剂。
1.3 仪器 AKTA prime Plus 蛋白纯化仪,美国Cytiva 公司;SynergyNeo2 多功能酶标仪,美国BioTek 公司;HFsafe-1200LC 生物安全柜,力康生物医疗科技控股有限公司;XS105 十万分之一天平,瑞士梅特勒-托利多公司;Agilent 1290 超高效液相色谱仪,美国Agilent 公司。
2 方法

根据金贝口服液在不同浓度下的细胞存活率,并采用GraphPad Prism 8.0 软件计算金贝口服液的半数毒性浓度CC50。
2.2 金贝口服液体外抗SARS-CoV-2 实验 在96 孔板上接种Vero 细胞(1×104个/孔),置于37 ℃、5%CO2细胞培养箱中培养24 h,弃去培养液。每孔加入100 μL 浓度为10 μL·mL-1的金贝口服液,同时设立空白对照组(无病毒与药物)和阴性对照组(无药物);作用1 h 后每孔再加入100 TCID50 SARS-CoV-2,继续作用1 h;弃去96 孔培养板中的细胞培养液。每孔加入100 μL 含金贝口服液(浓度为10 μL·mL-1)的2% DMEM,于37 ℃、5% CO2细胞培养箱中孵育5 d,光学显微镜下观察并记录细胞病变效应(cytopathic effect,CPE),药物孔及对照孔均为3 个复孔。
用蚀斑减数实验进一步验证金贝口服液抗SARS-CoV-2 的效果。具体实验步骤如下:在24 孔板上接种Vero 细胞(2×105个/孔),置于37 ℃、5%CO2细胞培养箱中培养16 h。当细胞融合度约90%时,弃去培养液。不同浓度的金贝口服液(10、5、3.3、2.5 μL·mL-1)与SARS-CoV-2 一起加入细胞中,同时设置阴性对照组(无药物只感染SARS-CoV-2)。将板在37 °C、5% CO2细胞培养箱中孵育1 h,每20 min 摇晃培养板1 次。随后加入2% DMEM 配制的1%低熔点琼脂糖。于37 °C、5% CO2细胞培养箱中培养72 h 后,用4%甲醛固定细胞并用0.2%结晶紫染色。最后用去离子水冲洗培养板,记录各组的蚀斑数量。根据不同药物浓度下蚀斑减少的数量计算药物的抑制率。

2.3 金贝口服液对3CLpro 活性的抑制实验 利用本实验前期建立的基于3CLpro 活性的高通量药物筛选体系,测定不同浓度的金贝口服液对3CLpro 活性的抑制效果。用DMSO 将金贝口服液从10 μL·mL-1开始进行2 倍稀释,共6 个梯度(10,5,2.5,1.25,0.63,0.31 μL·mL-1),计算其在不同浓度下的抑制率,并采用GraphPad Prism 8.0 软件计算金贝口服液对3CLpro 的半数有效抑制浓度IC50。
2.4 金贝口服液对PLP 活性的抑制实验 利用本实验前期建立的基于PLP 活性的高通量药物筛选体系,测定金贝口服液对PLP 活性的抑制效果。将其从50 μL·mL-1开始进行2 倍稀释,共6 个梯度(50,25,12.5,6.25,3.13,1.56 μL·mL-1),计算其在不同浓度下的抑制率,并采用GraphPad Prism 8.0 软件计算金贝口服液对PLP 的半数有效抑制浓度IC50。
2.5 金贝口服液成分鉴定
2.5.1 色谱条件设置 色谱柱:Agilent InfinityLab Poroshell 120 SB-C18(2.1 mm×150 mm,2.7 μm);柱温:25 ℃;流速:0.2 mL·min-1;检测波长:254 nm;进样量:1 μL;流动相:乙腈-0.2%磷酸水溶液,洗脱条件:0~2.7 min,4% 乙腈;2.7~6.6 min,4%~7% 乙腈;6.6~20.6 min,7%~14% 乙腈;20.6~30.7 min,14%~20% 乙腈;30.7~43.9 min,20%~30% 乙腈;43.9~54.3 min,30%~50% 乙腈;54.3~64 min,50%~70%乙腈。
2.5.2 对照品溶液、供试品溶液、单味药材对照溶液及缺味阴性对照溶液的制备 精密称取各对照品适量,加甲醇溶解并稀释至1 mL,制成混合对照品溶液。其中,新绿原酸、原儿茶醛、绿原酸、隐绿原酸、连翘酯苷A、异绿原酸B、异绿原酸C、黄芩苷、丹酚酸B、汉黄芩苷、甘草酸和汉黄芩素的浓度分别为45.16、10.42、63.51、22.20、29.35、17.58、28.60、82.79、23.95、37.92、34.97、10.50 μg·mL-1。
分别精密量取10 个批次的金贝口服液(批号:1708001、1708002、1708003、1906001、1906002、1906003、2001001、2001002、2001003 和2002001)各20 mL,置具塞锥形瓶中,精密加入50% 色谱甲醇60 mL,称定质量,超声(300 W,40 kHz)处理30 min,放至室温,补质量,摇匀,滤过,取续滤液,过0.22 μm 微孔滤膜,即得供试品溶液。
按照金贝口服液生产工艺规程分别制备黄芪、北沙参、丹参等12 种单味药材制剂样品,并按照供试品溶液的制备方法,分别制成单味药材对照溶液。
按照金贝口服液生产工艺规程分别制备黄芪、北沙参、丹参、金银花、黄芩、川贝母、清半夏、甘草、川芎、当归、川芎-当归、党参、甘草、连翘等13 种缺味制剂样品,并按照供试品溶液的制备方法,分别制成缺味阴性对照溶液。
2.5.3 方法学考察(完整性、稳定性、精密度、重复性) 取金贝口服液(批号:2002001)供试品溶液,按照“2.5.1”中色谱条件进样,64 min 后,将流动相(乙腈-0.2% 磷酸水溶液)比例从70%∶30% 逐渐升至95%∶5%,并持续运行120 min,得到完整性数据。同一供试品溶液分别在0、4、8、12、24 h 测定,以22 号峰为参照峰(S 峰),计算各个化合物含量的相对标准差(relative standard deviation,RSD)值,得到样品稳定性数据。在24 h 内对同一供试品溶液连续进样6 次,以22 号峰为S 峰,分别计算各个化合物的RSD 值,得到精密度数据;平行制备6 份样品溶液并分别测定,以22 号峰为S 峰,计算各个化合物含量的RSD 值,得到重复性数据。
2.5.4 金贝口服液成分的定性分析 取10 批金贝口服液供试品溶液进行测定。将10 批金贝口服液的指纹图谱以AIA 格式导入国家药典委员会《中药色谱指纹图谱相似度评价系统(2012 年版)》软件,以金贝口服液(批号:2002001)指纹图谱为参照图谱,时间窗宽度设为0.3 min,以此确定10 批金贝口服液的共有峰。
分别精密吸取金贝口服液供试品溶液(批号:2002001)、混合对照品溶液、空白溶液(甲醇),按照“2.5.1”项中色谱条件进样,通过色谱峰保留时间和紫外光谱信息对比确认特征峰。
2.5.5 金贝口服液成分归属分析 为确定各个共有峰的归属,分别取金银花、丹参、连翘等单味药材对照溶液,按照“2.5.1”项中色谱条件进样测定。通过保留时间和紫外光谱信息对比,对共有峰进行归属分析。
为进一步验证共有峰归属结果,分别取金银花、丹参、连翘等缺味阴性对照溶液,按照“2.5.1”项中色谱条件进样测定。
2.6 金贝口服液成分的分子对接 对金贝口服液中鉴定出的12 个成分进行分子对接。从PubChem 数据库(https://pubchem.ncbi.nlm.nih.gov/)下载12 个化学成分的二维结构,并以“SDF”格式保存。使用Chem 3D 将“SDF”格式转换为mol2 结构作为小分子配体。从PDB 数据库(https://www.rcsb.org/)中分别检索出靶点SARS-CoV-2 3CLpro(PDB ID:6LZE)和PLP(PDB ID:7CJM)的蛋白结构作为模板,并以“PDB”格式保存为蛋白质受体。使用PyMOL 软件(2.3.6 版)去除水分子,并从核心目标蛋白中分离出原始配体。处理后的蛋白质目标被导入AutoDock 软件(4.2.0 版)进行氢化、计算总电荷和设置原子类型。配体和蛋白质受体以PDBQT 格式记录。用AutoDock-Vina 软件(1.1.2 版)进行分子对接,以评估受体-配体复合物的亲和力,并给出综合评分。
3 结果
3.1 金贝口服液体外抗SARS-CoV-2 效果 为了在体外研究金贝口服液抗SARS-CoV-2 的效果,首先测定不同浓度的金贝口服液对Vero 细胞的毒性。在受试期内,阴性对照组及药物组细胞均为正常状态。金贝口服液最高终浓度为10 μL·mL-1时,未观察到明显的细胞毒性。因此,金贝口服液对药物的最大无毒浓度大于10 μL·mL-1(图1-A)。
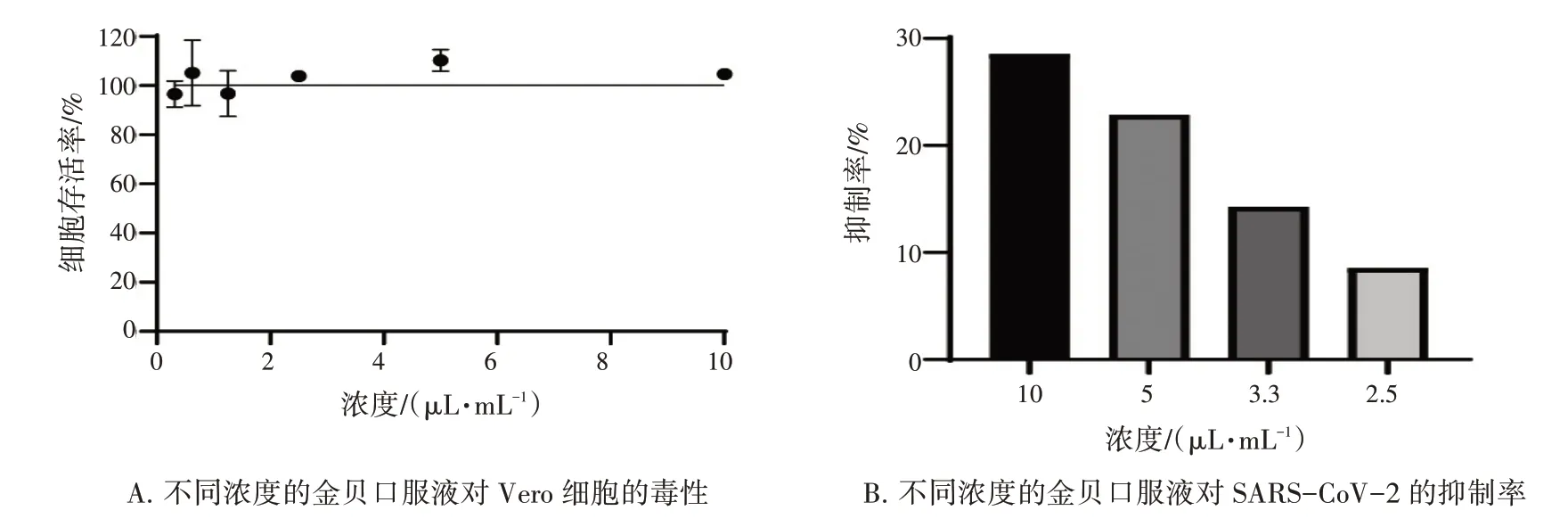
图1 金贝口服液对SARS-CoV-2 的抑制效果Figure 1 Inhibitory effect for Jinbei Oral Liquid on SARS-CoV-2
选择无毒浓度的金贝口服液(10 μL·mL-1)进行其抗SARS-CoV-2 效果的研究。首先用观察CPE 的方法,研究金贝口服液抑制SARS-CoV-2 的效果。实验结果表明金贝口服液在终浓度为10 μL·mL-1时,可以抑制约50% 的由SARS-CoV-2 导致的细胞病变(表1),说明金贝口服液对SARS-CoV-2 有一定的抑制效果。

表1 终浓度10 μL·mL-1 的金贝口服液对SARS-CoV-2 致细胞病变的抑制效果Table 1 Inhibitory effect of 10 μL·mL-1 of Jinbei Oral Liquid on cytopathy induced by SARS-CoV-2
进一步用蚀斑减数实验验证金贝口服液抑制SARS-CoV-2 的效果。不同浓度的金贝口服液与SARS-CoV-2 一起孵育感染细胞,3 d 后,记录蚀斑数量。根据药物组减少的蚀斑数量计算金贝口服液的抑制率。实验结果表明当金贝口服液终浓度为10、5、3.3、2.5 μL·mL-1时,其对SARS-CoV-2 的抑制率分别为28.57%、22.86%、14.29%、8.57%(图1-B),说明金贝口服液对SARS-CoV-2 具有一定的抑制效果,且呈剂量依赖性。
3.2 金贝口服液对3CLpro 活性的抑制效果 3CLpro为SARS-CoV-2 复制过程中的关键蛋白酶,为了进一步研究金贝口服液抗SARS-CoV-2 的作用机制,首先选择3CLpro 作为药物靶点,利用本实验室前期建立的基于3CLpro 活性的高通量药物筛选体系,评价不同浓度的金贝口服液对3CLpro 活性的抑制效果。实验结果表明,当金贝口服液终浓度为10、5、2.5、1.25、0.625、0.313 μL·mL-1时,1 h 内荧光强度的增加值大约分别为3 700、8 500、16 000、21 000、24 000、27 000(图2-A)。经计算,不同浓度的金贝口服液对3CLpro 的抑制率分别为(87.105±0.685)%、(70.040±0.686)% 、(44.587±1.069)% 、(24.834±0.908)%、(14.233±0.519)%和(4.029±0.507)%,说明金贝口服液对3CLpro 活性有良好的抑制作用,且呈现药物剂量依赖的关系。通过拟合计算,得出金贝口 服 液 对3CLpro 的IC50为(2.757±0.082)μL·mL-1(图2-B)。
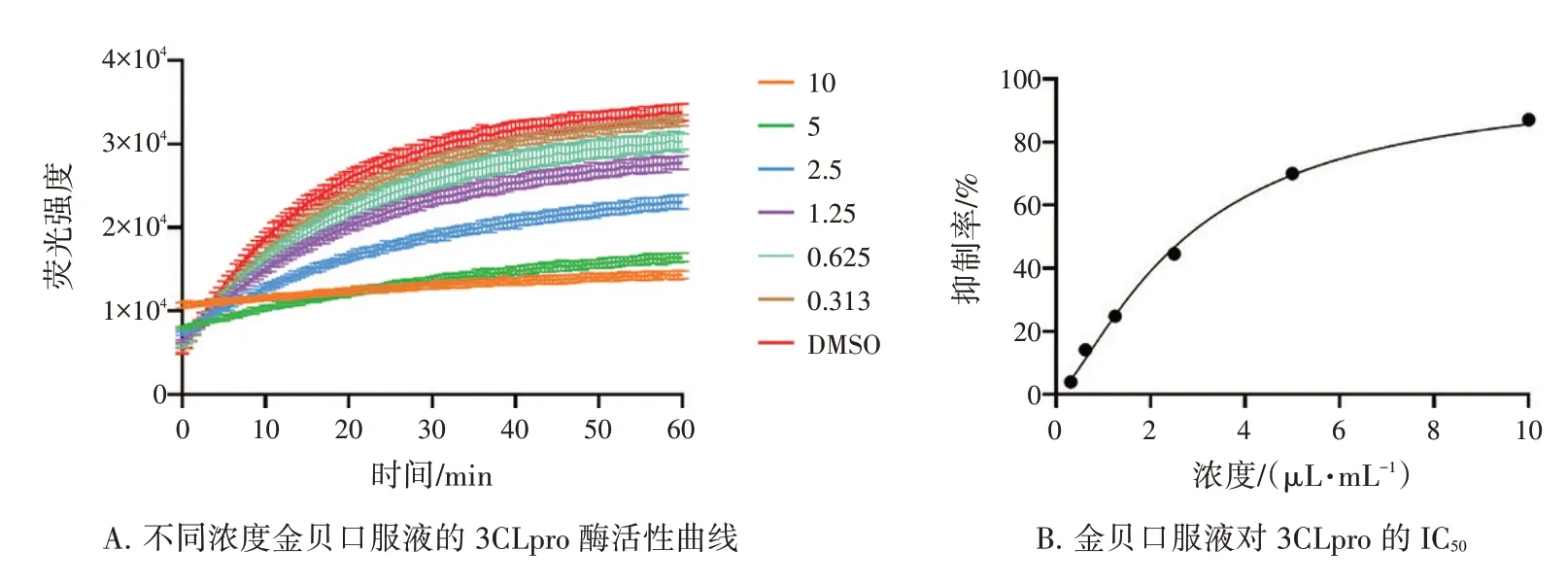
图2 金贝口服液对3CLpro 的抑制效果Figure 2 Inhibitory effect for Jinbei Oral Liquid on 3CLpro
3.3 金贝口服液对PLP 活性的抑制效果 为了进一步研究金贝口服液抗SARS-CoV-2 的作用机制,选择在SARS-CoV-2 复制过程中的另一关键蛋白酶PLP 作为药物靶点,利用本实验室前期建立的基于PLP 活性的高通量药物筛选体系,评价不同浓度的金贝口服液对PLP 活性的抑制效果。实验结果表明,当金贝口服液终浓度为50、25、12.5、6.25、3.125、1.563 μL·mL-1时,1 h 内荧光强度的增加值大约分别为-1 300、700、5 000、9 000、15 000、18 000、26 000(图3-A)。经计算不同浓度的金贝口服液对PLP 的抑制率分别为(105.058±1.101)%、(97.483±0.568)% 、(80.182±0.885)% 、(65.291±4.811)% 、(43.820±0.148)%、(30.776±0.533)%,说明金贝口服液对PLP 活性有良好的抑制作用,且呈现药物剂量依赖的关系(图3-B)。通过拟合计算,得出金贝口服液对PLP 的IC50为(3.527±0.188)μL·mL-1。
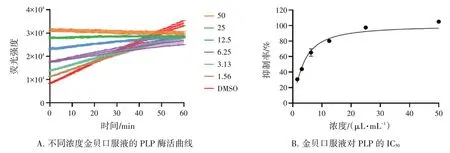
图3 金贝口服液对木瓜样蛋白酶(PLP)的抑制效果Figure 3 Inhibitory effect for Jinbei Oral Liquid on PLP
3.4 金贝口服液的成分分析 为了进一步阐明金贝口服液抗SARS-CoV-2 的作用机制,采用超高效液相色谱(ultraperformance liquid chromatography,UPLC)对其进行化学成分分析,以确定其化学组成。
首先对UPLC 的色谱条件进行方法学考察,包括完整性、稳定性、精密度、重复性试验。完整性试验结果显示,64 min 后基本无其他色谱峰出现,说明在64 min 内,本方法已将供试品的信息最大化体现。稳定性试验结果显示,各共有峰相对保留时间的RSD 均不高于0.35%;相对峰面积的RSD 均不高于1.43%,表明24 h 内供试品溶液各成分较稳定。精密度试验显示,各共有峰相对保留时间的RSD 均不高于0.12%,相对峰面积的RSD 均不高于1.29%,表明仪器精密度良好。重复性试验显示,各共有峰相对保留时间的RSD 均不高于0.08%,相对峰面积的RSD 均小于0.54%,表明本方法重复性良好。以上结果均符合指纹图谱分析要求,该色谱条件可用。
随后,对10 批金贝口服液供试品溶液进行测定,确定其共有峰。实验结果表明有28 个共有峰(图4-A),并生成对照指纹图谱共有模式(图4-B)。在各色谱峰中,22 号峰的峰形好、峰面积较大、分离度良好,故选作S 峰。
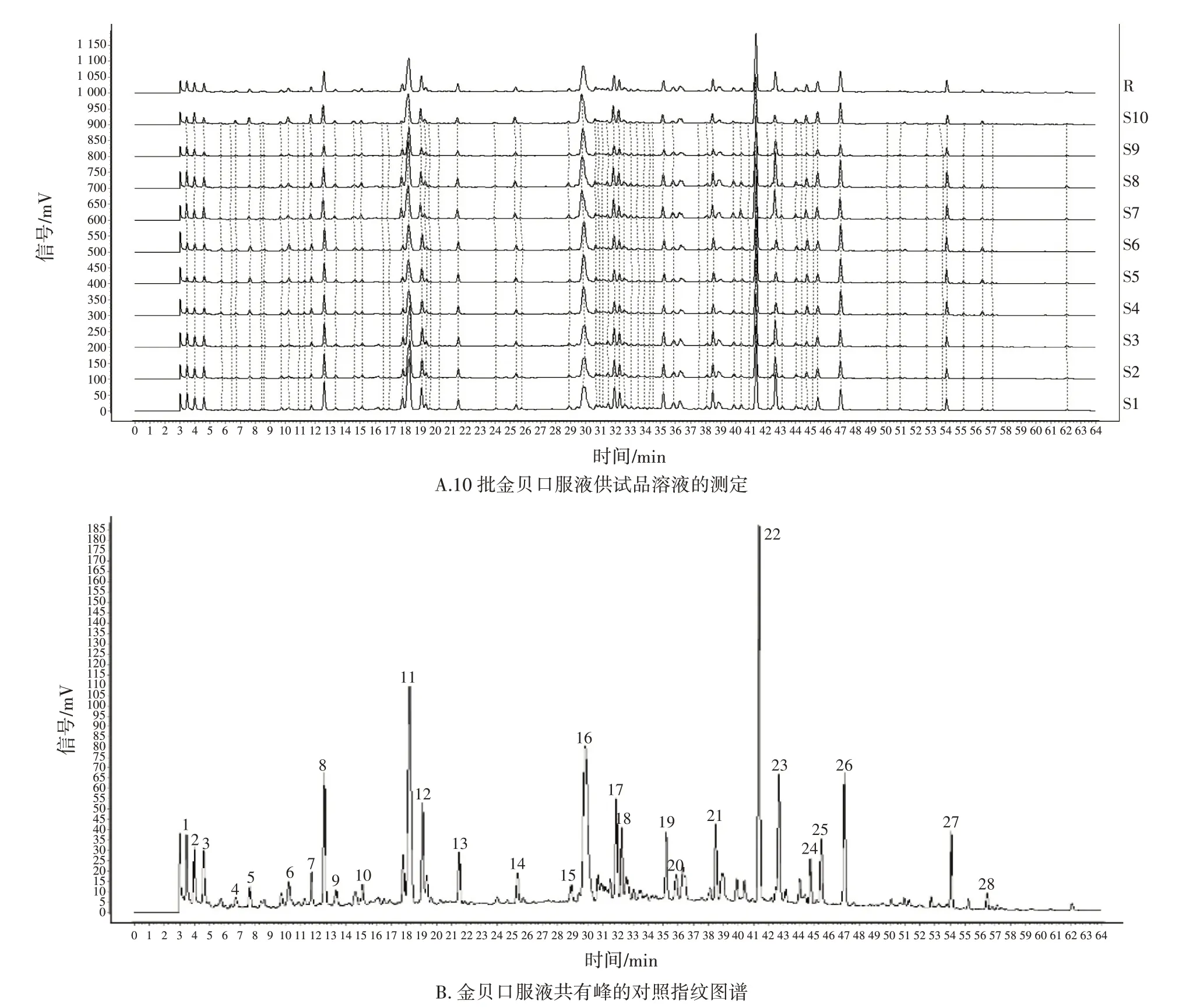
图4 不同批次金贝口服液共有峰的确认Figure 4 Confirmation of the common peaks in different batches of Jinbei Oral Liquid
随后继续对共有峰进行定性分析,将供试品溶液、混合对照品溶液、空白溶液(甲醇)的色谱峰保留时间和紫外光谱信息进行对比,最终鉴定出12 个成分,8 号峰为新绿原酸、9 号峰为原儿茶醛、11 号峰为绿原酸、12 号峰为隐绿原酸、18 号峰为连翘酯苷A、19 号峰为异绿原酸B、21 号峰为异绿原酸C、22 号峰为黄芩苷、23 号峰为丹酚酸B、26 号峰为汉黄芩苷、27 号峰为甘草酸、28 号峰为汉黄芩素(图5)。
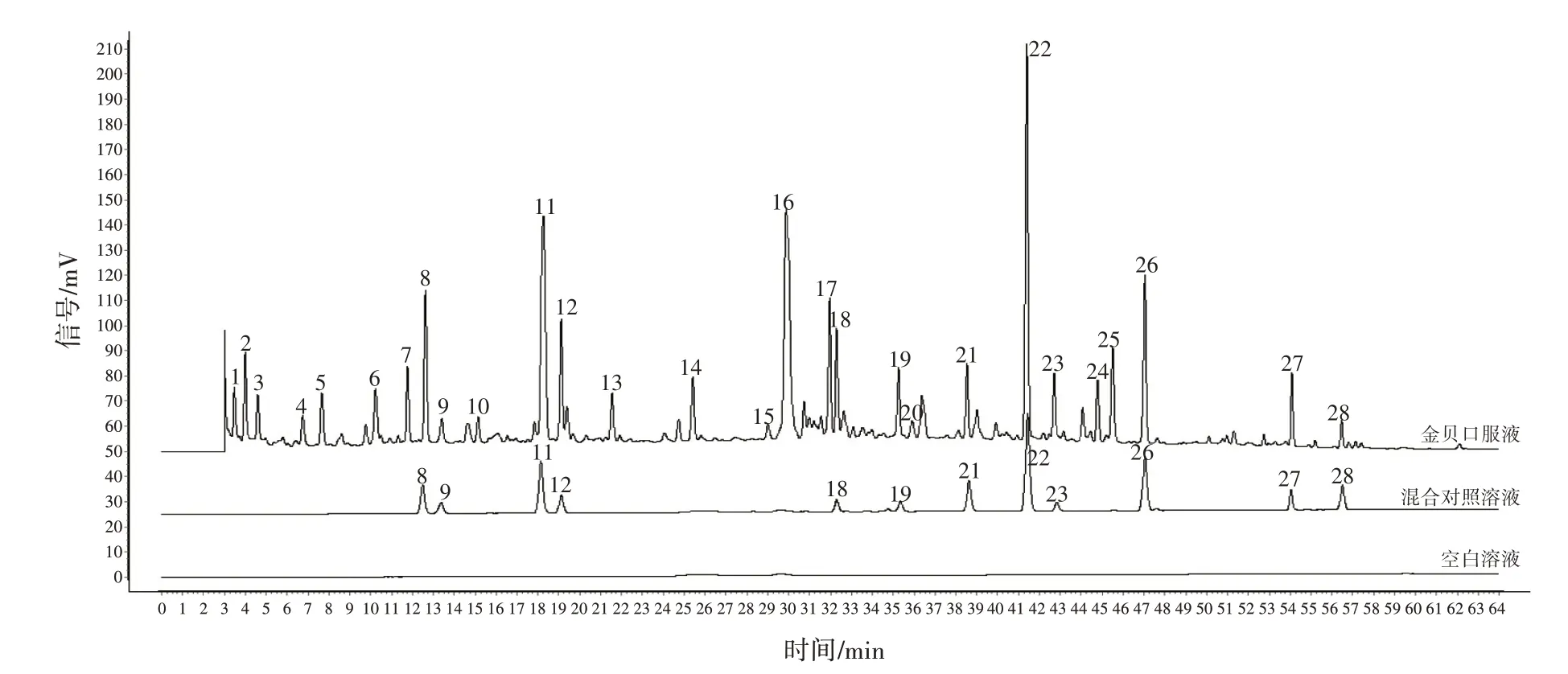
图5 金贝口服液共有峰的定性分析Figure 5 Qualitative analysis of the common peaks of Jinbei Oral Liquid
根据单味药材对照溶液,对鉴定出的12 个特征峰进行归属分析,结果发现:8、11 和12 号峰归属于金银花、川芎;9 号峰归属于丹参、金银花;18 号峰归属于连翘;19 和21 号峰归属于金银花;22、26和28 号峰归属于黄芩;23 号峰归属于丹参;27 号峰归性于甘草(图6-A)。为进一步验证此归属结果,对缺味阴性对照溶液进行测定,结果与上述研究结论一致(图6-B)。
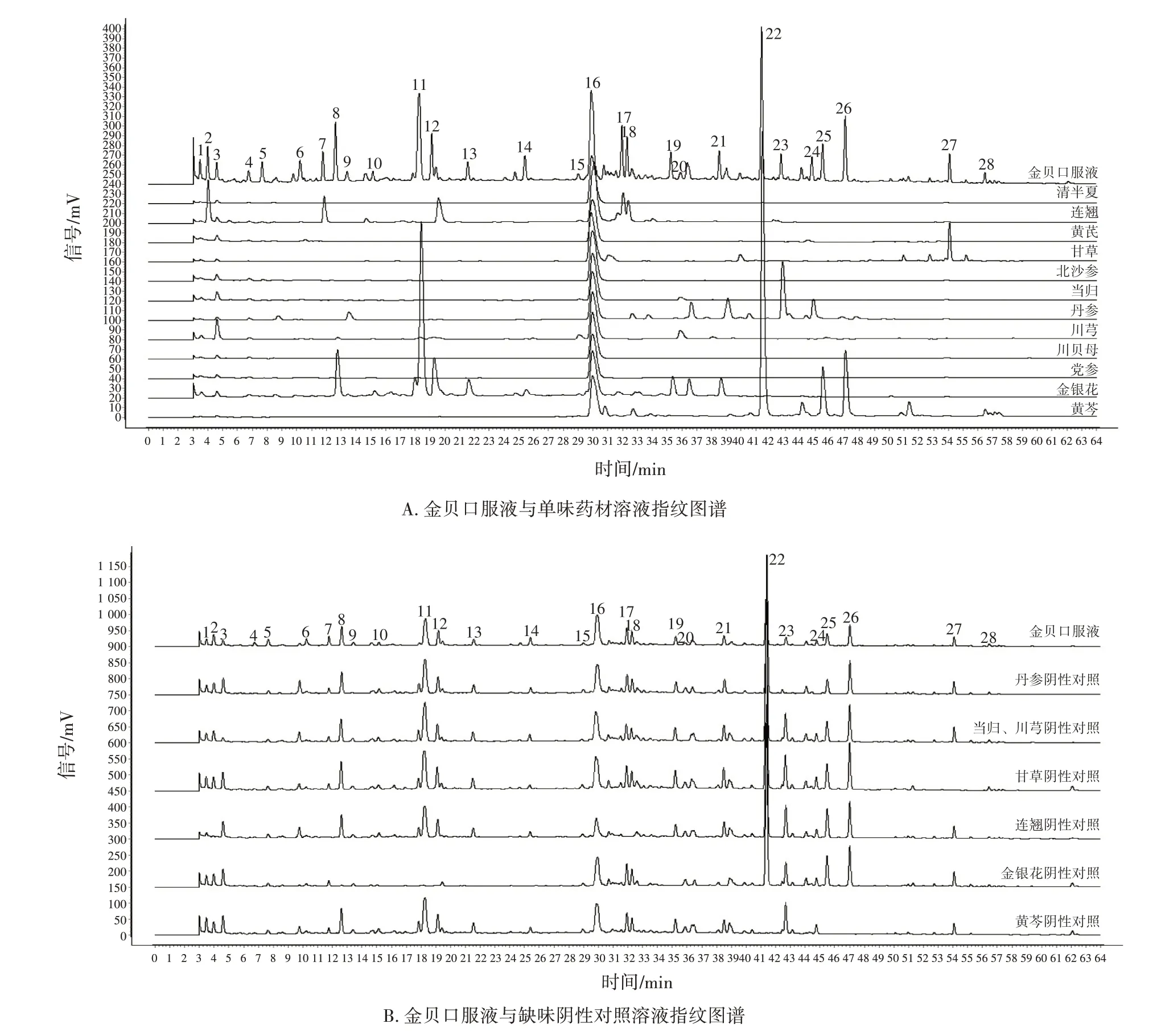
图6 金贝口服液共有峰的归属分析Figure 6 Attribution analysis of common peaks of Jinbei Oral Liquid
3.5 金贝口服液的12 种成分的分子对接 为进一步阐明金贝口服液抗SARS-CoV-2 的作用机制,对UPLC 指认的金贝口服液的12 种成分分别与3CLpro和PLP 进行分子对接。通常认为配体与蛋白受体结合形成稳定构象时的结合能越低,二者越契合,发生作用的可能性越大,故可以分子对接score 值为指标,评估关键活性化合物与3CLpro 和PLP 的结合能力。一般认为,结合能≤-5.0 kcal·mol-1表示两者可以结合,≤-7.0 kcal·mol-1表示两者有较好的结合能力[4]。分子对接结果表明连翘酯苷A、黄芩苷、丹酚酸B、汉黄芩苷、汉黄芩素、新绿原酸、隐绿原酸、异绿原酸B 与3CLpro 和PLP 均有较好的结合能力(表2),很有可能是金贝口服液抗SARS-CoV-2 的有效成分。
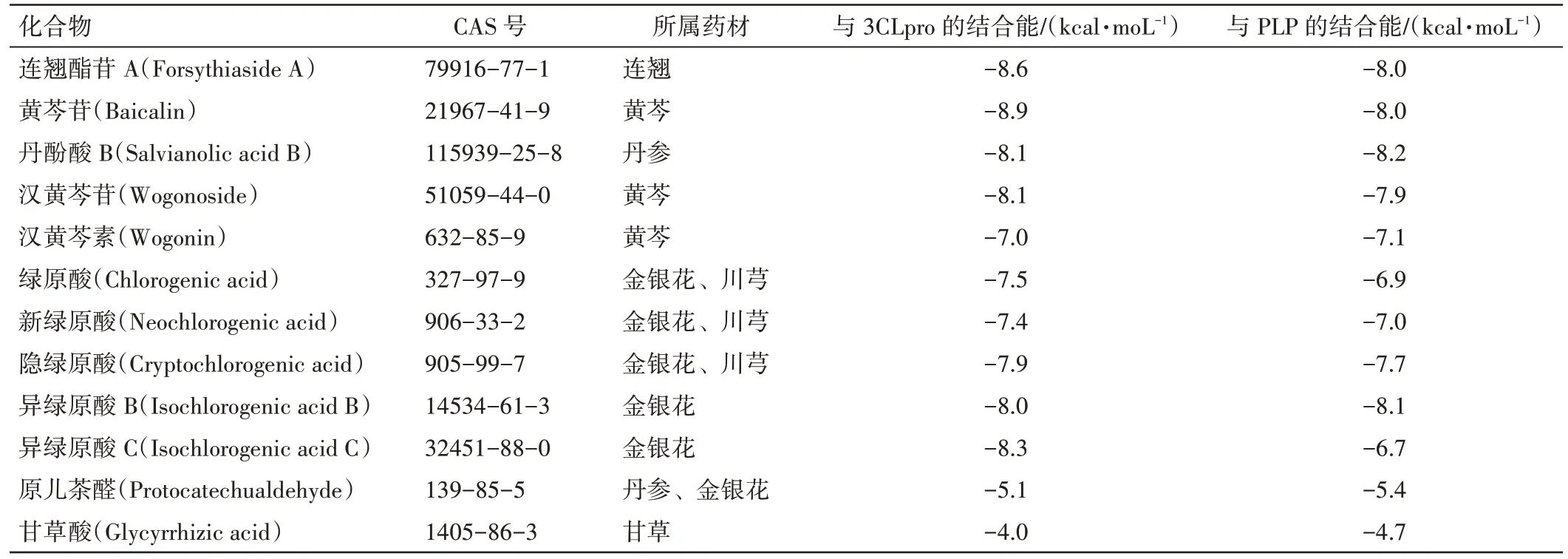
表2 金贝口服液中的12 种成分与SARS-CoV-2 3CLpro、PLP 的结合能Table 2 Binding energy of 12 components in Jinbei Oral Liquid with SARS-CoV-2 3CLpro and PLP
4 讨论
COVID-19 影响着人类生命健康,其病原体SARS-CoV-2 复制所必需的蛋白酶3CLpro 和PLP 是目前广谱抗冠状病毒药物研发的关键靶标。中医药在此次COVID-19 的防治中发挥了重要作用,已有研究[5-6]表明有较多中草药提取物及天然产物对SARS-CoV-2 3CLpro 和PLP 具有很好的抑制作用,这对于广谱抗冠状病毒候选药物的开发具有重要价值与意义。
金贝口服液是来源于临床经验方的中药口服液,最初主要用于治疗感冒咳嗽、气管炎和支气管炎等上呼吸道常见疾病。目前已有临床数据[3]证实金贝口服液能够有效治疗COVID-19,但其作用机制不明。本研究发现金贝口服液在体外能抑制SARS-CoV-2复制,并对SARS-CoV-2 的重要蛋白酶3CLpro 和PLP 具有较强的抑制作用。因此,我们合理推测金贝口服液可能通过抑制3CLpro 和PLP 活性,发挥其抗SARS-CoV-2 的作用。
随后,本研究采用UPLC 方法对金贝口服液的化学成分进行定性分析,共完成12 个成分的指认与归属分析。与传统的高效液相色谱比较,UPLC 具有更高的分离度、灵敏度、更大的信息量[7]。这12 个成分与3CLpro、PLP 的分子对接结果显示连翘酯苷A、黄芩苷、丹酚酸B、汉黄芩苷、汉黄芩素、新绿原酸、隐绿原酸、异绿原酸B 与3CLpro 和PLP 均有较好的结合能力,且这些化学成分口服生物利用度(OB)均大于30%,类药性(DL)均大于0.18。并且目前已有文献报道黄芩苷[8]、绿原酸、连翘酯苷A[9]可抑制3CLpro 活性,故我们合理推测这些成分能够直接作用于3CLpro 和PLP,阻止病毒增殖,从而使金贝口服液发挥抗SARS-CoV-2 的作用。此外,丹酚酸B 可以通过阻止病毒融合抑制SARS-CoV-2 感染靶细胞[10];甘草酸可以有效抑制SARS-CoV-2 S-RBD与ACE2 的相互作用[11],从而抑制病毒侵入细胞。这可能是金贝口服液能够抑制SARS-CoV-2 活性的原因之一。
一项关于新冠病者感染的临床中医证候文献计量学分析及证候规律总结的研究[12]显示,肺脾气虚、气阴两虚证是新冠病毒感染所致出现频数最多的证型,而金贝口服液还具有益气养阴的功效,这表明金贝口服液不仅可以直接抑制SARS-CoV-2 来发挥药效,还可作为对症治疗药物,具备作为COVID-19 临床用药的较大潜力。
