采用KOH 亚熔盐处理钛中矿富集钛资源研究
2022-11-05邹敏王琪琳江文世
邹敏,王琪琳,江文世
(西昌学院理学院,四川 西昌 615013)
0 引言
钛中矿是钒钛磁铁矿选矿尾矿经二次选矿后的产物,其TiO2含量在28%~36%,这部分产品因TiO2含量过低而不能直接作为钛白原料加以利用,一直以来是钒钛磁铁矿综合利用中重大难题和关键技术之一[1]。
目前针对钛中矿综合利用的相关研究较少,其中具有代表性的是吴恩辉等人的“盐酸浸出工艺”[2]和冯海亮等人的[3]“磁选-重选-浮选联合选矿工艺”。上述工艺虽然都能实现钛中矿中TiO2的进一步富集,但都一定程度上存在工艺流程复杂、设备种类较多、生产成本高以及环境污染大等问题,因此工业化受到限制。
亚熔盐是一种类似于熔盐,但含有少量水分的特殊熔体,其碱金属盐的浓度介于溶液和熔盐之间,具有反应活性高、沸点高、蒸气压低、性能可控等优点[4],是两性金属矿产资源分离提取的有效处理方式。中科院过程所等[5-8]单位已将亚熔盐体系应用于钒钛磁铁矿的综合利用中,实现了钛、铁等有价组分的高效分离。但目前尚未看到采用亚熔盐处理钛中矿的相关报道。
笔者采用KOH 亚熔盐和钛中矿为原料,研究了反应温度、反应时间、原料粒度以及亚熔盐浓度、碱矿比和搅拌速度等因素对钛中矿中TiO2富集情况的影响。
1 试验部分
1.1 试验原料
选用攀枝花恒誉工贸有限责任公司生产的钛中矿为试验原料,其化学成分如表1 所示。

表1 钛中矿的化学组成Table 1 Main chemical composition of the titanium middling ore %
此外,试验中还使用了氢氧化钾(分析纯)、硫酸(分析纯)、盐酸(分析纯)、焦硫酸钾(分析纯)和纯净水等原料。
1.2 试验原理
分析表1,可知氢氧化钾熔盐和处理钛中矿过程中发生的主要化学反应如下:
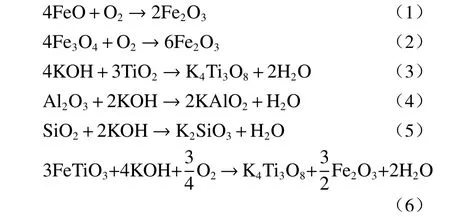
其中铝、硅等杂质元素生成可溶性产物在洗涤过程中可除去,钛、铁、钙、镁等组分可通过加酸水解等步骤予以分离,从而实现钛资源的富集。
1.3 试验设备与步骤
试验所使用的反应釜为自制,由于试验过程是在高温和强碱溶液下进行的,因此选择不锈钢烧杯为反应容器,电动搅拌器中的搅拌桨选择不锈钢搅拌桨。由于反应温度为200 ℃以上,为了防止反应过程中水分的散失对试验结果造成影响,在烧杯上盖上一块已按照相应尺寸打好孔的铁片,分别插入搅拌桨、测温棒和回流冷凝管,试验装置示意见图1。
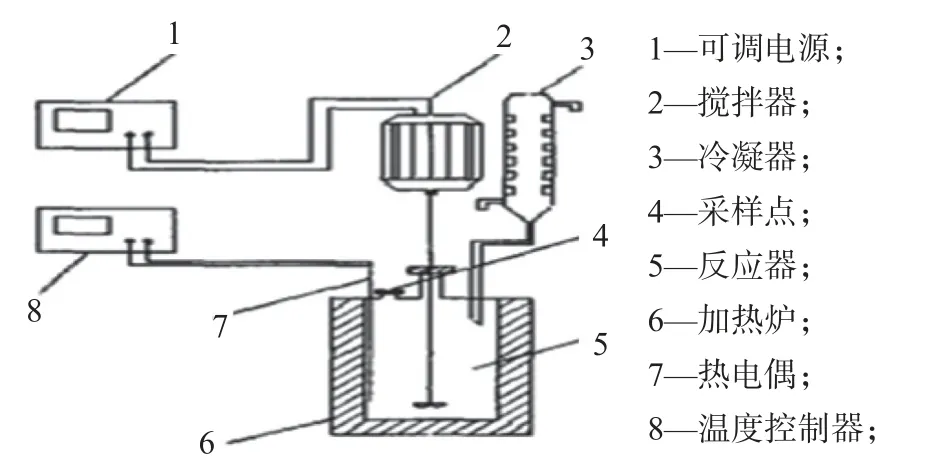
图1 试验装置示意Fig.1 Schematic diagram of experimental device
称取一定质量的KOH 固体于反应釜内,按所需浓度加入一定量的蒸馏水,将反应釜升温至反应温度,按一定碱/矿比加入钛中矿,开启电动搅拌器,反应一定的时间后关闭电源,待样品冷却后用5%左右的稀盐酸溶解、洗涤、过滤,用电感耦合等离子体原子吸收光谱(ICP-AES)分析滤液中的钛、铝、硅等元素。
1.4 分析测试方法
1)钛中矿钛分解率的计算
由于钛中矿在氢氧化钾亚熔盐介质中生成的产物钛酸钾K4Ti3O8不溶于水,因此采用稀盐酸与钛酸钾反应后生产可溶性的TiOCl2,通过测定TiOCl2水溶液中钛离子的含量来表征钛中矿中钛的分解率。钛中矿在KOH 亚熔盐中的分解率可按下式进行计算[9]:
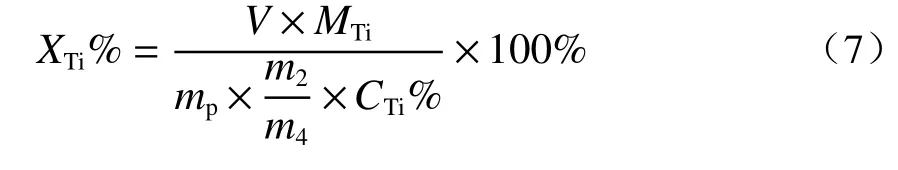
式中,XTi为钛中矿分解率,%;V为用来溶解亚熔盐反应产物的盐酸的体积,L;MTi为稀释后的滤液中Ti 离子的测量浓度,g/mL;m4为钛中矿的总质量,g;m2为反应所用原料的总质量,g;mp为盐酸溶解时称取的亚熔盐反应产物的质量,g;CTi为原料中Ti 的百分含量,%。
2)硅、铝转化率的计算
本研究采用焦硫酸钾法[10]对钛中矿进行熔样,采用电感耦合等离子体原子吸收光谱(ICP-AES)分析滤液中的钛、铝、硅等元素,从而获得钛中矿中各元素含量,进而计算转化率。
2 试验结果与讨论
2.1 反应温度对钛、铝、硅转化率的影响
反应温度是亚熔盐反应过程中的关键因素之一,温度过低会降低碳还原产物的分解率,温度过高一方面会增加能耗,另一方面会增加亚熔盐体系水分的散失,使得反应传质流动性变差,反而不利于反应的进行。固定搅拌速度400 r/min,碱矿质量比6∶1,碱浓度为80%,钛中矿粒度为70~80 μm,反应时间为180 min,考察了反应温度对钛中矿中钛、硅、铝等元素转化率的影响,结果如图2 所示。
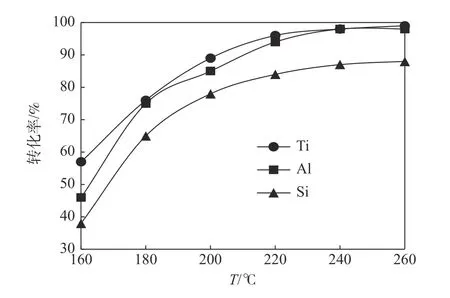
图2 反应温度对钛、铝、硅转化率的影响Fig.2 Effect of reaction temperature on conversion of Ti,Al and Si
从图2 可看出,钛中矿中各元素转化率随反应温度的升高而升高,当温度超过200 ℃后,钛中矿转化率增加缓慢,当温度240 ℃后,钛中矿中钛的转化率达99%,说明钛中矿中的钛基本转化完全,故本研究较佳反应温度为240 ℃。在此温度条件下,铝的转化率达97%,硅的转化率为87%。
2.2 反应时间对钛、铝、硅转化率的影响
固定搅拌速度400 r/min,碱矿质量比6∶1,碱浓度为80%,钛中矿粒度为70~80 μm,反应温度为240 ℃,考察了反应时间对钛中矿中钛、硅、铝等元素转化率的影响,结果如图3 所示。
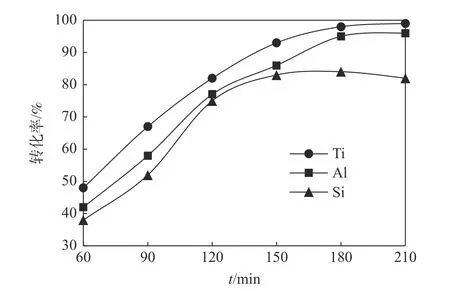
图3 反应时间对钛、铝、硅转化率的影响Fig.3 Effect of reaction time on conversion of Ti,Al and Si
从图3 可以看出,随着反应时间的延长,钛中矿中钛、铝、硅等元素的转化率均呈上升趋势。当反应时间超过150 min后,钛、铝的转化率升高速度减缓,并在180 min 左右接近最大值98%和95%。硅的转化率在150 min 之后逐渐呈下降趋势,其原因可能是由于反应初期硅与氢氧化钾反应生成可溶性的硅酸盐(SiO44-),但随着反应时间的延长,这种四面体结构的SiO44-数量增多,离子之间相互聚合生成不溶于水和稀酸的复杂硅酸盐,导致硅的转化率达到峰值后又随着时间的延长而降低[10],综合各种因素考虑,确定较佳的反应时间为180 min。
2.3 碱浓度对钛、铝、硅转化率的影响
固定搅拌速度400 r/min,碱矿质量比6∶1,钛中矿粒度为70~80 μm,反应温度为240 ℃,反应时间180 min,考察了碱浓度对钛中矿中钛、硅、铝等元素转化率的影响,结果如图4 所示。
从图4 可以看出,随着碱浓度的增加,钛、铝、硅三种元素的转化率都呈上升趋势。其中钛的转化率在碱浓度为80%左右接近最大值98%,在此条件下,Al、Si 的转化率分别为97%和86%。由于碱渣完全反应的理论质量比约为1∶1,本研究碱质量比6∶1,碱是过量的,为保证尽可能多的硅从钛中矿中溶出,故较佳的碱浓度为80%左右。
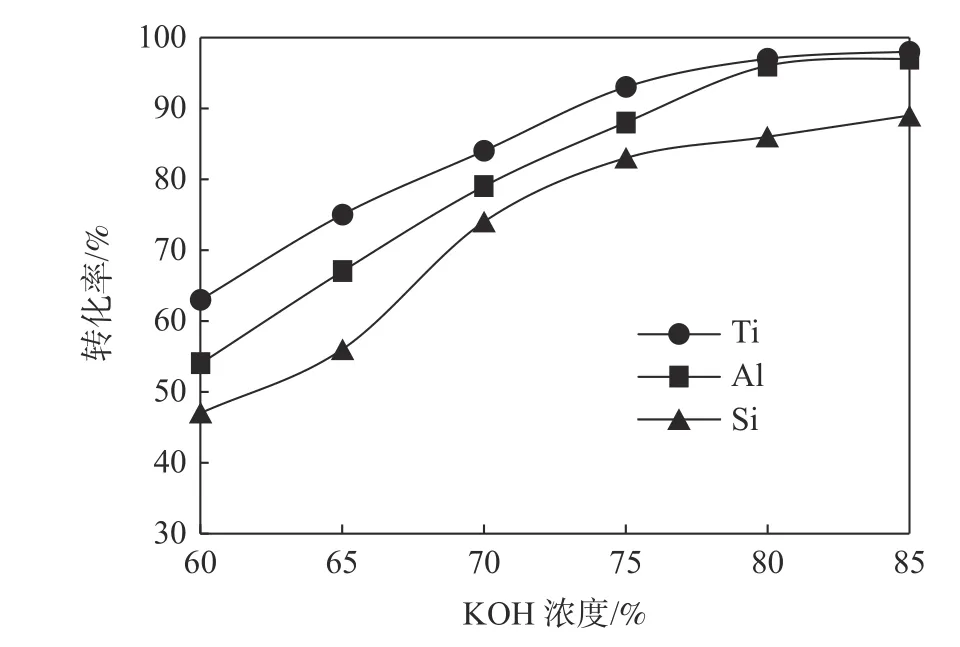
图4 碱浓度对钛、铝、硅转化率的影响Fig.4 Effect of KOH concentration on conversion of Ti,Al and Si
2.4 钛中矿粒径对钛、铝、硅转化率的影响
固定搅拌速度400 r/min,碱矿质量比6∶1,反应温度为240 ℃,反应时间180 min,碱浓度为80%,考察了钛中矿粒径对钛、硅、铝等元素转化率的影响,结果如图5 所示。
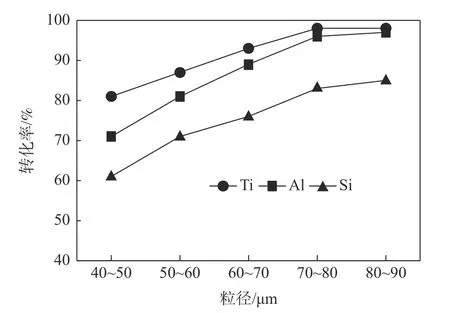
图5 粒度对钛、铝、硅转化率的影响Fig.5 Effect of mineral particle size on conversion of Ti,Al and Si
从图5 可以看出,随着钛中矿粒径的减小,钛、铝、硅三种元素的转化率均呈上升趋势。在70~80 μm时,钛、铝的转化率分别达最大98%和97%,硅的转化率也有83%,说明在此条件下,钛、铝的反应基本完全,综合成本等因素考虑,钛中矿粒径的较佳参数为70~80 μm。
2.5 碱矿比对钛、铝、硅转化率的影响
固定搅拌速度400 r/min,反应温度为240 ℃,反应时间180 min,碱浓度为80%,钛中矿粒径为70~80 μm,考察了碱矿比对钛、硅、铝等元素转化率的影响,结果如图6 所示。
从图6 可以看出,随着碱矿质量比逐渐增大,钛、铝、硅三种元素的转化率均呈上升趋势。在碱矿比为6∶1时,钛、铝的转化率分别达最大98%和99%,硅的转化率也有84%,之后进一步增加碱矿比对各元素转化率影响不大。说明在此条件下,钛、铝、硅的反应基本完全,综合成本等因素考虑,碱矿质量比的较佳范围为6∶1。
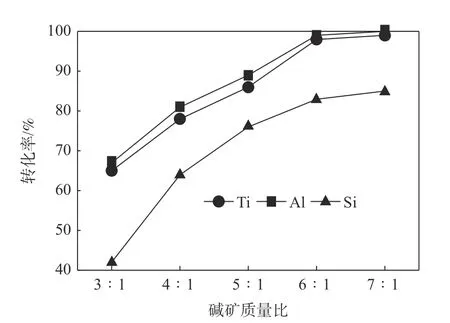
图6 碱矿质量比对钛、铝、硅转化率的影响Fig.6 Effect of mass ratio of alkali to ore on conversion of Ti,Al and Si
2.6 搅拌速度对钛、铝、硅转化率的影响
固定碱矿质量比6∶1,反应温度为240 ℃,反应时间180 min,碱浓度为80%,钛中矿粒径为70~80 μm,考察了搅拌速度对钛、硅、铝等元素转化率的影响,结果如图7 所示。
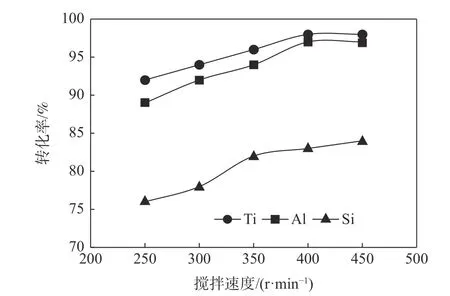
图7 搅拌速度比对钛、铝、硅转化率的影响Fig.7 Effect of stirring speed on conversion of Ti,Al and Si
从图7 可以看出,随着搅拌速度的增加,钛、铝、硅三种元素的转化率均呈上升趋势,但其增加幅度远不如其他因素的影响明显。当搅拌速度达到400 r/min时,钛、铝、硅的转化率分别达98%、97%和83%,之后再增加搅拌速度对上述元素的转化率影响不大,因此较佳的搅拌速度为400 r/min。
2.7 综合试验
在上述优化后的反应条件(即搅拌速度400 r/min,碱矿质量比6∶1,反应温度为240 ℃,反应时间180 min,碱浓度为80%,原料粒度70~80 μm)下,对钛中矿进行了3 次亚熔盐分解平行试验,考察了最佳条件下钛中矿的分解情况及稳定性,结果见表2。
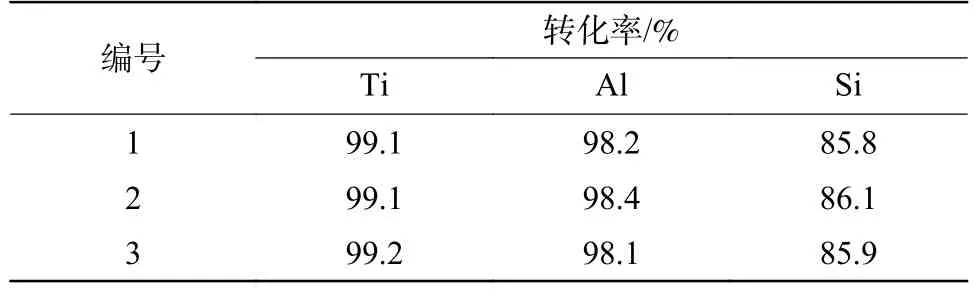
表2 优化工艺条件下钛中矿的分解情况Table 2 Decomposition of titanium middling ore under optimized process conditions
从表2 可以看出,在优化条件下,钛中矿中钛、铝、硅等元素不仅具有较高的转化率且重现性良好。
2.8 钛中矿分解产物的X 射线衍射分析
由于钛元素经亚熔盐分解后的产物K4Ti3O8为无定形钛,不能直接通过X 射线衍射分析其形貌,故将钛中矿经亚熔盐分解后的产物经水洗去除多余的氢氧化钾后,在电阻炉中800 ℃煅烧3 h 后进行XRD 分析,试验结果如图8 所示。
从图8 可以看出,亚熔盐水洗产物经煅烧后的主要物相组成为六钛酸钾(K2Ti6O13),此外,亚熔盐产物中含有的铁、镁、钙等元素也分别与钛元素在亚熔盐体系中反应生成了新的化合物。从图8 还可以看出,产物中未出现铝、硅等元素相关的物相,也进一步说明了在亚熔盐反应过程中,上述元素生成可溶性物质进入到液相之中。
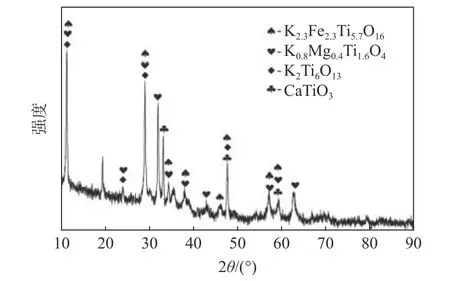
图8 产物经 800 ℃煅烧 3 h 后的 X 射线衍射谱Fig.8 X-ray diffraction spectrum of the product calcined at 800 ℃ for 3 h
3 结论
采用KOH 亚熔盐处理钛中矿,可有效分解原料中钛、铝、硅等元素,从而实现钛元素和硅、铝等杂质元素的有效分离,不溶于水的固相产物K4Ti3O8经酸洗后水解可制得TiO2,从而为采用钛中矿直接制备钛白粉开辟了一条新的途径,对实现钛中矿的综合利用具有重要意义。考察了反应温度、反应时间、碱浓度和钛中矿粒度等因素对钛中矿分解情况的影响,得出下述结论:
1)采用KOH 亚熔盐处理钛中矿可实现其有效分解,其较佳工艺参数为搅拌速度400 r/min,碱矿质量比6∶1,反应温度为240 ℃,反应时间180 min,碱浓度为80%,原料粒度70~80 μm。在此反应条件下,钛中矿中钛的转化率达99%以上,铝的转化率 98%以上,硅的转化率在85%以上。
2)较佳工艺条件下的重复性试验显示,该工艺不仅对钛中矿具有较好的分解效果,还具有重现性。
3)X 射线衍射分析表明,亚熔盐分解产物经800 ℃的高温下煅烧3 h 后测得的产物主要为六钛酸钾(K2Ti6O13),说明KOH 可与钛中矿充分反应并有效去除其中的铝、硅等元素。
