固体储氢材料研发技术进展
2022-11-05李锦山任春晓罗琛陈华祥
李锦山,任春晓,罗琛,陈华祥
中国石油天然气股份有限公司石油化工研究院
0 引言
当前,人类社会可持续发展正面临着传统化石能源枯竭和环境污染的双重压力。氢能作为一种清洁高效的二次再生能源,是能源结构调整的重要方向,其高效利用也是实现“双碳”目标的重要途径。氢能产业链涉及制备、储运和应用,是绿色经济发展的重要增长点。根据中国氢能联盟的预计,中国氢气需求量到2025年将达到2 900×104t,2030年将达3 500×104t,2050年将接近6 000×104t,氢能在中国终端能源体系中占比将超过10%,产业链年产值将达到12×1012元[1-2]。但中国氢能的规模化应用仍任重道远,特别是在制备、储运和应用等方面还存在技术、安全性、经济性等方面的巨大挑战。实现安全、低成本、高效的储氢和运输仍是当前的关键技术瓶颈,也是核心难题,相比气态和液态储氢而言,安全高效的固体储氢材料可望很好地解决这一难题。因此,更好地开发出高水平的固体储氢材料,使其储氢密度大,具有适宜的吸放氢压力和温度、良好的动力学特性,以及长寿命和经济环保等性能指标,最大限度满足车载氢燃料电池用氢,以及作为太阳能、风能等可再生能源的二次能源载体等应用成为固体储氢材料发展的重要研究方向。
1 氢及储氢技术
氢是结构最简单和最独特的化学元素,也是宇宙中分布最广、最丰富的元素。氢的高能密度和易与其他能源相互转化的特性,使其成为一种很好的能源载体。
早在2003年,DOE(美国能源部)就提出了车载储氢系统的要求和发展目标,并于2011年进行了修订(见表 1)。IEA(国际能源协会)也制订了可逆质量储氢密度大于5%的车载储氢系统目标,要求在低于80 ℃和1 kg/cm2压力下可释放氢气[3]。
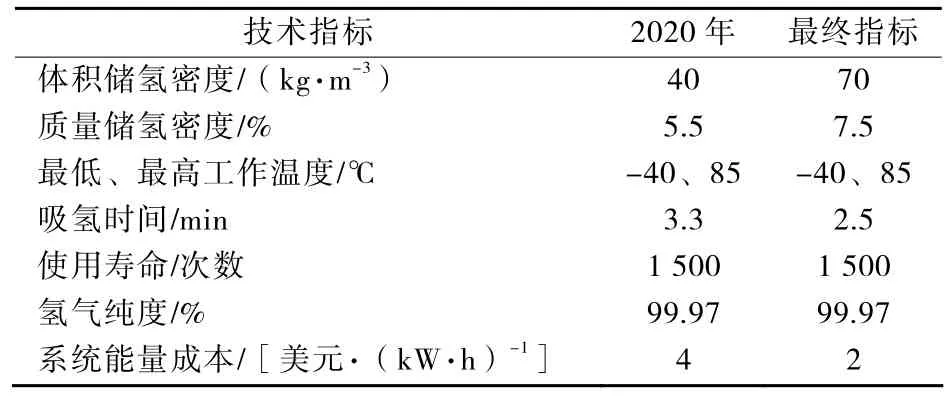
表1 美国能源部对车载储氢系统的技术指标(2011年)
储氢方式按照氢气的储运形式可分为高压储氢、液态储氢和固体储氢。
高压储氢主要是采用高压氢气钢瓶储氢,常见的高压钢瓶气压为15 MPa、35 MPa和75 MPa。氢气是偏离理想气体方程气体,其密度不随压力升高而线性增加,压力为35 MPa和70 MPa时,氢气的体积密度分别为 20 kg/m3和 330 kg/m3[4-5]。钢瓶会随压力增高而加重,为了保持高压下的钢瓶强度并减轻重量,现在多采用复合材料设计储氢瓶,例如:Ⅲ型瓶用铝合金做内胆,并用碳纤维缠绕保证强度;Ⅳ型瓶使用塑料内胆,进一步减轻气瓶重量。目前以塑代钢的全复合轻质纤维缠绕储罐已由日本丰田公司开发成功并投入应用,储存压力70 MPa,质量储氢密度约为 5.7%,容积 122.4 L,储氢总量 5 kg[6]。
液态储氢需要通过极低温度的制冷系统进行氢气液化,对能量消耗和容器设备的要求高,且液氢挥发难以避免,因此较少作为大规模氢源使用,但在航空和军事等领域有一定的优势,如用于火箭发动机的液体推进器等。液氢的另一种形式是将液态的芳香化合物作为储氢载体,如苯、甲苯、萘等,通过催化加氢和脱氢反应,实现氢的储存和释放,但催化加氢和脱氢成本高,工艺复杂,且存在一些副反应[7-8]。
固态储氢时,氢以分子、离子、原子等状态存在,有物理和化学两种机制,前者氢以分子态与材料结合,后者氢以离子键或共价键与其他组分结合,生成金属氢化物、配位氢化物等。固体储氢可以获得较高的体积储氢密度和质量储氢密度,而且安全性好。
2 基于物理吸附机制的储氢材料
这类材料主要是指内部形态结构各异的碳基材料或其他无机多孔类材料,包括活性炭、纳米纤维、纳米管、MOFs(金属-有机框架材料)或COFs(共价有机框架材料等,氢以分子形态与材料结合,作用力较弱,基本上为范德华力。
2.1 碳材料及其他无机材料
碳基材料主要有活性炭、石墨纤维、纳米纤维和碳纳米管等[4,10-11],其储氢性能特点见表2。
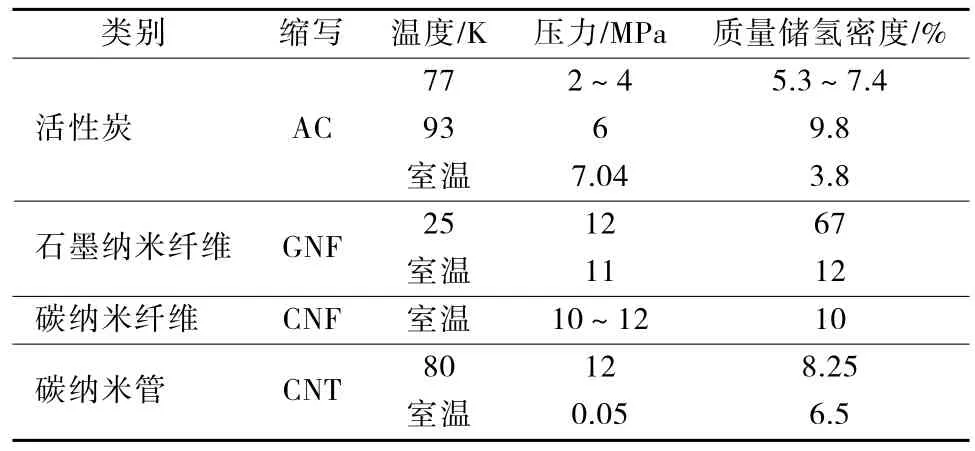
表2 4种碳基材料的储氢性能
石墨纳米纤维是多层的石墨材料,有薄片状、管状、带状、棱柱状和鲱鱼骨状等。研究表明改变GNF的形状可以改变储氢容量,特别是室温下的储氢容量很高,可达到超过10%的质量储氢密度,有研究曾经做到最高67%,但仅此一次[12-13]。碳纳米纤维主要是以镍、铜等金属为催化剂,经乙烯裂解制得。氢分子的动力学直径小于CNF的层间距,因而大量氢气可以进入层间。CNF有中空管,直径大约10 nm,氢气可凝结在中空管中,因而CNF储氢密度较高。研究表明,在常温、12 MPa条件下,对CNF材料表面处理后,质量储氢密度可达10%[13-14]。纯的碳纳米管的质量储氢密度也可达5%~10%,其他的无机材料如多孔的水合结晶硅铝酸盐等的储氢密度也尚可[15-16]。碳基材料的最大缺点是必须在极低的温度、较高压力下来完成氢的吸附,而且储氢量相对较低,在工业应用上还存在很大的局限性。目前,大家关注较多的仍是获取高的表面积,并提高吸附能。
2.2 MOFs和COFs储氢材料
MOFs是由无机金属中心与有机官能团分子通过自组装而形成的一类三维多孔结构的配位聚合物,金属与配体的作用力较强。COFs与MOFs具有不一样的特征,COFs是由B、C和N原子间以强的共价键连接刚性有机分子得到的多孔结构材料,该材料中化学键的联结方式要比 MOFs的配位键强,不含金属,因此具有更小的框架密度和更大的比表面积[17-20]。MOFs拥有极高表面积(实验值达到7 140 m2/g,理论值达到14 600 m2/g),极高孔隙率(自由体积达到 90%),而且孔径和内表面可调控[21]。近年来,MOFs的研究十分活跃,主要集中在比表面积、孔隙率、孔径大小、不饱和配位的金属中心及吸附热等对氢吸附能力的影响,为此有人提出了储氢策略,即:适宜孔径下的高孔隙率、注入形核、穿插、开放金属位、MOFs含轻金属和配体功能化等[17-18,21]。无论MOFs还是COFs,研究更多集中在极低温度下的氢气吸附,但这种作用力仍属于范德华力,与碳材料一样,吸附量仍然有限,除非加大吸附压力。有研究曾合成孔道1.2 nm,比表面积分别为3 472 m2/g和4 210 m2/g的COFs-102和COFs-104,在 77 K下的吸氢量分别达到 7.2%和7.1%,但还没有找到一种能在1个标准大气压下可逆质量储氢密度达到3%以上的MOFs材料[20-22]。
3 基于化学吸附机制的储氢材料
这类材料主要包括金属氢化物、配位氢化物和化学氢化物等。在这些材料中,氢是以原子或离子形式与其他元素相结合[4,17]。
3.1 金属氢化物及其储氢合金
金属氢化物的吸放氢热力学可以用压力-成分-温度曲线表征[15],亦称PCT曲线,这是衡量储氢性能的重要依据,它直接反映了储氢材料的可逆储氢容量、平衡氢压、平台斜率和滞后效应(见图1)。图1中的3条曲线分别表示3个温度下的压力与组成的关系,以T1为例,A点之前氢进入金属晶格中形成固溶体α相,到达A点后开始生成金属氢化物β相,AB为平台期,两相共存,超过 B点,完全变为β相,继续升高氢压,氢可以继续固溶进入β相,此时可能形成新的氢化物和出现新的平台,升高温度氢化物的平衡氢压也随之升高。
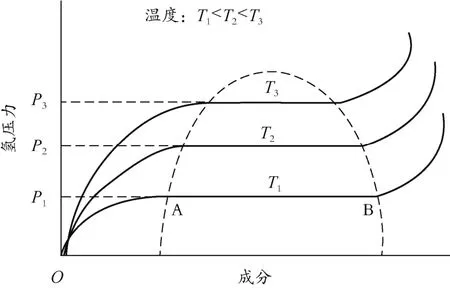
图1 金属氢化物的PCT曲线
采用式(1)所示van’t Hoff(范特霍夫)方程,可以计算储氢材料的吸放氢反应焓变和反应熵变,这是储氢材料重要的热力学性能参数,也是探索新型储氢合金的重要依据。
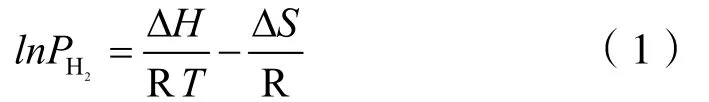
除镁基储氢合金外,其他金属储氢合金多为金属间化合物和多元合金。一般由与氢结合能为负的金属元素(与氢亲和的元素,习惯上称之为A元素)和与氢结合能为正的金属元素(与氢相排斥的元素,习惯上称之为B元素)构成。其中A主要为Mg、Ti、V、La、Zr等,而 B 为 Cr、Mn、Fe、Co、Ni、Cu、Zn、Al等[28]。目前,主要的储氢合金有以下几类:镁系(A2B型)、钛系(AB型)、钒系(BCC结构)、稀土系(AB5型)和锆系(AB2型)。
3.1.1 镁系储氢合金
研究最多且产业化前景较好的金属氢化物是镁基氢化物MgH2,这得益于金属元素镁的储量较为丰富、制备工艺相对成熟。镁在 300~400 ℃和较高氢压(2.4~40 MPa)的环境下可以直接与氢气反应生成 MgH2,MgH2具有性能稳定的红晶石结构,而且它的质量密度和体积密度分别达到 7.6%和 110 kg/m3。但相对于其高的储氢容量,它的吸放氢反应无论是从热力学还是动力学上都有很大的困难[25]。以热力学来看,MgH2的生成焓为-74 kJ/mol,平衡放氢温度289 ℃;以动力学来看,放氢的活化能160 kJ/mol,只有较高的温度才能实现较快地放氢,这是产业化应用的两个最大瓶颈。此外,镁的表面极易生成一层氧化膜,也是需要考虑的问题。
为了改善MgH2的吸放氢性能,克服纯镁的吸放氢速率慢、放氢温度高等难题,往往加入过渡金属TM,形成Mg-TM-H系氢化物,还有稀土改性和稀土及其过渡金属改性的Mg-Re-H系和Mg-TM-Re-H系氢化物,这些均称之为镁基储氢合金。对Mg-TM-H系氢化物而言,在平衡条件下,TM在镁中的固溶度很小,借此改善储氢性能还是有难度的,对此,可采用两种办法:一方面在高能球磨过程中加入少量的TM做催化剂,可改变MgH2的吸放氢动力学,但热力学性能并未好转;另一方面改变相结构来形成新的 Mg-TM-H系氢化物。该类氢化物过渡金属包括Ni、Fe、Co、Cu、Cr和Mn等。通过掺杂改性等手段形成不同结构的纳米晶、微晶、非晶和纳米复合材料等,将是镁基储氢材料制备领域的研究热点[26]。
有研究以储运2.5 t氢气为例,进行了高压气态、低温液态、镁基固态、有机物液态等4种方式的储运氢能耗对比,从加氢、运输、到加氢站全过程,按 500 km运输测距离算,其能耗分别为 26 300 kW·h,37 600 kW·h,7 700 kW·h 和 11 960 kW·h[27]。其中镁基固态储氢材料在吸氢时是放热过程,不损耗能量,循环寿命长、常温常压储氢,具有较强的竞争能力和较好的应用前景。目前,国内某些公司,如上海镁源动力,已建成百吨级镁基储氢器材生产装置,并计划扩建千吨级生产线。
3.1.2 钛系储氢合金
钛系储氢合金通常有 Ti-Fe、Ti-Mn、Ti-Cr、Ti-Zr等,主要以 AB型的 TiFe合金为代表。TiFe储氢合金成本低、易制取、室温下吸放氢速度快,另外其循环寿命长,可以达到2 000次以上,是稀土储氢合金的4倍,而原料成本仅为稀土储氢合金的三分之一[25-28]。但易生成致密的TiO2层而很难被活化,活化后极易与空气中的O2、CO2、H2O等杂质气体接触并丧失吸放氢活性。目前,主要通过元素合金化和表面处理等手段来解决这些问题,通常采用Ni、Mn、Cr等过渡元素来取代TiFe中部分Fe,从而改善合金的活化性能[28-29]。通过降低合金表面的致密性以促进氢原子快速进入合金表面、增加相界面或引入晶体缺陷以提高氢原子的扩散能力等已成为重点研究方向[29-30]。
3.1.3 钒系储氢合金
钒系储氢合金主要是具有BCC结构的钒基固溶体合金,包括Ti-V-Cr、Ti-V-Mn、Ti-V-Fe、Ti-V-Ni。钒基固溶体合金具有储氢量大(VH2的理论储氢密度为3.8%),可在常温下实现吸放氢且反应速度快,与钛系储氢合金类似,表面容易生成一层氧化膜,也可以通过元素的添加和替换来改变合金的组分,提高储氢性能[30-31]。但金属钒的价格高、常温常压下放氢不彻底,大范围应用尚有较大距离。
3.1.4 稀土系储氢合金
稀土系储氢合金主要以 AB5型合金 LaNi5为代表,LaNi5在温度为25 ℃,压力为0.2 MPa的条件下,储氢质量密度约为 1.38%。其优点是活化性能好、吸放氢反应速度快、滞后小、不易中毒。但是合金在吸氢后晶体会膨胀,从而导致合金粉化,而且原料成本过高。目前对稀土系合金的开发研究主要是把LaNi5中的部分La用混合稀土Mm(La、Ce、Nd、Pr)代替。另外,添加镁的 La-Mg-Ni储氢合金因独特的超堆垛晶格结构而具有非常出色的储氢性能,也正在成为金属储氢材料的研究热点[31-32]。
3.1.5 锆系储氢合金
锆系储氢合金主要以AB2型合金ZrMn2为代表,该合金具有储氢量高、吸放氢速度快、循环寿命长等优点,但其原料成本高、吸放氢平台压力低、不易活化。AB2型合金虽然存在初期活化困难、原料成本高等问题,但由于其出色的储氢量和循环寿命长的优势,被视为下一代Ni-MH电池的高容量负极材料[31-32]。
3.2 配位氢化物储氢材料
与金属氢化物不同,配位氢化物是一种盐,氢原子通过共价键连接到复合阴离子的中心原子上,形成络合物阴离子,后者再与金属离子以离子键结合形成氢化物[33]。一般氢化物可以用化学式AxMeyHz表示,A通常为元素周期表中第一或第二主族元素,Me通常为B、Al、N,其理论储氢质量密度为5.5%~21%。配位氢化物的放氢可以通过水解或热解两种方式进行。
按照配体的不同,氢化物可以分为3类[34]:第一类是以[AlH4]-基团为配位体的金属氢化物,其中较为突出的是 LiAlH4、Ca(AlH4)2、KAlH4;第二类金属氢化物的配位体为[NH2]-基团,此类金属氨基化物具有代表性的是Mg(NH2)2、NaNH2以及 LiNH2等;第三类是以[BH4]-基团为配位体的金属氢化物,典型的金属硼氢化物有LiBH4、NaBH4、KBH4、Mg(BH4)2等。其中最受关注的为第一类和第三类。从配位氢化物离子键或共价键的结构来看,其热稳定性较高,作为储氢材料有局限性:一是放氢温度很高,基本需要200 ℃以上,同时它的吸氢条件也较为苛刻;二是反应物和生成物多种形态并存,相分离和团聚同时发生,吸放氢反应很难完全完成,实际储氢量与理论值有偏差;此外,如果是金属硼氢化物和金属氮氢化物,吸放氢反应中会有副产物生成或产生杂质气体[4,24]。为克服这些问题,研究人员进行了很多工作,如阴阳离子替代,构建反应失稳体系和掺杂催化、纳米结构调制,采取新的框架材料与配位氢化物形成空间限域体系等[26,35-36],但这些工作仅仅调变了氢化物的某些性能,如降低吸放氢反应的温度、提高充放氢速率、减少杂质气体释放等,但真正实现完全可逆的吸放氢过程,解决配位氢化物有效质量储氢密度远低于理论氢含量的问题,尚有较大差距。
3.3 其他储氢材料
3.3.1 氨硼烷化合物储氢
氨硼烷化合物是一类通过化学反应实现放氢的含氢化合物,这类化合物可通过热解、水解等反应放氢,且放氢量高达 19.6%,已成为当前化学氢化物研究的热点[35-37]。目前,引人注目的是氨硼烷(NH3BH3,亦称AB分子),该化合物可以看成是电子富集的氨分子与电子贫乏的硼烷分子的加合物,B和N所形成的键为极性配位键,它的最大特点是分子内同时含有两种电荷相反的氢,即N上的正氢和B上的负氢,正是因为正氢和负氢的作用,促进了氢分子金属氨基化合物和氢化物两个固相之间存在的界面传质,显著降低了放氢动力学阻力[35-38]。这类化合物的热分解反应一般为三步,反应产物分别为氨基硼烷[NH2BH2]、亚氨基硼烷[NHBH2]和氮化硼BN,每步均可放氢,反应温度分别为 110℃、150 ℃、500 ℃。需要指出的是,第三步反应产物BN不会被氢气还原,所以一般只考虑前两步的放氢反应,热力学方面的障碍也基本得到了消除[22-39]。即便如此,作为储氢材料,它的热分解过程还是存在诸如热分解温度过高、放氢速度过慢、产生副产物B2H6和NH3等较多问题,但作为一种新型材料,还是展现出了较好的前景。因此,大量的研究工作集中在降低氨硼烷放氢温度、提高放氢速度、抑制副产物生成等方面,采用的主要手段是改性,包括元素替换、金属催化、酸催化、离子液体和纳米结构,其中,化学元素替换是当前在提高氨硼烷放氢动力学性能方面最有效的一种方法[23-40]。
3.3.2 高压复合储氢
高压复合储氢是一种满足车载应用要求,综合了气态储氢技术和固态储氢材料优点的一项储氢技术。车载用高压复合的想法早已有之,但最早的金属钢瓶本身重量很大,再加上金属储氢材料重量,气-固复合储氢的实际应用面临挑战。而现在新型的IV瓶体积大、重量轻、承受压力更强,为高压复合储氢提供了新的可行方案。实际应用时,是将固态储氢材料嵌装于高压容器中,这样的气-固复合储氢系统具有储氢量高、放热量少、安全性高、适用温度广等优点,展现出了较好的应用前景。
高压复合储氢的原理:一方面是储氢粉体材料本身可存储氢,表现出了固态储氢性能;另一方面由于储氢粉体材料有限的堆垛密度,粉体材料的空隙也可参与储氢。储氢罐充氢气时,当氢压高于储氢材料的吸氢平台压时,储氢材料会大量吸氢;使用过程中,当氢压下降至低于脱氢平台压时,固体储氢材料则成为补偿的氢源释放氢气。因此,高压复合储氢不但克服了高压气态储氢时单位体积储氢量不足的问题,还克服了金属氢化物质量储氢密度偏低的问题。
在高压条件下,优先考虑有效调控固体储氢材料的平台压力、容量和吸放氢动力,以及高压储氢特性等[9]。目前研究最多的高压储氢罐用轻质高压储氢材料为AB2型合金(Zr-Fe2、TiCr2)和Al基金属配位氢化物等[41]。
3.3.3 石墨烯储氢
石墨烯是一种新型的碳材料,二维结构、SP2杂化、比表面积大、导电、热导率高,与其他碳基材料一样也可以作为储氢材料使用。但因其结构的特殊性,特别是其离域π键的电子性质和轨道杂化等,与其他碳材料的吸附原理是不一样的。
石墨烯储氢不仅是物理吸附,还存在化学吸附作用,目前,被业内广泛认同的是物理吸附、元素掺杂或结构改性和电化学3种储氢机制[42]。物理吸附中,由于氢分子与石墨烯的结合能较低,氢的吸附是以分子氢而非原子态氢的形式结合,所以氢的储存需要很低的温度。元素掺杂或利用石墨烯的空位缺陷进行改性也可以改变其与氢分子的吸附能力,如,用Ni、Pd来修饰石墨烯,可在物理吸附基础上加持化学吸附,可改善可逆储氢能力。掺杂的元素有碱金属、碱土金属、过渡金属和 B、N、Si等非金属类元素[43],但还应注意掺杂的元素容易出现原子团聚现象,储氢的能力和效率会有所下降。采用电化学储氢是实现原子态储氢的重要途径,电化学储氢是利用石墨烯将氢能转化为化学能从而达到储氢的目的[44],主要利用的是石墨烯的储能特性,其本身就可作为二次电池或电池的负极。当石墨烯负载电化学催化剂进行工作时,在催化剂表面会将氢气解离为氢原子,氢原子再溢流到石墨烯上,通过表面扩散和化学吸附存储在石墨烯上。氢源除氢气外,也可以是水或其他的质子。该方法在化学电源领域具有很大的应用前景。此外,石墨烯在储氢领域中的应用范围正在逐步扩大,比如作为储氢合金的催化剂,可提高合金的活性和选择性,也可作为碳催化剂载体或助催化剂,使材料表现出高的氢吸附和解吸性能[45-46]。
3.3.4 玻璃微球储氢材料
HGM(空心玻璃微球)作为储氢材料,有其自身的特点。与常规气瓶比,HGM储运比较方便;HGM储氢质量分数为 15%~42%,其能量密度比高压储氢、固态储氢都要高,虽比液态储氢略低,但储运过程中的能量消耗较液态储氢低 10%~20%[47]。HGM储氢的充放氢过程是一个物理过程,微球具有的非渗透性直接决定了 HGM的充放氢效率。在低温和室温下,氢气无法进入内部;当温度升高至300~400 ℃时,HGM 的穿透率逐渐增大,内部充满氢气;此时若温度降至室温,其穿透率又降低,氢气无法溢出,从而实现氢气的储存。HGM主要有MgAlSi、石英、聚酰胺、聚乙烯三酚盐酸和N29等[48]。玻璃的材质和耐压强度、导热性等对充放氢有决定性作用,通过设计制备不同组成、不同形貌和不同尺寸大小的HGM可以强化充放氢效率,实验发现,过渡金属掺杂的碱硼酸盐玻璃则表现出了很好的光致释氢效果[49],这些工作都有利于推动HGM的工业化应用。
4 结束语
储氢材料的研究和应用已走过近 50年的发展历程,材料种类越来越丰富,性能不断提高,应用越来越广泛,其应用领域已涉及充电电池、混合动力汽车、燃料电池、氢分离等领域。目前其主要发展方向是满足车载动力要求和应用于智能电网系统的储能及分布式发电的储氢材料。
在现有的储氢体系中,固体储氢材料无论储放氢温度,还是可逆性和循环寿命等方面,均显出了比较好的市场前景。然而,固体储氢材料的发展也面临较大挑战。在性能上,由于热力学或动力学,或者二者兼有的限制,实际工况条件下的吸氢和放氢能力不足,而能够在适宜条件下工作的储氢材料,其储氢密度一般偏低,满足不了储能密度的要求。对固体储氢材料而言,不单需要廉价、可持续供应的金属原材料,还要克服高容量储氢材料高昂的制造成本,而且很多储氢材料在生产、使用和再生的全周期还存在诸多环保问题,因此大规模应用任重道远。
此外,储氢材料与系统集成的工程技术也面临较大的挑战。破解这些问题和挑战,推动产业的发展,应着力以下几个方面:一是要深入开展原创性基础研究,攻克一批关键科学问题,加强金属与氢的键合理论计算和氢化物的结构分析等基础研究,深入开展理论设计、制备技术、表征方法和催化或储氢机理等方面的基础研究;二是加快储氢材料的工艺工程技术开发,以产品开发和应用开发为主,尽快突破一批关键核心技术,坚持问题导向和目标导向,开发出市场认可并可接受的新的氢化体系和新型结构的储氢材料,低成本提升技术和产品的核心竞争力;三是加快储氢材料和储氢技术的工业转化与应用,大力加强储氢材料与集成的工程应用研究,针对不同的应用场景,积极布局和开展应用示范。
