氮氧化富氮骨架的含能材料合成研究进展
2022-11-04郭元盛弥阳丽南少聪
郭元盛,吕 玺,李 洋,薛 祺,弥阳丽,崔 伟,南少聪,刘 鹏,张 萌
(1.西安近代化学研究所,陕西 西安 710065;2.中国人民解放军驻845厂军代室,陕西 西安 710302;3.陆装驻西安地区航空军事代表室,陕西 西安 710065)
引 言
含能化合物是混合炸药、推进剂和发射药的能量来源[1],是航空航天、兵器装备、民用爆破等领域的基础性材料,而研发高性能骨架结构则是提升化合物能量密度水平最高效的途径之一[2-5]。研究表明[6-9],N-氧化物键的两性离子性质产生了较大的偶极矩,通常会导致晶体密度增加;同时,N-氧化物提升了整体的氧平衡水平,可以提供更多的氧化性元素来改善分子中燃料的整体燃烧。此外,N-氧化物往往能够产生额外的稳定作用,N-氧化物的官能团引入常常导致含能材料对外界刺激的敏感度(如冲击感度、摩擦感度、经典感度等)降低[10-11]。而从成键方式角度,根据N—O键的不同可以分为两类结构:一类为中性的芳香性N-氧化物(N-oxides);另一类则为羟胺失去质子后形成的N-氧阴离子(N-oxide anion),属于离子型化合物。前者氮原子中心为sp2杂化,N—O片段为氮原子提供孤对电子所形成的偶极键;后者氮原子中心为sp3杂化,N—O片段为氮氧原子分别贡献一个电子所形成的单键。基于氮氧化富氮骨架的含能材料由于其高生成焓水平以及突出的能量密度水平引起了含能材料研究工作者的重视,成为高性能含能材料结构设计与合成的重点研究方向[12-15]。
基于氮氧化富氮骨架的含能化合物设计与合成根据N—O键种类的不同分为富氮芳环N-氧化物及富氮N-氧化阴离子结构。而根据环系排列的不同则进一步可分为3类结构[16]:(1)单环型氮氧化富氮骨架含能材料;(2)串联型氮氧化富氮骨架含能材料(即以化学键将环系进行串联获得链式结构);(3)并联型氮氧化富氮骨架含能材料(即以氮氧化富氮骨架并联所形成的并环结构)。不同的结构类型带来迥异的性能特征,基于此,本文围绕氮氧化富氮骨架的含能化合物研究,按照其组成结构方式的不同进行了综述,并对代表性化合物的性能进行了分析,为含能N-氧化物的研发提供参考,同时也为新型含能化合物研究提供依据。
1 单环型氮氧化富氮骨架的含能材料
对比三类富氮芳环N-氧化物及富氮N-氧化阴离子结构(见图1),单环型氮氧化富氮骨架的含能材料的骨架结构最为简单。从合成角度,单环型芳环N-氧化物研究绝大多数是以杂环氮原子的直接氧化为关键反应步骤,形成N-氧化物片段,此类转化需要以氮氧化反应方法学研究为基础。氮氧化反应实现依赖于氧化剂的筛选,目前可用于氮氧化反应的氧化剂种类丰富,包括双氧水、间氯过氧苯甲酸(mCPBA)、次氟酸乙腈溶液(HOF/MeCN)、过氧化尿素(UHP)、过硫酸氢钾复合盐(Oxone)等[17-23]。如利用mCPBA可将1,2,3-三唑和1,2,4-三唑氧化为相应N-氧化物,其中1,2,3-三唑的N1、N3位易被氧化,1,2,4-三唑的N1、N4位易被氧化[8-10];利用次氟酸的乙腈溶液(HOF/MeCN)可将四唑氧化为四唑-2-氧化物[11-12];利用H2O2-TFAA可将氨基取代的1,2,4,5-四嗪氧化为1,2,4,5-四嗪-1,4-二氧化物等[13],见图2。

图1 三分子骨架体系中的富氮芳香族N-氧化物Fig.1 Nitrogen-rich aromatic N-oxides in three molecular skeleton systems


图2 氮氧化反应的方法学研究Fig.2 Methodological study of nitrogen oxidation reaction
1.1 吡唑N-氧化物结构
对于五元多氮杂环体系,依据氮含量的升高,二氮唑、三氮唑、四氮唑的芳环缺电子效应愈发明显,导致相关N-氧化转化反应的难度也逐步加大,同时此类结构中N-氧化物片段主要以N-氧阴离子形式存在。对于二氮唑结构,Shevelev[29]早在1996年即报道了N-羟基二硝基吡唑的合成,以KHSO5作为缓冲溶液可以以20%~48%的中等收率获得3,4-和3,5-二硝基吡唑的氧化产物,即1-羟基化合物,成为此类研究的起始性工作。在此基础上,2012年Shreeve[30]以Oxone作为氧化剂,对更加缺电子的3,4,5-三硝基吡唑体系进行了氧化,顺利引入了相应的N-羟基的氮氧化物结构。N-羟基结构进一步通过成盐反应可以获得各种高氮含量的盐类含能化合物,见图3,其中以铵盐结构的性能最为突出,理论爆速与爆压分别为8676m/s与35GPa,密度达到1.82g/cm3,生成焓达到118kJ/mol,热稳定性为176℃,撞击感度则与RDX相近。

图3 3,4,5-三硝基吡唑1-氧化物和相应盐的制备Fig.3 Preparation of 3,4,5-trinitropyrazole 1-oxides and corresponding salts
1.2 三氮唑N-氧化物结构
2012年,Petrie等[31]指出利用Oxone与K2HPO4形成的氧化剂体系具有较强的反应性,可以将4,5-二硝基-1,2,3-三唑以96%产率氧化为相应的N-氧阴离子结构,即4,5-二硝基-1,2,3-三唑-1-氧化物,进一步形成的铵盐的晶体密度为1.789g/cm3,热分解温度为195℃。类似的,当以次氟酸作为氧化剂氧化3,5-二硝基-1,2,4-三唑的钾盐时,可以65%的产率获得相应的N-氧化物钾盐,进一步可转化为铵盐结构,密度为1.784g/cm3,与其1,2,3-三唑类物密度相近,而分解温度则降为145℃,见图4。


图4 3,5-二硝基-1,2,4-三唑1-氧化物和4,5-二硝基-1,2,3-三唑1-氧化物的制备Fig.4 Preparation of 3,5-dinitro-1,2,4-triazole 1-oxide and 4,5-dinitro-1,2,3-triazole 1-oxide
1.3 四氮唑N-氧化物结构
与三唑体系类似,氮原子排布对四氮唑N-氧化物的热稳定性影响也非常显著。四氮唑是氮含量极高的骨架,Klapötke等[32]利用硝基四唑结构进行了Oxone氧化,实现了高氮氧含量的含能结构的制备(见图5),并以此为基础获得了大量的含能离子盐。但该类结构中中性羟基中性结构f的计算爆轰性能更加突出,密度1.94g/cm3,爆速9447m/s,爆压40.4GPa。

图5 硝基四唑N-氧化物的制备Fig.5 Preparation of nitrotetrazole N-oxide
1.4 哒嗪N-氧化物结构
虽然六元杂环体系的N-氧化物合成研究报道较五元环体系偏少,但化合物1-氧-2,6-二氨基-3,5-二硝基吡嗪(LLM-105)[33]一度被认为有望取代现役钝感炸药配方,因而引起各国的普遍关注,并被视为现役单环型富氮芳环N-氧化物最为重要的代表性化合物之一,其制备以2,6-二氨基-3,5-二硝基吡嗪(ANPz)与过氧三氟乙酸反应实现。2018年Klapoötke等[34]利用二羟甲基取代的氧化哒嗪实现了独特的3,5-二氨基-4,6-二硝基氧化哒嗪(DADNPO)结构的合成(见图6),作为LLM-105的同分异构体,DADNPO的密度1.84g/cm3,爆速8486m/s,爆压30.2GPa,与LLM-105相当。但其爆热达到4913J/g,爆温3470K,明显优于LLM-105(4506J/g和3202K)。

图6 3,5-二氨基-4,6-二硝基哒嗪-1-氧化物的合成Fig.6 Synthesis of 3,5-diamino-4,6-dinitropyridazine-1-oxide
1.5 嘧啶N-氧化物结构
2018年,张庆华等[35]以2,4,6-三胺-嘧啶通过硝化获得2,4,6-三氨基-5-硝基嘧啶,在此基础上利用氮氧化反应将硝基间位的氮原子转化为N-氧化物结构ICM-102(见图7)。ICM-102具有高实测密度(1.95g/cm3)、高热分解温度(284℃)、高爆速(9169m/s),机械感度较低,属于钝感炸药的理想结构。

图7 ICM-102的合成Fig.7 Synthesis of ICM-102
1.6 三嗪N-氧化物结构
2020年,王伯周等[36]以三聚氰胺为基础,在强氧化条件下获得了对应的双氮氧化产物,并利用成盐反应获得了多种盐类结构(MDOP、MDOMN、MDONA),其密度范围在1.75~1.89g/cm3,爆速范围8711~9085m/s,与RDX能量相当,但机械感度明显低于RDX,见图8。

图8 1,3,5-三嗪体系的氧化研究Fig.8 Oxidation study of 1,3,5-triazine system
2015年,Shreeve等[37]发展的双氧水-三氟乙酸酐体系的N-氧化方法学实现了对1,2,4,5-四嗪骨架的有效氧化,获得了2,4-双氮氧化1,2,4,5-四嗪的结构,形成了多种高密度、高性能含能材料,见图9。所得的新型双氧化四嗪化合物具有高密度、高热稳定性、正生成焓和优异爆轰性能等特征,密度1.92g/cm3,爆速9316m/s,爆压39.4GPa, 优于RDX,接近HMX水平。其中1,2,4,5-四嗪骨架两端分别连接的特定推拉电子基团对氧化性及氧化程度均发挥了关键作用。
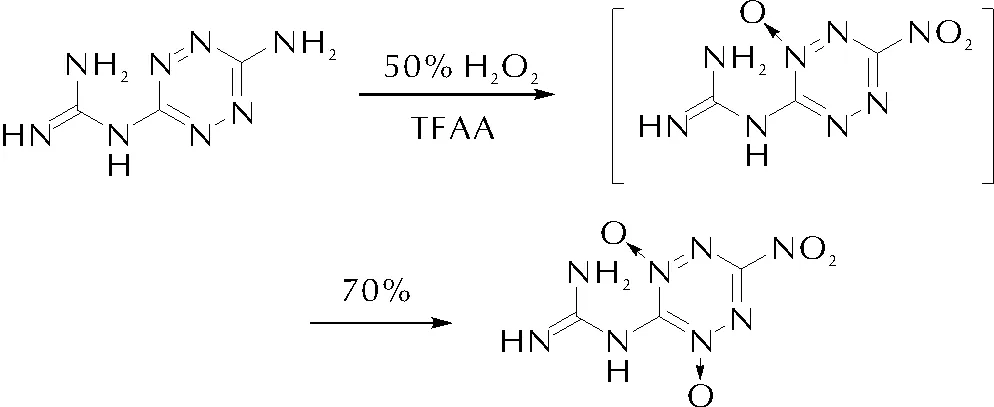
图9 1,2,4,5-四嗪的硝化研究Fig.9 Study on nitroxidation of 1,2,4,5-tetrazine
此外,单环型芳环N-氧化物也可以直接以环化途径进行构建,但通过这类方式所获得的含能材料主要指氧化呋咱衍生化的结构,其主要原因在于氧化呋咱结构本身当前仍无法通过呋咱进行氧化获取[38]。2016年,陈三平等[39]以氰基乙酸为原料,通过环化反应形成氧化呋咱骨架,将氰基结构通过含能衍生化转化为偕二硝甲基结构,获得了基于单环氧化呋咱的高能结构,见图10。

图10 4,5-双(二硝基甲基)-呋喃酸酯结构的制备Fig.10 Preparation of 4,5-bis(dinitromethyl)-furoxanate structure
2 串联型氮氧化富氮骨架的含能材料
串联型氮氧化富氮骨架含能材料是指以碳碳单键或其他基团将两片段的氮氧化富氮骨架结构进行链接。从制备方法角度,串联型氮氧化富氮骨架的含能材料构建可以基于氮杂环结构的氧化,也可以是在环化过程中直接形成N-氧化物结构。
2012年,Klapötke 等[40]合成了5,5′-双四唑 N,N′-二氧化物及其二羟基铵盐(TKX-50),成为串联型氮氧化富氮骨架含能结构的代表性化合物, 见图11。该化合物制备简便,以二氯乙二肟进行叠氮化转化并环化即可完成核心骨架的合成,其中N-氧化物片段在环化过程中直接形成。TKX-50具有优异的爆轰性能,密度为1.91g/cm3,爆速9698m/s,爆压42.4GPa,应用前景广阔。

图11 TKX-50的制备Fig.11 Preparation of TKX-50
2014年,Klapötke等[41]完成了双硝基氧化呋咱结构的制备。该类化合物制备以连续的乙二肟结构进行环化获得4,4′-二氨基-3,3′-二氧化呋咱的结构,见图12。在此基础上,进行氨基的氧化反应形成硝基结构,但最终硝基产物仅以痕量被检测到,尽管如此,计算结果表明硝基体系的密度在100K高达2.007g/cm3,爆速为9525m/s。

图12 二硝基双氧化呋咱结构的制备Fig.12 Preparation of dinitro bis-furoxan Structure
2018~2021年,Shreeve及王伯周等[42-44]陆续发展了基于碳碳单键所串联的三氧化呋咱骨架,分别与硝基及氟偕二硝基型致爆基团结合实现了串联型的三氧化呋咱体系的合成,各化合物能量密度水平较之传统含能化合物均有显著优势,见图13。
2013年Klapötke等[45]以缩合方式制备了联1,2,4-三唑结构,并通过氧化反应分别制备获得了氨基与杂环氮原子的氧化,最终将N-羟基片段转化为N-氧阴离子含能盐,获得了MAD-X1,同时研究表明MAD-X1-CMDB推进剂的理论比冲和特征速度分别达到了2449.6N·s/kg和1540.7m/s,见图 14。2014年,Shreeve等[46]对联1,2,3-三唑结构进行了氧化,获得了相似的串联型氮氧化富氮骨架的含能结构,见图15。

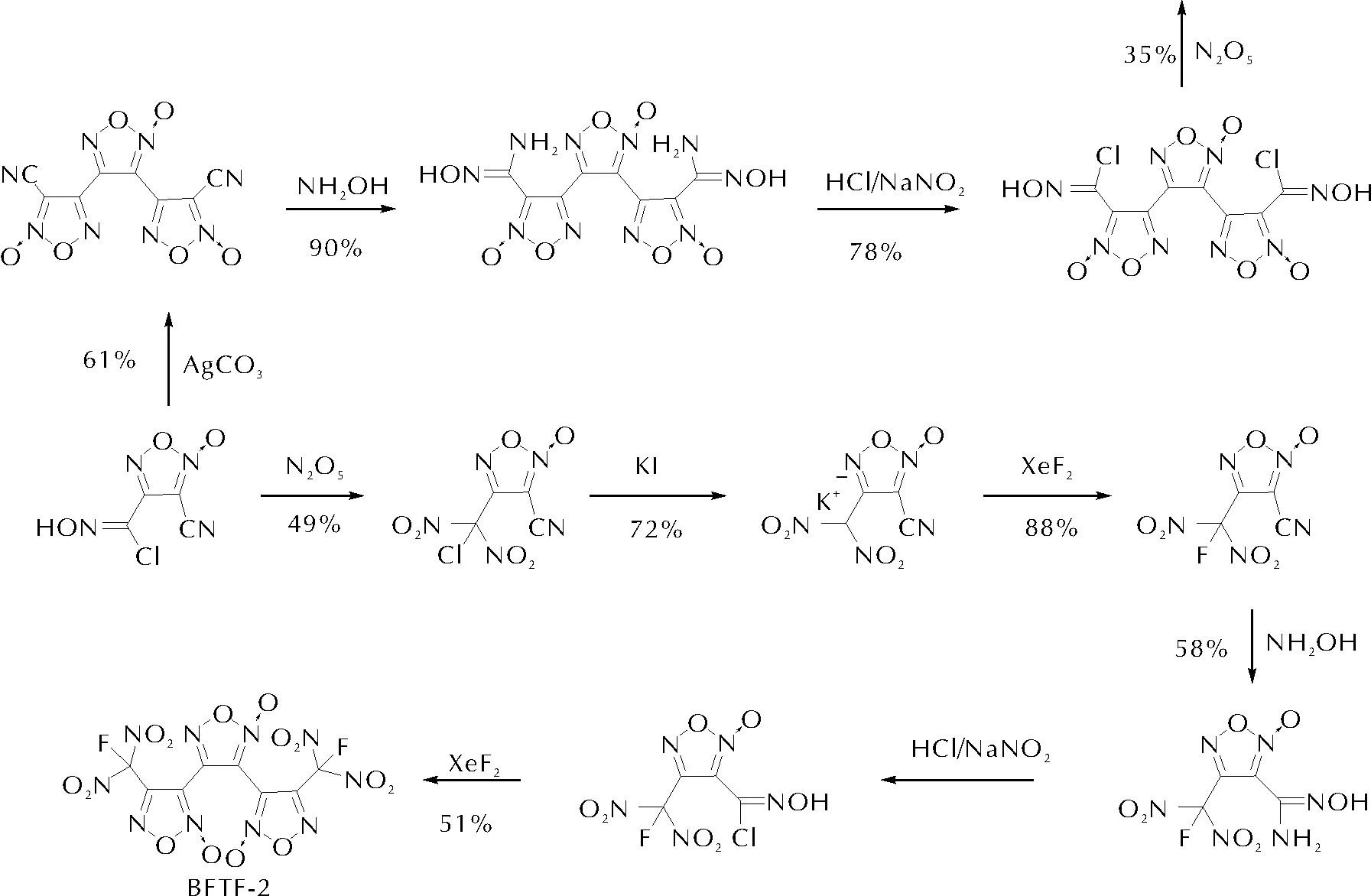
图13 含能三氧化呋咱结构的制备Fig.13 Preparation of energetic tri-furoxan structure

图14 MAD-X1制备Fig.14 Preparation of MAD-X1

图15 双1,2,3-三唑N-氧化物结构的制备Fig.15 Preparation of bi-1,2,3-triazole N-oxide structures
3 并联型氮氧化富氮骨架的含能材料
较之链式结构,氮氧化富氮骨架并联所形成的含能结构骨架更为致密,生成焓更高,且氧平衡更为理想,因而并联型氮氧化富氮骨架的设计与合成研究对于推动新型高能量密度材料的研发意义重大,因而也成为氮氧化富氮骨架的含能材料研究的重点。但需要指出,由于骨架结构的特殊性,并联型氮氧化富氮骨架合成难度通常显著高于单环及串联型氮氧化富氮骨架,此外,相比于串联型结构,并联型结构尤其是芳环结构骨架本身往往缺电子特点更加明显,因此直接氧化难度较之串联型结构难度也更大。2017年,Chavez等[47-48]利用氨基叠氮基四嗪环化所得的四唑并四嗪稠环进行氧化,成功实现了6-氨基-四唑并[1,5-b]-1,2,4,5-四嗪-3,7-二氧化物结构的构建,见图16。但整体而言,并联型富氮芳环N-氧化物更多倾向于采用直接环化的方法构建N-氧化物片段。

图16 6-氨基-四唑并[1,5-b]-1,2,4,5-四嗪-3,7-二氧化物的制备Fig.16 Preparation of 6-amino-tetrazolo[1,5-b]-1,2,4,5-tetrazine-3,7-dioxide structure
事实上,并联型富氮芳环N-氧化物往往存在高能量密度水平与低水解稳定性的矛盾。Rakitin等[49]将以并环策略将氧化呋咱环与哒嗪-1,2-二氧化物完成重组,成功实现了4,6-二硝基-呋咱[3,4-d]-1,5,6-三氧化物的合成,可能的转化机制如图17所示。该化合物晶体熔点在50~52℃,且无法在多种有机溶剂中稳定存在。该化合物密度达到了1.98g/cm3,理论爆速达到9.52km/s,与CL-20相当,但其较差的稳定性限制了其在配方研发中的应用。
通过直接环化合成的方式获得高氮氧含量的并联富氮稠环N-氧化物结构需要以富氮芳环N-氧化物的环合成方法学研究为基础。直接环化合成方式获得高氮氧含量富氮稠环N-氧化物的代表性工作是1,2,3,4-四嗪并[5,6-e]-1,2,3,4-四嗪-1,3,5,7-四氧化物(TTTO)的设计与合成研究。TTTO计算密度可达2.155g/cm3,生成焓836.8kJ/mol,爆速10.9km/s,爆压60GPa,氧平衡为零,各项指标均高于现有含能化合物,被一度视为C-H-O-N类含能化合物的能量极限,凸显了富氮稠环N-氧化物的研究价值。2016年,Anikin等[28, 50-52]首次通过独特的H2SO4-HNO3-Ac2O“一锅法”硝化环化方法突破了第二个高张力环境下的1,2,3,4-四嗪-1,3-二氧化物环系的构建,成功实现了TTTO合成。但新形成的双1,2,3,4-四嗪-1,3-二氧化物稠环极易水解为更稳定的1,2,3,4-四嗪-1,3-二氧化物并三唑,表明双1,2,3,4-四嗪-1,3-二氧化物稠环虽然能量密度水平优异,但近乎极限的高氮氧比例一定程度上影响了结构稳定性,见图18。

图17 4,6-二硝基-呋咱[3,4-d]-1,5,6-三氧化物的制备Fig.17 Preparation of 4,6-Dinitro-furazan[3,4-d]-1,5,6-trioxide

图18 TTTO的制备Fig.18 Synthesis of TTTO
氧化呋咱并二氧化四嗪结构氧平衡为零,结构高度紧凑,是极其理想的含能结构。针对这一结构,多个团队进行了长期的研究,但始终未能获得合成突破。2021年,Khakimov等[54]发表了关于氧化呋咱并二氧化四嗪研究的原理性探索结果,指出由于氧化呋咱中N-氧化物片段对硝酰阳离子[55-57]以及其他阳离子的吸引作用,将使得环化过程被锁死在中间体状态无法继续转化(见图19)。这一研究结果从理论角度揭示了N-氧化物体系硝化环化过程的深层次反应性问题,对基于二氧化四嗪体系并环类结构研究具有重要的指导意义。

图19 氧化呋咱-1,2,3,4-四嗪1,3-二氧化物的可能转化途径Fig.19 Possible transformation pathways towards furoxano-1,2,3,4-tetrazine 1,3-dioxides
王伯周等[58-59]利用3-氨基-4-(叔丁基-NNO-氧化偶氮基)氧化呋咱结构,开展了氧化三唑并二氧化四嗪结构的合成(见图20)。为实现合成目标,需要首先将3-氨基-4-(叔丁基-NNO-氧化偶氮基)氧化呋咱结构转化为3-氨基-4-(叔丁基-NNO-氧化偶氮基)氧化三唑的结构,这一反应通过加入叔丁胺顺利实现了相应的转化。此结构同时包含氧化偶氮片段和具有强吸电子效应的氧化三唑体系,利用这一体系在H2SO4-HNO3-Ac2O条件下进行硝化环化,顺利实现了二氧化四嗪片段的合成,对氧化三唑中所包含的叔丁基完成了同步脱除。需要指出,这一结构同时包含中性的芳香性N-氧化物(N-oxides)和羟胺型N-氧化物结构。

图20 氧化三唑-1,2,3,4-四嗪1,3-二氧化物的合成Fig.20 Synthesis of 1,2,3-triazole-1-oxide-1,2,3,4-tetrazine 1,3-dioxides
4 结束语
氮氧化富氮骨架是重要的含能材料骨架单元,通过不同结构的基于氮氧化富氮骨架含能材料合成方法及其能量密度水平的对比,可以得出以下结论:
(1)从合成方法角度,单环型结构的合成较为简单,N-氧化物主要以环系中氮原子的氧化方法为基础;而串联型结构较之单环型结构更加复杂,可以通过氧化或者环化的过程形成N-氧化物[60];与前两者相比,并联型结构的合成方法最为复杂,不仅直接氧化十分困难,同时环化形成N-氧化物的难度也显著高于其他体系;
(2)从能量密度水平角度,在N-氧化物片段引入后,由于正氧平衡水平和生成焓水平的提升,整体的能量密度水平得以显著提升,且容易形成多种含能离子盐结构,进一步丰富和调节了其能量特性。与此同时,盐类结构多存在于单环型及串联型N-氧化物结构当中,并联型结构由于其结构特殊性,一般较少形成相关盐类结构;
(3)在单环型结构与串联型结构中,N-氧化物片段的存在并未显著降低所得化合物的环系稳定性,同时由于氢键等效应的加强,其撞击感度及摩擦感度等往往会有一定的提升[61];而对于并联型结构,N-氧化物片段的大量引入,极大提升了整体骨架的致密程度,但骨架稳定性,尤其水解稳定性有所降低,这与稠环结构中N-氧化物提供了更多的活性反应位点有一定关联。
